第七章习题答案
生理学IV——第七章 能量代谢和体温 习题+答案

生理学——第七章能量代谢和体温一、单选题1.在物质代谢的过程中,伴随着能量的释放、转移、贮存和利用称为A.能量代谢B.能量代谢率C.基础状态D.基础代谢E.基础代谢率【答案】A2. 对能量代谢影响最大的因素是A.寒冷B.高温C.肌肉活动D.精神活动E.进食【答案】C3. 营养物质中最主要的供能物质是A.糖B.脂肪C.蛋白质D.维生素E.无机盐【答案】A4. 当外界温度等于或高于机体皮肤温度时,机体的散热方式是A.辐射散热B.传导散热C.对流散热D.蒸发散热E.传导和对流散热【答案】D5. 1克食物氧化进所释放的热量称为A.食物的卡价B.氧热价C.呼吸商D.非蛋白呼吸商E.能量代谢【答案】A6. 进食后,使机体产生额外热量最多的物质是A.糖B.脂肪C.蛋白质D.混合食物E.维生素【答案】C7. 能量代谢率与下列哪项具有比例关系A.体重B.身高C.体表面积D.环境温度E.进食量【答案】C一、问答题1.影响能量代谢的因素。
答:肌肉活动对人体能量代谢的影响最为显著,任何轻微活动都可提高能量代谢率。
剧烈运动或劳动因做功更多,故影响更明显。
环境温度人在安静时的能量代谢,在20℃-30℃的环境中最为稳定。
当环境温度降低人感到寒冷时,机体就会发生寒战和骨骼肌张力增高等现象,使能量代谢率增高;当环境温度升高时,可使体内生化反应速度加快,汗腺分泌旺盛和呼吸循环机能增强,以至产热量升高。
食物的特殊动力效应在进食后1-8小时左右,机体即使处于安静状态,其产热量也会比进食前提高。
这种食物引起机体产生额外热量的作用称为食物的特殊动力效应。
食物的特殊动力作用以蛋白质为最强,一般可以产生30%额外热量。
脂肪和糖类增加的热量约为4-6%。
精神活动当精神紧张或情绪激动时,由于骨骼肌张力增加、交感神经兴奋、促进可产热激素甲状腺激素和肾上腺激素的释放,使能量代谢可显著提高。
2.什么是体温。
体温有哪些的生理变异?答:体温是指体内深部的平均温度。
高等数学第七章 习题答案

习题7-11. 下列向量的终点各构成什么图形?(1)空间中一切单位向量归结为共同的始点;(2)平行于同一平面的一切单位向量归结为共同的始点;(3)平行于同一直线的所有单位向量归结为同一始点;(4)平行于同一直线的所有向量归结为同一始点。
答:(1)单位球面 (2)单位圆 (3)两个点 (4)直线。
2. 设点O 是正六边形ABCDEF 的中心,在向量,,,,,,,,OA OB OC OD OE OF AB BC ,,,CD DE EF FA 中,哪些向量是相等的? 答:,OA EF =,OB FA =,OC AB =,OD BC =,OE CD =.OF DE =3.平面四边形,ABCD 点,,,K L M N 分别是,,,AB BC CD DA 的中点,证明:.KL NM =当四边形ABCD 是空间四边形时,上等式是否仍然成立?证明:连结AC, 则在∆BAC 中,21AC. 与方向相同;在∆DAC 中,21AC. NM 与AC 方向相同,从而KL =NM 且KL 与NM 方向相同,所以KL =NM .当四边形ABCD 是空间四边形时,上等式仍然成立。
4. 解下列各题:(1)化简()()()()2332;x y x y -+-+-a b a b(2)已知12312323,322,=+-=-+a e e e b e e e 求,,32+--a b a b a b.解:(1)()()()()2332x y x y -+-+-a b a b()()()()23322332x y x y x y x y =--++-++⎡⎤⎡⎤⎣⎦⎣⎦a b()()55x y x y --+-=a b;(2)()()123123123233225;+=+-+-+=++a b e e e e e e e e e()()12312312323322;-=+---+=-+a b e e e e e e e +e e()()()()123123123123323232322693644-=+---+=+---+a b e e e e e e e e e e e e 235.=+e e5.四边形ABCD 中,2,568AB CD =-=+-a c a b c,对角线,AC BD 的中点分别是,,E F 求.EF 解:()()111156823352222EF CD AB =+=+-+-=+-a b c a c a b c.6. 设ABC ∆的三条边,,AB BC CA 的中点分别为,,,L M N 另O 为任意一点,证明: .OA OB OC OL OM ON ++=++证明:(1)如果O 在ABC ∆内部(如图1),则O 把ABC ∆分成三个三角形OAB,OAC,OBC 。
普通化学第七章课后习题解答

第七章沉淀反应参考答案P 142【综合性思考题】:给定体系0.02mol/LMnCl 2溶液(含杂质Fe 3+),经下列实验操作解答问题。
(已知K θSPMn(OH)2=2.0×10-13,K θSPMnS =2.5×10-13,K θbNH3=1.8×10-5,K θaHAc =1.8×10-5①与0.20mol/L 的NH 3.H 2O 等体积混合,是否产生Mn(OH)2沉淀?解:等体积混合后浓度减半,[Mn 2+]=0.01mol/L ,c b =[NH 3.H 2O]=0.10mol/L∵是一元弱碱体系,且c b /K b θ>500∴10.0108.1][5⨯⨯=⋅=--b b c K OH θ又∵ 622108.101.0][][--+⨯⨯=⋅=OH Mn Q c=1.8×10-8> K θSPMn(OH)2=2.0×10-13∴ 产生Mn(OH)2沉淀。
②与含0.20mol/L 的NH 3.H 2O 和0.2mol/LNH 4Cl 的溶液等体积混合,是否产生Mn(OH)2沉淀? 解:混合后属于NH 3.H 2O~NH 4Cl 的碱型缓冲液体系此时浓度减半:c b =[NH 3.H 2O]=0.2V/2V=0.1(mol.L -1)c S= [NH 4+]=0.2V/2V=0.1(mol.L -1)[Mn 2+]=0.02V/2V=0.01(mol.L -1)A 、求[OH -] 用碱型缓冲液计算式求算:s b b c c K OH ⋅=-θ][ 55108.11.01.0108.1--⨯=⨯⨯= B 、求Qc 22][][-+⋅=OH Mn Q c=0.01×[1.8×10-5]2=3.24×10-12C 、比较θ2)(,OH Mn SP K ∵13)(,100.22-⨯=>θOH Mn SP C K Q故有Mn(OH)2沉淀产生。
第七章 习题答案
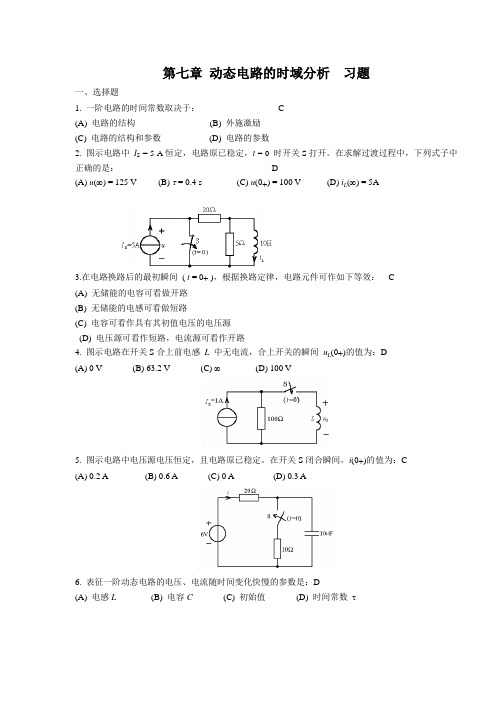
第七章动态电路的时域分析习题一、选择题1. 一阶电路的时间常数取决于: C(A) 电路的结构(B) 外施激励(C) 电路的结构和参数(D) 电路的参数2. 图示电路中I S = 5 A恒定,电路原已稳定,t = 0时开关S打开。
在求解过渡过程中,下列式子中正确的是: D(A) u(∞) = 125 V (B) τ = 0.4 s (C) u(0+) = 100 V (D) i(∞) = 5AL3.在电路换路后的最初瞬间( t = 0+ ),根据换路定律,电路元件可作如下等效: C(A) 无储能的电容可看做开路(B) 无储能的电感可看做短路(C) 电容可看作具有其初值电压的电压源(D) 电压源可看作短路,电流源可看作开路(0+)的值为:D4. 图示电路在开关S合上前电感L中无电流,合上开关的瞬间uL(A) 0 V (B) 63.2 V (C) ∞(D) 100 V5. 图示电路中电压源电压恒定,且电路原已稳定。
在开关S闭合瞬间,i(0+)的值为:C(A) 0.2 A (B) 0.6 A (C) 0 A (D) 0.3 A6. 表征一阶动态电路的电压、电流随时间变化快慢的参数是:D(A) 电感L(B) 电容C(C) 初始值(D) 时间常数τ7. 图示正弦脉冲信号的数学表达式为:B (A) sin ω t ⋅ ε (t ) + sin ω ( t - T ) ⋅ ε ( t - T ) (B) sin ω t ⋅ ε (t ) - sin ω t ⋅ ε ( t - T ) (C) sin ω t ⋅ ε (t ) - sin ω ( t - T ) ⋅ ε ( t - T ) (D) sin ω t ⋅ ε (t ) + sin ω t ⋅ ε ( t - T )8. 图示电路中,原已达稳态, t = 0开关 S 打开,电路的时间常数为:D (A)s 41 (B) s 61(C) s 4 (D)s 69. 示电路中,t = 0 时开关打开,则 u (0+)为:C(A) 0V (B) 3.75V (C) – 6V (D) 6V10.图示电路中,开关打开已久,在 t = 0 时开关闭合,i (0+) 为:D(A) 0A (B) 0.8A(C) 2A (D)1A11.R 、C 串联电路,已知全响应()()10C 83V,0t u t e t -=-≥,其零状态响应为:(A )(A) 1088V te-- (B) 1083V t e -- (C) 103V t e -- (D) 105V t e -12. .一阶电路的全响应()()10C 106V,0tu t et -=-≥若初始状态不变而输入增加一倍,则全响应u C (t)为 ( D ) (A) 20-12e -10t ; (B) 20-6e -10t ; (C) 10-12e -10t ; (D) 20-16 e -10t 。
第七章习题及答案

第七章习题及答案第七章习题及答案1. 如果要设置幻灯片“水平百叶窗”播放效果,应使用菜单“幻灯片放映”中的(b)a. 动作设置b. 自定义动画c. 预设动画2. 列方法中不能启动PowerPoint 2003的是(前提为已正常安装好PowerPoint 2003)( c)a. 选择“开始”—“程序” —“ Microsoft Office 2003 ” —“ Microsoft Office PowerPoi nt 2003 ”命令b. 用鼠标左键双击桌面上的PowerPoint 2003快捷方式图标c. 用鼠标右键双击桌面上的PowerPoint 2003快捷方式图标d. 用鼠标左键双击已建立好的PowerPoint 2003文件3. 显示和隐藏工具栏的操作是(d )a. 隐藏“浮动工具栏”,可双击它b. 通过“工具”菜单的“自定义”命令进行操作c. 用鼠标右键单击此工具栏d. 点击“视图”菜单中的“工具栏”,在弹出的菜单中单击需要显示或隐藏的工具栏名称4. powerPoint 2003 有__d ___ 中显示视图。
a. 5b. 2c. 3d. 45. “文件”菜单中的“打印”命令,其快捷键是(c )a. Ctrl+Nb. Ctrl+Sc. Ctrl+Pd. Ctrl+X6. 在PowerPoint 2003中,“文件”菜单中的“打开”命令的快捷键是(a)a. Ctrl+O b. Ctrl+S c. Ctrl+P d. Ctrl+N7. 计算机没有接打印机,Powerpoint2003将_______a ____ 。
a. 可以进行幻灯片的放映,但不能打印b. 不能进行幻灯片的放映,也不能打印c. 按文件类型,有的能进行幻灯片的放映,有的不能进行幻灯片的放映d. 按文件大小,有的能进行幻灯片的放映,有的不能进行幻灯片的放映8. Powerpoint 2003演示文稿的默认扩展名是(c)a. DOCb. XLSc. PPTd. PTT9. 在用PowerPoint 2003制作的幻灯片中__d ______ 。
第七章练习题及答案(可编辑修改word版)

第七章练习题及答案一.单项选择题1.根据我国《宪法》、《立法法》等的规定,()行使国家立法权。
A.国务院B.全国人民代表大会及其常务委员会C.地方政府 D 地方人民代表大会及其常务委员会2.国务院有权根据宪法和法律制定()。
A.部门规章B.地方性法规C.行政法规D.地方政府规章3.国务院各部门可以根据宪法、法律和行政法规,在本部门的权限范围内,制定()。
A.部门规章B.地方性法规C.行政法规D.地方政府规章4.省、自治区、直辖市的人民代表大会及其常委会根据本行政区域的具体情况和实际需要,在不同宪法、法律和行政法规相抵触的前提下,可以制定()。
A.部门规章B.地方性法规C.行政法规D.地方政府规章5.省、自治区、直辖市、较大的市的人民政府可以根据法律、行政法规和本省、自治区、直辖市的地方性法规,制定()。
A.部门规章B.地方性法规C.行政法规D.地方政府规章6.在广义上,法律执行是指(),在国家和公共事务管理中依照法定职权和程序,贯彻和实施法律的活动。
A.国家公务员B.国家机关及其公职人员C.社会组织D.公民7.法律适用是指()依照法定职权和程序适用法律处理案件的专门活动。
A.国家立法机关及其公职人员B.国家行政机关及其公职人员C.国家司法机关及其公职人员D.国家机关及其公职人员8.依法治国的主体是()。
A.行政机关B.立法机关C.司法机关D.人民群众9.从法律运行的环节来看,法律公正包括()两个方面。
A.守法公正和司法公正B.立法公正和执法公正C.实体公正和程序公正D.权利公正与义务公正10.从法律公正的内涵来看,法律公正包括()两个方面。
A.守法公正和司法公正B.立法公正和执法公正C.实体公正和程序公正 D.权利公正与义务公正11.()是国家安全的支柱与核心。
A.政治安全和国防安全B.经济安全与科技安全C.文化安全与生态安全D.社会公共安全与政治安全12.()是维护国家安全的专门法律,规定了国家安全机关在国家安全工作中的职责以及公民和组织维护国家安全的权利和义务,规律了各类危害国家安全行为所应承担的法律责任。
有机化学课后习题答案7第七章答案
4.
V2O5, O2
一. 命名或写出结构式
1.
2. C2H5
NO2
Br2 Fe
NO2 Br
O
O
O
O
浓H2SO4
AlCl3 O
COOH
O
习题 B 答案
CH3 3.
OH 4.
SO3H
H3C
5.
6.
7. 2-乙基-9,10-蒽醌 8. 2-环丙基萘
9. 1,4-二甲基萘 10. 邻苯二甲酸酐
二.用休克尔规则判断下列化合物是否有芳香性
CHO
CHO
CH3 NBS
O2, V2O5 400-500℃
CH2MgBr 无水乙醚
CH2Br Mg 无水乙醚
CH2MgBr
O
O AlCl3
O
O Zn-Hg HCl
HOOC
H2SO4 HOOC
H3O+
H2/Ni HO CH2
H2SO4 HO CH2
O CH2
5.
O
O
Zn-Hg
浓H2SO4
O AlCl3
第七章 稠环芳香烃
一.写出下列化合物的结构式
习题 A 答案
NO2
Cl
Br
OH
1.
2.
3. NO2
4.
5.
6.
7.
8.
CH3 H3C
9.
10.
二.用系统命名法命名下列化合物 1、8-溴-1-萘甲醚 2、1-萘甲醛(α-萘甲醛) 3、8-氯-1-萘甲酸 4、2-氯-6ˊ-溴联苯 5、9-硝基菲 6、2-甲基蒽 7、2,6-二甲基萘 8、2-萘酚(β-萘酚) 三、选择题 1、C 2、A 3、B 4、AD 5、C 6、D 四.下列化合物有无芳香性,为什么? 解:(1)的π电子数为 4 个,不符合 4n+2 规则,没有芳香性。
(完整版)高等代数(北大版)第7章习题参考答案

第七章 线性变换1. 判别下面所定义的变换那些是线性的,那些不是:判别下面所定义的变换那些是线性的,那些不是:1) 在线性空间V 中,A αξξ+=,其中∈αV 是一固定的向量;是一固定的向量; 2) 在线性空间V 中,A αξ=其中∈αV 是一固定的向量;是一固定的向量;3) 在P 3中,A),,(),,(233221321x x x x x x x +=; 4) 在P 3中,A ),,2(),,(13221321x x x x x x x x +-=; 5) 在P[x ]中,A )1()(+=x f x f ;6) 在P[x ]中,A ),()(0x f x f =其中0x ∈P 是一固定的数;是一固定的数;7) 把复数域上看作复数域上的线性空间,把复数域上看作复数域上的线性空间,A ξξ=。
8) 在P nn ⨯中,A X=BXC 其中B,C∈P nn ⨯是两个固定的矩阵. 解 1)当0=α时,是;当0≠α时,不是。
不是。
2)当0=α时,是;当0≠α时,不是。
不是。
3)不是.例如当)0,0,1(=α,2=k 时,k A )0,0,2()(=α, A )0,0,4()(=αk ,A ≠)(αkk A()α。
4)是.因取),,(),,,(321321y y y x x x ==βα,有A )(βα+= A ),,(332211y x y x y x +++=),,22(1133222211y x y x y x y x y x ++++--+ =),,2(),,2(1322113221y y y y y x x x x x +-++- = A α+ A β, A =)(αk A ),,(321kx kx kx),,2(),,2(1322113221kx kx kx kx kx kx kx kx kx kx +-=+-==k A )(α, 故A 是P 3上的线性变换。
上的线性变换。
5) 是因任取][)(],[)(x P x g x P x f ∈∈,并令并令 )()()(x g x f x u +=则A ))()((x g x f += A )(x u =)1(+x u =)1()1(+++x g x f =A )(x f + A ))((x g , 再令)()(x kf x v =则A =))((x kf A k x kf x v x v =+=+=)1()1())((A ))((x f , 故A 为][x P 上的线性变换。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第七章习题答案第7章练习第7章1。
计算氢原子核外的电子从第三能级跃迁到第二能级时产生的谱线H?波长和频率解决方案:?=右侧??1?n2?1??1n2?= 3.289?1015??1?1??1??2232?s??= 4.57?1014s?1??c?2.998?108米?s?1=4.57?1014s?1= 656?10?9m= 656nm2。
基态氢原子的电离能是多少?解决方案:我=?E = h?= 6.626?10?34 J?s?3.289?1015s?1(1/12?1/?)=2.179?10?18J3。
以下哪个量子数是不合理的?为什么?n l m(1)2 1 0(2)229?1(3) 2 3 +2解决方案:(1)合理;(2)L值不合理,应小于N;(3)l和m的值不合理,l应该小于n,m应该为0,?1,?2,??l;4.用合理的量子数表示:(1)三维能级;(2)4s1电子溶液:(1)3d能级:n=3,l = 2;(2)4s1电子:n=4,l=0,m = 0;;5。
分别写出下列元素基态原子的电子分布,并分别指出元素周期表中各元素的位置9f10 ne25 Mn29 Cu24 Cr55 cs71 Lu解决方案:9 F1s 22s 22 p 59第二周期VIIA组10Ne [He]2s22p6第二周期VIIIA组5 2以(1)为例,完成以下(2)?(4)问题1(1)Na(Z = 11)Ne]3s;(2)1s 22s 22p 63s 23p 3;溶液:(1)na(z = 11)[ne]3s 1;26233(3)(Z = 24)[?]3d 4s;(4)[?]3d 104s 24 p 6;(3)铬(Z = 24)[氩]3d 54s 1;102651(2)P(Z = 15)1s 2s 2p 3s 3p;(4)氪(Z = 36)[氩]3d 4s 4p;7。
写出下列离子的最外层电子分布:S?解决方案:S2?3 s3p262K K+3 s3p26+9 Pb2+6s22+6尝试完成下表原子序数价层电子分布11 21 35 48 60 82溶液:原子序数11 21 35 48价层电子分布3 S1 3d 14s 2 254 s4p 4d 105s各层电子数2,8,1 2,8,已知子组元素a的原子和电子最终填充在3d轨道中,最大氧化值为4;对于元素B的原子,个电子最终被填充在最高氧化值为5的4p轨道上:(1)写出元素A和元素B原子的电子分布;根据电子分布,(2)表示它们在周期表中的位置(周期、区域、族)。
解:原子a的最后一个电子填充在3d轨道上,它应该是第四周期d 或ds区域元素;最高氧化值为4,其价电子构型应为3d24s2,22Ti元素;填充在4p轨道中的B原子的最终电子应该是第四周期p区的元素,最高氧化值为5,其价电子构型为4s4p,应该是33As元素。
(1)22Ti:[Ar]3d 24s 2;33As:[Ar]4s24p 3;(2) 22Ti:位于第四周期D区IVB;;第四周期P区的33As:Va;10。
第四阶段有三个要素。
它们的价电子数是1、2和7,它们的原子序数按A、B和C的顺序增加众所周知,外层A和B中的电子数是8,而外层C中的电子数是18。
根据结构,什么是223第7章练习(1) C和A的简单离子?在(2) B和c之间可以形成什么化合物?试着写下化学式解答:根据问题的含义,a应该是19K,b应该是20Ca,c应该是35Br;(1) C和a的简单离子是溴和钾;离子化合物可以在(2) B和c: CaBr2之间形成11。
指出第四周期中具有下列性质的元素:(1)最大原子半径;(2)最大电离能;(3)最强的金属度;(4)非金属性最强;(5)最大电子亲和能;(6)化学性质最不活跃;溶液:(1)最大原子半径:k;(2)最大电离能:氪;(3)最强金属度:k;(4)最强非金属性:br;(5)最大电子亲和力:溴;(6)化学性质最不活跃:KR;12.一种元素的原子在其最外层只有一个电子。
电子的量子数是n = 4,l = 0,m = 0,ms = +1/2,q:(1)有多少元素能满足上述条件?原子序数是多少?(2)写出了相应元素原子的电子分布,并指出它在周期表中的位置溶液:(1)有三种元素满足上述条件:钾、铬、铜;原子序数分别是19、24和29。
(2)对应元素原子的电子分布为:[氩]4s1,[氩]3d54s1,[氩]3d 104 S1;分别位于元素周期表第四周期的S区1A、D区VIB和ds区1B13.在下面的电子构型中,第一电离能最低的原子通常有哪种构型?(1)ns2np 3;(2)ns2np 4;(3)ns2np 5;(4)ns2np 6;溶液:通常,第一电离能最小的原子具有(2) ns2np4构型,失去一个电子后变成np半全稳定构型,因此其电离能较小14。
一种元素的原子序数小于36。
当这个元素的原子失去3个电子时,它的角动量量子数等于2。
轨道中的电子数正好是一半:(1)写出了这个元素原子的电子排列;(2)这个元素属于哪个周期、哪个组和哪个区域?元素符号是什么?溶液:分析:原子序数小于36的应是前四个周期元素;角动量量子数等于2,l = 2,这应该是轨道的D轨道。
只有前四个周期中的第四个周期有D轨道,所以它应该是第四个周期的元素。
在(1)失去3个电子之后,3d轨道中的电子数是半满的,元素应该具有3d64s2构型,并且元素原子的电子排列应该是[氩]3D 4s;(2)此元素属于第四周期VIIIB组d区,元素符号为Fe15。
已知H2O(克)和H2O2(克)?fH?m是?241.8千焦?摩尔。
1 、?136.3千焦?摩尔。
1,H2 (g)和O2(g)的离解能分别为436 kJ?摩尔。
1和493千焦?摩尔。
1.求过氧化氢中氧-氧键的键能?H溶液:氢(克)+1/2氧(克)?f m(H2O)HO(g)22262?+?h?乙(氢-氢)1/2?h?b(O-O) 2?h?b(H-O)2H(g)+O(g)?fH?m(H2O) + 2?h?乙(氢氧基)=?h?b(高-高)+ 1/2?h?b(O-O) 2?h?乙(氢氧基)=?h?b(高-高)+ 1/2?h?b(O-O)??fH?m(H2O) = [436 + (1/2)?493?(?241.8) ] kJ?摩尔。
1 = 924.3千焦?mol?13无机和分析化学学习指南?fH?m(H2O 2)H2(g)+O2(g)H2O 2(g)?h?b(高-高)?h?b(O-O)?rH?m2H(g) + 2O(g)?fH?m(H2O2) +?rH?m =?h?b(H-H) +?h?b(O-O)?rH?m =?h?b(H-H) +?h?b(O-O)??fH?m(H2O2)= [436 + 493?(?136.3)] kJ?摩尔= 1065.3千焦?mol?rH?m = 2?h?乙(氢氧基)+?h?b(-O-O-)?h?b(-O-O-) =?rH?m?2?h?英国(海外)= [1065.3?924.3]千焦?摩尔= 141千焦?摩尔。
1 = e (-o-o-)16。
已知NH3(g)?fH?m=?46kJ?摩尔。
1,H2N-NH2 (G)?fH?m= 95kJ?摩尔。
1,E(H―H)= 436千焦?摩尔,E(N≡N) = 946千焦?Mol计算e (n-h)和e (h2n-NH2)?fH?M(NH3)溶液:1/2 N2(g)+3/2 H2(g)NH3(g)1/2?h?b(N2)3/2?h?b(H2) 3?h?乙(男-女)?1?1?1?1?1N(g) + 3H(g)?fH?m(NH3) + 3?h?b(N-H) = 1/2?h?b(N2) + 3/2?h?(H2)?h?b(N-H) = 1/3[1/2?h?b(N2) + 3/2?h?(H2)??fH?m(NH3)] = 1/3[ (1/2)?946 + (3/2)?436?(?46)] kJ?摩尔。
1 = 391千焦摩尔?1 =东(北――西)?fH?m(N2H 4)N2(g)+2H 2(g)N2H 4(g)?h?b(N2)2?h?(H2)?rH?m2N(g) + 4H(g)?fH?m(N2H4) +?rH?m =?h?b(N2) + 2?h?b(H2)?rH?m =?h?b(N2) + 2?h?(H2)??fH?m(N2H4)= [946 + 2?436?95]千焦?摩尔。
1 = 1723千焦?摩尔。
1?rH?m =?h?b(H2N-NH2) + 4?h?乙(不含乙)?h?b(H2N-NH2) =?rH?m?4?h?乙(北半球)= [1723?4?391]千焦摩尔?1?1= 159 kJ摩尔= E (H2N-NH2)17。
写出O2分子的分子轨道表达式,并据此判断下列双原子分子或离子:O2+,O2,O2?、O22?它们中有多少是单电子,从强到弱排列它们的键的强度,并猜测它们的磁性4第7章练习解:O2分子的分子轨道表达式是O2 [(?1s)2(?*1s)2(?2s)2(?*2s)2(?2px)2(?2py)2(?2pz)2(?*2py)1(?*2pz)1]O2+、O2?、O22?分子轨道表达式为O2 [(?1s)(?1s)(?2s)(?2s)(?2px)(?2py)(?2pz)(?2py)]O2??(?1s)2(?*1s)2(?2s)2(?*2s)2(?2px)2(?2py)2(?2pz)2(?*2py)2(?*2pz)1?O22??(?1s)2(?*1s)2(?2s)2(??2s)2(?2px)2(?2py)2(?2pz)2(?*2py)2(?*2pz)2?+?2?O2、O2、O2和O2的单电子数分别为1、2、1和0,分别具有顺磁、顺磁、顺磁和反磁。
O2+、O2、O2?、O22?的焊接等级为焊接等级(O2+)=(8?3)/2 = 2.5;焊接等级(O2) = (8?4)/2 = 2;粘合水平(O2?)=(8?5)/2 = 1.5;关键级别(O22?)=(8?6)/2 = 1;O2+、O2、O2?、O22?化合物的结合强度依次降低。
18。
根据电负性的不同,确定下列化合物对中键的极性(1) FeO和FeS (2) AsH3和NH3(3) NH3和NF3 (4)四氯化碳和四氯化硅溶液:(1) xO > xS,FeO极性大于FeS;(2) xN > xAs,氮氢极性大于砷氢极性;(3)?x(N-H)=(3.0?2.1)=0.9,?x(N-F)=(4.0?3.0)=1.0,正-反极性大于正-反极性;(4) xC > xSi,硅-氯极性大于碳-氯;19。
用混合轨道理论解释为什么三氯苯酚是一个键角为101的三角锥,而三氯苯酚是一个平面三角几何溶液:p原子的外电子构型为3s23p3。
