三元系相图绘制
三元相图教程ppt课件

6
确定一点的组成
1、平行线法(三线法)
7
2、双线法确定三元组成
b
c
a
8 8
• 如果三元相图的组分已知就可以在浓度三 角形中确定相应的位置。
O的组成为: A——30% B——60% C——10% 那么O点应该 在哪里呢?
9
三、三元系统组成
C
中的一些关系
1、等含量规则
在等边三角形
B
M1+M2-M3=M
从M1+M2中取出M3愈多,则M点离M3愈远。 16
(3) 共轭位置规则
在三元系统中,物质
组成点M在的一个角顶
之外,这需要从物质M3中 取出一定量的混合物质M1 +M2,才能得到新物质M, 此规则称为共轭位置规则。
由重心规则:
M1+M2+M=M3 或:M= M3 -(M1+M2)
液相点
固相点
49
C
D
F
C .G
e4
3 E Pm
A
S
A
e1
Q
析晶路程:
液相点
e3
.B
S
(3).分析:3点在C的初晶区内,开始
析出的晶相为C,在ASC内,最终析 晶产物为A、S、C,析晶终点在E点, 结晶终产物是A、S、C。途中经过P 点,P点是转熔点,同时也是过渡点。 B L+B S+C
固相点
50
Q/
S/
A/
L+B
B/ 29
1) 几条重要规则
(1)连线规则:用来判断界线的温度走向;
定义:将界线(或延长线)与相应的组成点的连线
相交,其交点是该界线上的温度最高点;温度走
向是背离交点。在连线的同时也就划出了副三角
三元系统相图

三元系统相图
一、三元系统相图概述
三元凝聚系统相律: F=C-P+1=4-P
1、三元系统组成表示方法
——浓度(组成)三角形 应用: 1)已知点 的位置, 确定其组成; 2)已知组成,确定 点的位置;
双线法:
2、浓度三角形规则
(1)等含量规则 等含量规则:平行于浓度 三角形一边的直线上的各点, 其第三组分的含量不变,即: MN线上C%相等。
在在mn外mpn二三元系统相图基本类型一具有一个低共熔点的简单三元系统相图二生成一个一致熔融二元化合物的三元系统相图三具有一个一致熔融三元化合物的三元系统相图四生成一个不一致熔融二元化合物的三元系统相图五具有一个不一致熔融三元化合物的三元系统相图六生成一个固相分解的二元化合物的三元系统相图七具有多晶转变的三元系统相图八形成一个二元连续固溶体的三元系统相图九具有液相分层的三元系统相图一具有一个低共熔点的简单三元系统相图1立体相图2平面投影图投影图上温度表示法
T转 > Te3 、 T转 < Te2——多晶转变点P
T转 < Te2 、Te3——多晶转变点P1、P2
(八)形成一个二元连续固溶体的三元系统相图
(九)具有液相分层的三元系统相图
总结:
分析实际三元系统(复杂三元系统)相图的步骤
一、判断化合物的性质;
二、划分副三角形; 三、判断界线上温度变化——连(结)线规则; 四、判断界线性质——切线规则; 五、确定三元无变量点的性质——重心原理;
(三) 具有一个一致熔融三元化合物的三元系统相图
(四) 生成一个不一致熔融二元化合物的三元系统相图 1、相图组成
(1)不一致熔融化合物S不在自己的相区内; (2)化合物S性质的改变,导致CS连线、无变 量点P、界线的性质改变。 (a)CS连线 (b)无变量点:P点
三元相图ppt

相态的分析
确定三元相图的三个相态
根据三元相图中的三个区域,可以确定三元相图的三个相态,即液相、固相和气 相。
确定相态之间的转化
三元相图中不同相态之间的转化与成分和温度有关,可以根据相图中的成分和温 度范围确定不同相态之间的转化条件。
结晶过程的分析
分析结晶过程
三元相图中的结晶过程分析需要了解不同成分的溶液中结晶 过程的特点,以及结晶过程中成分的变化规律。
材料科学的基础研究
三元相图的研究也是材料科学基础研 究的重要组成部分。通过对三元相图 的深入研究,可以更好地理解物质的 本质和规律,为材料科学的其他领域 提供基础支撑。
THANKS
谢谢您的观看
新型材料的探索
研究者们通过实验探索新型材料的三元相图,以寻找具有更优性能的相变材料, 应用于能源、环保等领域。
理论研究进展
计算方法的改进
研究者们不断改进计算方法,以更准确地预测三元相图中的 相行为。
分子动力学模拟
利用分子动力学模拟技术,研究者们可以模拟真实材料的三 元相图,为理论预测提供更为准确的依据。
多晶型和同素异构体的存在
在某些三元体系中,可能存在多种晶型和同素异构体,这些不同结构的物质在物理和化学 性能上可能存在显著的差异,因此如何考虑这些差异对三元相图的影响也是一个重要的问 题。
三元相图未来研究方向的建议
加强实验研究
由于三元相图的复杂性,实验研究仍然是确定三元相图最准确的方法。因此,需要发展新的实验技术,提高实验的精度和效 率,同时需要建立更加完善的数据库和理论模型来描述和预测三元相图。
应用研究进展
能源储存与运输
研究者们正在研究如何利用三元相图优化能源储存与运输过程中的性能。例 如,优化相变材料在储存和运输过程中的热力学性质。
三元相图的绘制详解

三元相图的绘制详解在材料科学、化学等领域,三元相图是一种非常重要的工具,它能够直观地展示三种组分在不同条件下的相态变化和平衡关系。
三元相图的绘制并非易事,需要对相关的理论知识有深入的理解,并掌握一定的实验技巧和数据处理方法。
下面,就让我们一起来详细了解三元相图的绘制过程。
要绘制三元相图,首先得明确什么是三元相图。
简单来说,三元相图是表示在恒压和恒温下,由三种组分构成的系统中,各相的状态与成分之间关系的图形。
它通常由等边三角形组成,三角形的三个顶点分别代表三种纯组分。
绘制三元相图的第一步是确定研究的体系和实验条件。
这包括选择要研究的三种物质,设定温度、压力等参数。
在确定了体系和实验条件后,接下来就是进行实验获取数据。
实验方法多种多样,常见的有热分析法、金相法、X 射线衍射法等。
以热分析法为例,我们将不同成分的样品加热或冷却,通过测量样品的温度随时间的变化,来确定相变点。
在实验过程中,需要精确控制温度变化的速率,以确保测量结果的准确性。
同时,要对多个不同成分的样品进行测试,以获得足够的数据来绘制相图。
当我们获得了大量的实验数据后,就可以开始着手绘制相图了。
绘制的过程中,需要将实验得到的相变温度和成分数据标注在等边三角形的坐标上。
在标注数据时,要注意坐标的转换和计算。
因为在三元相图中,成分通常用质量分数或摩尔分数来表示,而不是直接用实验中测量得到的数值。
比如说,如果我们知道了三种组分 A、B、C 的质量分数分别为 wA、wB、wC,那么在等边三角形坐标中,对应的坐标点可以通过以下公式计算:对于 A 组分,横坐标 xA = wA /(wA + wB + wC) ×边长对于 B 组分,纵坐标 yB = wB /(wA + wB + wC) ×边长通过这样的计算,我们就可以将实验数据准确地标注在相图上。
标注完数据点后,接下来就是连接这些点,形成相区的边界线。
这需要根据相律和热力学原理来判断。
三元相图(2)

是三元系中的杠杆定律。
由直线法则及杠杆定律可作出下列推论:当给定材料在一定温度下处于两相平衡 状态时,若其中一相的成分给定,另一相的成分点必在两已知成分点连线的延长线 上;若两个平衡相的成分点已知,材料的成分点必然位于此两个成分点的连线上。
三元相图与二元相图比较。组元数增加了一个,即成分变量为两个,故表示成分的坐标轴 应为两个,需要用一个平面来表示,再加上一个垂直该成分平面的温度坐标轴,这样三元相 图就演变成一个在三维空间的立体图形。这里,分隔每一个相区的是一系列空间曲面,而不 是平面曲线。
要实测一个完整的三元相图,工作量很繁重,加之应用立体图形并不方便。因此,在研究 和分析材料时,往往只需要参考那些有实用价值的截面图和投影图,即三元相图的各种等温 截面、变温截面及各相区在浓度三角形上的投影图等。立体的三元相图也就是由许多这样的 截面和投影图组合而成的。
2.截面图 rs和At垂直截面如下图所示。rs截面的成分轴与浓度三角形的AC边平行,图中re
和es是液相线,相当于截面与空间模型中液相面Ae1Ee3A和Ce2Ee3C的截线;曲线 r1d′是截面与过渡面fe1Emf的截痕,de,ei和isl分别是截面与过渡面le3Eml, ke3Epk和je2Epj的交线;水平线r2s2是四相平衡共晶平面的投影。 利用这个垂直截面可以分析成分点在rs线上的所有合金的平衡凝固过程,并可确定 其相变临界温度。以合金O为例。当其冷到1点开始凝固出初晶A,从2点开始进入L +A+C三相平衡区,发生L→A+C共晶转变,形成两相共晶(A+C),3点在共晶 平面mnp上,冷至此点发生四相平衡共晶转变L→A+B+C,形成三相共晶(A+B +C)。继续冷却时,合金不再发生其他变化。其室温组织是初晶A十两相共晶(A +C)十三相共晶(A+B+C)。
第五章 三元相图
B1
AБайду номын сангаас
B
C
(二)等温截面及其投影
L+C L
L+C L
L+A
L+A+C L+A L+C L
L+A+C L L+B
L+B
L+A+C L+A+B+C
C B
A+B+C
A
L+A+C L+A+B+C L+A+C L L+B
1.等温截面上的三相平衡区都是直边三角形,与 三角形相邻接的是两相平衡区 2.三角形的顶点与单相区相接,分别表示该温度 下三个平衡相的成分
LA+ C
TA C1 A3 A2 A1
E
L B + C
四三 相相 平平 衡衡 共共 晶晶 转 变 结 束
——
TB E1 B3 B2 E2 E B1
A
E3
TC
B
C3 C2 C1
C
中 转平 间 变衡 开 共 三面
始晶相
A3
A2 A1
E1
B2
B1
LA+ B
——
TA
A3 A2 A1
E TB E1 E3 TC E2 B3 B2 B1 B3 E2 B1 E C2 C1
B 10 20 30 40
50
C% 60 70 80 90
50 40 ← A%
30
20 10
C
课堂练习
90 3. 标出 50%A+20%B+30%C 80 的合金 70 60 B% 50 40 30 20 10 A 90 80 70 60
三元体系相图的绘制
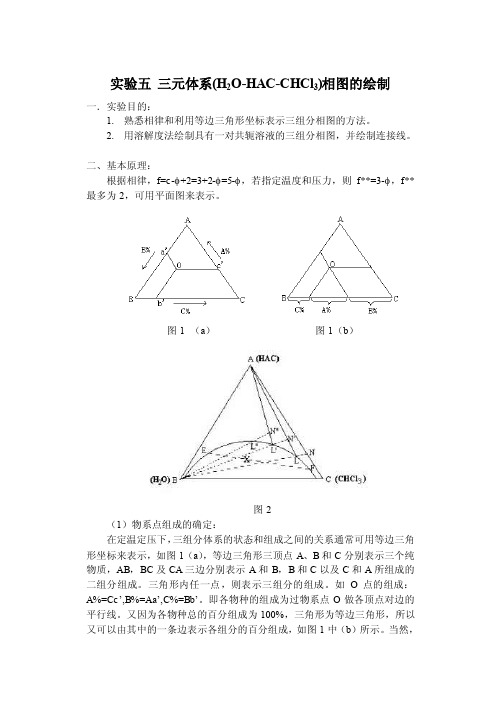
实验五三元体系(H2O-HAC-CHCl3)相图的绘制一.实验目的:1.熟悉相律和利用等边三角形坐标表示三组分相图的方法。
2.用溶解度法绘制具有一对共轭溶液的三组分相图,并绘制连接线。
二、基本原理:根据相律,f=c-φ+2=3+2-φ=5-φ,若指定温度和压力,则f**=3-φ,f**最多为2,可用平面图来表示。
图1 (a)图1(b)图2(1)物系点组成的确定:在定温定压下,三组分体系的状态和组成之间的关系通常可用等边三角形坐标来表示,如图1(a),等边三角形三顶点A、B和C分别表示三个纯物质,AB,BC及CA三边分别表示A和B,B和C以及C和A所组成的二组分组成。
三角形内任一点,则表示三组分的组成。
如O点的组成:A%=Cc’,B%=Aa’,C%=Bb’。
即各物种的组成为过物系点O做各顶点对边的平行线。
又因为各物种总的百分组成为100%,三角形为等边三角形,所以又可以由其中的一条边表示各组分的百分组成,如图1中(b)所示。
当然,给出一定组成的溶液百分比,按照上述表示方法,也应该能找出对应的物系点。
(2)溶解度曲线的绘制对于具有一对共轭溶液的三液系相图,如图2,该三液系相图中A和B,A和C为完全互溶而B和C为部分互溶,曲线abc为溶解度曲线。
曲线上方为单相区,曲线下方为二相区,物系点落在二相区内,即分为二相,如X 点则分成组成为E和F的二相,而EF线称为连接线。
对于溶解度曲线的绘制,本实验是先以完全互溶的两个组分(如A和C),以一定的比例混合所组成的均相溶液,如图2上的N点,滴加入组分B,根据平衡相图的直线规则,物系点则沿着NB移动,直至溶液变混,即为L点。
再加入A,物系点由LA上升至N’点而变清。
再加入B,此时物系点又沿着N’B由N’移动至L’而再次变混,再滴加A使变清……,如此反复,最后连接L,L’,L’’……即可画出溶解度曲线。
(3)连接线的绘制由于连接线是表示在两相区内呈平衡两相的组成(或A在两相中的分配),所以可以在两相区内配制溶液,待平衡后分析每相中的任何一种组成的含量,连接在溶解度曲线上该两含量的组成点而得出。
三元相图

e
Pb Sn Sn
液相(单相 区 液相面以上的空间区域 区域; 液相 单相)区:液相面以上的空间区域; 单相 两相区 两相区:3个 个 液相面以下,二次结晶面以上的空间区域; 液相面以下,二次结晶面以上的空间区域; 区域
T
三相区 三相区:3+1个 个 二次结晶面以下, 二次结晶面以下,三元共晶 面以上——两个固相 液相 两个固相+液相 面以上 两个固相 三元共晶面以下 ——三个固相 三个固相
§9. 三元系相图简介
一、三元系相图组成的表示法 f* = 3-Φ + 1= 4 –Φ, Φmin = 1 , f*max= 3 , 三维坐标→ 三维坐标 等边三角立柱 等边三角形——组成三角形 组成三角形 等边三角形 三个立柱侧面——二元相图面 二元相图面 三个立柱侧面 组成三角形的边——二元组成 二元组成 组成三角形的边 组成三角形的顶点——纯组元 纯组元 组成三角形的顶点
Bi
三、三元水盐系相图 水+两种盐,且两盐有共同的一种离子 两种盐, 1.纯盐( 1.纯盐(B+C)与水(A)体系 纯盐 )与水( ) 纯盐: 纯盐:不形成共溶盐 不形成化合物 不形成水合盐 D点:B盐在纯水中的 点 盐在纯水中的
B F D E A(H2O)
C
溶解度; 点 盐在纯水中的溶解度; 溶解度; F点:C盐在纯水中的溶解度; 盐在纯水中的溶解度 E点:共饱和点(三相点) 点 共饱和点(三相点)
A C B T T
T
Cb = Bb’=Pa: : 代表体系P中 物的含量 物的含量; 代表体系 中A物的含量; ba’= Cc’=Pb: : 代表体系P中 物的含量 物的含量; 代表体系 中B物的含量; Aa’= cb’=Pc: : 代表体系P中 物的含量 物的含量; 代表体系 中C物的含量;
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
实验三组分相图的绘制
一实验目的
绘制苯一醋酸一水体系的互溶度相图。
为了绘制相图就需通过实验获得平衡时,各相间的组成及二相的连结线。
即先使体系达到平衡,然后把各相分离,再用化学分析法或物理方法测定达成平衡时各相的成分。
但体系达到平衡的时间,可以相差很大。
对于互溶的液体,一般平衡达到的时间很快;对于溶解度较大,但不生成化合物的水盐体系,也容易达到平衡;对于一些难溶的盐,则需要相当长的时间,如几个昼夜。
由于结晶过程往往要比溶解过程快得多,所以通常把样品置于较高的温度下,使其较多溶解,然后把它移放在温度较低的恒温槽中,令其结晶,加速达到平衡。
另外摇动、搅拌、加大相界面也能加快各相间扩散速度,加速达到平衡。
由于在不同温度时的溶解度不同,所以体系所处的温度应该保持不变。
二实验原理
水和苯的互溶度极小,而醋酸却与水和苯互溶,在水和苯组成的二相混合物中加入醋酸,能增大水和苯之间的互溶度,醋酸增多,互溶度增大。
当加入醋酸到达某一定数量时,水和苯能完全互溶。
这时原来二相组成的混合体系由浑变清。
在温度恒定的条件下,使二相体系变成均相所需要的醋酸量,决定于原来混合物中水和苯的比例。
同样,把水加到苯和醋酸组成的均相混合物中时,当水达到一定的数量,原来均相体系要分成水相和苯相的二相混合物,体系由清变浑。
使体系变成二相所加水的量,由苯和醋酸混合物的起始成分决定。
因此利用体系在相变化时的浑浊和清亮现象的出现,可以判断体系中各组分间互溶度的大小。
一般由清变到浑,肉眼较易分辨。
所以本实验采用由均相样品加人第三物质而变成二相的方法,测定二相间的相互溶解度。
当二相共存并且达到平衡时,将二相分离,测得二相的成分,然后用直线连接这二点,即得连结线。
一般用等边三角形的方法表示三元相图(图1)。
等边三角形的三个顶点各代表纯组分;三角形三条边AB、BC、CA分别代表A和B、B和C、C和A所组成的二组分的组成;而三角形内任何一点表示三组分的组成。
例如图1-1中的P点,其组成可表示如下:经P点作平行于三角形三边的直线,并交三边于a、b、c三点。
若将三边均分成100等分,则P点的A、B、C组成分别为:
A%=Cb,B%=Ac,C%=Ba
对共轭溶液的三组分体系,即三组分中二对液体AB及AC完全互溶,而另一对BC则不溶或部分互溶的相图,如图1-2所示。
图中EK1K2K3DL3L2L1F是互溶度曲线,K1L1、K2L2等是连结线。
互溶度曲线下面是两相区,上面是一相区。
图1-1等边三角形法表示三元相图图1-2共轭溶液的三元相图
三仪器药品
100 ml磨口锥形瓶,50ml磨口锥形瓶,50ml滴定管,200ml锥形瓶,2ml移液管,1ml 移液管,苯,醋酸,NaOH溶液(0.5mol/dm3),酚酞指示剂。
四实验步骤
(1)测定互溶度曲线
取三根洁净的滴定管分别装入苯、醋酸及水(装苯和醋酸的滴定管应事先干燥)。
用滴定管加5ml苯于干净的100ml磨口锥形瓶内,再用滴定管滴入1ml醋酸。
摇匀成均相后,由滴定管慢慢滴入蒸馏水,边滴边摇动,并仔细观察有无浑浊现象,直到有浑浊的“油珠”出现,记下这时所用水的体积。
再加入2ml醋酸,体系又成均相。
继续用水滴定、使体系再由清变浑。
分别记下这时体系中苯、醋酸及水所加入的总毫升数。
而后依次再加入3、3、5、5、5ml醋酸。
同法分别用水进行滴定,并记录体系中各组分的含量。
测定后,在体系中再加人10ml苯,使体系分成二相,塞好塞子,留给下面测定连结线用。
另取一干净的100ml磨口锥形瓶,先用滴定管加入1ml苯及5ml醋酸,摇成均相后,用水滴定,使其成两相。
以后再依次加人1、2、5ml的醋酸,用水滴定,方法同前。
滴完后,加苯15ml,使体系分成两相。
塞好瓶塞留待测连结线用。
再取一个100ml磨口锥形瓶,用滴定管加入0.5ml苯及8ml醋酸,摇匀后,用水滴定,使其由清变浑,记下所用水的体积数。
然后,再依次加入2、5ml醋酸,继续用水滴至终点。
在滴定时要一滴一滴慢慢地加,特别是醋酸含量很少时,更应特别注意。
在醋酸含量较多时,开始时可滴得快一些,接近终点要慢慢地滴定,因为这时溶液接近饱和,溶解平衡需要较长的时间,因此更要多加振荡。
由于分散的“油珠”颗粒能散射光线,所以只要体系出现浑浊,而在2—3分钟内仍不消失,即可认为已到终点。
此实验由于有水参加,故所用装苯和醋酸的容器都必须干燥。
(2)连结线的测定
将由上述所得的二个溶液中各个组分的含量准确地记录下来。
将瓶塞塞紧后,用力摇动,摇动时勿使瓶内液体流出。
然后每隔5分钟摇一次,约半小时后,分别倒入二个干净的分液漏斗内。
待二液分层后,分别将各层液体放入干净的磨口锥形瓶中,用2ml移液管取上层溶液2ml置于已称好的25ml磨口锥形瓶内,准确称其质量,然后用水洗入200ml锥形瓶中,加少许酚酞,用NaOH标准溶液滴定其中醋酸的含量。
同样用1ml移液管取下层液体1ml,称量,以酚酞为指示剂,用NaOH滴定醋酸的含量。
在不用分液漏斗分离,直接采用移液管取下层液体时,可采用洗耳球吹气法。
即在轻轻吹气的同时使移液管插入下层液体,这样可防止上层液体进入移液管中。
五数据处理
(1)互溶度曲线的绘制
根据各次所用的苯、醋酸和水的体积以及在实验所处的温度下水、苯、醋酸的密度,求算每次体系出现复相时这三种组分的质量及体系的总质量。
计算三种组分所占的质量百分数。
按下表列出各次所得的数据:
根据上表数据,在三角坐标纸上,画出各次的组成点。
然后用曲线板,将这些点连结成一光滑的曲线。
标明由曲线分割开的各相区的意义
(2)连结线的绘制
a.计算二瓶中苯、醋酸和水的质量百分数,画于上面的三角相图内。
b.由所取各相的质量及由NaOH滴定所得的数据,求出醋酸在各相内的质量百分数。
c.将醋酸的质量百分数画在三角相图的互溶度曲线上。
水层内的醋酸含量画于含水成分多
的一边,苯层内的醋酸含量画于含苯成分多的另一边。
联结由c所得的二个成平衡的液层的组成点,即为连结线。
该连结线应通过由a所得的体系的总组成点。
