片剂中抗坏血酸(Vc)含量的测定(直接碘量法)
直接碘量法测定药片中维生素C的含量

直接碘量法测定药片中维生素C的含量11化学曾凯平11218022一实验目的1.掌握碘标准溶液的配制注意事项。
2. 通过维生素C的测定了解直接碘量法的过程。
二实验原理维生素C又叫抗坏血酸,分子式C6H4O6。
由于分子中的烯二醇基具有还原性,能被I2定量地氧化成二酮基,其反应式为:碱性条件下可使反应向右进行完全,但因维生素C还原性很强,在碱性溶液中尤其易被空气氧化,在酸性介质中较为稳定,故反应应在稀酸(如稀乙酸、稀硫酸或偏磷酸)溶液中进行,并在样品溶于稀酸后,立即用碘标准溶液进行滴定。
由于碘的挥发性和腐蚀性,不宜在分析天平上直接称取,需采用间接配制法;通常用基准As2O3对I2溶液进行标定。
As2O3不溶于水,溶于NaOH:As2O3+6NaOH═2Na3AsO3+3H2O由于滴定不能在强碱性溶液中进行,需加H2SO4中和过量的NaOH,并加入NaHCO3使溶液的pH=8。
I2与亚砷酸之间的反应为:AsO32-+I2+H2O═AsO43-+2I-+2H+三器皿和试剂酸式滴定管;NaHCO3、KI、I2(以上为AR),As2O3(于105 C 干燥至恒重),6mol·L-1NaOH,0.5mol·L-1H2SO4,10%HAc,1%淀粉溶液,维生素C片剂。
四实验步骤1. 0.1mol·L-1I2标准溶液的配制称取10.8gKI,溶于10mL蒸馏水中,再用表面皿称取I2约6.5g,溶于上述KI溶液,加1滴浓盐酸,加水稀释至300mL,摇匀,用玻璃漏斗过滤,贮存于棕色试剂瓶中并置于暗处。
2.0.1mol·L-1I2标准溶液的标定准确称取基准As2O30.15g,加6mol·L-1NaOH溶液10mL,微热使溶解,加水20mL,加甲基橙指示剂1滴,加0.5mol·L-1H2SO4试液至溶液由黄色变为粉红,再加NaHCO32g、水30mL、淀粉指示剂2mL,用碘标准溶液滴定至蓝色,半分钟内不褪色,计算I2的浓度。
抗坏血酸药品中维生素C含量的测定(碘量法)

抗坏血酸药品中维生素C 含量的测定一、实验目的1.掌握碘标准溶液的配制注意事项;2.通过维生素C 的测定了解直接碘量法和间接碘量法的过程;3.掌握碘量法测定抗坏血酸药品中维生素C 含量的原理和方法。
二、实验用品 1.仪器全自动分析天平;台秤;碘量瓶;玻璃棒;洗瓶;试剂瓶;烧杯;酸式滴定管;量筒;胶头滴管;容量瓶;移液管;洗耳球。
2.试剂分析纯O H O S 23225Na ⋅,分析纯2I ;7221-r mol 017.0O C K L ⋅标准溶液;)s (KI 、KI 溶液100-1L g ⋅,使用前配制;淀粉指示剂1-g 5L ⋅;)(s a 32CO N ;l HC 溶液1-mol 6L ⋅;败坏血酸片。
三、实验原理抗坏血酸又名维生素C ,分子式686O H C 。
由于分子中的烯二醇基具有还原性,能被2I 定量地氧化成二酮基,其反应式为:碱性条件下可使反应向右进行完全,但因维生素C 还原性很强,在碱性溶液中尤其易被空气氧化,在酸性介质中较为稳定,故反应应在稀酸(如稀乙酸、稀硫酸或偏磷酸)溶液中进行,并在样品溶于稀酸后,立即用碘标准溶液进行滴定。
根据滴定消耗的2I 标准溶液的体积,便可计算出抗坏血酸药品中维生素C 的含量。
计算公式:%100m %100m m 68622⨯=⨯=药品药品维生素O H C I I C M V C W2I 标准溶液的配制和标定:由于通常使用的市售2I 试剂纯度不高,故需先配成近似浓度,然后在进行标定。
2I 微溶于水而易溶于KI 溶液中,但在稀的KI 溶液中溶解得很慢,故配制2I 溶液时应先在较浓的KI 溶液中进行,待溶解完全后再稀释到所需浓度。
2I 溶液可以用32s O A 为基准物对I 2溶液进行标定,但32s O A (俗称砒霜)有剧毒,故用322a O S N 标准溶液进行标定。
322a O S N 标准溶液的配制和标定:固体试剂O H O S N 23225a ⋅通常含有一些杂质,且易风化和潮解,因此,322a O S N 标准溶液采用标定法配制。
碘量法测维生素C含量

I2 溶液的标定用Na2S2O3标准溶液: 基本反应式:2S2O32-+I2=S4O62-+2I-
I2溶液(0.05mol/L): Na2S2O3标准溶液(0.01mol/L) 淀粉溶液(2g/L) HAc(1+1) 固体Vc样品(维生素片剂) 重铬酸钾(A.R) KI溶液(约200g/L)
维生素C含量的测定:
Na2S2O3标准溶液浓度:
实验序号 记录项目 M药片质量/g V消耗I2体积/ml ω维C含量/% ω维C平均含量/% 1 2
I2标准溶液的浓度:
3
1. 配制I2标准溶液时,为什么要加过量KI?可否 将称得的I2和KI一起加水至一定体积? 2 .溶解样品时,为什么要用新煮沸并冷却的蒸馏 水? 3.加醋酸的目的是什么?
碱性条件下可使反应向右进行完全,但因维生素 C还原性很强,在碱性溶液中尤其易被空气氧化, 在酸性介质中较为稳定,但是在强酸性溶液中I也易被氧化。 故反应应在稀酸(pH为3—4)(如稀乙酸、稀 硫酸或偏磷酸)溶液中进行,并在样品溶于稀酸 后,立即用碘标准溶液进行滴定。
由于碘的挥发性和腐蚀性,不宜在分析天平上直 接称取,需采用间接配制法;用Na2S2O3标准溶 液标定I2 溶液。 标定Na2S2O3溶液: 6I-+Cr2O72-+14H+=2Cr3++3I2+7H2O 2S2O32-+I2=S4O62-+2I- n(K2C2O7): 6n(Na2S2O3)=1:6
I2微溶于水而易溶于KI溶液,但在稀的KI溶液中溶 解得很慢,所以配制I2溶液时不能过早加水稀释,应 先将I2和KI混合,用少量水充分研磨,溶解完全后 再加水稀释。 I与KI间存在如下平衡:I2+I- =I3- 游离I2容易挥发损失,这是影响碘溶液稳定性的原因 之一。因此溶液中应维持适当过量的I-离子 ,以减 少I2的挥发。空气能氧化I-离子,引起I2浓度增加: 4 I-+O2+4H+ =2I2+2H2O 此氧化作用缓慢,但能为光,热,及酸的作用而加 速,因此I2溶液应处于棕色瓶中置冷暗处保存。I2能 缓慢腐蚀橡胶和其他有机物,所以I应避免与这类物 质接触。
实训x:直接碘量法测定维生素C片的含量

实训x :直接碘量法测定维生素C 片的含量一、目的要求:通过实训掌握直接碘量法测定Vc 片含量的原理及其操作。
熟悉片剂通过滴定分析测定含量时的处理方法。
二、原理:维生素C(C 6H 8O 6),分子结构中的烯二醇基具有还原性,能被I 2定量地氧化成二酮基,抗坏血酸分子中的二烯醇基被I 2完全氧化后,则I 2与淀粉指示剂作用而使溶液变蓝,因此当滴定到溶液出现蓝色时即为终点。
维生素C 在空气中极易被氧化,尤其在碱性介质中更甚,故该滴定反应在稀HAc 中进行,以减少维生素C 的副反应。
该反应产物HI 为酸性,醋酸酸性条件下不利于反应向右进行,但由于维生素C 的还原性很强,即使在弱酸性条件下,上述反应也进行得相当完全。
三、操作步骤:直接碘量法:取本品10片,精密称定,研细,精密称取适量(约相当于维生素C0.2g ),置100ml 锥形瓶中,加新沸过的冷水100ml 与稀醋酸10ml 的混合液适量,振摇使维生素C溶解并稀释至刻度,迅速滤过,精密量取续滤液50ml ,加淀粉指示液1ml ,立即用碘滴定液(0.05mol ·L -1)滴定,至溶液显蓝色并持续30秒钟不褪。
每1ml 碘 滴定液(0.05mol ·L -1)相当于8.806mg 的C 6H 8C 6。
平行测定3份,计算含量。
四、计算:维生素C 含量以标示量来计算,按下式计算: F (I 2)×V (I 2)×T (C 6H 8O 6)×W 平%(C 6H 8O 6)=—————————————————×100% m ×规格F-----滴定液浓度有效因数V-----供试品消耗碘滴定液的体积 T-----滴定度W 平-----平均片重g m------供试品取用量g 五、注意点:1、在稀醋酸酸性介质中,维生素C 受空气中氧的氧化速度减慢,但供试品溶于稀醋酸后仍应立即进行滴定。
2、溶剂使用新沸过的冷水以减少水中溶解氧对测定的影响。
维生素C的含量测定(直接碘量法)
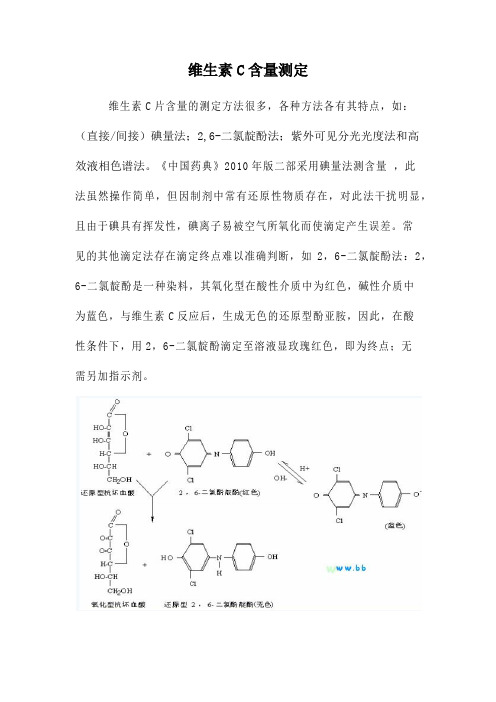
维生素C含量测定维生素C片含量的测定方法很多,各种方法各有其特点,如:(直接/间接)碘量法;2,6-二氯靛酚法;紫外可见分光光度法和高效液相色谱法。
《中国药典》2010年版二部采用碘量法测含量,此法虽然操作简单,但因制剂中常有还原性物质存在,对此法干扰明显,且由于碘具有挥发性,碘离子易被空气所氧化而使滴定产生误差。
常见的其他滴定法存在滴定终点难以准确判断,如2,6-二氯靛酚法:2,6-二氯靛酚是一种染料,其氧化型在酸性介质中为红色,碱性介质中为蓝色,与维生素C反应后,生成无色的还原型酚亚胺,因此,在酸性条件下,用2,6-二氯靛酚滴定至溶液显玫瑰红色,即为终点;无需另加指示剂。
分光光度法运用维生素C的旋光性能进行含量测定,但操作费时,而高效液相色谱法是目前发展较为迅速的一种方法,灵敏度高,选择性好,是一个准确高效的测定维生素C含量的方法。
我们主要介绍的是直接碘量法。
直接碘量法一.实验原理维生素C是人体重要的维生素之一,它影响胶元蛋白的形成,参与人体多种氧化-还原反应,并且有解毒作用。
人体不能自身制造维生素C,所以人体必须不断地从食物中摄入维生素C,通常还需储藏能维持一个月左右的维生素C。
缺乏时会产生坏血病,故又称抗坏血酸。
维生素C属水溶性维生素,分子式C6H8O6。
分子中的烯二醇基具有还原性,能被I2定量地氧化成二酮基,因而可用I2标准溶液直接测定。
简写为:C6H8O6+I2= C6H6O6+2HI使用淀粉作为指示剂,用直接碘量法可测定药片、注射液、饮料、蔬菜、水果中维生素C的含量。
由于维生素C的还原性很强,较容易被溶液和空气中的氧氧化,在碱性介质中这种氧化作用更强,因此滴定宜在酸性介质中进行,以减少副反应的发生。
考虑到I - 在强酸性中也易被氧化,故一般选在pH为3~4的弱酸性溶液中进行滴定。
由于碘具有挥发性,碘离子易被空气所氧化而使滴定产生误差;又由于碘的挥发性和腐蚀性,使碘标准滴定溶液的配制及标定比较麻烦。
维生素C药片中Vc含量的测定

维生素C 药片中含量的测定(碘量法)一、实验目的1、 掌握直接碘量法测定的原理及其操作。
2、 掌握碘标准溶液的配制及标定。
3、 掌握维生素C 的测定方法。
二、实验原理 (一)碘量法碘量法是以I 2的氧化性和I -的还原性为基础的滴定分析方法。
在一定条件下,用碘离子来还原,定量的析出碘单质,然后用2S 2O 3 标准溶液来滴定析出的I 2。
这种方法叫做间接碘量法。
本实验采用间接碘量法测碘的浓度。
以淀粉为指示剂,2S 2O 3 标准溶液来滴定析出的I 2,以蓝色消失为终点,即可算出碘的浓度。
维生素C 又称抗坏血酸,分子式C 6H 8O 6。
具有还原性,可被I 2定量氧化,因而可用I 2标准溶液直接测定。
其滴定反应式:(二)碘溶液的配制与标定OHOOHO CH OH CH 2OH +I 2OOOO C H OH CH 2OH +2HIHOAcI 2微溶于水而易溶于溶液,但在稀的溶液中溶解得很慢,所以配制I 2溶液时不能过早加水稀释,应先将I 2和混合,用少量水充分研磨,溶解完全后再加水稀释。
I 2 溶液的标定可以用2O 3或2S 2O 3标定,因为2O 3是剧毒物质,我们用2S 2O 3来标定。
(三)硫代硫酸钠溶液的配制与标定2S 2O 3一般含有少量杂质,在9-10间稳定,所以在2S 2O 3溶液中加入少量的23,2S 2O 3见光易分解可用棕色瓶储于暗处,经一周后,用K 2C 2O 7做基准物间接碘量法标定2S 2O 3溶液的浓度。
根据K 2C 2O 7标准溶液的物质的量浓度和滴定消耗的体积,就可计算出溶液中2S 2O 3的浓度。
其过程为:K 2C 2O 7与先反应析出I 2:析出的I 2再用标准的2S 2O 3溶液滴定:从而求得2S 2O 3的浓度。
这个标定2S 2O 3的方法为间接碘量法。
碘量法的基本反应式:2S 2O 32-+I 24O 62-+2I - 标定2S 2O 3溶液时有:6I -+2O 72-+14H +=23++3I 2+7H 2O 2S 2O 32-+I 24O 62-+2I -2S 2O 3标定时有(K 2C 2O 7): n(2S 2O 3)=1:6三、实验药品及仪器 实验药品和试剂:I 2分析纯 溶液100g ·1 2S 2O 3·5H 2O 溶液 0.01701K 2C 2O 7溶液 淀粉指示剂5 g ·1 23 固体 溶液 6 1 冰醋酸 维生素C 药片 主要仪器:分析天平、天平、量筒、烧杯、酸式碱式滴定管、表面皿、容量瓶(250)、锥形瓶(250)、碘量瓶(250)、移液管(25)、洗瓶等常规分析仪器 四、实验步骤(一)、2S 2O 3 溶液的配制及标定1、配制0.10 2S 2O 3溶液500 称取132S 2O 3·5H 2O ,溶于500新煮沸的蒸馏水中,加入0.123,保存于棕色瓶中,放置一周后进行标定。
vc片中维生素c的测定

VC片中维生素C的测定1. 引言维生素C,也称为抗坏血酸,是一种重要的水溶性维生素。
它在人体内具有许多重要的功能,包括抗氧化、参与胶原蛋白合成和免疫调节等。
准确测定VC片中维生素C的含量对于保证产品质量和满足消费者需求至关重要。
本文将介绍一种常用的方法——碘滴定法来测定VC片中维生素C的含量。
该方法基于VC与碘溶液反应生成碘化物的化学反应,通过测定反应前后溶液中未反应的碘量来计算VC含量。
2. 实验步骤2.1 材料准备•VC片样品•碘标准溶液•淀粉指示剂•硫酸•蒸馏水•称量瓶、容量瓶、烧杯等实验器具2.2 碘滴定法测定步骤步骤1:制备标准曲线1.准备一系列不同浓度的VC标准溶液。
2.取一定体积的VC标准溶液,加入烧杯中。
3.加入适量的碘标准溶液,使反应完全。
4.加入淀粉指示剂,继续滴定至溶液呈现蓝黑色。
5.记录滴定所需的碘标准溶液体积。
步骤2:测定样品1.取一定质量的VC片样品,加入称量瓶中。
2.加入适量蒸馏水,使VC片完全溶解。
3.加入硫酸,使样品酸化。
4.将样品转移至容量瓶中,并用蒸馏水稀释到刻度线处。
5.取一定体积的稀释后的样品溶液,加入烧杯中。
6.加入适量的碘标准溶液,使反应完全。
7.加入淀粉指示剂,继续滴定至溶液呈现蓝黑色。
8.记录滴定所需的碘标准溶液体积。
3. 数据处理与结果分析3.1 标准曲线绘制根据步骤2中制备的标准曲线数据(VC标准溶液浓度与滴定所需的碘标准溶液体积),绘制标准曲线图。
横坐标为VC标准溶液浓度,纵坐标为滴定所需的碘标准溶液体积。
3.2 样品测定结果计算根据步骤2中测定样品时记录的滴定所需的碘标准溶液体积,结合标准曲线,计算出样品中维生素C的含量。
3.3 结果分析将样品测定结果与产品规格要求进行比较,评估样品是否符合要求。
如果样品中维生素C的含量低于规定范围,则可能需要调整生产工艺或增加添加量。
4. 实验注意事项1.实验过程中应注意安全操作,避免接触皮肤和吸入有害气体。
直接碘量法测定维生素c含量

直接碘量法测定维生素c含量
维生素C,也被称为抗坏血酸,是一种水溶性维生素。
它在许多生物体内起着重要的生理作用,并且对人体有益。
维生素C含量测定是基于一种叫做碘量法的化学方法。
该方法利用碘酸钾溶液与维生素C反应的化学性质,通过了解反应后剩余的碘酸钾的含量来测定维生素C含量。
碘量法测定维生素C的过程如下:
准备样品:将要测定的样品加入到3%的浓磷酸中,并将其加热到约80℃,然后再冷却。
制备碘酸钾溶液:将20克的碘酸钾加入到1000毫升的蒸馏水中,并充分搅拌,以制备出0.1N的碘酸钾溶液。
测定过程:将取出的样品加入到定容瓶中,加入足够的蒸馏水,直至瓶子充满为止。
然后取出1毫升的样品溶液,并将其加入到滴定瓶中。
加入几滴淀粉溶液。
此时,溶液会变成淡蓝色。
准备滴定剂:将制备好的碘酸钾溶液滴加到另一个滴定瓶中,并加入适量的酒精。
通过滴加,将滴定剂加入到样品溶液中,直至溶液变成深蓝色。
读取数据:记录滴定剂滴入样品溶液的次数,并且根据已知的滴定剂浓度计算出维生素C的含量。
利用碘量法可以准确地测定含有维生素C的食物以及药品的维生素C含量。
然而,由于该测量方法需要使用化学试剂和复杂的实验过程,所以在实践中不太实用。
为了更加方便测量维生素C的含量,也出现了其他测量方法,例如高效液相色谱法和光谱法。
无论使用哪种方法测量维生素C的含量,都可以帮助人们了解他们摄入的营养成分,以及制定更加健康的膳食计划。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
西北大学基础化学实验
二、实验步骤
1. Na2S2O3溶液的标定:移取25.00 mL K2Cr2O7于锥形瓶中, 加入5 mL (1+1) HCl、5 mL 200g ·L-1 KI,盖上表面皿于暗 处反应5分钟后,用水冲洗表面皿,加入60~80 mL H2O稀 释。立即用Na2S2O3滴定至黄绿色,加入2 mL淀粉溶液, 继续用Na2S2O3滴定至亮绿色即为终点。(平行三份) 2. I2溶液的标定:移取25.00 mL Na2S2O3于锥形瓶中,加入 50 mL H2O、2 mL淀粉溶液,用I2溶液滴定至稳定的蓝色 即为终点。(平行三份) 3. 片剂中Vc含量的测定:减量法准确称取Vc 粉末0.2~0.3 g 于锥形瓶中,用100 mL H2O、10 mL HAc溶解后,加入2 mL淀粉溶液,用I2溶液滴定至稳定的蓝色即为终点。(平 行两份)
西北大学基础化学实验
西北大学基础化学实验
三、结果表示
用片剂中Vc的质量百分含量(Vc%)表示,保留四位 有效数字。 计算公式:
mK 2Cr2O7 × 3 × 2 × 1000 M K 2Cr2O7 × 4 × V Na 2S2O3
c Na 2S2O3 =
c I2
c Na 2S2O3 × 25.00 = 2 ×V I2
c I 2 × VI 2 × M Vc 1000 × ms × 100%
西北大学基础化学实验
wVcБайду номын сангаас=
四、有关常数
M K 2Cr2O 7 = 294.18 g·mol-1
MVc = 176.12 g·mol-1
西北大学基础化学实验
五、注意事项
1. 终点变色都很敏锐,小心滴过量。 2. 用K2Cr2O7标定Na2S2O3时,用H2O冲洗 表面皿且用H2O稀释后,慢摇快滴至黄绿 色。 3. 称量Vc时,注意勿将Vc从称量瓶口撒 出,慢盖瓶盖。
片剂中抗坏血酸(Vc)含量的测定 含量的测定 片剂中抗坏血酸 (直接碘量法 直接碘量法) 直接碘量法
西北大学基础化学实验
一、主要试剂 二、实验步骤 三、结果表示 四、有关常数 五、注意事项
西北大学基础化学实验
一、主要试剂
1. 0.05 mol·L-1 I2溶液:3.3 g I2 + 5 g KI研磨后, 用H2O溶解→ 250 mL。 2. 0.1 mol·L-1 Na2S2O3溶液:7.5 g Na2S2O3·5H2O溶于水 →300 mL。 3. K2Cr2O7标准溶液:减量法准确称取K2CrO7 0.45~0.55 g,溶于水后转入100 mL容量瓶中 定容。
