锂亚硫酰氯电池电极反应式
2020届人教版高考化学专题复习:锂系电池

2 高考复习专题——锂系电池学习目标1. 识别锂电池和锂离子电池的工作原理。
2. 根据试题中提供的信息书写电极反应。
知识贮备1. 原电池正极得电子,发生还原反应;阳离子移向正极;电子流入正极;电流从正极流出。
负极失电子,发生氧化反应;阴离子移向负极;电子从负极流出;电流流入负极。
2. 锂电池是一种一次电池。
锂电池是一类由锂金属或锂合金为负极材料、一般是使用二氧化锰为正极材料使用非水电解质溶液的电池。
电池放电反应方程式为:Li+MnO 2=LiMnO 2。
常见锂电池:锂-氟化石墨(正极)电池 (n Li +(CF )n = nLiF + nC ) 锂-二氧化锰(正极)电池锂-亚硫酰氯(正极)电池 锂-硫化铁(正极)电池 锂-氧化铜(正极)电池 上述均为锂作负极,非水系有机电解液。
3. 锂离子电池:是一种二次电池(充电电池),它主要依靠锂离子在正极和负极之间移动来工作。
在充放电过程中,Li + 在两个电极之间往返嵌入和脱嵌:充电时,Li +从正极脱嵌,经过电解质嵌入负极,负极处于富锂状态;放电时则相反。
它是把锂离子嵌入碳(石油焦炭和石墨)中形成负极。
正极材料常用 LixCoO 2 , (也用 LiCoO 2 Li 2Mn 2O 4 LiFePO 4 Li x NiO 2 Li 2FePO 4F ,和 Li x MnO 4 ),电解液使用非水液态有机电解质【LiPF 6+二乙烯碳酸酯(EC )+二甲基碳酸酯(DMC )】。
锂离子二次电池充、放电时的反应式为LiCoO 2+C=Li 1-x CoO 2+Li x C【学生活动一】1.写出锂电池放电反应方程式为:Li+MnO 2=LiMnO 2 的电极反应2.写出锂离子电池锂离子二次电池充、放电时的反应式为 LiCoO 2+C=Li 1-x CoO 2+Li x C 的充电和放电时的电极反应小结书写锂电池和锂离子电池的电极反应方法:锂电池(如 Li-FeS 2)通常已知总反应负极反应:4Li –4 e - =4Li +正极反应:FeS +4e -=Fe +2S 2- 锂离子电池总反应 Li (1-x)MO 2 + Li X C nn C + LiMO 2 正 极 材 料 :LiMO 2 ( M 为 Co Ni Mn)LiM 2O 4 ( M 为 Co Ni Mn)LiMPO 4 ( M 为 Fe )负极材料:石墨(能吸附锂原子)正极反应:Li X C n—x e-= x Li+ + n C负极反应:Li(1-x)MO2+ x Li+ + x e-= LiMO22 2 2 2 2 检测:1. 有一种新型的锂电池,其制作是利用了金属锂和石墨作电极,其电解质溶液是四氯合铝酸锂(LiAlCl 4)溶解在二氯亚硫酰(其化学式是 SOCl 2)中形成的,原电池的电极总反应式是:8Li +3SOCl 2=6LiCl +Li 2SO 3+2S 下列关于这种新型电池的说法中错误的是() A. 电池工作过程中,SOCl 2 被还原为Li 2SO 3 B. 锂作为电池的负极,石墨作电池的正极C. 该电池内环境应该是无水环境,否则影响电池的寿命D. 电池工作时,锂提供的电子的物质的量与析出硫的物质的量之比是 4∶12. Li-FeS 2 电池是目前电池中综合性能最好的一种电池,其结构如图所示。
高中化学 2020高考帮·化学-专题十四 原电池

A.在外电路中,电子由铜电极流向银电极
B.正极反应:Ag++e-
Ag
C.实验过程中取出盐桥,原电池仍继续工作
D.将铜片浸入AgNO3溶液中发生的化学反应与该原电池反应相同
题十四 原 电池
解析 该原电池中铜作负极,银作正极,在外电路中,电子由铜电极流向银电极,A正确;
[续表]
2C4H10+26O2-52e8CO2+10H2O
示例3 [电极反应式的书写][高考组合题]请回答下列问题。 (1)[2015海南,15(4),1分]如图所示原电池正极的反应式为
题十四 原 电池
。
(2)[2013北京,26(4),4分]
通过NOx传感器可监测NOx的含量,其工作原理示意图如图所示:
题十四 原 电池
一看有无外接电源,若有外接电源则为电解池,若无外接电源则可能为原电池;二看电极是
否用导线相连,并与电解质形成闭合电路;三看电极能否发生氧化反应或还原反应。
2.原电池的工作原理 (以Zn-Cu原电池为例)
题十四 原 电池
甲(双液电池)
乙(单液电池)
(1)原理分析
题十四 原 电池
电极名称 电极材料
普通锌锰电池
装置
负极
锌筒(作外壳)
碱性锌锰电池 锌粉(在电池内部)
电解质 及pH
电极 反应
NH4Cl糊 pH<7
题十四 原 电池
续表
湿KOH pH>7
负极:Zn+2OH--2e- Zn(OH)2 正极: 2MnO2+2H2O+2e2MnOOH+2OH总反应:Zn + 2MnO2+2H2O 2MnOOH+Zn(OH)2
常见化学电源及电极反应式的书写

常见化学电源及电极反应式的书写一、常见化学电源:(大体可分为三类)1、燃料电池:(1)氢氧燃料电池:2H2+O2=2H2O当电解质溶液呈酸性时;负极:2H2-4e-=4H+正极:O2+4e-+4H+=2H2O当电解质溶液呈碱性时;电解质溶液为KOH溶液,负极:2H2-4e-+4OH-=4H2O 正极:O2+4e-+2H2O=4OH-(2)甲烷燃料电池:用金属铂作电极,用KOH溶液作电解质溶液。
负极:CH4+ 10 OH--8e-==CO3 2- +7H2O 正极:2O2+ 4H2O +8e- == 8OH-总反应式为:CH4+ 2O2+2KOH==K2CO3+ 3H2O用酸液作电解质溶液负极:CH4 + 2H2O - 8e- = CO2 + 8H+ 正极:2O2 + 8H+ + 8e- = 4H2O总反应:CH4 + 2O2 = CO2 + 2H2O(3)甲醇燃料电池:强碱作为电解质溶液负极:2CH4O + 16OH--12e-==2CO3 2- +12H2O 正极:3O2+ 6H2O +12e- == 12OH-总反应式为:2CH4O + 3O2+4OH-==2CO3 2- + 6H2O(4)熔融盐燃料电池:该电池用Li2CO3和的Na2CO3熔融盐混合物作电解质,CO为阳极燃气,空气与CO2的混合气为阴极助燃气,负极:2CO+2CO3 2- -4e-==4CO2正极:O2 + 2CO2+4e- ==2CO3 2-总反应式为:2CO +O2==2CO2(5)固体氧化物燃料电池:固体氧化锆—氧化钇为电解质,这种固体电解质在高温下允许O 2-在其间通过。
负极:2H2+ 2O2--4e- = 2H2O 正极:O2+4e- = 2O 2-总反应式为:2H2 + O2= 2H2O2、蓄电池:(1)铅蓄电池: Pb和PbO2作电极材料,H2SO4作电解质溶液。
负极:Pb+SO4 2- -2e- = PbSO4正极:PbO2+4H++ SO4 2- +2e- = PbSO4+2H2O 总反应式为:Pb+ PbO2+2H2SO4==2PbSO4+2H2O(2)碱性镍—镉电池该电池以Cd和NiO(OH) 作电极材料,NaOH作电解质溶液。
原电池(第2课时 化学电源)(课件)高二化学(人教版2019选择性必修1)

燃料电池
(2)甲烷燃料电池
用导线连接的两个铂电极插入电解质溶液中,然后向两极分别 通入CH4和O2,该电池的反应式:
② KOH溶液: 负极:CH4+10OH--8e-==CO32-+7H2O 正极:2O2+4H2O+8e-==8OH- 总反应式:CH4+2O2+2OH-==CO32-+3H2O
燃料电池
一次电池
4.锂亚硫酰氯(Li/SOCl2)电池
Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是 LiAlCl4-SOCl2。电池的总反应可表示为8Li+3SOCl2===6LiCl+Li2SO3+2S。 (1)负极材料为__锂__,电极反应为__8_L__i-__8_e_-_=_=_=__8_L_i+_。 (2)正极的电极反应为__3_S_O__C_l_2_+__8_e-__=_=_=_2_S_+__S_O__23-__+__6_C_l_-。
【课堂练习】
3、锂电池是一代新型高能电池,它以质量轻、能量高而受 到了普遍重视,目前已研制成功多种锂电池,某种锂电池的
总反应为Li + MnO2=LiMnO2,下列说法正确的是( B )
A、Li是正极,电极反应为 Li-e- =Li+ B、Li是负极,电极反应为 Li-e- =Li+ C、Li是负极,电极反应为 MnO2 +e-=MnO2 – D、Li是负极,电极反应为 Li-2e- = Li2+
一次电池
1) 锌-锰干电池 (酸性电解质溶液) 正极:
2MnO2 + 2NH4+ + 2e- = 2MnO(OH) + 2NH3↑
负极: Zn – 2e- = Zn2+
高考电化学专题复习知识点总结完美版
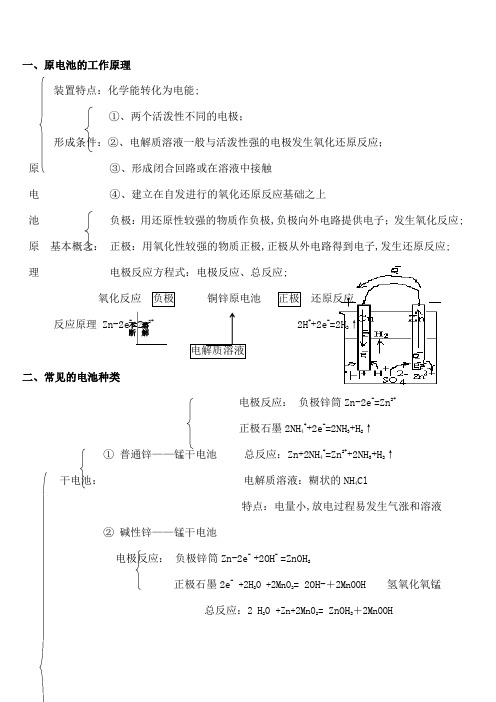
一、原电池的工作原理装置特点:化学能转化为电能;①、两个活泼性不同的电极;形成条件:②、电解质溶液一般与活泼性强的电极发生氧化还原反应;原③、形成闭合回路或在溶液中接触电④、建立在自发进行的氧化还原反应基础之上池负极:用还原性较强的物质作负极,负极向外电路提供电子;发生氧化反应; 原基本概念:正极:用氧化性较强的物质正极,正极从外电路得到电子,发生还原反应;理电极反应方程式:电极反应、总反应;氧化反应负极铜锌原电池正极还原反应反应原理 Zn-2e-=Zn2+ 2H++2e-=2H2↑电解质溶液二、常见的电池种类电极反应:负极锌筒Zn-2e-=Zn2+正极石墨2NH4++2e-=2NH3+H2↑①普通锌——锰干电池总反应:Zn+2NH4+=Zn2++2NH3+H2↑干电池:电解质溶液:糊状的NH4Cl特点:电量小,放电过程易发生气涨和溶液②碱性锌——锰干电池电极反应:负极锌筒Zn-2e- +2OH- =ZnOH2正极石墨2e-+2H2O +2MnO2= 2OH-+2MnOOH 氢氧化氧锰总反应:2 H2O+Zn+2MnO2= ZnOH2+2MnOOH溶解不断电极:负极由锌改锌粉反应面积增大,放电电流增加;使用寿命提高 电解液:由中性变为碱性离子导电性好;正极PbO 2 PbO 2+SO 42-+4H ++2e -=PbSO 4+2H 2O 负极Pb Pb+SO 42--2e -=PbSO 4总反应:PbO 2+Pb+2H SO 4 2PbSO 4+2H 2O电解液:cm 3~cm 3的H 2SO 4 溶液特点:电压稳定, 废弃电池污染环境 Ⅰ、镍——镉Ni ——Cd 可充电电池;其它 负极材料:Cd ;正极材料:涂有NiO 2,电解质:KOH 溶液NiO 2+Cd+2H 2O NiOH 2+ CdOH 2Ⅱ、银锌蓄电池正极壳填充Ag 2O 和石墨,负极盖填充锌汞合金,电解质溶液KOH;反应式为: 2Ag+ZnOH 2 ﹦ Zn+Ag 2O+H 2锂亚硫酰氯电池Li-SOCl 2:8Li+3SOCl 2 = 6LiCl+Li 2SO 3+2S锂电池 用途:质轻、高能比能量高、高工作效率、高稳定电压、工作温度宽、高使用寿命,广泛应用于军事和航空领域; ①、燃料电池与普通电池的区别不是把还原剂、氧化剂物质全部贮藏在电池内,而是工作时不断从外界输入,同时燃 料 电极反应产物不断排出电池;放电 充电放电放电` 充电 放电`充电放电`电池②、原料:除氢气和氧气外,也可以是CH4、煤气、燃料、空气、氯气等氧化剂;③、氢氧燃料电池:总反应:O2+2H2=2H2O 特点:转化率高,持续使用,无污染;2.氢氧燃料电池反应汇总:介质电池反应2H2 +O2= 2H2O酸性负极 2H2- 4e- = 4H+正极O2 + 4H+ + 4e-= 4H2O中性负极 2H2- 4e- = 4H+正极O2 + 2H2O + 4e-= 4OH-碱性负极2H2 +4OH-- 4e- = 4H2O正极O2 + 2H2O + 4e-= 4OH-3.固体氢氧燃料电池:固体电解质介质电池反应: 2H2 +O2= 2H2O负极2H2 - 4e- +2O2-= 2H2O正极O2+ 4e-= 2O2-负极 2H2- 4e- = 4H+正极O2 + 4H+ + 4e-= 2H2O4.甲烷新型燃料电池以两根金属铂片插入KOH溶液中作电极,又在两极上分别通入甲烷和氧气;电极反应为:负极:CH4+ 10OH --8e-= CO32- + 7H2O正极:2O2+ 4H2O +8e-= 8OH -电池总反应:CH 4+ 2O 2 + 2KOH = K 2CO 3 + 3 H 2O分析溶液的pH 变化;C 4H 10、空气燃料电池、电解质为熔融K 2CO 3, 用稀土金属材料作电极具有催化作用负极:2C 4H 10 -52e- + 26CO32-- = 34 CO 2+ 10H 2O 正极:13O 2 +52e- + 26CO 2 =26CO3 2-电池总反应:2C 4H 10+ 13O 2 = 8CO 2 + 10 H 2O 5.铝——空气燃料电池海水: 负极:4Al -12e- = 4Al 3+ 正极:3O 2 +12e- + 6H 2O =12OH - 电池总反应:4Al +3O 2 +6H 2O = 4AlOH 3 三、原电池的主要应用:1.利用原电池原理设计新型化学电池;2.改变化学反应速率,如实验室用粗锌与硫酸反应制取氢气;3.进行金属活动性强弱比较;4.电化学保护法,即将金属作为原电池的正极而受到保护;如在铁器表面镀锌;5.解释某些化学现象 四、金属的腐蚀与防护腐蚀概念:金属或合金与周围接触到的气体或液体进行化学反应而腐蚀损耗的过程;概述: 腐蚀危害:腐蚀的本质:M-ne -→M n+氧化反应分类:化学腐蚀金属与接触到的物质直接发生化学反应而引起的腐蚀、电化腐蚀电化学腐蚀定义:因发生原电池反应,而使金属腐蚀的形式; 负极Fe :Fe-2e -=Fe 2+; 吸氧腐蚀: 正极C :O 2+2H 2O+4e -=4OH - 总反应:2Fe+O 2+2H 2O=FeOH 2后继反应:4FeOH 2 +O 2 +2H 2O =4FeOH 3钢铁的腐蚀 2FeOH 3====Fe 2O 3 +3H 2O负极Fe :Fe-2e -=Fe 2+;析氢腐蚀: 正极C :2H ++2e -=H 2↑总反应: Fe+2H +=Fe 2++H 2↑影响腐蚀的因素:金属本性、介质;金属的防护: ①、改变金属的内部组织结构;保护方法: ②、在金属表面覆盖保护层;③、电化学保护法牺牲阳极的阴极保护法电解池原理 一、 电解池基础定义:使电流通过电解质溶液而在阴阳两极引起氧化还原反应的过程; 装置特点:电能转化为化学能;①、与电源本连的两个电极;形成条件 ②、电解质溶液或熔化的电解质③、形成闭合回路;金属的腐蚀与防护电极 阳极:与直流电源正极相连的叫阳极;概念 阴极:与直流电源负极相连的叫阴极;电极反应:原理:谁还原性或氧化性强谁先放电发生氧化还原反应离子放电顺序: 阳极:阴离子还原性 S 2->I ->Br ->Cl ->OH ->SO 42-含氧酸根>F -阴极:阳离子氧化性 Ag +>Fe 3+>Cu 2+>Pb 2+>Sn 2+>Fe 2+>Zn 2+>H +>Al 3+>Mg 2+>Na +电子流向 e - e-氧化反应 阳极 阴极 还原反应反应原理:4OH --4e -=2H 2O +O 2 Cu 2++2e -=Cu 电解质溶液电解结果:在两极上有新物质生成;总反应:2CuSO 4+ 2H 2O= 2Cu+2H 2SO 4+O 2↑ 二、 电解池原理粗铜板作阳极,与直流电源正极相连; ①、装置 纯铜作阴极,与直流电源负极相连;用CuSO 4 加一定量H 2SO 4作电解液; 阴极:Cu 2++2e -=Cu电解精炼铜 阳极:Cu-2e -=Cu 2+、Zn-2e -=Zn 2+②、原理: Ni-2e -=Ni 2+阳极泥:含Ag 、Au 等贵重金属; 电解液:溶液中CuSO 4浓度基本不变③、电解铜的特点:纯度高、导电性好;移向阴离子移向 阳离子电解池原理①、概念:利用电解原理在某些金属的表面镀上一薄层其它金属或合金的过程;②、方法:镀层金属与电源正极相连作阳极; 将待镀金属与电源负极相连作阴极;电镀: 用含镀层金属离子的电解质溶液配成电镀液;③、原理:阳极 Cu-2e -=Cu 2+ ;Cu 2++2e -=Cu ④、装置 如图⑤、电镀工业:镀件预处理→电镀液添加剂→装置:现象 ①、阴极上有气泡;②、阳极有刺激性气体产,能使湿润的淀粉KI 变蓝;电解食盐水 ③、阴极区附近溶液变红,有碱生成通电前: NaCl =Na ++Cl - H 2O H ++OH -原理 阴极Fe:Na +,H +移向阴极;2H ++2e -=H 2↑还原反应 通电后: 阳极C :Cl -、OH -移向阳极;2Cl --2e -=Cl 2↑氧化反应总反应:2NaCl +2H 2O 2NaOH +Cl 2↑+H 2↑阳极、阴极、离子交换膜、电解槽、导电铜棒等 ①、组成:阳极:金属钛网涂有钌氧化物;阴极:碳钢网涂有Ni 涂层阳离子交换膜:只允许阳离子通过,阻止阴离子和空气通过;电解的应氯碱工业 电解离子交换膜法制烧碱②、装置:食盐 湿氯气 氯气 ③生成流程: 淡盐水 氢气 NaOH 溶液 → NaOH 固体精制食盐水 + — 纯水含少量NaOH 粗盐水含泥沙、Cu 2+、Mg 2+、Ba 2+、SO 42-等阳离子交换树脂:除Cu 2+、Mg 2+等 加BaCl 2,Ba 2++SO 42-=BaSO 4↓④、粗盐水精制: 加Na 2CO 3:Ca 2++CO 32-=CaCO 3↓;Ba 2++CO 32-=BaCO 3↓加NaOH :Mg 2++2OH -=MgOH 2↓;Fe 3++3OH -=FeOH 3↓三、电解实例及规律电解液 溶质类别 电解总反应式相当于电解溶液pH NaOH 溶液 强碱 2H 2O电解2H 2↑+O 2↑水升高 H 2SO 4溶液 含氧酸 降低 Na 2SO 4溶液 活泼金属的含氧酸盐 不 变 两极混合液 CuCl 2溶液 不活泼金属的无氧酸盐 CuCl 2 电解Cu+Cl 2↑ 电解质本身接近7HCl 溶液无氧酸2HCl电解H 2↑+Cl 2↑升高NaCl 溶液 活泼金属的无氧酸盐2NaCl+2H 2O 电解H 2+2NaOH+Cl 2↑ om电解质与水升高。
高中化学常见原电池方程式

1.电化腐蚀:发生原电池反应,有电流产生〔1〕吸氧腐蚀负极:Fe-2e-==Fe2+正极:O2+4e-+2H2O==4OH-总式:2Fe+O2+2H2O==2Fe(OH)24Fe(OH)2+O2+2H2O==4Fe(OH)32Fe(OH)3==Fe2O3+3H2O〔2〕析氢腐蚀:CO2+H2O H2CO3H++HCO3-负极:Fe -2e-==Fe2+正极:2H+ + 2e-==H2↑总式:Fe + 2CO2 + 2H2O = Fe(HCO3)2 + H2↑Fe(HCO3)2水解、空气氧化、风吹日晒得Fe2O3。
常见原电池(1)一次电池①碱性锌锰电池构成:负极是锌,正极是MnO2,正极是KOH工作原理:负极Zn+2OH—-2e-=Zn(OH)2;正极:2MnO2+2H2O+2e-=2MnOOH+2OH-总反应式:Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2特点:比能量较高,储存时间较长,可适用于大电流和连续放电。
②钮扣式电池(银锌电池)锌银电池的负极是Zn,正极是Ag20,电解质是KOH,总反应方程式:Zn+Ag20=2Ag+ZnO特点:此种电池比能量大,电压稳定,储存时间长,适宜小电流连续放电。
③锂电池锂电池用金属锂作负极,石墨作正极,电解质溶液由四氯化铝锂(LiAlCl4)溶解在亚硫酰氯(SOC12)中组成。
锂电池的主要反应为:负极:8Li-8e—=8Li+;正极:3SOC12+8e—=SO32-+2S+6Cl—总反应式为:8Li+3SOC12=6LiCl+Li2SO3+2S特点:锂电池是一种高能电池,质量轻、电压稳定、工作效率高和贮存寿命长的优点。
(2)二次电池①铅蓄电池:(1)铅蓄电池放电原理的电极反应负极:Pb+S042—-2e—=PbSO4;正极:Pb02+4H++S042—+2e—=PbSO4+2H20总反应式:Pb+PbO2+2H2SO4=2PbS04+2H2O(2)铅蓄电池充电原理的电极反应阳极:PbSO4+2H2O-2e-=PbO2+4H++SO42-;阴极:PbSO4+2e-=Pb+SO42-总反应:2PbSO4+2H2O=Pb+PbO2+2H2SO4②镍一镉碱性蓄电池构成:放电时镉(Cd)为负极,正极是NiO(OH),电解液是KOH工作原理:负极:Cd+2OH—-2e-=Cd(OH)2;正极:2NiO(OH)+2H2O+2e -=2Ni(OH)2+2OH—总反应式:特点:电压稳定、使用方便、安全可靠、使用寿命长,但一般体积大、废弃电池易污染环境。
电化学复习

宏观判断: ①根据电极材料 较活泼的电极材料 ——负极
②根据原电池电极 发生的反应
较不活泼的电极材料——正极 发生氧化反应的极 ——负极
发生还原反应的极 ——正极 质量增加的电极 ——正极 ③根据电极增重还是减重 工作后 质量减少的电极 ——负极 ④根据电极有气泡冒出: 工作后,有气泡冒出的电极为正极
燃料电池是利用氢气、天然气、甲醇等燃 料与氧气或空气进行电化学反应时释放出来的 化学能直接转化成电能的一类原电池。目前燃 料电池的能量转化率可达近80%,约为火力发 电的2倍。这是因为火力发电中放出的废热太 多。燃料电池的噪声及硫氧化物、氮氧化物等 废气污染都接近零;燃料电池发明于19世纪30年代
末,经反复试验、改进,到20世纪60年代才开始进入 实用阶段。第一代燃料电池的 大致情况如下:
氢氧燃料电池工作原理
介质
电池反应: 2H2 +O2 = 2H2O
酸性
中性
负极
正极 负极 正极 负极 正极
(二)二次电池(可充电)
电池-铅蓄电池
1、电极材料及原料
正极:PbO2 负极:Pb
2、电解质溶液 H2SO4溶液 (放电时) 3、电极反应式:
负极(Pb):
Pb- 2e-+ SO4 2 - =PbSO4
正极(PbO2): PbO2+4H++SO42 -+ 2e-= PbSO4 +2H2O
总反应: Pb+PbO2+2H2SO4 =2PbSO4 +2H2O
知识点2:各类电池
锂电池
各 类 电 池
干电池
叠层电池
纽扣电池
(一) 一次电池
1、干电池(普通锌锰电池)
亚硫酰氯锂电池 (ER)

管和be保low护. 电N阻ot时e t应ha参t t考he以po下in注ts意de事sc项ri。bed below should be taken into
careful consideration when selecting diodes and protective resistors.
ܾट!࠶
The battery may be regulated by 国n家at和ion地al区or可lo能ca设l r立eg了ula电tio池n.管P理lea法se规。 请f遵oll守ow相th应e 的ins相tru关ct法io规ns。of因pr为op废er弃电池
中r有eg残ula余tio电n.容A量s ,ele而ct接ric触ca到pa金ci属ty可is 能导 致l变eft形in、a 泄dis漏ca、rd过ed热b或att爆er炸y a。nd所it以在处 理c废om弃es电in池to之co前nt,ac应t w使ith用ot绝he缘r 胶 带 或
锂
operating, please take into consideration these voltage drops for
请勿Wa将rn电in池gs置an于d阳Ca光u直tio射ns、on过h热an和dl过ing湿. 环境。电池存储应远离雨水和
电 池
■su使pp用lie二d v极olt管ag防e t止o l充oa电d.
■ 严禁加热。
硫 酰 氯
璃密封。如果密封损坏,可能出现泄漏并产生刺激性/腐蚀性气体。
将电池加热到100℃以上可能提高电池内压,造成变形、泄漏、过
锂
热、爆炸、起火或产生刺激性/腐蚀性气体。
电 池
■ 严禁摔落。 电池摔落可能损坏玻璃密封,导致泄漏并产生刺激性/腐蚀性气体。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
锂亚硫酰氯电池电极反应式
锂亚硫酰氯电池是一种重要的电化学储能设备,其电极反应式是锂金属与亚硫酰氯之间的化学反应。
锂亚硫酰氯电池在储能领域具有广泛应用前景,因其具有高能量密度、长循环寿命和较低成本等优点,成为了当前研究的热点之一。
锂亚硫酰氯电池的电极反应式可以表示为:
Li + SOCl2 → LiCl + SO2
在这个反应中,锂金属(Li)与亚硫酰氯(SOCl2)发生反应生成氯化锂(LiCl)和二氧化硫(SO2)。
锂金属在反应中失去电子,被氯化锂中的锂离子取代,而亚硫酰氯则被还原为二氧化硫。
这个反应是可逆的,可以在放电和充电过程中进行。
锂亚硫酰氯电池的工作原理如下:在放电过程中,锂金属在负极释放电子,被氯化锂中的锂离子取代,同时亚硫酰氯在正极被还原为二氧化硫。
电子通过外部电路流动,提供电力。
在充电过程中,反应反向进行,锂离子从正极回到负极,同时二氧化硫在正极被氯化锂氧化为亚硫酰氯。
锂亚硫酰氯电池的反应速率和电池性能受到多种因素的影响,如电极材料的选择、电解液的浓度和温度等。
为了提高电池的性能,研究人员通过改变电极结构、优化电解液配方以及控制反应条件等手
段进行了大量研究。
例如,采用纳米材料作为电极材料可以增加电极表面积,提高反应速率;调节电解液中SOCl2的浓度可以改善电池容量和循环寿命。
锂亚硫酰氯电池的应用前景广阔。
由于其高能量密度和长循环寿命,锂亚硫酰氯电池被广泛应用于无线通信、电力系统备份、军事设备和医疗器械等领域。
与传统的锂离子电池相比,锂亚硫酰氯电池具有更高的能量密度和更低的成本,可以满足不同领域对电池能量密度和成本的需求。
锂亚硫酰氯电池的电极反应式为Li + SOCl2 → LiCl + SO2。
锂亚硫酰氯电池具有高能量密度、长循环寿命和较低成本等优点,在储能领域具有广泛应用前景。
通过优化电极结构、电解液配方和控制反应条件等手段,可以进一步提高电池的性能。
锂亚硫酰氯电池在无线通信、电力系统备份、军事设备和医疗器械等领域有着广泛的应用。
未来随着技术的进一步发展,锂亚硫酰氯电池有望成为一种重要的电化学储能设备。
