第二章 有机质谱
有机质谱的基本原理及组成

有机质谱(Organic Mass Spectrometry)是一种广泛应用于有机化学和生物化学领域的分析技术,用于确定有机化合物的分子结构和化学特性。
它基于质谱仪的原理,将化合物中的分子离子进行分离、检测和分析。
有机质谱的基本原理如下:离子化(Ionization):首先,待分析的有机化合物会被引入质谱仪中,并通过不同的离子化方法转化为带电离子。
常见的离子化方法包括电子轰击电离(Electron Impact, EI)、化学电离(Chemical Ionization, CI)、电喷雾电离(Electrospray Ionization, ESI)等。
离子分离(Ion Separation):离子化后的化合物会进入质谱仪的质量分析器中,其中最常用的是质谱仪的四极杆质量分析器。
四极杆通过调节电场使得具有不同质量/电荷比(m/z)的离子能够通过,而其他质量/电荷比的离子则被滤除。
检测(Detection):经过质谱分析器的离子会被检测器探测,并产生相应的电信号。
常见的检测器包括离子倍增器(Electron Multiplier)和离子落点探测器(Ion Counting Detector)等。
数据分析:检测到的信号将转化为质谱图,其中横轴表示质荷比(m/z),纵轴表示信号强度。
通过分析质谱图,可以得到有机化合物的分子质量、分子结构和碎片离子信息等。
有机质谱的组成包括:离子源(Ion Source):负责将待分析的有机化合物转化为带电离子的装置。
质谱分析器(Mass Analyzer):负责将离子按照质量/电荷比进行分离和筛选的部分。
常见的质谱分析器有四极杆质量分析器、飞行时间质谱仪、离子阱质谱仪等。
检测器(Detector):负责检测和转化离子信号为电信号的装置。
数据系统(Data System):负责接收、处理和分析检测到的电信号,并生成质谱图和相关的数据信息。
以上是有机质谱的基本原理和组成的简要介绍,有机质谱技术在化学和生物领域有着广泛的应用,可以用于物质的鉴定、结构分析、代谢研究等方面。
有机质谱原理及应用PPT课件

13
1.1
15
0.37
17
0.04
29
5.10
33
0.80
A+2
质量
%
18
0.20
30
3.40
34
4.40
37
32.5
81
98.0
元素类型
A A+1
A A+2
A A+1,A+2
A A+2 A+2 A+2
A
元素 分类情况: A: H, F, P, I
A+1: C, N
A+2: O, Si, Cl, Br
为其百分强度,百分强度= (Ii/ Ii) × 100% Ii,第i 个离子的 强度。 基峰强度:质谱图中离子强度最大的峰称为基峰,定义它的强 度为100,即IB=100, 其它离子强与之相比的百分强度称为 该离子的强度。
三、同位素
化学上,氖的原子量为20.2, 质谱上:氖不在m/z20.2处出峰,而是在m/z20和m/z22处各出一个峰,
Herzog 和 Hintenberger 电磁场组合,离子光学系统 1940年,Nier 扇形磁场偏转质谱计,双聚集系统 商品仪器的雏形
235U,电磁制备方法,第二次世界大战期间 在石油、化工等领域的应用 1946年,Stephens 飞行时间质谱(Time-of flight mass analysis)
化学、化工
药学、毒物 学、刑侦
§1.3 质谱学的开展历史 一、质谱学领域的诺贝尔〔Nobel〕奖 1906年:物理奖
J. I. Thomson 奉献:正电荷离子束在磁场中的偏转 磁质谱仪的基
础同位素分析 1989年:物理奖
第二章 有机质谱3-裂解反应+非氢重排
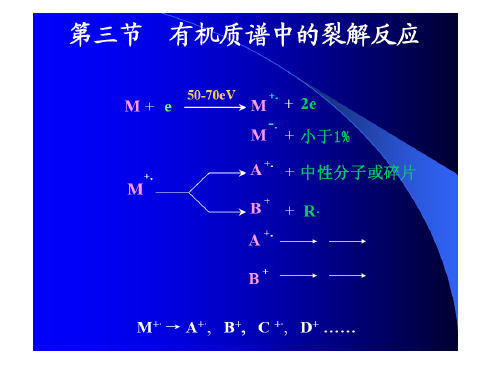
R
+
H2C
+ NHR' + OH(R' ) + SH(R' )
R
CH2
R
+
H2C
R
CH2 + O + S
R
+
H2C
R R
R+ + R+ +
OR' SR'
or or
R' R'
+ +
1. 偶电子规律
OE+ ·→ OE+ ·, OE+ ·→ EE+ EE+ → EE+ , EE+ → OE+ · ?
如何识别质谱图中的的OE+·?
不含氮的化合物, m/z 为偶数的离子是奇电子离子 在质谱图中, 奇电子离子并不多见, 但重要.
2. 烃类化合物的裂解规律:
烃类化合物的裂解优先生成稳定的正碳离子
+
re
CO2 + C6H5NH C2H5
+
m/z = 121
+ re RCH2O CH2O CH2R'
CH2O + RCH2O
CH2R'
+
re与氢的重排类似,反应过程中迁移的是一种基团,而不是氢自由基 消去反应中消去的是小分子或自由基碎片。
2. 苯基迁移
O SCH3
O S
+
有机质谱中的裂解反应

2. 重排裂解 ① 麦氏重排(自由基引发的重排反应):具有γ-H的侧链苯、烯烃、
环氧化合物、醛、酮等经过六元环过渡态使γ-H转移到带有正电荷的原 子上,同时在α 、β 原子间发生裂解,这种重排称为麦克拉夫悌重排裂解。
第二章 有机质谱
2.3 有机质谱中的裂解反应
一、有机质谱裂解反应机理 二、有机化合物的一般裂解规律
一、有机质谱裂解反应机理
裂解方式:1. 简单裂解 2. 重排开裂
1. 简单裂解 电荷-自由基定位理论:分子离子中电荷或自由基定位在分子的
某个特定位置上(首先先确定这个特定位置),然后以一个电子或 电子对的转移来“引发”裂解。单电子转移发生的裂解称为均裂, 双电子转移发生的裂解称为异裂。
+ O = CH2
+
R2
α
CH2 = O
R2 + R1
α
+ OH
H
N
R2
+
+
+ OH
α
R1
H N = CH2 + R2 +
H
α
CH2
=
N +
R2 + R1
② 异裂—正电荷引发裂解—i 裂解
正电荷引发的i断裂反应:是由正电荷引发的碎裂过程,它涉及两个 电子的转移,动力来自于电荷的诱导。
R1
酮:
均裂
异裂
① 均裂—自由基引发裂解—α裂解
自由基引发的ɑ断裂反应:动力来自自由基强烈的电子配对倾向。该 反应由自由基中心提供一个电子与邻接的原子形成一个新键,而邻 接原子的另一个化学键则发生断裂。下面列举几种含n、π电子化合 物发生ɑ断裂反应的情况:
有机质谱原理

1.3-0.13Pa
b) 直接探针进样:高沸点液体及固体 探针杆通常是一根规格为25cm6mm i.d.,末端有一装样品的黄金杯(坩埚) ,将探针杆通过真空闭锁系统引入样品,如图所示。 优点: 1)引入样品量小,样品蒸汽压 可以很低; 2)可以分析复杂有机物; 3)应用更广泛。
c) 色谱进样:利用气相和液相色谱的分离能力,与质谱仪联用,进行多组份复 杂混合物分析。
二、质谱仪性能指标 1. 质量测量范围 质量测定范围以原子质量单位量度,1个原子质量单位:
1u=1.6605410-27kg/12C原子
如12C=12u, CH4=16.xxxx u 在非精确测量中,常直接以原子或分子量大小来表示。 2. 分辨本领
指质谱仪分辨相邻质量数离子的能力。定义为:两个相等强度的相邻峰(质 量分别为m1和m2),当两峰间的峰谷不大于峰高的10%时,则可认为两已分开, 其分辨率R为:
下图是单聚焦型质量分析器更直观地的工作过程。
单聚焦质量分析器只是将 m/z 相同而入射方向不同的离
子聚焦到一点(或称实现了
方向聚焦)。 但 对 于 m/z 相 同 而 动 能 (或速度)不同的离子不能
聚焦,故其分辨率较低,一
般为5000。
双聚焦型(Double focusing mass spectrometer) 为克服动能或速度“分散”的问题,即实现所谓的“速度(能量)聚焦”,在 离子源和磁分析器之间加一静电分析器 ( ESA) ,如下图所示,于两个扇形电 极板上加一直流电位Ve,离子通过时的曲率半径为re=U/V,即不同动能的离子re 不同,换句话说,相同动能的离子的re相同----能量聚焦了! 然后,改变V值可使不同能量的离子从其“出射狭缝”引出,并进入磁分析 器再实现方向聚焦。双聚焦质量分析器可高达150,000!
有机质谱中的裂解反应

α
α
CH2 = O
R2 + R1
醇:
+ OH
+ + OH
α
胺:
R1 H N + R2
R1
H N = CH2 + R2 +
α
H CH2 = N +
R2 + R1
② 异裂—正电荷引发裂解—i 裂解
正电荷引发的i断裂反应:是由正电荷引发的碎裂过程,它涉及两个 电子的转移,动力来自于电荷的诱导。
R1
酮:
R2
C
O
+
i
R1
+
+ R2
C
O
氯代物:
+ Cl
i
+ (CH3)2CH + CH2 = C l
酯:
+ O O i + +
O C O
i断裂与α 断裂小结
1、杂原子为单键时,i断裂和α 断裂所引起的断键位置是不同的。杂 原子为重键时,i断裂并不导致重建的断裂。 2、产物的电荷稳定通常比游离基稳定更重要,因此不同的物质断键
R
C O
a
R
C
a
R'
R . + 'R C
O+
2. 烃类化合物的裂解规律 烃类化合物的裂解优先失去大的基团生成稳定的正碳离子
+ CH2 > H2C CH + + + + + CH2 > CR3 >CHR2>CH2R >CH3
m/z = 91, tropylium
H2C CH
+ CH2
有机质谱-分子离子与分子式

质荷比最大的是M++2峰,M+峰对应的质荷比数值是该 化合物的分子量。
例如:CH4 M=16
12C+1H×4=16 13C+1H×4=17
M
分子离子峰
16 15
M+1
12C+2H+1H×3=17
13C+2H+1H×3=18
M+1
M+2
同 位 素 峰
m /z R A 3 .1 1 12 1 .0 13 3 .9 14 9 .2 15 85 ,H,O 组成的化合物,M +的 m/e 一定是偶数; • 由C,H,O,N 组成的化合物,N原子的个数为 奇数, M +的 m/e 一
定是奇数;
• 由C,H,O,N 组成的化合物,N原子的个数为偶数 , M +的 m/e 一 定是偶数; • 分子离子峰与相邻峰的质量差必须合理。
五、分子式的推导
1. 低分辨质谱法
准确地测定常见各种分子式的(M++1)/ M+ 、 (M++2) /M+ 的 百分比。可查贝农表对化合物的分子式进行推断。
例1:某化合物,M+ 、M++1、M++2的相对强度如下。推测其分子式。 m/e 强度比 150( M+ ) 100 151(M++1) 10.2 152( M++2 ) 0.88
解:根据M++2 /M+ =0.88%,对照上页同位素丰度表,可知此分子中不
含S以及卤素。在贝农表中,分子量为150的分子式共有29个,其中M++1/
M+ =9~11之间的分子式共有7个:
根据N规律,表中C8H8NO2、 C8H12N3
有机质谱解析2

质谱,即质量的谱图。
物质的分子经物理作用或化学反应等途径形成带电粒子,某些带电粒子可进一步断裂。
如用电子轰击有机化合物(M),使其产生离子的过程如下:每一离子的质量与所带电荷的比称为质荷比(m/z ,曾用m/e表示)。
不同质荷比的离子经质量分离器一一分离后,由检测器测定每一离子的质荷比及相对强度,由此得出的谱图称为质谱。
下面为甲醇的质谱分析实例。
表1-1甲醇的质谱数据图1-5 甲醇的质谱图从质谱分析中可以得到有机化合物分子结构信息,上图中只失去一个电子的离子(m/z 32)被称为分子离子。
其质荷比与母体分子的分子量相等。
母体分子或分子离子裂解形成碎片离子,这种裂解与分子结构有密切关系。
此外,谱图中同位素离子的丰度与天然元素中同位素的丰度有相关性,由此可推测样品中某种元素的存在。
质谱分析与核磁共振波谱及红外光谱分析相结合,便可以确定有机化合物的分子结构。
质谱分析中常用术语和缩写式如下:质谱图上反应各离子的质荷比及丰度的峰被称为某离子峰。
在质谱图上可以看到各种离子及其相对强度,这些信息与分子结构有关。
本章主要介绍电子电离质谱中各种离子的形成、特点及其在质谱解析中的作用。
第一节分子离子分子离子(M+。
)是质谱图中最有价值的信息,是测定化合物分子量的依据。
用高分辨质谱可以直接测定化合物的分子式。
用低分辨质谱得到的数据,结合同位素离子、碎片离子也可以推测化合物的分子式。
一、分子离子的形成分子失去一个电子后形成分子离子。
一般来讲,从分子中失去的电子应该是分子中束缚最弱的电子,如双键或叁键的π电子、杂原子上的非键电子等,失去电子的难易顺序为:杂原子> C=C > C-C > C-H易难有机化合物在质谱中的分子离子稳定度有如下次序:芳香环 > 共轭烯 > 烯 >环状化合物 > 羰基化合物 > 醚 >酯 > 胺 > 酸 > 醇 >高度分支的烃类。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
【基本要求】
理解质谱的基本原理 熟悉质谱中离子的主要类型 掌握有机化合物质谱碎裂规律 掌握运用质谱解析分子结构的方法
【重点难点】
质谱中离子的主要类型 有机化合物质谱碎裂规律 质谱解析分子结构的方法
2.1 质谱基本知识
质谱,即质量的谱图,物质的分子在高真空下,经物理作用或化学反应等 途径形成带电粒子,某些带电粒了可进一步断裂。如用电子轰击有机化合物 (M),使其产生离子的过程如下:
由 M 所形成的峰称为分子离子峰。因此,分子离子峰的m/z 的数值就是该化合物的相对分子质量Mr。是有机化合物的重要质谱 数据
分子离子峰若能出现,应位于质谱图的右端。 几乎所有的有机分子都可以产生可以辨认的分子离 子峰。有些分子如芳香环分子可产生较大的分子离子峰, 而高分子量的脂肪醇、醚及胺等则产生较小的分子离子 峰。若不考虑同位素的影响,分子离子应该具有最高质 量。 其相对强弱随化合物结构而变化,其强弱顺序一般 为芳环 > 共轭多烯 > 烯 > 环状化合物 > 羰基化合物 > 醚 > 酯 > 胺 > 酸 > 醇 > 高度分支的烃类。分子离子峰 的强弱也与实验条件有关。
优点: 准分子离子峰强度高,便于推算分子量; 缺点: 1)只适用于易挥发、受热不分解的样品; 2)碎片离子峰少,强度低。
3.场致电离(field ionization, FI)和 场解吸电离(field desorption, FD)
场致电离:是一种软电离技术。当样品蒸汽邻近或接触到带高正电位的金属 针时,由于高曲率的针端产生很强的电位梯度,样品分子可被电离。 优点:电离快速,适合于和气相色谱联机; 缺点:要求样品汽化,灵敏度低。 场解吸电离:原理与FI相同,但样品是被沉积在电极上。 FD适用于难汽化的、热不稳定样品。FD的准分子离子峰比FI的强,质谱图比 FI的还要简单。
c、离子源
离子源是质谱仪的心脏部分,是样品分子的离子化场所,最早使用的电 子轰击离子源(electron impact sourse, EI)。至今仍是使用最广泛的最 重要的离子源。 它具有如下特点:电离效率高,灵敏度高;应用最广,标准质谱图基本都 是采用EI源得到的;稳定,操作方便,电子流强度可精密控制;结构简单, 控温方便;
离子作弧形运动的离心力( 大小相等。
1 m B2 R2 2 结合 2 mv zV ,导出 z 2V 当仪器的狭缝固定(R=常数),B由小到大改变(扫场),
mv 2 Bzv R
mv 2 )和受磁场作用的向心力( R
Bzv )
则离子按m/z由小到大通过狭缝,到达检测器,被收集并记
录下各质荷比的离子的相对强度。 相同m/z的离子,速度相同,色散角不同,经磁场偏转 后,会重新聚在一点上。即静磁场具有方向聚焦,称之单聚焦。
静电分析器 + 磁分析器- 双聚焦质谱计
静电分析器由两个同心圆板组成,两圆板之间保持一定的电位差(E)。
静电分析器加在磁分析器之前。加速后 的离子在静电分析器中, 受到外斥内吸的电 场力(zE)的作用, 迫使离子作弧形运动。
mv zE R
结合
2
1 mv 2 zV , 导出 2
2V R E
脉冲式激光
优点: 1)使一些难于电离的样品电离,且无明显的碎裂,从而得到完整的被分 析化合物分子的电离产物; 2)特别适用于与飞行时间质谱相配(MALDI-TOFMS)。
2.1.3质量分析器
◆质量分析器是质谱计的核心。 ◆不同类型的质量分析器构成不同类型的质谱计。 ◆不同类型的质谱计其功能,应用范围,原理,实验方法均有所不同。 质量分析器有两种: 磁分析器和静电分析器
2. 碎片离子(fragment Ion) 分子离子中的某个化学键断裂而形成的离子,即碎片离子,有些 碎片离子获得能量,会进一步裂解成更小的碎片离子。 特点:m/z较分子离子小,碎片离子峰出现在分子离子峰的左侧。 作用:反映分子的结构信息。
72 27 55
45
20
40
60
80
质谱中常用的电离电压为70电子伏特,使结构裂解,产
5. 电喷雾电离(electrospray ionization, ESI) 主要应用于高效液相色谱HPLC与质谱仪的联用。 从雾化器套管的毛细管端喷出的带电液滴,随着溶剂的不断快速蒸发,液滴 迅速变小,表面电荷密度不断增大。由于电荷间的排斥作用,就会排出溶剂 分子,得到样品的准分子离子。
HPLC
样品溶液 雾化管端 施加高电压
氮气雾化 通过加热 管被汽化 加热管端 尖端
保温层
单电荷或多 电荷离子
6.基质辅助激光解吸电离(matrix-assisted laser desportion ionization, MALDI)
在一个微小的区域内,在极短的时间间隔,激光可对靶物提供高的能量,对 它们进行极快的加热,可以避免热敏感的化合物加热分解。 MALDI的方法:将被分析化合物的溶液和某种基质溶液相混合。蒸发掉溶剂,则 被分析物质与基质形成晶体或半晶体。用一定波长的脉冲式激光进行照射。基质 分子能有效地吸收激光的能量,并间接地传给样品分子,从而得到电离。
d、质量分析器——质谱仪的主体 质量分析器的作用是将离子源产生的离子按照质荷比 m / z 的大小分离,使符合条件的离子飞过分析器,不符合条件的离子 即被过滤掉 常见的有单聚焦质量分析器,双聚焦质量分析器和四极滤质 器等 e、检测器 最主要的检测器是电子倍增管,它可以测出10-17A微弱电流。 如果电流更微弱,则需采用渠道式电子倍增器阵列,它可以使电流 放大。
质谱表 质谱表是把质荷比和相对强度以表格形式表示,可以有数据 表示法和论文记录法。
m / z值 相对强度
27 —
39
51 —
二.质谱中的离子
1.分子离子(molecular Ion )
化合物分子通过某种电离方式,失去一个外层价电子而形成带 正电荷的离子称为分子离子。常用符号M+·表示。
M e M 2e
每一离子的质量与所带电荷的比称为质荷比(m/z ,曾用m/e)。不同质荷比 的离子经质量分离器一一分离后,由检测器测定每一离子的质荷比及相对 强度,由此得出的谱图称为质谱
每一线段(棒)代表一种质量的离子; 纵坐标表示离子的相对丰度 横坐标表示离子的质荷比
质谱的优点
灵敏度特别高
进样量非常少,通常只用几微克 (μ g),甚至更少的样品 (10-10 g) 便可给出一张满意的质谱图。检出极限可达10-14 g
质谱是唯一可以给出分子量, 确定分子式的方法
分子式的确定对化合物的结构鉴定至关重要
适用范围广(气体、液体、固体) 联用技术
2.1.1 质谱计
质谱计 进样系统 真空系统 离子源 加速区 质量分析器 计算机数据 处理系统
电离部分
离子分 离检测 部分
检测器
a、真空系统:
离子与气体分子的碰撞,离子源和质量分析器的压力在10–4 - 10–5
2.1.4 质谱术语及质谱中的离子
一、质谱术语 基峰:
质荷比:
RI
100 ,
RA
100
m / z , z = 1, z = 2;
m的计算:组成离子的各元素同位素的质子和中子之和。
精确质量: 精确质量的计算基于天然丰度最大的同位素 的精确原子量,如:
1H
1.007825 、
12C
12.000000、
2.1.2 离子化的方法
离子化的方法有很多,用于有机质谱计的主要有电子轰击、化学 电离、场致离和场解离、快原子轰击、电喷雾电离、激光解析电离等 1. 电子轰击电离(electron impact ionization, EI) 质谱中最常用的离子化方法,一般为70eV的电子束,远大于大多数 有机化合物的电离电位(7~15eV),会使相当多的分子离子进一步裂 解,产生广义的碎片离子。
枪内进行电荷交换反应:
MS 分析系统
Ar+ Ar+枪
Ar 碰撞室
Ar (6kV)
探头 样品
FAB离子源原理示意图
FAB可完成连FD都有困难的、高极性、难汽化的化合物的电离。样品多 调匀于基质(一般为甘油等)中。基质应具有流动性、低蒸气压、化学惰 性、电解质性和好的溶解性。 FAB得到的是准分子离子峰(M+H)+; 当分析极性样品(糖类),常加入NaCl水溶液,得到(M+Na)+离子 峰。
只有一扇形磁场的质量分析器又称为磁分析器。单聚焦质谱计-磁分析器
加速后离子具有一定的动能: ( 电势能(zV)转化的。
1 2 ),该动能是由离子在加速电场获得的 mv 2
1 mv 2 zV 2
加速后的离子进入磁场, 其运动方向( I )和磁力线的方向(B)相互垂直。 离子受到一个与其运动方向和磁力线 的方向都垂直的力(F)的作用,三者的关 系可用左手定则确定。 离子沿着I和B合力的方向运动,即 受到磁场的偏转作弧形运动。
Pa 和 10–5 - 10–6 Pa。因为:
b、进样系统
进样系统的作用是将待测物质(即试样)送进离子源。一般有直接进样、
间接进样、色谱进样三种方式: 直接进样——高沸点的试液、固体试样可用探针或直接进样器送入离子 源,调节温度使试样气化 间接进样——一般气体或易挥发试样 色谱进样——色谱-质谱联用仪器中,经色谱分离的组分通过接口元件直 接导入离子源。
图中除可见分子离子峰外,还可见m/z31,45等碎片离子峰
2. 化学电离(chemical ionization, CI)
化学电离是通过离子-分子反应来完成的。反应气体一般是甲烷、异 丁烷、氨等, 生成(M+H)+, (M-H)+, (M+NH4)+ 的准分子离子。
