第七章 晶体的点阵结构和晶体的性质习题答案
第七章晶体的点阵结构和晶体的性质习题

第七章晶体的点阵结构和晶体的性质习题第七章晶体的点阵结构与晶体的性质习题一、填空题1.从CsCl晶体中能抽出________点阵,结构基元是________,所属晶系的特征对称元素是________。
2.属于立方晶系的点阵类型有________________,属于四方晶系的点阵类型有___________。
3.晶体宏观外形中的对称元素可有________,________,________,______四种类型;晶体微观结构中的对称元素可有________,________,________,________,________,________,______七种类型;晶体中对称轴的轴次(n)受晶体点阵结构的制约,仅限于n=_________;晶体宏观外形中的对称元素进行一切可能的组合,可得________个晶体学点群;分属于________个晶系,这些晶系总共有________种空间点阵型式,晶体微观结构中的对称元素组合可得________个空间群。
4.晶体中可能存在的全部宏观对称元素是:。
5.晶体的宏观对称操作集合构成____________个晶体学点群;晶体的微观对称操作集合构成____________个空间群。
6.没有四方F和四方C,因为四方F可以化为___________,四方C可以化为_________。
7.(312)晶面在a,b,c轴上的截距分别为______,______,______。
8.金属钠具有立方体心点阵结构,其(110)晶面间距为303pm,其(111)晶面间距则为________。
9.从某晶体中找到C3,3C2,σh,3σd等对称元素,该晶体属________晶系是_____点群。
10.晶体按对称性分,共有______________个晶系。
11.晶体的空间点阵型式共有____________种。
12.晶体的点对称性共有___________种点群。
13.晶体的衍射方向可用以测定晶体的______________数据。
晶体的点阵结构和晶体的性质
2
7.1.1 点阵、结构基元和晶胞
一、结构基元与点阵
晶体的周期性结构使得我们可以把它抽象成“点阵”来 研究。在晶体内部,原子和分子按照周期性重复排列,就 要有重复单位,每个重复单位的化学组成相同,空间结构 相同,周围环境也相同。(周期性重复的内容) 晶体中重复出现的最小单元,为结构基元。各个结构基 元相互之间化学内容相同,它们所处的环境也完全相同。 每个结构基元可以用一个数学上的点来代表,称为点 阵点(或结点)。于是,整个晶体就被抽象成一组点,称 为点阵。
第七章 晶体的点阵结构 和晶体的性质
1
7.1 晶体结构的周期性和点阵
晶体 是由原子或分子在空间按一定规律周期重复地排列
构成的固体物质。 原子、分子、离子在空间按周期性规律排列是晶体结构最 基本的特征。 晶 体 (具有周期性) 固态物质 非晶态物质(无周期性)
晶体结构:按周期性规律重复排列
非晶体结构
角 , , 称为点阵参数。
3.晶格反映了晶体结构的周期性。
28
按照周期性规律分类 单晶体:一整块固体基本上为一个空间点阵所贯穿 多晶:由许多小的单晶体按不同的取向聚集而成的固体
晶 体
微晶:结构重复的周期数很少,只有几个到几十个周期 的固体,微晶是介于晶体和非晶体物质之间的物质。 纤维多晶物质:棉花、蚕丝、毛发及各种人造纤维等物 质,一般具有不完整的一维周期性的特征,并沿纤维轴 择优取向。
21
<1> 直线点阵
所有点阵点都分布在同一条直线上。
•
1. 2. 3.
•
a
•
•
•
连接相邻两个点阵点的向量 a 是直线点阵的单位向量。
向量长度 a a 称为点阵参数。
第七章 晶体的点阵结构和晶体的性质

900
dh*k*l*
dhk l
dh*k*l*
(a)
(b)
t/min
图7.4 晶体(a)与非晶体(b)的步冷曲线
辽宁石油化工大学
结构化学2
7.2 晶体结构的周期性和点阵
NaCl 晶体结构
辽宁石油化工大学
结构化学2
7.2 晶体结构的周期性和点阵
一、晶体结构的点阵理论 1. 结构基元与点阵
晶体的周期性结构使得人们可以把它抽象成
“点阵”来研究。将晶体中重复出现的最小单元
辽宁石油化工大学
结构化学2
7.1 晶体的结构和性质
辽宁石油化工大学
一、晶体的定义
由原子、分子或离子等微粒在空间按一定 规律、周期性重复排列所构成的固体物质。
图7.1 晶态结构示意图
图7.2 非晶态结构示意图
辽宁石油化工大学
结构化学2
7.1 晶体的结构和性质
二、 晶体结构的特征
固体物质按原子 ( 分子、离子 ) 在
Mn
(立方简单)
Li Na K Cr Mo W…...
(立方体心)
以上每一个原子都是一个结构基元,都可以抽象成一个点阵点.
实例:Ni Pd Pt Cu Ag Au ……
立方面心是一种常见的
金属晶体结构,其中每
个原子都是一个结构基 元,都可被抽象成一个 点阵点.
CsCl型晶体结构
CsCl型晶体中A、B是不同的原子,不能都被抽象为点阵 点. 否则,将得到错误的立方体心点阵!这是一种常见的错误:
将晶体中重复出现的最小单元作为结构基元,用 一个数学上的点来代表, 称为点阵点,整个晶体就被 抽象成一组点,称为点阵。
《结构化学》(7-10章)习题答案全解
《结晶学基础》习题答案目录第7章答案----------------------------------------------------------------------1第8章答案---------------------------------------------------------------------12第9章答案---------------------------------------------------------------------20第10章答案------------------------------------------------------------------251《结晶学基础》第七章习题答案7001 单晶:一个晶体能基本上被一个空间点阵的单位矢量所贯穿。
多晶:包含许多颗晶粒,这些晶粒可能为同一品种,也可能不同品种,由于各晶粒在空间取向可能不同,不能被同一点阵的单位矢量贯穿。
7002 (D) 7004 简单立方; Cs +和Cl -; 4C 37005 (1) 立方F (2) A 和 B (3) 4 个 (4) 4 组 (5) 3a (6) a /2 7007 4n 个 A, 8n 个 B, n 为自然数。
7010 d 111= 249 pm ; d 211= 176 pm ; d 100= 432 pm 7011 六方; D 3h 70127013 依次为立方,四方,四方,正交,六方。
7014 立方 P ,立方 I ,立方 F ; 四方 P ,四方 I 。
7015 旋转轴,镜面,对称中心,反轴; 旋转轴,镜面,对称中心,反轴,点阵,螺旋轴,滑移面;n =1,2,3,4,6; 32个; 七个晶系; 14种空间点阵型式; 230个空间群。
7016 (1) 四方晶系 (2) 四方 I (3) D 4 (4) a =b ≠c , α=β=γ=90° 7017 (1) 单斜晶系,单斜 P (2) C 2h (3) C 2, m , i 7018 (2a ,3b ,c ):(326); (a ,b ,c ):(111); (6a ,3b ,3c ):(122); (2a ,-3b ,-3c ):(322)。
王顺荣编高教版社结构化学习题答案第7章
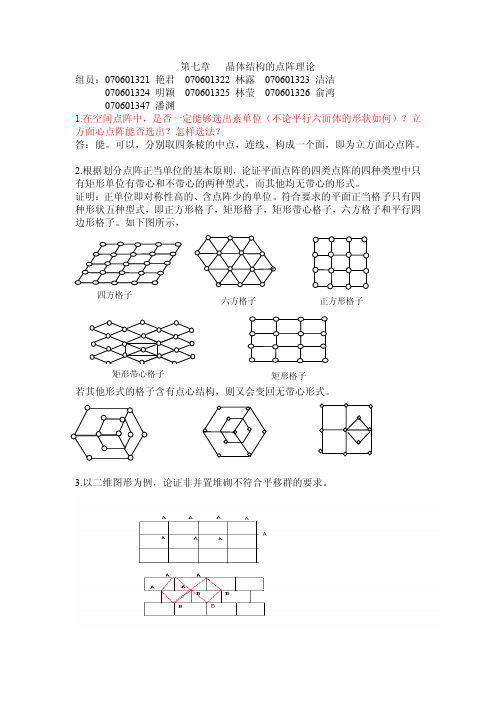
(010)与(210)的夹角为 arc tan1/2 (110)与(210)的夹角为 arc tan1/2-45° 13、利用立方体图形,计算 CH4 正四面体结构 C-H 键的夹角是 109o28' A、B、C、O 为 CH4 中 4 个 H,D 为 CH4 的 C A、O、D 的原子坐标分别为(1,0,1) ,(0,0, 0), (1/2,1/2,1/2) AD=√3/2 , OD=√3/2, AO=√2 ∠AOD 为两个 C-H 键的夹角 Cos∠AOD=(AD2+ OD2- AO2)/2 AD· OD=-1/3 ∠AOD=109o28' 即 CH4 中 C-H 键夹角为 109o28' 14.利用三角函数法,证明由于点阵结构的制约,晶体结构中不存在 5、7 及更高 次轴。
,
解: 设 A 的射散因子为 fa,B 的射散因子为 fb F(hkl)= faei2π(0+0+0) +fbei2π( =fa+ fbeiπ(h+k+l) =fa+ fb[cosπ(h+k+l)+i sin(h+k+l)] 当 fa=fb,即 AB 为相同物质时: 当 h+k+l=奇数时,F(hkl)=0 当 h+k+l=偶数时,F(hkl)=2f 在奇数时不衍射,故为体心点阵(I) 当 fa≠fb,即 AB 为不同物质时: 无消光现象,故为简单点阵(P)
b (s s 0) k
c (s s 0) l
式中 a,b,c 反映了晶胞大小形状和空间取向; s 和 s 0 反映了衍射 X 射线和入射 X 射线的方向;h,k,l 为衍射指标, 为 X 射线波长。 衍射强度 Ihkl 和结构因子 Fhkl 成正比,而结构因子和晶胞中原子种类及其坐标参数 x,y,z 有关:
第七章 晶体的点阵结构和晶体的性质

第七章晶体的点阵结构和晶体的性质一、概念及问答题1、由于晶体内部原子或分子按周期性规律排列,使晶体具有哪些共同的性质?答:a. 均匀性,一块晶体内部各个部分的宏观性质是相同的。
b. 各向异性,在晶体中不同的方向上具有不同的物理性质。
c. 自发地形成多面体外形,晶体在生长过程中自发地形成晶面,晶面相交成为晶棱,晶棱会聚成项点,从而出现具有多面体外形的特点。
2、点阵答:点阵是一组无限的点,连结其中任意两点可得一向量,将各个点按此向量平移能使它复原,凡满足这条件的一组点称为点阵。
点阵中的每个点具有完全相同的周围环境。
3、晶体的结构基元点阵结构中每个点阵点所代表的具体内容,包括原子或分子的种类和数量及其在空间按一定方式排列的结构,称为晶体的结构基元。
结构基元与点阵点是一一对应的。
4、晶体结构在晶体点阵中各点阵点的位置上,按同一种方式安置结构基元,就得整个晶体的结构,所以地晶体结构示意表示为:晶体结构=点阵+结构基元5、直线点阵根据晶体结构的周期性,将沿着晶棱方向周期地重复排列的结构基元,抽象出一组分布在同一直线上等距离的点列,称为直线点阵。
6、晶胞按照晶体内部结构的周期性,划分出一个个大小和形状完全一样的平行六面体,以代表晶体结构的基本重复单位,叫晶胞。
晶胞的形状一定是平行六面体。
晶胞是构成晶体结构的基础,其化学成分即晶胞内各个原子的个数比与晶体的化学式一样,一个晶胞中包含一个结构基元,为素晶胞,包今两个或两个以上结构基元为复晶胞,分别与点阵中素单位与复单位相对应。
7、晶体中一般分哪几个晶系?根据晶体的对称性,可将晶体分为7个晶系,每个晶系有它自己的特征对称元素,按特征对称元素的有无为标准划分晶系。
一般分为7个晶系,有立方晶系、六方晶系、四方晶系、三方晶系、正交晶系、单斜晶系和三斜晶系。
8、CsCl 是体心立方点阵还是简单立方点阵?是简单立方点阵。
在CsCl 晶体中,结构基元是由一个Cs +和一个Cl -构成,点阵点可以选Cs +的位置,也可以选Cl -的位置,还可以选在其他任意位置,但不能同时将Cs +和Cl -作为点阵点,因为这样选取不符合点阵的定义,同时也不能将晶体CsCl 误认为是体心立方点阵,因为每个点阵点代表一个Cs +和一个Cl -。
材料化学李奇陈光巨习题解答全
习题一答案1、晶体一般的特点是什么?点阵和晶体的结构有何关系?答:(1)晶体的一般特点是:a 、均匀性:指在宏观观察中,晶体表现为各部分性状相同的物体b 、各向异性:晶体在不同方向上具有不同的物理性质c 、自范性:晶体物质在适宜的外界条件下能自发的生长出晶面、晶棱等几何元素所组成凸多面体外形d 、固定熔点:晶体具有固定的熔点e、对称性:晶体的理想外形、宏观性质以及微观结构都具有一定的对称性(2)晶体结构中的每个结构基元可抽象成一个点,将这些点按照周期性重复的方式排列就构成了点阵。
点阵是反映点阵结构周期性的科学抽象,点阵结构是点阵理论的实践依据和具体研究对象,它们之间存在这样一个关系:点阵结构=点阵+结构基元点阵=点阵结构-结构基元2、下图是一个伸展开的聚乙烯分子,其中C—C化学键长为1.54Å。
试根据C原子的立体化学计算分子的链周期。
答:因为C原子间夹角约为109.5°,所以链周期=2×1.54Å×sin(109.5°/2)=2.51Å链周期3、由X射线法测得下列链型高分子的周期如下,试将及前题比较思考并说明其物理意义。
化学式聚乙烯醇 2.52聚氯乙烯 5.1聚偏二氯乙烯 4.7答:由题中表格可知,聚乙烯醇的链周期为2.52 Å,比聚乙烯略大,原因可能是-OH体积比H大,它的排斥作用使C原子间夹角变大,因而链周期加长,但链周期仍包含两个C原子;聚氯乙烯的链周期为5.1 Å,是聚乙烯链周期的两倍多,这说明它的链周期中包含四个C原子,原因是原子的半径较大Cl原子为使原子间排斥最小,相互交错排列,其结构式如下:聚偏二氯乙烯链周期为4.7 Å比聚乙烯大的多,而接近于聚氯乙烯的链周期为5.1 Å,可知链周期仍包含4个C原子。
周期缩短的原因是由于同一个C原子上有2个Cl原子,为使排斥能最小它们将交叉排列,即每个Cl原子在相邻2个Cl原子的空隙处。
晶体学课后习题参考答案
第一章习题1.晶体与非晶体最本质的区别是什么?准晶体是一种什么物态?答:晶体和非晶体均为固体,但它们之间有着本质的区别。
晶体是具有格子构造的固体,即晶体的内部质点在三维空间做周期性重复排列。
而非晶体不具有格子构造。
晶体具有远程规律和近程规律,非晶体只有近程规律。
准晶态也不具有格子构造,即内部质点也没有平移周期,但其内部质点排列具有远程规律。
因此,这种物态介于晶体和非晶体之间。
2.在某一晶体结构中,同种质点都是相当点吗?为什么?答:晶体结构中的同种质点并不一定都是相当点。
因为相当点是满足以下两个条件的点:a.点的内容相同;b.点的周围环境相同。
同种质点只满足了第一个条件,并不一定能够满足第二个条件。
因此,晶体结构中的同种质点并不一定都是相当点。
3.从格子构造观点出发,说明晶体的基本性质。
答:晶体具有六个宏观的基本性质,这些性质是受其微观世界特点,即格子构造所决定的。
现分别叙述:a.自限性晶体的多面体外形是其格子构造在外形上的直接反映。
晶面、晶棱与角顶分别与格子构造中的面网、行列和结点相对应。
从而导致了晶体在适当的条件下往往自发地形成几何多面体外形的性质。
b.均一性因为晶体是具有格子构造的固体,在同一晶体的各个不同部分,化学成分与晶体结构都是相同的,所以晶体的各个部分的物理性质与化学性质也是相同的。
c.异向性同一晶体中,由于内部质点在不同方向上的排布一般是不同的。
因此,晶体的性质也随方向的不同有所差异。
d.对称性晶体的格子构造本身就是质点周期性重复排列,这本身就是一种对称性;体现在宏观上就是晶体相同的外形和物理性质在不同的方向上能够有规律地重复出现。
e.最小内能性晶体的格子构造使得其内部质点的排布是质点间引力和斥力达到平衡的结果。
无论质点间的距离增大或缩小,都将导致质点的相对势能增加。
因此,在相同的温度条件下,晶体比非晶体的内能要小;相对于气体和液体来说,晶体的内能更小。
f.稳定性内能越小越稳定,晶体的稳定性是最小内能性的必然结果。
第七章晶体的点阵结构和晶体的性质附答案
第七章晶体的点阵结构和晶体的性质附答案《结构化学》补充习题第七章晶体的点阵结构和晶体的性质第十章次级键及超分子结构化学一、填空题1、晶体按对称性分共有___________个晶系;晶体的空间点阵形式共有_________种。
2、晶体的宏观对称操作集合构成______个对称类型,晶体的微观对称操作集合构成_______个空间群。
3、(312)晶面在a、b、c轴上的截距分别为______,______,______。
4、从CsCl晶体中能抽出________点阵,结构基元是。
5、NaCl晶体的空间点阵形式为___________。
6、范德华力又称范德华键,它主要有三方面的作用力组成:______力、_______力和__________力。
7、氢键与范德华力最大的区别是__________________________________。
答案:1、7, 14;2、32, 230;3、2a,6b, 3c;4、立方简单,Cs+或Cl-;5、立方面心,简单立方;6、静电,诱导,色散;7、氢键具有方向性和饱和性。
二、选择题1、X射线的产生是由于:············································································( )A、原子内层电子能级简单跃迁B、原子的价电子能级间的跃迁C、原子轨道能级间的跃迁D、分子转动能级间的跃迁2、有一AB晶胞中A和B原子的分数坐标为A(0,0,0),B(1/2,1/2,1/2),它属于:············( )A、立方体心点阵B、立方面心点阵C、立方底心点阵D、立方简单点阵3、(211)晶面表示了晶面在晶轴上的截距为:····················································( )A、2a,b,cB、a,2b,2cC、a,b,cD、2a,b,2cE、2a,2b,c4、与a轴垂直的面的晶面指标为:································································( )A、(112)B、(100)C、(010)D、(001)E、(111)5、晶体不可能属于的点群是:············································································( )A、D3hB、O hC、D5hD、T d6、分子间范德华力与分子间距离的关系正比于:····················································( )A、1/RB、1/R2C、1/R3D、1/R6答案:1、A;2、D;3、B;4、B;5、C;6、D 1。
材料化学 化工大学课后习题答案
第一章1、晶体一般的特点是什么?点阵和晶体的结构有何关系?答:(1)晶体的一般特点是:a 、均匀性:指在宏观观察中,晶体表现为各部分性状相同的物体b 、各向异性:晶体在不同方向上具有不同的物理性质c 、自范性:晶体物质在适宜的外界条件下能自发的生长出晶面、晶棱等几何元素所组成凸多面体外形d 、固定熔点:晶体具有固定的熔点e、对称性:晶体的理想外形、宏观性质以及微观结构都具有一定的对称性(2)晶体结构中的每个结构基元可抽象成一个点,将这些点按照周期性重复的方式排列就构成了点阵。
点阵是反映点阵结构周期性的科学抽象,点阵结构是点阵理论的实践依据和具体研究对象,它们之间存在这样一个关系:点阵结构=点阵+结构基元点阵=点阵结构-结构基元2、什么是同质多晶?什么是类质同晶?一些组成固定的化合物,由于其内部微粒可以以不同的方式堆积,因而产生不同种类的晶体,我们把这种同一化合组成存在两种或两种以上晶体结构形式的现象为同质多晶现象。
在两个或多个化合物中,如果化学式相似,晶体结构形式相同,并能互相置换的现象,我们称之为类质同晶现象。
3、产生晶体缺陷的原因是什么?晶体缺陷对晶体的物理化学性质的影响如何?答:晶体产生缺陷的原因主要有:(1)实际晶体中的微粒总是有限的;(2)存在着表面效应;(3)存在着表面效应;(4)粒子热运动;(5)存在着杂质。
在实际晶体中缺陷和畸变的存在使正常的点阵结构受到了一定程度的破坏或扰乱,对晶体的生长,晶体的力学性能、电学性能、磁学性能和光学性能等到都有很大的影响,在生产和科研中非常重要,是固体物理、固体化学和材料科学等领域的重要内容。
第二章1、晶体的结构特性是什么?这些特性是什么原因引起的?(1)晶体的均匀性:晶体的均匀性是焓因素决定的;非晶体的均匀性是由熵因素引起的。
(2)晶体的各向异性:由于晶体在各个方向上的点阵向量不同,导致了晶体在不同方向上具有不同的物理性质(3)晶体的自范性:在适宜的外界条件下,晶体能自发生长出晶面,晶棱等几何元素所转成的凸多面体,晶体的这一性质即为晶体的自范性。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
一、填空题 1.简单立方; Cs +和 Cl -; 4C 3 2.立方 P ,立方 I,立方 F ; 四方 P, 四方 I 。 3.旋转轴, 镜面,对称中心, 反轴; 旋转轴, 镜面,对称中心, 反轴,点阵, 螺旋轴,滑移面;n=1,2,3,4,6; 32 个; 七个晶系; 14 种空间点阵型式; 230 个空间群。 4.C1 ,C 2, C3 ,C4 , C6; I1=i, I2 =m,I4 。 5.32 个; 230 个 6.四方 I ; 四方 P 7.2a,6b,3c 8.247 pm 9.六方; D3h 10.7 11.14 12.32 13.晶胞参数 14.3,4,8,11,12 15.2,4,6,8,10 16.1,2,3,4,5 17.四方 8 18.Td 立方 4 个 C 3 19.D3h 六方
2
(3) 八面体空隙, 100%; (4) ○──○──○ | | | ● ● ● | | | ○──○──○
� c
� � a+b
15. (1) cF; (2) 111,200,220,311,222,400,331,420; (3) 564.0pm, 564.4pm,564.5pm;564.3pm; (4) 4. 16. A1 型堆积点阵型式为立方面心,第三对谱线对应于 220 衍射。 晶胞参数 a = 2 2r = 2 2 ×128.0pm = 362.0pm
d=
168.4 (411 ×10 ) × 6.023 × 10 23
-10 3
g·cm-3 =4.02g·cm-3
12 .应用 Laue 方程 , 可得衍 射 线 7 条 , 分别对 应 于 h=1,0,-1,-2,-3,-4, 和 -5 。衍射 方 向 α=39.3°,60°,76.9°,92.8°,108.8°,126.6°,150.4°。 13. (1) cF; (2) a=417.5 pm (3) 24.02 14. (1) 417.5pm; (2) 68.75pm;
6
20.2;4;2;4 21.略 22.点阵; 平移群的表达式。 二、选择题 1 .D 2. A 3. B 4. E 5 .C 12.B 13.D 三、计算题 1.a= 6.279×10-8cm N A= 6.08×1023mol-1 2.d100 = a= 597 pm d010 = b= 1247 pm d001 = c= 435.4 pm V= 3.31×108 pm3 4 个 3.s/mm θ (deg)=s/2 sin2 θ 37.8 18.9 0.1049 44.2 22.1 0.1415 63.8 31.9 0.2792 76.6 38.3 0.3841
da 3 N A 19.30g ⋅ cm −3 × (319.6 ×10 −10 cm ) 3 × 6.023 ×10 23 mol −1 = =2 M 189.9g ⋅ mol −1
属于 A2 型堆积。 平行于 C3 轴。 四、回答问题 1. (1) 立方 F (2) A 和 B (3) 4 个 (4) 4 组 (5)
a2=(
λ 2 ) ·(h2+k2 +l2); 2sin θ
a= 421 pm
晶胞中含有 4 个 M 和 4 个 O (3) MO 分子量为 40.23 金属原子 M 的相对原子质量为 40.23-16.00= 24.23 (4)氧原子采取立方面心 A1 型密堆积 (5)r+/r -=0.429, 则 0.414<0.429<0.732,金属原子 M 占据由 O2-围成八面体空隙中,其配位数 为 6 。 7.6.022094×1023 8.(1) 111, 200, 220, 222 (2) a= 570.5 pm (3) 对 111 反射, d111 = 5.705/ 3 pm = 329.4 pm
3a
(6) a/ 2 2.正交晶系有简单正交, 正交面心,正交体心, 正交底心,四种点阵型式。 3.晶胞的大小形状和晶胞中原子的坐标位置 ; 前者用晶胞参数 (a, b,c ,α, β,γ) 表示, 后者用原 子分数坐标 (x, y,z ) 表示。 4.(123) 5.立方 P: 1:2:3:4:5:6:8:9:...( 缺 7),没有系统消光。 立方 I: 1:2:3:4:5:6:7:8:...(有 7), h+k +l=奇数, 消光。 立方 F: 3:4:8:11:12:16:19:20:...(二密一稀),h, k, l 奇偶混合, 消光。 6.(1) AB (2) 立方 (3) 立方 F (4) AB (5) 4,4 (6) A:(1/2,1/2,1/2)(0,0,1/2),(0,1/2,0),(1/2,0,0) B:(0,0,0)(0,1/2,1/2),(1/2,0,1/2),(1/2,1/2,0) 7.(2) 立方 (3) 立方 F (4)AB 2
密度: d =
nM 4 × 63.54 g ⋅ mol −1 = = 8.89g ⋅ cm −3 3 −10 3 23 −1 a N A ( 362.0 ×10 cm) × 6.023 ×10 mol
17.根据 d =
ZM a3 N A
得 Z=
da 3 NA 8.906 g ⋅ cm−3 × (352.4 ×10 −10 ) 3 cm 3 × 6.023 × 1023 mol −1 = =4 M 58.70g ⋅ mol −1
4
(5)A:4 个 (0,0,0)(1/2,1/2,0),(0,1/2,1/2),(1/2,0,1/2) B:8 个 (1/4,1/4,1/4)(1/4,3/4,3/4),(3/4,1/4,3/4),(3/4,3/4,1/4) (3/4,3/4,3/4)(3/4,1/4,1/4),(1/4,3/4,1/4),(1/4,1/4,3/4)
sin θ =
λ 154.2pm h2 + k 2 + l 2 = ⋅ 2 2 + 22 + 0 2 = 0.6023 2a 2 × 362.0 pm
θ = 37 .04 �
2L = 4θ ⋅ π ⋅ R 4 × 37 .04 × 3.14 × 57.3mm = = 74.05mm 180� 2 ×180 �
6 .A
7 .B,C
8 .C
9 .E
10 .D
11. A,C,E
h 1 0 0 1
k 1 0 2 1
l 1 2 2 3
a/pm 412.3 409.9 412.7 412.6
1
80.8 40.4 0.4200 2 2 2 412.1 97.8 48.9 0.5679 0 0 4 409.2 110 55.0 0.6710 1 3 3 410.2 116 58.0 0.7192 0 2 4 406.0 2 由 sin θ之比知为立方面心点阵, a 平均值为 410.6 pm 。 4.(1) θ=11.15°; a= 1127.7 pm (2) Z =31.9≈32 5.根据相机半径得 θ= 13.69 deg 2dhklsinθ hkl= λ d111 = 325.6 pm a= 564.0 pm 2 2 6.(1)sin θi /sin θ1 为 3:4:8:11:12:16:19:20 晶体为立方面心结构。 (2)
5
该晶体的空间点阵型式为立方 I。 20.第二对衍射线对应的衍射指标为 200。 晶胞参数 a = 2 2r = 362.0pm
sin θ =
λ 154.2 pm h 2 + k 2 +l 2 = 2 2 + 02 + 02 = 0.4260 2a 2 × 362.0pm
θ = 25.21�
3
4θπR 4 × 25.21� × 3.14 × 57.3mm 2L = = = 50.42mm 180 � 2 ×180 �
摩尔体积
V=
Байду номын сангаас
NA 6.023 ×10 23 mol −1 V晶胞 = × ( 362.0 ×10 −12 m ) 3 = 7.143 ×10− 6 m 3 ⋅ mol −1 4 4
2L 2 L 180° = R (弧度 ) R π
21.根据 4θ =
θ=4
22. n =
2 L 180 4.972cm = × 57.3 = 23.96� R π 4 × 28.65mm
属 ccp,即立方最密堆积。 18. 2 L =
θ ⋅ 4πR 22.25 × 4π × 5 = cm = 7 .767 cm 180° 18
19. Z =
VDN A (3.157 × 10−8 )3 cm 3 × 19.1g ⋅ cm −3 × 6.02 × 1023 mol −1 = =2 M 183.92g ⋅ mol −1
θ= 13.53°
9.θ=
20 .77 弧度×57.3°/弧度=13.22° 2 × 45.0
10 . sin2 θ 分别 为 :0.0920,0.1840,0.2761,0.3681,0.4601,0.5519 和 0.7360, 这些 值 之 比 { 即 (h2+k2 +l2)之比}为 1:2:3:4:5:6:8, 因而该晶体的点阵型式是简单立方。 11.Cl -: (0,0,0); Cs +: (1/2,1/2,1/2)
