常见离子符号
常见的离子符号,化学式

铜 CuO 氧化亚铜 Cu2O氧化汞 HgO 二
氧化锰MnO2 氧化铁(又叫三氧化二铁)
Fe2O3 氧化铝(又叫三氧化二铝)
2.酸: 盐酸HCl 硫酸 碳酸 H2CO3 醋酸 CH3COOH 3.碱
H2SO4 硝酸 HNO3 亚硫酸 H2SO3
氢氧化钠 氢氧化钙 氢氧化铜 氢氧化铁
NaOH Ca(OH)2 Cu(OH)2 Fe氢(O氧H化)3钾 氢氧化钡 氢氧化镁
KCl NaCl MgCl2 AgCl CuCl2
氯化钙 氯化锌 氯化铁 氯化钡 氯化亚铁
氯化铝 AlCl3
c.碳酸盐
碳酸钙 氢钠
CaCO3
碳酸钡
碳酸钠 Na2CO3 NaHCO3 碳酸钾 碳酸氢铵
BaCO3 K2CO3 NH4HCO3
碳酸
d.硝酸盐
硝酸银
硝酸钠
硝酸铜 硝
酸钡
AgNO3 NaNO3 Cu(NO3)2
常见的离子符号
氢离子、 钠离子、钾离子、镁离子、钙离子、铝离子
H+
Na+
K+
Mg2+
Ca2+
Al3+
铁离子. 亚铁离子 . 氯离子. 氧离子.
Fe3+、 Fe2+
Cl-、 O2-、
钡离子 铜离子 银离子 锌离子
硫离子. S2-、
;
Ag+
Zn2+
CO32氢氧根离子 硫酸根离子、 硝酸根离子 铵根离子
KOH
Ba(OH)2
Mg(OH)2
4.盐
a.硫酸盐
硫酸亚铁 硫酸铁 硫酸铝 硫酸钾 硫酸铵
FeSO4 Fe2(SO4)3 Al2(SO4)3 K2SO4 (NH4)2SO4 硫酸钠 硫酸锌 硫酸镁 硫酸铜 硫酸钡 Na2SO4 ZnSO4 MgSO4 CuSO4 BaSO4
初中化学离子符号大全

初中化学离子符号大全1. 氢离子,H+。
氢离子是最简单的离子之一,它是一个带正电荷的离子,由一个质子组成。
在化学反应中,氢离子可以与其他离子或分子结合,形成各种化合物。
2. 氧离子,O2-。
氧离子是带有负电荷的离子,它通常与金属元素结合形成氧化物。
氧离子在自然界中广泛存在,是许多化合物的重要组成部分。
3. 氯离子,Cl-。
氯离子是氯元素失去一个电子后形成的带负电荷的离子,它是常见的阴离子之一。
氯离子可以与钠离子结合形成氯化钠,也就是我们常说的食盐。
4. 钠离子,Na+。
钠离子是钠元素失去一个电子后形成的带正电荷的离子,它是常见的阳离子之一。
钠离子在生活中有着广泛的应用,比如在食盐生产、金属加工等领域。
5. 氮离子,N3-。
氮离子是氮元素失去三个电子后形成的带负电荷的离子,它在化学反应中起着重要的作用。
氮离子可以与氢离子结合形成氨气,也可以与氧离子结合形成硝酸盐等化合物。
6. 铁离子,Fe2+、Fe3+。
铁离子是铁元素失去两个或三个电子后形成的离子,它们分别带有2+和3+的电荷。
铁离子是许多生物体内重要的金属离子,也是许多化合物的重要组成部分。
7. 氧化氢离子,OH-。
氧化氢离子是氢氧化物中的主要离子之一,它是带有负电荷的离子。
氧化氢离子在化学反应中起着重要的中和作用,也是许多碱性物质的组成部分。
8. 氟离子,F-。
氟离子是氟元素失去一个电子后形成的带负电荷的离子,它是非常活泼的阴离子。
氟离子在生活中有着广泛的应用,比如在牙膏中的氟化物可以预防蛀牙。
以上就是初中化学离子符号大全,希望对大家有所帮助。
掌握这些离子的符号和性质,可以帮助我们更好地理解化学反应和化合物的形成,也为进一步学习化学打下坚实的基础。
希望大家能够认真学习,加强练习,取得更好的成绩。
常见的离子符号,化学式

氢气H2 氧气 O2 氮气 N2 氯气 Cl2 溴
二.化合物 1.氧化物:
水 H2O 双氧水H202 二氧化碳 CO2
一 氧化碳 CO 二氧化硫SO2 二氧化氮
NO2 二氧化硅SiO2 五氧化二磷 P2O5
氧化钾K2O
氧化钙 CaO 氧化钠
Na2O 氧化镁 MgO
氧化锌
ZnO 氧化亚铁FeO 四氧化三铁Fe3O4 氧化
KOH
Ba(OH)2
Mg(OH)2
4.盐
a.硫酸盐
硫酸亚铁 硫酸铁 硫酸铝 硫酸钾 硫酸铵
FeSO4 Fe2(SO4)3 Al2(SO4)3 K2SO4 (NH4)2SO4 硫酸钠 硫酸锌 硫酸镁 硫酸铜 硫酸钡 Na2SO4 ZnSO4 MgSO4 CuSO4 BaSO4
b.盐酸盐(氯化物)
氯化钾 氯化钠 氯化镁 氯化银 氯化铜
谢 谢!
让我们共同进步
铜 CuO 氧化亚铜 Cu2O氧化汞 HgO 二
氧化锰MnO2 氧化铁(又叫三氧化二铁)
Fe2O3 氧化铝(又叫三氧化二铝)
2.酸: 盐酸HCl 硫酸 碳酸 H2CO3 醋酸 CH3COOH 3.碱
H2SO4 硝酸 HNO3 亚硫酸 H2SO3
氢氧化钠 氢氧化钙 氢氧化铜 氢氧化铁
NaOH Ca(OH)2 Cu(OH)2 Fe氢(O氧H化)3钾 氢氧化钡 氢氧化镁
OH-
SO42- 、
NO3-、
NH4+
常见物质的化学式
一.单质
1.金属单质:
钾 K 钙 Ca 钠 Na 镁 Mg 铝Al 锌 Zn 铁Fe 锡 Sn 铅 Pb 铜 Cu 汞Hg 银 Ag 铂 Pt 金
Au
2、稀有气体:氦气 He 气Ar
初中化学常见的离子符号及化学用语的含义

初中化学离子符号及化学用语的含义常见离子名称和符号:氢离子:H+;钠离子:Na+;钾离子:K+;银离子:Ag+;铵根离子:NH4+;镁离子:Mg2+;钙离子:Ca2+;铜离子:Cu2+;亚铁离子:Fe2+;钡离子:Ba2+;锌离子:Zn2+;铝离子:A13+;铁离子:Fe3+;氯离子:C1-;氟离子:F-;氢氧根离子:OH-;硝酸根离子:NO3-碳酸根离子:CO32-;硫酸根离子:SO42-;硫离子:S2-;氧离子:O2-化学用语的含义:一、元素符号、化学式、离子符号前面..的数字表示几个某原子或几个某分子或几个某离子:例:下列符号中“2”所表示的含义:2SO3:表示2个三氧化二硫分子2H:表示2个氢原子2.SO42-:表示2个硫酸根离子二、元素符号右下角...的数字表示一个某分子中含几个某原子:例:下列符号中“2”的含义:SO2:表示一个二氧化硫分子中含有2个氧原子H2:表示一个氢气分子中含有2个氢原子三、元素符号右上角...的数字表示某离子带几个单位正(负)电荷(数字先写,正负号后写,1可省略)如H-、NO3-:例:下列符号中“2”的含义:CO32-:表示碳酸根离子带2个单位负电荷Ca2+:表示钙离子带2个单位正电荷SO42-:表示硫酸根离子带2个单位负电荷四、元素符号正上方...的数字表示某物质中某元素的化合价(正负号先写,数字后写,1不能省略);+1 -2如: H2O; H2SO4;例:下列符号中“2”的含义:+2CuSO4:表示硫酸铜中铜元素的化合价为+2价-2CO:表示一氧化碳中氧元素的化合价为-2价+2BaCO3:表示碳酸钡中钡元素的化合价为+2价离子符号中,数字表示电荷数目,正负号表示电性。
常见的离子符号
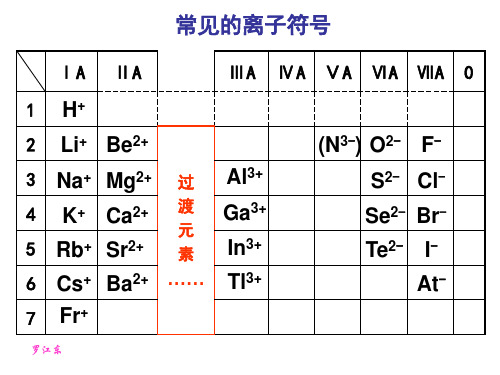
ⅠA 1 2 3 4 5 6 7 ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0
H+ Li+ Be2+ Na+ Mg2+ K+ Ca2+ Rb+ Sr2+ Fr+
过 渡 元 素(N3-)源自O2- F-Al3+ Ga3+ In3+ Tl3+
S2- ClSe2- BrTe2-
IAt-
Cs+ Ba2+ ……
罗江东
重要阳离子: 银离子)、 铵离子) 重要阳离子: Ag+ (银离子 、 NH4+ (铵离子 、 银离子 铵离子 锌离子) 亚铁离子, 锌离子 亚铁离子 、 Zn2+ (锌离子 、 Fe2+ (亚铁离子, 浅绿 色)、 铜离子, 铁离子, 铜离子 铁离子 Cu2+ (铜离子, 蓝 色) 、 Fe3+ (铁离子, 黄 色) 重要阴离子: OH- (氢氧根 、 NO3- (硝酸根 、 氢氧根) 硝酸根) 重要阴离子: 氢氧根 硝酸根
MnO4- (高锰酸根, 紫红 色)、 高锰酸根, 高锰酸根 、
CO32-(碳酸根 、 SO32- (亚硫酸根 、 碳酸根) 亚硫酸根) 碳酸根 亚硫酸根 SO42- (硫酸根 、 PO43- (磷酸根 硫酸根) 磷酸根) 硫酸根 磷酸根
罗江东
常见的离子符号,化学式

2.酸:
盐酸HCl 硫酸
碳酸
H2CO3
醋酸 CH3COOH
3.碱
H2SO4 硝酸 HNO3 亚硫酸 H2SO3
氢氧化钠 氢氧化钙 氢氧化铜 氢 氧化铁
NaOH
Ca(OH)2
Cu(OH)2
Fe氢 镁(OK氧HO)H化3 钾
氢氧化钡 Ba(OH)2
硝酸钠
硝酸铜 硝
Hale Waihona Puke 酸钡AgNO3 NaNO3 Cu(NO3)2 Ba(NO3)2 硝酸钾 硝酸铵 硝酸镁 硝酸铝
KNO3 NH4NO3
Mg(NO3)2
硝酸铁 硝酸亚铁
Al(NO3)3
Fe(NO3)3 Fe(NO3)2
钾盐:
高锰酸钾 KMnO4 锰酸钾 K2MnO4 氯酸钾KClO3
SUCCESS
THANK YOU
氢气H 氧气 O 氮气 N 氯气 Cl 溴Br
二.化合物 1.氧化物:
水 H2O
双氧水H202 二氧化碳 CO2
一 氧化碳 CO 二氧化硫SO2 二氧化氮
NO2 二氧化硅SiO2 五氧化二磷 P2O5 氧化
钾K2O 氧化钙 CaO 氧化钠 Na2O
氧化镁 MgO
氧化锌ZnO 氧化
亚铁FeO 四氧化三铁Fe3O4 氧化铜 CuO 氧 化亚铜 Cu2O氧化汞 HgO 二氧化锰MnO2
氢氧化
Mg(OH)2
4.盐
a.硫酸盐
硫酸亚铁 硫酸铁 硫酸铝 硫酸钾 硫酸铵 FeSO4 Fe2(SO4)3 Al2(SO4)3 K2SO4 (NH4)2SO4
硫酸钠 硫Na酸2S钡O4
化学用语
化 学 用 语一、常见离子符号氢离子H + 钠离子Na + 钙离子 Ca 2+ 铝离子 Al 3+ 硫离子 S 2- 氯离子 Cl - 钾离子K + 镁离子 Mg 2+ 钡离子 Ba 2+ 亚铁离子 Fe 2+ 铁离子Fe 3+ 铜离子 Cu 2+硫酸根离子SO 42- 碳酸根离子 CO 32- 硝酸根离子NO 3- 氢氧根离子 OH -铵根离子 NH 4+ 二、化学式水H 2O 二氧化碳 CO 2 五氧化二磷P 2O 5 四氧化三铁 Fe 3O 4 二氧化硫SO 2 氧化铁 Fe 2O 3 氧化铝Al 2O 3 氧化镁MgO 氧化亚铁FeO 双氧水H 2O 2 氢氧化钠NaOH 氢氧化钙Ca(OH)2 氯化钠 NaCl 碳酸钠Na 2CO 3 硫酸铁 Fe 2(SO 4)3 硫酸铜 CuSO 4 氯化锌ZnCl 2 氯化镁 MgCl 2 硫酸锌 ZnSO 4 硫酸镁 MgSO 4 硫酸亚铁FeSO 4 碳酸钙CaCO 3 硝酸银 AgNO 3 氯化铵NH 4Cl 高锰酸钾 KMnO 4 氯酸钾KClO 3三、化学方程式1. 磷在空气(氧气)中燃烧 4P + 5O 2 2P 2O 52. 硫在空气(氧气)中燃烧 S +O 2 SO 23. 碳在空气(氧气)中燃烧 C +O 2 CO 24. 镁在空气(氧气)中燃烧 2Mg + O 2 2MgO5. 铁在氧气中燃烧 3Fe + 2O 2 Fe 3O 46. 氢气燃烧 2H 2 + O 2 2H 2O7. 紫黑色固体(高锰酸钾)制氧气 2KMnO 4 K 2MnO 4 + MnO 2 +O 2↑8. 过氧化氢制氧气 2H 2O 2 2H 2O +O 2↑9. 白色固体(氯酸钾)和黑色固体(MnO 2)制氧气 2KClO 32KCl + 3O 2↑ 10. 水的电解 2H 2O 2H 2↑+ O 2↑ 11. 实验室制氢气 Zn + H 2SO 4(稀) === ZnSO 4 + H 2↑12. 氢气还原氧化铜 H 2 + CuO Cu + H 2O 13. 铁与硫酸铜的反应 Fe + CuSO 4 === FeSO 4 + Cu14. 碳酸钠与盐酸的反应 Na 2CO 3 + 2HCl === 2NaCl + H 2O +CO 2↑15. 硫酸铜与氢氧化钠的反应 CuSO 4 + 2NaOH === Cu(OH)2 ↓+ Na 2SO 4点燃点燃点燃点燃点燃点燃△MnO 2 △ MnO 2通电△。
离子的五大原子符号
离子的五大原子符号离子的五大原子符号1. Na+ :钠离子2. Cl^- :氯离子3. Ca2+ :钙离子4. Fe3+ :铁离子5. Mg2+ :镁离子离子是带电的原子或原子团,其带电性质是由失去或获得电子而形成的。
原子中的电子带有负电,当原子失去或获得电子时,就会形成正离子或负离子。
在化学中,离子扮演着至关重要的角色。
离子的形成可以导致物质在化学反应中的电荷变化,从而影响物质的性质和反应过程。
下面将逐一介绍离子的五大原子符号。
1. Na+ - 钠离子:钠离子是最常见的正离子之一,在化学中以Na+表示。
它是由钠原子在化学反应中失去一个电子而形成的。
钠离子在体内起着重要作用,维持着电解质平衡,调节神经和肌肉功能。
2. Cl^- - 氯离子:氯离子是最常见的负离子之一,以Cl^-表示。
它是由氯原子在化学反应中获得一个电子而形成的。
氯离子广泛存在于盐和海水中,起着维持酸碱平衡和细胞膜电位的关键作用。
3. Ca2+ - 钙离子:钙离子是带有2个正电荷的离子,以Ca2+表示。
钙是人体中的重要元素,它在骨骼和牙齿的形成中起着重要作用。
钙离子还参与维持神经传递、肌肉收缩和血液凝固等生理过程。
4. Fe3+ - 铁离子:铁离子是带有3个正电荷的离子,以Fe3+表示。
铁是一种重要的微量元素,对红细胞的氧气运输至关重要。
铁还参与体内的许多生化反应,包括DNA合成和能量代谢。
5. Mg2+ - 镁离子:镁离子是带有2个正电荷的离子,以Mg2+表示。
镁是人体中第四丰富的阳离子,它对骨骼的健康和肌肉功能的正常运作至关重要。
镁离子还参与许多细胞反应和酶催化的过程。
以上介绍了离子的五大原子符号及其重要性。
离子在化学和生命科学中具有广泛的应用,它们的形成和性质对于理解物质的特性和反应机制非常重要。
希望本篇文章能够为你提供对离子概念的全面理解,并对离子的五大原子符号有更深入的了解。
参考资料:1. Lide, D. R. (2004). Handbook of chemistry and physics. CRC press.2. Nelson, D. L., Cox, M. M., Lehninger, A. L., & Lehninger Principles of Biochemistry. (2017). W. H. Freeman.3. Berg, J. M., Tymoczko, J. L., & Gatto, G. J. (2018). Stryer's biochemistry. Macmillan.4. Marye, P. K., Gallagher, R. J., Routh, R. L., & Boyle, W. S. (1963). Ionic radii for the Fe3+ and Mg2+ ions. The Journal of Chemical Physics, 39(2), 482-487.1. 我们都知道,化学和物理是自然科学的重要分支之一。
