化学反应工程(第三版)
化学反应工程(第三版)陈甘棠主编第八章气液两相反应器PPT课件

(8-14)
定常态操作时,单位界面上反应量等于扩散通量,即
NA(rA )d SA n dtD LA ddA czz0
将A的浓度分布对z求导后代入上式得
式中,
N A( rA )D L LA cA 1 i b D L L D c B c B A AL i kLc A Ai
k LA
DLA L
,称为液膜传质系数。
(8-16)
1 DLBcBL bDLAcAi
,称为瞬间反应的增强系数。物理意义是气
液反应条件下组分A的消失速率与最大物理吸收速率 kLAcAi 之比。 13
式(8-15)中cAi是界面浓度,难以测定,工程设计中通常将 其换算为容易测量的pA来表示的反应速率。因为,
N AkG(A p Ap A)i( rA )kLc A A 1 ib D L L D c c B B A A L i
第八章 气液两相反应器
1
整体概况
概况一
点击此处输入 相关文本内容
01
概况二
点击此处输入 相关文本内容
02
概况三
点击此处输入 相关文本内容
03
2
8.1 概述
气-液相反应是一类重要的非均相反应。主要分为二种类型: (1)化学吸收: 原料气净化、产品提纯、废气处理等。 (2)制取化工产品
a.
b.
c.
(淤浆床)
A ( g b) l) B P(( r A ) k A c B c
定常态条件下,在单位面积的液膜中取一厚度为dz的微元层,对组分
A作物料衡算:
D Ld A dAc z( rA )d z D Ld A d c zAd dAc d z z
整理得
DLAdd2cz2A kcAcB 0
化学反应工程(第三版)陈甘棠主编_第五章_催化剂与催化动力学基础
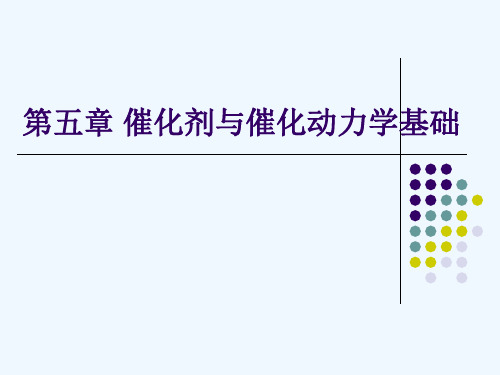
Ki 称为吸附平衡常数,是i组分吸附速率常数与脱附速率常数之比。 式(5-28)即为过程的总速率方程。由该式的分母可知,反应物和产物 均被吸附。分母的方次表明该反应是在A、B两个活性中心之间进行的。
若控制步骤为可逆反应 过程总速率:
Aσ + Bσ
k1
k2
Rσ + Sσ
r k k A 1 A B 2 R S
第五章 催化剂与催化动力学基础
5.1 催化剂
能够改变化学反应速率而本身在反应前后不发生组成变化的物质。 (1)类型 金属(良导体)、金属氧化物和硫化物(半导体)以及盐类和 酸性催化剂(大多数是绝缘体) (2)载体 活性炭、硅胶、活性白土、硅藻土、沸石(分子筛)、骨架Ni、 活性Al2O3、 Fe等 (3)性能要求 活性好、选择性高、寿命长。 (4)结构
k k K K 1 A B
K
k1K A KB k2 KR KS
比较式(5-28)和式(5-30)可见,表面反应为控制步骤时,可逆反 应与不可逆反应速率式的分母相同,区别在于分子。可逆反应的分子上有两 项,不可逆反应只有一项。
A在吸附时解离 A + 2σ B + σ 2A1/2σ + Bσ Rσ Sσ 按上述方法可得到
几种常用催化剂的结构
无定形颗粒 球形 柱形 长柱形 三叶草形
环形
多孔柱形 车轮形
比表面积
破碎强度
压降
独石形
金属独石形
Foam
(5)制备方法
① 混合法
② 浸渍法 ③ 沉淀法或共沉淀法 ④ 共凝胶法 ⑤ 喷涂法及滚涂法 ⑥ 溶蚀法 ⑦ 热熔法
5.3 气固相催化反应动力学
气-固相反应速率的定义式
化学反应工程教案
化学反应工程课程教案课次17课时 2 课型(请打√)理论课√讨论课□实验课□习题课□其他□授课题目(教学章、节或主题):第7章气固相催化反应流化床反应器7、3流化床反应过程的计算教学目的、要求(分掌握、熟悉、了解三个层次)::1、掌握流化床的基本概念;2、掌握流化床的工艺计算;教学重点及难点:重点:固定床催化反应器的特点、类型和设计要求。
难点:一维拟均相理想流动模型对反应器进行设计计算、教学基本内容方法及手段7、1流化床的基本概念流态化现象:使微粒固体通过与气体或液体接触而转变成类似流体的操作。
固体颗粒层与流体接触的不同类型:7、1、1流化床的基本概念1)当通过床层的流体流量较小时,颗粒受到的升力(浮力与曳力之和)小于颗粒自身重力时,颗粒在床层内静止不动,流体由颗粒之间的空隙通过。
此时床层称为固定床。
讲解2)随着流体流量增加,颗粒受到的曳力也随着增大、若颗粒受到的升力恰好等于自身重量时,颗粒受力处于平衡状态,故颗粒将在床层内作上下、左右、前后的激烈运动,这种现象被称为固体的流态化,整个床层称为流化床、曳力(表面曳力、形体曳力)曳力是流体对固体的作用力,而阻力是固体壁对流体的作用力,两者是作用力与反作用力的关系。
表面曳力由作用在颗粒表面上的剪切力引起,形体曳力由作用在颗粒表面上的压强力扣除浮力部分引起、3)。
流化床类似液体的性状(a) 轻的固体浮起;(b)表面保持水平;(c)固体颗粒从孔中喷出;(d)床面拉平;(e)床层重量除以截面积等于压强流化床的优点(1) 颗粒流动类似液体,易于处理、控制;(2) 固体颗粒迅速混合,整个床层等温;(3) 颗粒能够在两个流化床之间流动、循环,使大量热、质有估计在床层之间传递;(4) 宜于大规模操作;(5) 气体和固体之间的热质传递较其它方式高;(6) 流化床与床内构件的给热系数大、浓相段和稀相段(P185-186)1)、当流体通过固体床层的空塔速度值高于初始流化速度但低于逸出速度(p188),颗粒在气流作用下悬浮于床层中,所形成的流固混合物称为浓相段。
化学反应工程第三版答案

化学反应工程第三版答案【篇一:化学反应工程试卷3答案】xt>的_温度_梯度和_浓度_梯度。
11、对于气-固系统的流化床反应器的粗颗粒系统,气速超过起始流化速度后,就出现气泡,气速愈高,气泡的聚并及造成的扰动亦愈剧烈,使床层波动频繁,这种流化床2014级化学工程与工艺(本)称为_聚式流化床_。
《化学反应工程》试卷312、当前用于描述气-液两相流相间传质的模型有两大类:一是按稳态扩散来处理的_双膜模型_;一是按非稳态扩散处理模型,如溶质渗透模型和表面更新模型。
13、活化能的大小直接反映了_反应速率_对温度的敏感程度。
14、生成主产物的反应称为_主反应__,其它的均为副反应。
15、固定床中颗粒的体积相当直径定义为具有相同体积vp的球粒子直径,表达式dv=__(6vp/1、不论是设计、放大或控制,都需要对研究对象作出定量的描述,也就要用数学式来表1/3_。
达个参数间的关系,简称_数学模型_。
二、单项选择题(选择正确的答案,将相应的字母填入括号中每题??nk0?nk2分,共30分)k1、对于气-液相反应几乎全部在液相中进行的极慢反应,为提高反应速率,应选用___c____2、着眼反应组分k的转化率的定义式为_nk0_。
装置。
3、理想反应器是指全混流反应器、平推流反应器。
a. 填料塔b. 喷洒塔c. 鼓泡塔d. 搅拌釜4、具有良好搅拌装置的釜式反应器按全混流反应器处理,而管径小,管子较长和流速?d??kmdtdci?d较大的管式反应器按平推流反应器处理。
2、催化剂在使用过程中会逐渐失活,其失活速率式为,当平行失活对dq反应物有强内扩散阻力时,d为__c__。
rdq5、全混流反应器稳定的定常态操作点的判据为qg?q?gra. ≈0 b. =1 c. →3 d. ≈1、 ,dtdt 3、不属于气固相催化反应固定床反应器拟均相二维模型的特点是__a__。
6、平推流反应器的返混为____0___。
a. 粒子与流体间有温度差b. 粒子与流体间无温度差7、一个可逆的均相化学反应,如果正、逆两向反应级数为未知时,采用_初始速率法_c. 床层径向有温度梯度d. 床层轴向有温度梯度 4、属于气固相催化反应固定床反应器拟均相二维模型的特点是___a____。
化学反应工程(第三版)陈甘棠主编共92页文档

1、战鼓一响,法律无声。——英国 2、任何法律的根本;不,不成文法本 身就是 讲道理 ……法 律,也 ----即 明示道 理。— —爱·科 克
3、法律是最保险的头盔。——爱·科 克 4、一个国家如果纲纪不正,其国风一 定颓败 。—— 塞内加 5、法律不能使人人平等,但是在法律 面前人 人是平 等的。 ——波 洛克
谢谢!
61、奢侈是舒适的,否则就不是奢侈 。——CocoCha nel 62、少而好学,如日出之阳;壮而好学 ,如日 中之光 ;志而 好学, 如炳烛 之光。 ——刘 向 63、三军可夺帅也,匹夫不可夺志也。 ——孔 丘 64、人生就是学校。在那里,与其说好 的教师 是幸福 ,不如 说好的 教师是 不幸。 ——海 贝尔 65、接受挑战,就可以享受胜利的喜悦 。——杰纳勒 尔·乔治·S·巴顿
化学反应工程第三版课后答案

化学反应工程第三版课后答案【篇一:化学反应工程第二版课后习题】> 2何谓基元反应?基元反应的动力学方程中活化能与反应级数的含义是什么?何谓非基元反应?非基元反应的动力学方程中活化能与反应级数含义是什么? 345现有如下基元反应过程,请写出各组分生成速率与浓度之间关系。
(1)a+2b?c a+c? d (2)a+2b?c b+c?d c+d→e (3)2a+2b?ca+c?d10mkmols。
现以气相分压来表示速率方程,即(?ra)=kppapb,求kp=?(假定气体为理想气体)46-2-12化学反应式与化学计量方程有何异同?化学反应式中计量系数与化学计量方程中的计量系数有何关系?若将反应速率写成?ra??dcadt,有什么条件?为什么均相液相反应过程的动力学方程实验测定采用间歇反应器? 78反应a(g) +b(l)→c(l)气相反应物a被b的水溶液吸收,吸收后a与b生成c。
反应动力学方程为:?ra=kcacb。
由于反应物b在水中的浓度远大有一反应在间歇反应器中进行,经过8min后,反应物转化掉80%,经过18min后,转化掉90%,求表达此反应的动力学方程式。
反应2h2?2no?n2?2h2o,在恒容下用等摩尔h2,no进行实验,测得以下数据总压/mpa 半衰期/s10 考虑反应a?3p,其动力学方程为?ra??容下以总压表示的动力学方程。
11 a和b在水溶液中进行反应,在25℃下测得下列数据,试确定该反应反应级数和反应速度常数。
116.8 319.8 490.2 913.8 1188 时间/s-312 丁烷在700℃,总压为0.3mpa的条件下热分解反应:c4h10→2c2h4+h2 (a) (r)(s)起始时丁烷为116kg,当转化率为50%时?dprdnsdya,?。
dtdtdtdpadt?0.24mpa?s?13-1-1-3-33-10.0272265 0.0326 186 0.0381 135 0.0435 104 0.0543 67求此反应的级数。
反应工程第三版第八章答案

第八章习题1. 以25℃的水用逆流接触的方法吸收空气中的CO 2,试求在操作时(1) 气膜和液膜的相对阻力是多少?(2) 采用哪种最简单形式的速率方程来设计计算吸收塔。
已知CO 2在空气和水中的传质数据如下: k AG =0.789mol·hr -1·m -2·kPa -1 k AL =0.025m·h -1H A =0.329mol·m -3·kPa -1 解74.24000417.004.019.3039789.01251111110139.8596.121267.11259.3039789.01111AAL AL AL 3ALA AGAG =+=⨯+=+=⨯=+=+=+=-H k k K k H k K总阻力:122.863 气膜1.267,占1.03% 液膜121.596 占98.97% 总阻力:0.040417 气膜0.000417 占1.03% 液膜0.04 占98.97% 所以忽略气膜阻力()⎪⎪⎭⎫ ⎝⎛-=-=-=-AL A AG AL AAAG AI AL AI AL Ad d d d c H p S k t n H p c c c S k tn2. 若采用NaOH 水溶液吸收空气中的CO 2,反应过程属瞬间反应CO 2+2OH -=2H 2O+CO 32-吸收温度为25℃(题1数据可用),请计算:(1) 当p CO2=1.0133kPa ,c NaOH =2mol·L -1时的吸收速率; (2) 当p CO2=20.244kPa ,c NaOH =0.2mol·L -1时的吸收速率; (3) 他们与纯水吸收CO 2比较,速率比是多少? 解 (1)2 12AG AG AAI 0BL BL 3BL 3AGBL AL AL AG A B 0BL h m mol 8.00133.1789.0d d 0m kmol 2m kmol 064.00133.125789.012----⋅⋅=⨯==-∞→=>⋅=⋅=⨯⎪⎭⎫ ⎝⎛⎪⎭⎫ ⎝⎛--=⎪⎪⎭⎫ ⎝⎛⎪⎪⎭⎫ ⎝⎛⎪⎪⎭⎫ ⎝⎛=p k tn p c c c p D D k k c βαα((2)12AL A AG A 3AIBL AL BLB A 3A AI AI BL 0BL 3BL 3AG BLAL ALAG A B 0BL h m mol 285.2244.20015.16259.3039789.01111d d 015.161066.62.012111066.69.303920244m kmol 2.0m kmol 28.1244.2025789.012------⋅⋅=⨯⨯+=+=-=⎪⎭⎫ ⎝⎛⨯⎪⎭⎫ ⎝⎛--+=⎪⎪⎭⎫ ⎝⎛⎪⎪⎭⎫ ⎝⎛⎪⎪⎭⎫⎝⎛+=⨯===>⋅=⋅=⨯⎪⎭⎫ ⎝⎛⎪⎭⎫ ⎝⎛--=⎪⎪⎭⎫ ⎝⎛⎪⎪⎭⎫⎝⎛⎪⎪⎭⎫ ⎝⎛=βααβααk H k t n c c D D H p c c c c p D D k k c (3) 纯水吸收CO 2时,β =1 p =1.0133kPa 时,纯水00825.0259.3039789.010133.1d d A=+=-tn用NaOH 吸收8.0d d A =-t n速率比为0.8/0.00825=97纯水吸收CO 2时, p =20.244kPa 时,纯水1648.0259.3039789.01244.20d d A=+=-tn速率比为2.285/0.1648=13.873. 用纯水分别吸收氮气中的NH 3,以及CO 和O 2,已知在操作温度(10℃)下NH 3的溶解度系数H A =990mol·m -3·kPa -1;CO 、O 2溶解度系数H A =9.9×10-3 mol·m -3·kPa -1。
《化学反应工程》第三版(陈甘堂著)课后习题答案

《化学反应工程》第三版(陈甘堂著)课后习题答案第二章均相反应动力学基础2-4三级气相反应2NO+O22NO2,在30℃及1kgf/cm2下反应,已知反应速率常数2kC=2.65×104L2/(mol2 s),若以rA=kppApB表示,反应速率常数kp应为何值?解:原速率方程rA=dcA2cB=2.65×104cAdt由气体状态方程有cA=代入式(1)2-5考虑反应A课所以kp=2.65×104×(0.08477×303) 3=1.564后当压力单位为kgf/cm2时,R=0.08477,T=303K。
答p p 2rA=2.65×10 A B =2.65×104(RT) 3pApBRT RTp表示的动力学方程。
解:.因,wwnAp=A,微分得RTVdaw案24网pAp,cB=BRTRT3P,其动力学方程为( rA)=dnAn=kA。
试推导:在恒容下以总压VdtVδA=3 1=21dnA1dpA=VdtRTdt代入原动力学方程整理得wdpA=kpAdt设初始原料为纯A,yA0=1,总量为n0=nA0。
反应过程中总摩尔数根据膨胀因子定义δA=n n0nA0 nA若侵犯了您的版权利益,敬请来信通知我们!Y http://.cn.co(1)mol/[L s (kgf/cm2) 3]m(1)则nA=nA01(n n0)δA1(P P0)δA(2)恒容下上式可转换为pA=P0所以将式(2)和式(3)代入式(1)整理得2-6在700℃及3kgf/cm2恒压下发生下列反应:C4H10发生变化,试求下列各项的变化速率。
(1)乙烯分压;(2)H2的物质的量,mol;(3)丁烷的摩尔分数。
解:P=3kgf/cm2,(1)课MC4H10=58,(2)w.krC2H4=2( rC4H10)=2×2.4=4.8kgf/(cm2 s)PC4H10=PyC4H101 dpC4H10= P dt2.4-1==0.8 s 3w(3)nC4H10=nyC4H10=n0(1+δC4H10yC4H10,0xC4H10)yC4H10dnH2dtdnH2dt=hdaw后n0=nC4H10,0=δC4H10rC4H10=反应开始时,系统中含C4H*****kg,当反应完成50%时,丁烷分压以2.4kgf/(cm2 s)的速率dyC4H10dt答1rCH=2.4224wdnC4H10dt案116×1000=2000mol582+1 1==21网dyC4H10=n0(1+δC4H10yC4H10,0xC4H10) dt=2000×(1+2×1×0.5)×0.8=3200 mol/s若侵犯了您的版权利益,敬请来信通知我们!Y http://.cno2C2H4+H2,dP=k[(δA+1)P0 P]=k(3P0 P)dtm(3)dpA1dP= dtδAdt2-9反应APS,( r1)=k1cA , ( r2)=k2cp,已知t=0时,cA=cA0 ,cp0=cS0=0, k1/k2=0.2。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
(4)若单一反应的各计量系数满足 i 0
反应。
,则称为等分子
2.1 基本概念及术语
2.1-2 反应速率的定义
单位时间、单位反应容积内着眼组分K的物质的量的变化。
对单一反应
A
P
反应物A消耗速率
rA
dnA Vdt
恒容过程
rA
dcA dt
产物生成速率 注意:
rP
dnP Vdt
恒容过程
(3)k是反应速率常数,反映了反应温度对反应速率的影响。
Arrhenius式
E
k k0e RT
式中,E是反应活化能,表示反应速率对反应温度的敏感程
度。
升高温度,k总是增大的,但增大幅度与E值大
小有关。
T↑,有利于E值大的反应;T↓,有利于E值小
的反应。
2.1.2 均相反应动力学方程
解:将Arrhenius式取对数,则有
MPa h1 Leabharlann MPa)2 [MPa h]1
(2)设气体服从理想气体状态方程,则
pA
nA
RT V
cART
dpA dt
dnA dt
RT V
3.709(cART)2
dnA Vdt
3.709RTcA2
k 3.709 8.314 103 400 12.34 [l / mol h]
得
dnA Vdt
12.34cA2
[mol/L h]
2.2 单一反应速率式的解析
反应速率的定义式是微分式,将其与动力学方程关联并积分,可
得到反应物浓度随时间变化的关系。该过程称为反应速率式的解析。
本节介绍等温、恒容、间歇操作条件下单一反应速率式的解析。
2.2-1 不可逆反应
一、一级不可逆反应
yK
nK n
n0 yK 0 (1 xK )
n0 (1 K yK 0 xK )
yK 0 (1 xK )
1 K yK0xK
(2-1-19)
注意:不同反应物的膨胀因子值不同,使用时必须注明下标。
2.1 基本概念及术语
例 计算下列气相反应的膨胀因子 1. A+B→P+S 2. A→P+S 3. A+3B→2P
例:在反应温度为400K时,某气相反应的速率方程为
dpA dt
3.709
p
2 A
MPa/h
问:(1)速率常数的单位是什么?
(2)如速率表达式为
(rA )
dnA Vdt
k cA2
速率常数等于多少?
mol/l h
dpA dt
3.709 pA2
MPa/h
解:(1)k的单位是
[k]
第二章 均相反应动力学基础
均相反应:参与反应的各物质都处于同一个相内 进行的化学反应。
均相反应动力学:研究各种因素如温度、催化剂、 反应物组成和压力等对反应速率、反应产物分布 的影响,并确定表达这些影响因素与反应速率之 间定量关系的速率方程。
均相反应动力学是研究均相反应过程的基础。
本章主要介绍:化学计量方程;反应速率的定义; 反应转化率;反应速率方程;不同反应的速率式 及其解析式。
2.1 基本概念及术语
2.1-4 反应速率方程
一、函数形式
r f (T , P, cA, cB......)
(1)双曲函数型 由反应机理导出,常用于反应机理分析。
(2)幂函数型 由质量作用定律得到,函数中的参数需通过实验测 定,常用于工程计算。
二、动力学方程
设一均相不可逆反应 动力学方程
aA bB pP
ln
k
E RT
ln
k0
由式可见,lnk与1/T之间为线性关系。整理表2.1-1中数据可得
B
-7.2
-7.4
lnk
-7.6
-7.8
-8.0
-8.2
-8.4
2.30
2.32
2.34
2.36
2.38
2.40
2.42
1/T
2.1.2 均相反应动力学方程
k0 e16.58 1.587 10 6
rA kcAcB
式中,k、α、β是动力学参数,由实验测定。
2.1.2 均相反应动力学方程
讨论
rA kcAcB
(1)一般情况下,总压P 对反应速率的影响不大,可忽略。
(2)α、β称为反应级数,表示反应速率对反应物浓度的敏感程度。 α与β之和称为总反应级数。
注意反应级数与化学计量系数之间的区别。
A
P
由反应速率定义式和动力学方程,
(rA )
dcA dt
kcA
等温条件下, 分离变量积分得
2.1 基本概念及术语
二、膨胀因子(气相反应)
物理意义:每消耗1mol反应物K,引起整个物系总物质的量的变化。
(1)由化学计量式计算
K
i K
(2-1-16)
(2)由总物料衡算计算
K
n n0 nK 0 xK
n n0 n0 yK 0 xK
(2-1-17)
整理得
n n0 (1 K yK 0 xK )
由定义式可得:
nk nk0 (1 xk )
则组分A的反应速率可用转化率表示为:
(rA )
dnA Vdt
nA0 V
dxA dt
恒容条件下
(rA )
cA0
dxA dt
讨论:转化率是衡量反应物转化程度的量,若存在多种反应物
时,不同反应物的转化率可能不相同。为什么?
着眼组分: 能够完全反应的体系中,最先消失的反应组分。
rP
dcP dt
(1)反应速率前冠以负号,避免反应速率出现负值;
(2)各组分反应速率的关系:
rA rP
A P
(3)以上定义式仅适用于分批式操作的反应速率。
2.1 基本概念及术语
2.1-3 反应转化率和膨胀因子
一、转化率:
xk
nk 0 nk nk 0
反应掉的 K的物质的量 反应开始时 K的物质的量
k
1.857
106
e
85800 RT
注意:① k0,E在一定温度范围内可以当着常数,若实际反应温度超 出实验温度范围时,将会产生误差。② k仅是温度的函数,其量纲
与反应的总级数有关。③ 气相反应用分压表示浓度时,k kp pA pB
可利用气体状态方程对k值进行换算,这时k的量纲也相应改变。
2.1 基本概念及术语
2.1-1 化学计量方程
表示各反应物、生成物在反应过程中量的变化关系的方程。
一般化形式 注意以下几点:
i Ai 0
(1)反应物计量系数为负数,反应产物计量系数为正数。
(2)化学计量方程本身与反应的实际历程无关。
(3)只用一个计量方程即可唯一给出各反应组分之间量的变化关系的 反应称为单一反应;必须用两个以上计量方程才能确定各反应组分量 的变化关系的反应称为复合反应。
