附录目录
2020国家医保目录附录-全

伏龙肝
256
延胡索
257
华山参
258
自然铜
259
血余炭
260
全蝎
□
261
合欢皮
262
合欢花
263
冰片(合成龙脑)
264
决明子
□
265
关白附
266
关黄柏
267
关黄柏炭
268
米炒党参
269
米斑蝥
270
灯心草
271
灯心炭
272
灯盏细辛(灯盏花)
273
安息香
274
寻骨风
275
阳起石
276
阴起石
277
防己
278
205
白蔹
206
白鲜皮
207
白薇
208
瓜子金
209
瓜蒌
210
瓜蒌子
211
瓜蒌皮
212
冬瓜子
213
冬瓜皮
214
冬凌草
215
冬葵果
216
玄明粉
217
玄参
218
玄精石
219
半边莲
220
半枝莲
221
辽藁本片
222
母丁香
223
丝瓜络
224
老鹳草
225
地龙
226
地耳草(田基黄)
227
地枫皮
228
地肤子
229
地骨皮
炒苦杏仁
449
炒使君子仁
450
炒茺蔚子
451
炒栀子
452
炒牵牛子
453
炒莱菔子
454
工程建设标准强制性条文 房屋建筑部分 版 附录 标准目录

1 《建筑抗震设计规范》GB50011-2010 2010-05-31 2010-12-012 《湿陷性黄土地区建筑规范》GB50025-2004 2004-03-01 2004-08-013 《滑动模板工程技术规范》GB50113-2005 2005-05-16 2005-08-014 《混凝土外加剂应用技术规范》GB50119-2003 2003-04-25 2003-09-015 《电气装置安装工程高压电器施工及验收规范》GB50147-2010 2010-05-31 2010-12-012010-05-31 2010-12-01 6 《电气装置安装工程电力变压器、油浸电抗器、互感器施工及验收规范》GB50148-20107 《电气装置安装工程母线装置施工及验收规范》GB50149-2010 2010-11-03 2011-10-018 《混凝土质量控制标准》GB50164-2011 2011-04-02 2012-05-019 《土方与爆破工程施工及验收规范》GB50201-2012 2012-03-30 2012-08-0110 《建筑地基基础工程施工质量验收规范》GB50202-2002 2002-04-01 2002-05-0111 《砌体结构工程施工质量验收规范》GB50203-2011 2011-02-18 2012-05-0112 《混凝土结构工程施工质量验收规范》GB50204-2002(2010年版)2002-03-15 2002-04-0113 《钢结构工程施工质量验收规范》GB50205-2001 2002-01-I0 2002-03-0l14 《木结构工程施工质量验收规范》GB50206-2012 2012-03-30 2012-08-0115 《屋面工程质量验收规范》GB50207-2012 2012-05-28 2012-10-0116 《地下防水工程质量验收规范》GB50208-2011 2011-04-02 2012-10-0117 《建筑地面工程施工质量验收规范》GB50209-2010 2010-05-31 2010-12-0118 《建筑装饰装修工程质量验收规范》GB50210-2001 2001-11-01 2002-03-0119 《建筑防腐蚀工程施工质量验收规范》GB50224-2010 2010-07-15 2011-02-0120 《建筑给水排水及采暖工程施工质量验收规范》GB50242-2002 2002-03-15 2002-04-0121 《通风与空调工程施工质量验收规范》GB50243-2002 2002-03-15 2002-04-0122 《建筑工程施工质量验收统一标准》GB50300-2001 2001-07-20 2002-01-0123 《建筑电气工程施工质量验收规范》GB50303-2002 2002-04-01 2002-06-0124 《电梯工程施工质量验收规范》GB50310-2002 2002-04-01 2002-06-0125 《民用建筑工程室内环境污染控制规范》GB50325-2010 2010-08-18 2011-06-0126 《建筑边坡工程技术规范》GB50330-2002 2002-05-30 2002-08-0127 《智能建筑工程质量验收规范》GB50339-2003 2003-07-01 2003-10-0128 《太阳能供热采暖工程技术规范》GB50495-2009 2009-03-19 2009-08-0129 《大体积混凝土施工规范》GB50496-2009 2009-05-13 2009-10-0130 《建筑基坑工程监测技术规范》GB50497-2009 2009-03-31 2009-09-0131 《墙体材料应用统一技术规范》GB50574-2010 2010-08-18 2011-06-0132 《铝合金结构工程施工质量验收规范》GB50576-2010 2010-05-31 2010-12-0133 《洁净室施工及验收规范》GB50591-2010 2010-07-15 2011-02-0134 《建筑物防雷工程施工与质量验收规范》GB50601-2010 2010-07-15 2011-02-0135 《智能建筑工程施工规范》GB50606-2010 2010-07-15 2011-02-0136 《建筑电气照明装置施工与验收规范》GB50617-2010 2010-08-18 2011-06-0137 《房屋建筑和市政基础设施工程质量检测技术管理规范》2011-04-02 2012-10-01 GB50618-201138 《钢管混凝土工程施工质量验收规范》GB50628-2010 2010-11-03 2011-10-0139 《无障碍设施施工验收及维护规范》GB 2010-12-24 2011-06-0140 《钢结构焊接规范》GB50661-2011 2011-12-05 2012-08-0141 《混凝土结构工程施工规范》GB50666-2011 2011-07-29 2012-08-0142 《钢筋混凝土筒仓施工与质量验收规范》GB50669-2011 2011-02-18 2011-05-0143 《预制组合立管技术规范》GB50682-2011 2011-02-18 2012-01-0144 《坡屋面工程技术规范》GB50693-2011 2011-05-12 2012-05-0145 《通风与空调工程施工规范》GB50738-2011 2011-09-16 2012-05-0146 《复合土钉墙基坑支护技术规范》GB50739-2011 2011-09-16 2012-05-0147 《钢结构工程施工规范》GB50755-2012 2012-01-21 2012-08-0148 《建筑变形测量规范》JGJ8-2007 2007-09-04 2008-03-0149 《轻骨料混凝土结构技术规程》JGJ12-2006 2006-03-08 2006-07-0150 《钢筋焊接及验收规程》JGJ18-2012 2012-03-01 2012-08-0151 《轻骨料混凝土技术规程》JGJ51-2002 2002-09-27 2003-01-0152 《普通混凝土用砂、石质量及检验方法标准》JGJ52-2006 2006-12-20 2007-06-0153 《普通混凝土配合比设计规程》JGJ55-2011 2011-04-22 2011-12-0154 《电影院建筑设计规范》JGJ58-2008 2008-02-29 2008-08-0155 《混凝土用水标准》JGJ63-2006 2006-07-25 2006-12-0156 《建筑工程大模板技术规程》JGJ74-2003 2003-06-03 2003-10-0157 《建筑地基处理技术规范》JGJ79-2012 2012-8-23 2013-06-0158 《建筑钢结构焊接技术规程》JGJ81-2002 2002-09-27 2003-01-0159 《钢结构高强度螺栓连接技术规程》JGJ82-2011 2011-01-07 2011-10-0160 《预应力筋用锚具、夹具和连接器应用技术规程》JGJ85-2010 2010-04-17 2010-10-0161 《无粘结预应力混凝土结构技术规程》JGJ92-2004 2005-01-13 2005-03-0162 《建筑桩基技术规范》JGJ94-2008 2008-04-22 2008-10-0163 《钢框胶合板模板技术规程》JGJ96-2011 2011-01-07 2011-10-0164 《玻璃幕墙工程技术规范》JGJ102-2003 2003-11-14 2004-01-0165 《塑料门窗工程技术规程》JGJ103-2008 2008-08-05 2008-11-0166 《建筑基桩检测技术规范》JGJ106-2003 2003-03-21 2003-07-0167 《钢筋机械连接技术规程》JGJ107-2010 2010-02-io 2010-10-0168 《建筑工程饰面砖粘结强度检验标准》JGJ110-2008 2008-03-12 2008-08-0169 《冷轧扭钢筋混凝土构件技术规程》JGJ115-2006 2006-07-25 2006-12-01-70 《建筑基坑支护技术规程》JGJ120-2012 2012-04-05 2012-10-0171 《金属与石材幕墙工程技术规范》JGJ133-2001 2001-05-29 2001-06-0172 《通风管道技术规程》JGJ141-2004 2004-06-04 2004-10-0173 《混凝土异形柱结构技术规程》JGJ149-2006 2006-03-09 2006-08-0174 《擦窗机安装工程质量验收规程》JGJ150-2008 2008-01-31 2008-07-0175 《清水混凝土应用技术规程》JGJ169-2009 2009-03-04 2009-06-0176 《地下建筑工程逆作法技术规程》JGJ165-2010 2010-12-20 2011-08-0177 《湿陷性黄土地区建筑基坑工程安全技术规程》JGJ167-2009 2009-03-15 2009-07-0178 《多联机空调系统工程技术规程》JGJ174-20i0 2010-03-31 2010-09-0179 《铝合金门窗工程技术规范》JGJ214-2010 2010-07-20 2011-03-0180 《冰雪景观建筑技术规程》JGJ247-2011 2011-08-29 2012-04-0181 《钢筋锚固板应用技术规程》JGJ256-2011 2011-08-29 2012-04-0182 《家用燃气燃烧器具安装及验收规程》CJJ12-99 1999-04-26 1999-09-0183 《城镇燃气室内工程施工与质量验收规范》CJJ94-2009 2009-04-07 2009-10-0184 《建筑排水金属管道工程技术规程》CJJ127-2009 2009-04-20 2009-09-0185 《城镇地热供热工程技术规程》CJJ138-2010 2010-04-17 2010-10-0186 《二次供水工程技术规程》CJJ140-2010 2010-04-17 2010-10-0187 《埋地塑料排水管道工程技术规程》CJJ143-2010 2010-05-18 2010-12-0188 《燃气冷热电三联供工程技术规程》CJJ145-2010 2010-08-18 2011-03-0189 《二次供水工程技术规程》CJJ 140 - 2010 2010-04-17 2010-10-0190 《埋地塑料排水管道工程技术规程》CJJ 143- 2010 2010-05-18 2010-12-0191 《燃气冷热电三联供工程技术规程》CJJ 145- 2010 2010-08-18 2011-03-01。
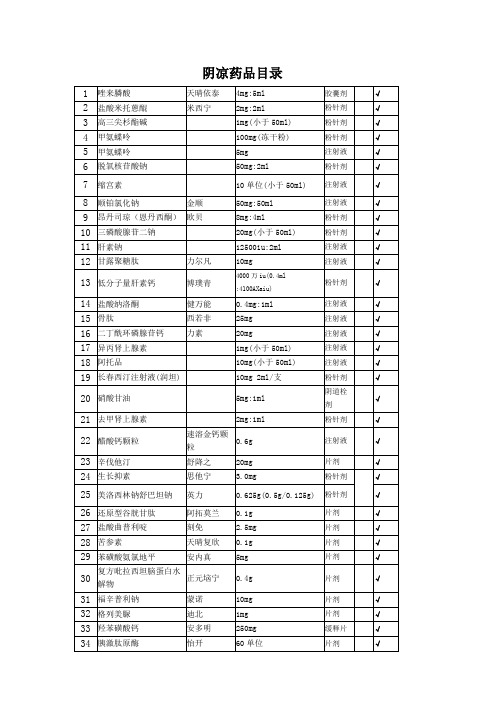
附录5.阴凉药品目录
62
阿莫西林克拉维酸钾
安奇片
0.3125g(0.25g/62.5mg)
颗粒剂
√
63
阿维A胶囊
方希
10mg
胶囊剂
√
64
利福平
150mg
胶囊剂
√
65
头孢地尼
希福尼
50mg*6片
分散片
√
66
多巴丝肼
美多巴
0.25g(左旋多巴200mg,苄丝肼0mg)
片剂
√
67
复方角菜酸酯
太宁
3.4g
栓剂
√
68
肠内营养粉剂(TP)
0.625g
片剂
√
195
九华痔疮栓
√
196
风油精
√
197
清凉油
√
198
银杏蜜环口服液
心脑宁
10ml
口服溶液
√
199
鸦胆子油乳注射液
√
10g:100ml
注射液
√
123
注射用头孢替唑钠(卓迈)
0.75g
√
124
薄芝糖肽
赛升
5mg:2ml
注射液
√
125
小牛血去蛋白提取物
生祺
0.4g(总固体)
粉针剂
√
126
盐酸吡柔比星
10mg
粉针剂
√
127
阿莫西林钠舒巴坦钠
来切利
1.5g(1.0g/0.5g)
粉针剂
√
128
盐酸头孢吡肟
马斯平
1g
粉针剂
√
安素
400g
粉剂
√
69
聚维酮碘
论文目录正文附录参考文献的要求

平顶山学院本科毕业论文11 绪企业,日发电综合指标和月发电综合指标是体现企业效益的标准.…在系统设计方案上,我们不仅要满足基本数据处理的需求,而且要面向企业的可扩展化、规范化、集成化的高指标要求,为此,在结合企业实际生产环节的各种数据基础上,结合计算机1.1 二级标题1.1.1 OOA/OOD 即方法简单、易学,适合于面向对象技术的初学者使用.UML 中的视图包括:用例视图(Use-case view )、逻辑视图(Logical view )、组件视图(Component view )、并发视图(Concurrency view )、展开视图(Deployment view )等五种,能够使用其他的视图还有静态-动态视图、逻辑-物理视图、工作流程视图等.(1) (2) ① ②基于UML 的电厂信息管理系统建模研究297.11.1797.9公布97.1公布96.6和96.10UML1.1被OMG 接纳为标准图1-1 UML1.2 二级标题1.2.1 三级标题图、表、公式等与正文之间要有一行的间距.文中的定义、定理、例题、图、表、附注、公式的序号一律采用阿拉伯数字分章编号.如:例3.1,图2-5,表3-2,公式(5-1)等.定义1.1 定理1.1 例1.1.0sin()y t ωϕ=+ (1-1) 表: 表格应随文给出,先见文后见表;表中参数应标明量和单位的符号;表序及表名置于表的上方,居中排写;一张表格应为一个整体,表格一页排不下允许下页接写,表题可省略,表头应重复写,并在右上方写“续表××”.表格不加左右边线.表格应为标准科技论文三线表格式!平顶山学院本科毕业论文UML不仅可以为软件系统创建模型,还可以描述其它非计算机软件的系统,或是商业机构或过程.1.2.3 三级标题UML不仅可以为软件系统创建模型,还可以描述其它非计算机软件的系统,或是商业机构或过程.1.3 二级标题UML不仅可以为软件系统创建模型,还可以描述其它非计算机软件的系统,或是商业机构或过程.3基于UML 的电厂信息管理系统建模研究42 解决问题数学与应用数学数学与应用数学,数学与应用数学数学与应用数学数学与应用数学数学与应用数学.2.1 二级标题数学与应用数学数学与应用数学,数学与应用数学数学与应用数学数学与应用数学.2.2 二级标题数学与应用数学数学与应用数学数学与应用数学数学与应用数学,数学与应用数学数学与应用数学数学与应用数学.2.2.1三级标题数学与应用数学数学与应用数学数学与应用数学,数学与应用数学数学与应用数学数学与应用数学数学与应用数学.2.2.2三级标题数学与应用数学数学与应用数学数学与应用数学,数学与应用数学数学与应用数学数学与应用数学.平顶山学院本科毕业论文53 结 语学数学与应用数学.基于UML 的电厂信息管理系统建模研究6程序代码:代码1typedef struct{int size; } SeqList; { L->size=0; }int ListLength(SeqList L) { return L.size; }int ListInsert(SeqList *L,int i,DataType x) { int j; if (L->size>=MaxSize) { printf("顺序表已满无法插入!\n"); return 0; } else if(i<0||i>L->size) { printf("参数不合法!\n"); return 0; } else { for(j=L->size;j>i;j--) L->list[j]=L->list[j-1]; L->list[i]=x; L->size++; return 1; } }int ListGet(SeqList L,int i,DataType *x) { if(i<0||i>L.size-1) { printf("参数i 不合法!\n"); return 0; } else { *x=L.list[i]; return 1; } };平顶山学院本科毕业论文7程序代码:主程序SeqList_main.c : #include <stdio.h> #define MaxSize 100 typedef int DataType; #include "SeqList.h" void main(void) { SeqList myList; int i,x; ListInitiate(&myList); for(i=0;i<10;i++) { if(ListInsert(&myList,i,i+1)==0) { printf("错误\n"); return; } } for(i=0;i<ListLength(myList);i++) { if(ListGet(myList,i,&x)==0) { printf("错误\n"); return; } else printf("%d ",x); } }基于UML 的电厂信息管理系统建模研究8[J].华中科技大学学报.2002,30(4):93-95. [2]蒋慧.UML 设计核心技术[M].北京:北京希望电子出版社,2001.[3]王红燕. UML 建模在常住人口管理信息系统开发中的应用[J]. 计算机工程与应用 .2002,19:238-241.[4]刘胜超等.UML 在工业锅炉控制系统设计中的应用[J].华中科技大学学报.2002,30(4): 93-95.… …参考文献书写格式规定:专著:注释编号.作者.专著.书名[M].出版社,出版年.起止页码. 期刊:注释编号.作者.期刊.题名[J].刊名,出版年(卷、期):起止页码.论文集:注释编号.作者.论文名称: 论文集名[C].出版地:出版社,出版年度.起止页码. 学位论文:注释编号 .作者.题名[D].保存地点:保存单位,写作年度. 专利文献:注释编号 .专利所有者.题名[P].专利国别:专利号, 出版日期.光盘:注释编号.责任者.电子文献题名[电子文献及载体类型标识],出版年(光盘序号) . 互联网:注释编号.责任者.文献题名.电子文献网址.访问时间(年-月-日).文献作者3名以内的全部列出;3名以上则列出前3名,后加“等”(英文加“etc.”) .参考文献应保证在6篇以上,并有2000年以后的最新文献2-3篇.。
2010版GMP完整版(11个附录)

药品生产质量管理规范(2010年修订)目录《药品生产质量管理规范(2010年修订)》发布 (1)关于发布《药品生产质量管理规范(2010年修订)》无菌药品等5个附录的公告 (3)关于实施《药品生产质量管理规范(2010年修订)》有关事宜的公告 (4)国家食品药品监督管理总局关于发布《药品生产质量管理规范(2010年修订)》计算机化系统和确认与验证两个附录的公告(2015年第54号) (6)药品生产质量管理规范(2010年修订)(卫生部令第79号) (7)7第一章总则......................................................................................................................7第二章质量管理..................................................................................................................第一节原则...............................................................................................................78第二节质量保证...........................................................................................................9第三节质量控制...........................................................................................................第四节质量风险管理 (9)9第三章机构与人员..............................................................................................................9第一节原则...............................................................................................................10第二节关键人员.........................................................................................................12第三节培训.............................................................................................................12第四节人员卫生.........................................................................................................13第四章厂房与设施............................................................................................................13第一节原则.............................................................................................................13第二节生产区.............................................................................................................14第三节仓储区.............................................................................................................15第四节质量控制区.....................................................................................................第五节辅助区.............................................................................................................1515第五章设备....................................................................................................................15第一节原则.............................................................................................................16第二节设计和安装.....................................................................................................16第三节维护和维修.....................................................................................................16第四节使用和清洁.....................................................................................................17第五节校准.............................................................................................................17第六节制药用水.........................................................................................................17第六章物料与产品............................................................................................................17第一节原则.............................................................................................................18第二节原辅料.............................................................................................................第三节中间产品和待包装产品 (19)19第四节包装材料.........................................................................................................20第五节成品.............................................................................................................第六节特殊管理的物料和产品 (20)第七节其他.............................................................................................................2021第七章确认与验证............................................................................................................22第八章文件管理................................................................................................................22第一节原则.............................................................................................................23第二节质量标准.........................................................................................................23第三节工艺规程.........................................................................................................第四节批生产记录.....................................................................................................2425第五节批包装记录.....................................................................................................第六节操作规程和记录 (26)第九章生产管理................................................................................................................2626第一节原则.............................................................................................................第二节防止生产过程中的污染和交叉污染 (27)第四节包装操作 (28)第十章质量控制与质量保证 (29)第一节质量控制实验室管理 (29)第二节物料和产品放行 (33)第三节持续稳定性考察 (33)第四节变更控制 (34)第五节偏差处理 (35)第六节纠正措施和预防措施 (35)第七节供应商的评估和批准 (36)第八节产品质量回顾分析 (37)第九节投诉与不良反应报告 (38)第十一章委托生产与委托检验 (38)第一节原则 (38)第二节委托方 (38)第三节受托方 (39)第四节合同 (39)第十二章产品发运与召回 (39)第一节原则 (39)第二节发运 (40)第三节召回 (40)第十三章自检 (40)第一节原则 (40)第二节自检 (40)第十四章附则 (41)附录1:无菌药品 (45)第一章范围 (45)第二章原则 (45)第三章洁净度级别及监测 (45)第四章隔离操作技术 (48)第五章吹灌封技术 (49)第六章人员 (49)第七章厂房 (50)第八章设备 (51)第九章消毒 (51)第十章生产管理 (51)第十一章灭菌工艺 (53)第十二章灭菌方法 (53)第十三章无菌药品的最终处理 (55)第十四章质量控制 (56)第十五章术语 (56)附录2:原料药 (57)第一章范围 (57)第二章厂房与设施 (57)第三章设备 (57)第四章物料 (58)第五章验证 (58)第六章文件 (60)第七章生产管理 (60)第八章不合格中间产品或原料药的处理 (62)第九章质量管理 (63)第十章采用传统发酵工艺生产原料药的特殊要求 (64)66第一章范围........................................................................................................................66第二章原则........................................................................................................................66第三章人员........................................................................................................................67第四章厂房与设备............................................................................................................第五章动物房及相关事项................................................................................................6868第六章生产管理................................................................................................................70第七章质量管理................................................................................................................第八章术语........................................................................................................................7071附录4:血液制品........................................................................................................................71第一章范围........................................................................................................................71第二章原则........................................................................................................................71第三章人员........................................................................................................................71第四章厂房与设备............................................................................................................第五章原料血浆................................................................................................................7273第六章生产和质量控制....................................................................................................第七章不合格原料血浆、中间产品、成品的处理 (73)74附录5:中药制剂........................................................................................................................第一章范围........................................................................................................................7474第二章原则........................................................................................................................74第三章机构与人员............................................................................................................第四章厂房设施................................................................................................................7475第五章物料........................................................................................................................76第六章文件管理................................................................................................................76第七章生产管理................................................................................................................77第八章质量管理................................................................................................................77第九章委托生产................................................................................................................第十章术语........................................................................................................................7879附录 6:中药饮片.................................................................................................................79第一章范围......................................................................................................................79第二章原则......................................................................................................................79第三章人员......................................................................................................................80第四章厂房与设施............................................................................................................第五章设备......................................................................................................................8181第六章物料和产品............................................................................................................82第七章确认与验证............................................................................................................第八章文件管理................................................................................................................8384第九章生产管理................................................................................................................84第十章质量管理................................................................................................................85第十一章术语..................................................................................................................86附录 7:医用氧.......................................................................................................................86第一章范围....................................................................................................................第二章原则....................................................................................................................8686第三章人员....................................................................................................................87第四章厂房与设备............................................................................................................87第五章文件管理................................................................................................................88第六章生产管理................................................................................................................90第七章质量控制................................................................................................................90第八章贮存、放行与销售................................................................................................91第九章术语........................................................................................................................92附录 8:取样...........................................................................................................................第三章取样设施 (92)第四章取样器具 (93)第五章取样人员和防护 (93)第六章文件 (93)第七章取样操作 (94)第八章样品的容器、转移和贮存 (96)第九章术语 (96)附录9:放射性药品 (98)第一章范围和原则 (98)第二章机构与人员 (98)第三章厂房设施与设备 (98)第四章物料管理 (100)第五章生产管理 (101)第六章质量管理 (101)第七章辐射安全管理 (102)第八章附则 (102)附录 10:计算机化系统 (104)第一章范围 (104)第二章原则 (104)第三章人员 (104)第四章验证 (104)第五章系统 (105)第六章术语 (106)附录11:确认与验证 (107)第一章范围 (107)第二章原则 (107)第三章验证总计划 (107)第四章文件 (107)第六章工艺验证 (108)第七章运输确认 (110)第八章清洁验证 (110)第九章再确认和再验证 (111)第十章术语 (111)《药品生产质量管理规范(2010年修订)》发布2011年02月12日发布历经5年修订、两次公开征求意见的《药品生产质量管理规范(2010年修订)》(以下简称新版药品GMP)今天对外发布,将于2011年3月1日起施行。
中国GMP及目前所有11个附录汇编

德亦诚《GMP法规汇编》(第一册)(中国GMP2010年版,含11附录)天津德亦诚医药咨询有限公司企业介绍“德亦诚《GMP法规汇编》”是天津德亦诚医药咨询有限公司为公司员工及客户专门汇总整理的GMP相关法规、指南,本册为第一册,为中国GMP2010版及自2011年至2015年12月CFDA为2010版GMP先后发布的11个附录,供大家学习参考使用。
德亦诚将继续推出针对FDA cGMP法规、欧盟GMP、PIC/s GMP、WHO GMP、ICH、ISO等相关汇编,欢迎关注我司微信公众号(dycgmp)以获取最新消息。
天津德亦诚医药咨询有限公司总部位于天津,致力于为国内中小型制药企业提供GMP咨询、培训、计算机化系统验证、质量管理信息化咨询等服务。
德亦诚顾问皆来自国内外大中型制药企业,多任职过QA经理或质量负责人,且从事GMP咨询多年,具有丰富的咨询和培训经验。
公司成立以来,已为北京、天津、山东、山西、河北、上海、江苏等地多家制药企业提供咨询服务,帮助客户提升质量管理体系,顺利通过GMP认证和核查,得到客户的一致好评。
若有GMP咨询、GMP培训、验证、计算机化系统、数据完整性等方面的需求,可通过以下方式联系我们:客服:400-728-0190邮箱:gmp@Q Q:gmp@目录第一章总则 (2)第二章质量管理 (3)第一节原则 (3)第二节质量保证 (3)第三节质量控制 (4)第四节质量风险管理 (4)第三章机构与人员 (6)第一节原则 (6)第二节关键人员 (6)第三节培训 (8)第四节人员卫生 (9)第四章厂房与设施 (10)第一节原则 (10)第二节生产区 (10)第三节仓储区 (11)第四节质量控制区 (12)第五节辅助区 (12)第五章设备 (13)第一节原则 (13)第二节设计和安装 (13)第三节维护和维修 (13)第四节使用和清洁 (13)第五节校准 (14)第六节制药用水 (14)第六章物料与产品 (16)第一节原则 (16)第二节原辅料 (17)第三节中间产品和待包装产品 (17)第四节包装材料 (17)第五节成品 (18)第六节特殊管理的物料和产品 (18)第七节其他 (18)第七章确认与验证 (20)第八章文件管理 (22)第一节原则 (22)第二节质量标准 (23)第三节工艺规程 (24)第五节批包装记录 (25)第六节操作规程和记录 (26)第九章生产管理 (28)第一节原则 (28)第二节防止生产过程中的污染和交叉污染 (28)第三节生产操作 (29)第四节包装操作 (29)第十章质量控制与质量保证 (31)第一节质量控制实验室管理 (31)第二节物料和产品放行 (35)第三节持续稳定性考察 (36)第四节变更控制 (37)第五节偏差处理 (37)第六节纠正措施和预防措施 (38)第七节供应商的评估和批准 (38)第八节产品质量回顾分析 (39)第九节投诉与不良反应报告 (40)第十一章委托生产与委托检验 (42)第一节原则 (42)第二节委托方 (42)第三节受托方 (42)第四节合同 (42)第十二章产品发运与召回 (44)第一节原则 (44)第二节发运 (44)第三节召回 (44)第十三章自检 (45)第一节原则 (45)第二节自检 (45)第十四章附则 (46)附录一无菌药品 (51)第一章范围 (51)第二章原则 (51)第三章洁净度级别及监测 (51)第四章隔离操作技术 (55)第五章吹灌封技术 (55)第六章人员 (56)第八章设备 (58)第九章消毒 (58)第十章生产管理 (58)第十一章灭菌工艺 (60)第十二章灭菌方法 (61)第十三章无菌药品的最终处理 (63)第十四章质量控制 (63)第十五章术语 (64)附录二原料药 (65)第一章范围 (65)第二章厂房与设施 (65)第三章设备 (65)第四章物料 (65)第五章验证 (66)第六章文件 (67)第七章生产管理 (68)第八章不合格中间产品或原料药的处理 (70)第九章质量管理 (71)第十章采用传统发酵工艺生产原料药的特殊要求 (72)第十一章术语 (73)附录三生物制品 (75)第一章范围 (75)第二章原则 (75)第三章人员 (75)第四章厂房与设备 (76)第五章动物房及相关事项 (77)第六章生产管理 (78)第七章质量管理 (79)第八章术语 (79)附录四血液制品 (81)第一章范围 (81)第二章原则 (81)第三章人员 (81)第四章厂房与设备 (81)第五章原料血浆 (82)第六章生产和质量控制 (83)第七章不合格原料血浆、中间产品、成品的处理 (84)附录五中药制剂 (85)第一章范围 (85)第二章原则 (85)第三章机构与人员 (85)第四章厂房设施 (85)第五章物料 (86)第六章文件管理 (87)第七章生产管理 (87)第八章质量管理 (88)第九章委托生产 (89)第十章术语 (89)附录六放射性药品 (91)第一章范围和原则 (91)第二章机构与人员 (91)第三章厂房设施与设备 (91)第四章物料管理 (93)第五章生产管理 (94)第六章质量管理 (94)第七章辐射安全管理 (95)第八章附则 (95)附录七中药饮片 (96)第一章范围 (96)第二章原则 (96)第三章人员 (96)第四章厂房与设施 (97)第五章设备 (97)第六章物料和产品 (98)第七章确认与验证 (98)第八章文件管理 (99)第九章生产管理 (100)第十章质量管理 (100)第十一章术语 (100)附录八医用氧 (102)第一章范围 (102)第二章原则 (102)第三章人员 (102)第四章厂房与设备 (102)第五章文件管理 (103)第六章生产管理 (104)第七章质量控制 (105)第八章贮存、放行与销售 (105)第九章术语 (105)附录九取样 (107)第一章范围 (107)第二章原则 (107)第三章取样设施 (107)第四章取样器具 (107)第五章取样人员和防护 (108)第六章文件 (108)第七章取样操作 (108)第八章样品的容器、转移和贮存 (110)第九章术语 (110)附录十计算机化系统 (112)第一章范围 (112)第二章原则 (112)第三章人员 (112)第四章验证 (112)第五章系统 (113)第六章术语 (114)附录十一确认和验证 (116)第一章范围 (116)第二章原则 (116)第三章验证总计划 (116)第四章文件 (116)第五章确认 (117)第六章工艺验证 (118)第七章运输确认 (120)第八章清洁验证 (120)第九章再确认和再验证 (121)第十章术语 (122)中华人民共和国卫生部令第79 号《药品生产质量管理规范(2010年修订)》已于2010年10月19日经卫生部部务会议审议通过,现予以发布,自2011年3月1日起施行。
建筑施工合同附录:2024年通用规范
20XX 标准合同模板范本PERSONAL RESUME甲方:XXX乙方:XXX建筑施工合同附录:2024年通用规范本合同目录一览第一条合同主体1.1 发包方1.2 承包方第二条工程概况2.1 工程名称2.2 工程地点2.3 工程规模2.4 工程内容第三条合同金额3.1 合同总价3.2 预付款3.3 进度付款3.4 竣工结算第四条合同工期4.1 开工日期4.2 竣工日期4.3 工期延误第五条质量标准5.1 工程质量5.2 材料质量5.3 施工工艺第六条合同履行6.1 承包方义务6.2 发包方义务6.3 变更处理第七条安全生产7.1 安全生产管理7.2 安全事故处理7.3 安全生产费用第八条违约责任8.1 承包方违约8.2 发包方违约8.3 违约赔偿第九条争议解决9.1 协商解决9.2 调解解决9.3 仲裁解决9.4 法律途径第十条合同的生效、变更和终止10.1 合同生效条件10.2 合同变更10.3 合同终止第十一条合同附件11.1 工程图纸11.2 技术说明书11.3 材料供应清单11.4 其他附件第十二条其他条款12.1 保密条款12.2 知识产权保护12.3 不可抗力12.4 法律法规规定的其他事项第十三条合同的修订和补充13.1 修订条件13.2 补充协议第十四条合同解除14.1 解除条件14.2 解除程序14.3 解除后的责任处理第一部分:合同如下:第一条合同主体1.1 发包方1.1.1 发包方全称:_______ 1.1.2 注册地址:_______1.1.3 法定代表人:_______1.1.4 联系人:_______1.1.5 联系电话:_______1.2 承包方1.2.1 承包方全称:_______1.2.2 注册地址:_______1.2.3 法定代表人:_______1.2.4 联系人:_______1.2.5 联系电话:_______第二条工程概况2.1 工程名称:_______2.2 工程地点:_______2.3 工程规模:_______2.4 工程内容:包括但不限于_______第三条合同金额3.1 合同总价:人民币(大写):_______元整(小写):_______元3.2 预付款:人民币(大写):_______元整(小写):_______元3.3 进度付款:按工程进度分阶段支付,具体支付比例和时间如下:3.3.1 工程进度达到_______时,支付合同价的_______%;3.3.2 工程进度达到_______时,支付合同价的_______%;3.3.3 工程进度达到_______时,支付合同价的_______%;3.4 竣工结算:工程竣工后,按照实际完成工程量进行结算。
目录设计范本
目录设计范本一、引言二、目录的重要性三、目录的基本结构3.1 主目录3.1.1 一级标题3.1.1.1 二级标题3.1.1.2 二级标题3.1.2 一级标题3.1.2.1 二级标题3.1.2.2 二级标题3.2 附录目录四、目录的设计原则4.1 明确层次关系4.2 简洁明了4.3 一致性4.4 可读性五、目录的设计步骤5.1 确定主题5.2 列出所有章节和标题5.3 定义层次结构5.4 编辑和整理目录内容5.5 设计目录样式六、目录的设计技巧6.1 使用编号和标题6.2 使用缩进和对齐6.3 使用精确的词语6.4 使用清晰的标点符号6.5 使用合适的字体和格式七、目录的更新与维护7.1 更新目录7.2 校对目录7.3 维护目录的一致性八、目录设计的案例分析8.1 学术论文目录设计8.2 企业报告目录设计8.3 书籍目录设计九、结论十、参考文献引言目录是指对文档、书籍、报告等内容进行分类和索引的一种方式,它能够提供读者快速了解和查找所需信息的途径。
一个清晰、简洁、美观的目录设计不仅可以提高文档的可读性和可理解性,还能够提升整体的学术水平和专业形象。
本文将介绍目录的重要性、基本结构、设计原则、设计步骤、设计技巧以及目录的更新与维护等内容,并通过案例分析来进一步说明目录设计的实际应用。
目录的重要性目录在文档中起到了承上启下的作用,它能够为读者提供一个整体的概览,帮助读者快速了解文档的结构和内容,从而更好地掌握文档的核心思想和主题。
同时,目录还可以作为导航工具,帮助读者在需要的时候快速定位和查找具体章节或内容,提高阅读效率和准确性。
目录的基本结构目录通常由主目录和附录目录组成。
主目录是对文档主体部分的分类和索引,包含了所有的章节和标题。
附录目录是对文档附录部分的分类和索引,包含了附录的章节和标题。
主目录和附录目录可以根据实际需要进行调整和扩展,以满足不同文档类型和内容的要求。
目录的设计原则目录的设计应遵循以下原则:明确层次关系、简洁明了、一致性和可读性。
附录:目录自动生成方法
图7
6.检查完之后如没有问题,就可以回到前言之前的目录页,插入目录,插入办法:
插入——引用——索引和目录(如图8),选中目录,其他默认设置就可以
图8
7.这样就可以在目录页中看到已经插入的目录,调整目录格式,段落为1.5倍行距,字体设置为小四号宋体,段前段后都问0行,其他无需改动
8.目录的更新:如果正文中进行了改动,可以将光标放在目录页中,显示灰色时右击鼠标,选择更新域,如只需改变页码选择只更新页码,如果标题也改变了,需要更新整个目录,并重新调整下格式。
目录自动生成方法:
1.在前言之前的一页最下方加入一个分节符,插入方式:插入—分隔图1
2.从第一章前言的第一页中插入-页码-设置页码格式,首页显示页码,并且起始页码为1,如图2;
图2
3.在正文第一页的页脚部分双击,取消与上节相同,按钮为图中黄颜色如图3所示左边那个;取消之后的图示如图4;
图3
图4
4.在正文中,需要将所有的标题设置成需要的级别
例如:前言,选中,点击格式-段落-大纲级别,章标题设置为一级标题,用同样的方法或格式刷将文中其他的一级标题设置好;二级标题(1)同样的方法设置成大纲级别为二级标题,其他所有的标题都按照这个方法设置好。如图5.
图5
5.如需检验下自己是否将所有的标题都设置好,可以点击一下文档结构图(图6),就是图中放大镜样子的图标,左边就可以看到自己所设置的所有标题(如图7)
附录4:城建档案馆档案归档目录
(3)砼:配合比试验报告、预拌砼站原材料 出厂质量证明及试验报告、砼站抽样试验报 告。汇总表、见证取样送检书、结构用砼试块 强度评定验收记录、现场抽样试验报告、结构 砼施工记录、浇注令、隐蔽验收记录、。粗细 骨料及砼外加剂出厂材质证明;现场抽样试验 报告
施 2002-31 /40/41/20 /43
八.分户工程验收 1.住宅工程质量分户验收表 2.住宅工程质量分户验收记录表(包 九.工程竣工图 1,建筑竣工图(含总图) 竣 2.基础竣工图 工 图 3.结构竣工图 4.给排水与采暖及电气工程竣工图
档案资料内 容
(2)砼试块强度试验报告、汇总表、 及评定
施 2002-43/40
9
(3)桩施工记录;测量复核记录; 施 2002-46
基
焊接检查验收记录
/47/48/49/50
桩 (4)桩静荷载试验报告;动测等试
验报告
(5)分部、分项工程及检验批验收 记录
施 2002-5/ 6
10.其他隐蔽工程验收记录
施 2002-20
建 3.施工技术交底记录
施 2002-11
4.工程开工/复工报审表 筑
5.设计变更、洽商记录及工程变更单
施 2002-12 施 2002-19
电 6.材料、配件、设备进场验收记录;见证
施 2002-29
取样送检书、出厂质量证明书、现场抽样
梯 检验报告及开箱检验记录
施 2002-31
工 7.接地、绝缘电阻测试见证记录 8.与建筑结构交接验收记录
文 标通知单
件
材 料
三.工程勘测、设计、监理、施工合同
︹ 建 四.工程地质勘察报告
设 五.施工图设计审查文件(含附件)
单
