氢氰酸生产工艺
工业氢氰酸的技术要求

工业氢氰酸的技术要求工业氢氰酸是一种广泛应用于化工、医药、金属冶炼等领域的重要化学品。
为了确保其生产质量和安全性,我们有必要了解工业氢氰酸的技术要求。
下面,将从原材料、生产工艺、质量控制和安全管理等方面进行介绍。
首先,我们需要使用高纯度的原材料进行生产。
一般来说,工业氢氰酸的主要原料是氨气和甲烷,因此需要确保这两种原料的纯度高。
氨气需达到99.99%以上的纯度,而甲烷则需要达到99.9%以上的纯度。
这样可以有效地避免杂质对氢氰酸质量的影响。
其次,生产工艺也是影响工业氢氰酸质量的重要因素。
工业氢氰酸生产通常采用氨法或者甲烷法。
其中,氨法主要通过氨与空气中的氮气在催化剂的作用下发生反应制得氢氰酸。
而甲烷法则是甲烷在高温条件下与氮气反应得到氢氰酸。
在生产过程中需要控制反应温度、压力、催化剂的种类和用量等参数,确保反应的顺利进行。
在质量控制方面,我们需要对工业氢氰酸的含量、纯度、杂质以及其它物化性质进行检测和分析。
氢氰酸的含量一般应在95%以上,纯度应达到99.9%以上。
同时,还需要检测有害杂质如游离酸、游离氰化物等,确保氢氰酸的质量符合标准要求。
此外,对产品的密度、沸点、凝固点等物理性质也有一定的要求,以便于后续工艺的应用和产品的贮存。
最后,安全管理是工业氢氰酸生产过程中至关重要的一环。
氢氰酸是一种有毒品,具有剧毒和腐蚀性,因此在生产、储存和运输过程中必须采取严格的控制措施。
操作人员需要穿戴防护装备,保持良好的通风条件,并进行相关的安全培训和意识教育,以防止事故发生。
此外,还需要建立完善的事故应急预案和危险品管理制度,确保在发生意外情况时能够及时响应和处理。
综上所述,工业氢氰酸的生产需要遵循严格的技术要求。
从原材料的选择到生产工艺的控制,再到质量控制和安全管理的实施,都需要严格把控。
只有做到这些,才能保证工业氢氰酸的质量和安全性,为相关产业的发展提供稳定的化学品支撑。
氢氰酸工艺技术

氢氰酸工艺技术
氢氰酸,又称硫酸氢氯酰、硫氰酸、腐蚀酸等,是一种无色、具有强烈刺激气味的液体。
它是重要的有机合成原料,广泛应用于制药、染料、农药、塑料、涂料等产业。
下面将介绍氢氰酸的工艺技术。
氢氰酸的生产工艺主要分为两种:苏联工艺和德国工艺。
在苏联工艺中,以甲醇和氨为原料。
首先,将甲醇与氨以一定摩尔比混合后,通过加热反应得到甲醇胺。
然后,将甲醇胺和硫反应生成硫醚,并在连续反应系统中加入催化剂,将硫醚转化为硫化碳。
接着,在连续反应系统中将硫化碳与氨反应得到氨基硫醇。
最后,将氨基硫醇和氯反应生成氢氰酸。
德国工艺主要以天然气和氨为原料。
首先,将天然气经过一系列处理得到合成气。
然后,将合成气与水蒸气经高温反应生成一氧化碳和氢气。
接着,将氢气与氨在一定温度下反应得到氰氢酸氢钾。
最后,将氰氢酸氢钾与硫酸反应生成氢氰酸。
无论是苏联工艺还是德国工艺,氢氰酸的生产过程都需要严格控制温度、压力等反应条件。
同时,由于氢氰酸具有很强的毒性和危险性,对工艺中的安全措施也要非常重视。
除了生产工艺之外,氢氰酸的储存和运输也是需要特别注意的环节。
由于其对常见材料有很强的腐蚀性,储存罐必须选用防腐材料。
此外,还要采取避光、密封、防潮等措施,以防止氢氰酸挥发、泄漏或被氧化分解。
总结起来,氢氰酸的工艺技术主要包括原料制备、反应过程控制、安全措施以及储存与运输等方面。
只有掌握了科学准确的工艺技术,才能确保氢氰酸的生产过程安全可靠,并为其广泛应用于各类产业提供有力的支持。
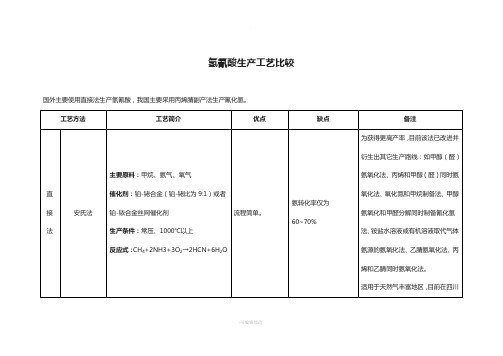
氢氰酸生产工艺比较
打造全网一站式需求
欢迎您的下载,资料仅供参考
生产条件:440~450℃
主副反应方程式为:
2CH6+2NH3+3O2→2C3H3N+6H2O
生成氰化氢的副反应为:
CH3CH=CH2+O2→3HCN+6H2O
副产品氰化氢约为主产品丙烯腈的0.1~0.15倍。
大型丙烯腈装置副产氢氰酸在目前是成本最低、最经济
的方法。
易燃易爆气体的泄露
THANKS !!!
2NH3→N2+ 3H2
CnH2n+2→nC + (n+1)H2
原料易得;尾气可回收利用。
1、耗电高(1吨氢氰酸耗电6400Kw/h);
2、原料、中间产品和最终产品多为易燃易爆或剧毒有害物质,生产操作安全风险大;
3、反应炉运转周期短,检修频繁;
4、副产炭黑污染环境
间
接
法
丙烯腈副产法
主要原料:丙烯、氨和空气;
氨转化率仅为60~70%
为获得更高产率,目前该法已改进并衍生出其它生产路线:如甲醇(醛)氨氧化法、丙烯和甲醇(醛)同时氨氧化法、氧化氮和甲烷制备法、甲醇氨氧化和甲醛分解同时制备氰化氢法、铵盐水溶液或有机溶液取代气体氨源的氨氧化法、乙腈氨氧化法、丙烯和乙腈同时氨氧化法。
适用于天然气丰富地区,目前在四川地区常用
2、反应使劲较长,NH3和CH4可分解为N2和焦炭,影响产率。
为改进技术,原料方面:加氢使碳、氮、氢的摩尔比为1:1.33:13,避免炭黑形成;催化剂方面:在铂催化剂中掺杂0.01~20mol铜、银、金、钯、钨等元素,或通过使用Al2O3改善催化剂,提高产率;设备方面,通过在原反应管中放入有小孔的导气管,加速混合反应气的速度来提高产率。
氢氰酸生产乳酸的工艺流程

氢氰酸生产乳酸的工艺流程英文回答:Hydrocyanic acid (HCN) is an important chemical compound used in various industries, including pharmaceuticals, plastics, and dyes. One of the processes to produce lactic acid from HCN involves several steps.The first step is the hydrolysis of HCN to form ammonium formate (NH4HCOO). This reaction is typically carried out in the presence of a catalyst, such as sulfuric acid (H2SO4) or phosphoric acid (H3PO4). The reaction can be represented as follows:HCN + 2H2O → NH4HCOO.In the next step, the ammonium formate is subjected to a thermal decomposition process to produce formic acid (HCOOH) and ammonia (NH3). The reaction is typically carried out at elevated temperatures, around 200-250°C,and under pressure. The reaction can be represented as follows:NH4HCOO → HCOOH + NH3。
The formic acid produced in the previous step is then subjected to a catalytic hydrogenation process to convertit into lactic acid. This reaction is typically carried out in the presence of a suitable catalyst, such as a metal catalyst like platinum (Pt) or palladium (Pd). The reaction can be represented as follows:HCOOH + H2 → CH3CHOHCOOH.The lactic acid produced in the previous step can be further purified and concentrated through various separation techniques, such as distillation or crystallization, to obtain the desired product.中文回答:氢氰酸(HCN)是一种重要的化学物质,广泛应用于制药、塑料和染料等多个行业。
氢氰酸的制法

氢氰酸的制法氢氰酸的制法:在装有饱和碳酸氢钠溶液的试管中加入少量铝粉,若发生爆鸣声则表示反应进行完毕。
取出上层清液加热浓缩,冷却后加稀硫酸煮沸,若红色褪去,证明已反应。
向剩余物加热至无红色反应为止,放冷后加稀盐酸搅拌,过滤。
滤液蒸干,残渣用少量水溶解,再加盐酸使成碱液,滤过,沉淀用水洗涤数次,洗水合并入滤液,蒸干。
取此液的固体氢氰酸用稀硫酸酸化,蒸发至干,得白色粉末,即氢氰酸成品。
若未全部反应,可再加热,趁热过滤,再蒸干,如此反复进行,直至不再产生气体,即为合格。
现举一例:将两克氢氧化钠溶于三毫升水中并加热煮沸,使其溶解,再加入20毫升浓氨水。
充分搅拌使其溶解后,再加热,在产生大量的白烟后加入2克无水碳酸氢钠,加热,趁热将所得溶液蒸干,趁热过滤[gPARAGRAPH3]即得。
注意:要使这种方法大量生产氢氰酸,需要利用过量的碳酸氢钠在高温下与氰化物反应生成碳酰胺,而氰化物在较低温度下才能与碳酸氢钠反应生成碳酸氢钠,因此需要在试管口塞入一块石棉,加热时使碳酸氢钠和氰化物同时挥发出来,在回流中吸收过量的碳酸氢钠生成碳酰胺,同时蒸干,就可使过量的碳酸氢钠被蒸出来,并且有效地控制了反应温度。
同样也是可以通过提高反应温度使得碳酸氢钠和氰化物同时挥发出来,从而避免损失,另外,由于没有额外添加助剂,因此保持了原料本身的物理特性。
5。
通过电解氰化钠的溶液或以液态的溶液为原料与二氧化碳反应而得到氢氰酸。
另外,以二氧化碳或碳酸钠为原料,在催化剂存在下,用盐酸或氢氧化钠进行复分解反应而得到氢氰酸。
4。
由氰化银与氢氧化钠溶液作用制得,或将碳酸钠和氰化银溶于水,通入二氧化碳制得。
注意:实际上氢氰酸常采用间歇法生产,也即将适量碳酸氢钠、氢氧化钠加热,使其溶解,然后通入二氧化碳,继续反应。
每生成10g氢氰酸约需要消耗25kg的氢氧化钠、 10kg的碳酸氢钠和50kg的二氧化碳。
但是由于二氧化碳和氢氰酸的摩尔比为1: 5,相对氢氰酸的生成速率要快得多,因此可以大幅度提高生产效率。
氢氰酸生产工艺

氢氰酸生产工艺1、氢氰酸的用途氰化氢HCN亦名无水氢氰酸。
是一种剧毒化学品在常温常压下极易扩散。
这种性质使它在运输和使用中受到限制,甚至还可能被恐怖分子用来危害人类。
鉴于这些,主要的氢氰酸生产国家开始对氢氰酸的生产和使用进行了严格的限制。
在美国一些主要道路上已被禁止运输氢氰酸,一些出口商必须从相关政府获得出口证书,同时保证它的合法使用才可以出口。
氢氰酸的用途很广,可用于制造尼龙、杀虫剂、丙烯腈和丙烯酸树脂、金银铜等的电镀、金银等的采矿业、制药灭鼠药、有机合成等离子蚀刻等。
尤其是已二醇和甲基丙烯酸酯树脂,对氢氰酸的需求就显示出很大的市场强劲。
仅在美国2007年对氢氰酸的需求量将达84.8万吨,就世界范围来说全世界氢氰酸年产量约120万吨左右,且每年以1~1.5的速度递增,其中74%来源于直接法生产,其余来自丙烯腈的副产。
为了确保使用安全、减少对环境的影响、提高生产效率、合理利用资源,必须加快对氢氰酸合成技术与生产工艺的研究,以满足不断增长的市场需求。
2、氢氰酸生产工艺生产HCN的传统工艺主要有Andrussow法以及由它引出的一系列氨氧化法、BMA 法、丙烯腈副产法、轻油裂解法。
在国外主要使用直接法,也就是Andrussow法。
我国主要采取丙烯腈副产法生产氰化氢。
主要氢氰酸生产企业有上海石化股份有限公司、大庆石化总厂、抚顺石化公司、河北诚信、安徽曙光等。
2.1、安氏法氨氧化法就是在氨氧化催化剂的存在下,将氨源和氧源以及可氨氧化的有机物高温转化为氰化物的方法。
最传统的氨氧化法是Andrussow法,是由德国I.G公司安德罗索夫(L.Andrussow)提出,并在德国首先实现工业化生产氢氰酸的一种方法。
Andrussow法亦称安氏法或直接法,采用的主要原料是甲烷、氨气和氧气,故又叫甲烷氨氧化法。
它是20世纪50年代完成的工业生产方法,是生产氢氰酸的主要方法。
该法是在常压、1000℃以上的条件下,将原料混合气通入由铂、铑合金催化剂(铂和铑按9:1制成直径为0.076 mm的丝网)或由铂铱合金制成的丝网状催化剂床,进行的氨氧化反应,其反应式为:2CH4+2NH3+3O2→2HCN+6H2O需要注意的是,该法的转化率一般为60~70%,且为保证产率,生产过程要求较高的温度和较短的时间,使反应速度达到平衡。
工业氢氰酸的技术要求

工业氢氰酸的技术要求1. 引言工业氢氰酸(Hydrogen Cyanide,简称HCN)是一种重要的化工原料,在许多工业领域有着广泛的应用。
本文将详细介绍工业氢氰酸的技术要求,包括生产过程、质量控制、安全环保等方面。
2. 生产过程工业氢氰酸的生产过程通常采用丙烯腈法(Acrylonitrile process)。
该方法以丙烯腈为原料,在催化剂的作用下与水反应生成氨基丙腈,再经过水解得到氢氰酸。
具体步骤如下:1.原料准备:准备高纯度的丙烯腈和水。
2.反应器装置:选择合适的反应器装置,确保反应能够顺利进行。
3.催化剂选择:选择合适的催化剂,常见的催化剂有碱金属盐类或过渡金属络合物。
4.反应条件控制:控制反应温度、压力和反应时间等参数,以提高产率和选择性。
5.分离纯化:采用适当的方法对反应产物进行分离和纯化,得到高纯度的氢氰酸。
3. 质量控制为了确保工业氢氰酸的质量符合要求,需要进行严格的质量控制。
以下是常见的质量控制要求:3.1 纯度工业氢氰酸的纯度要求通常在99%以上,其中杂质含量需控制在一定范围内。
常见的杂质包括水、丙烯腈、氰化物等。
3.2 含水量工业氢氰酸中水分含量对产品性能有重要影响,通常要求含水量低于0.5%。
可以通过适当的干燥方法降低含水量。
3.3 酸碱度工业氢氰酸的酸碱度需控制在一定范围内,以确保其稳定性和安全性。
一般要求酸碱度在pH 2-4之间。
3.4 杂质检测对工业氢氰酸中可能存在的有害杂质进行检测和限制,以确保产品符合相关标准和法规要求。
4. 安全环保在工业氢氰酸生产过程中,安全环保是至关重要的。
以下是一些常见的安全环保措施:4.1 生产设备安全确保生产设备的完好性和可靠性,定期进行维护和检修,防止泄漏和事故发生。
4.2 废气处理对生产过程中产生的废气进行有效处理,采用合适的废气处理设备,如吸附剂、催化剂等。
4.3 废水处理对生产过程中产生的废水进行有效处理,采用合适的废水处理方法,如中和、沉淀、膜分离等。
氢氰酸的制法

氢氰酸的制法
1.制法
可由氰化钠、氨水和氢氧化钾溶液的反应,即[gPARAGRAPH3]和氢氧化钠固体混合,通入氨气(来自空气中)制得。
(参见教材35页图5-26)氢氰酸,也叫氰化氢,有剧毒,用途很广。
它可作为化学试剂,医药工业的原料和防腐剂等,也用于灭火器的制造。
2.药物用作催眠药、镇痛药、麻醉剂及解救氰化物中毒的特效药。
具镇静、镇痛、止呕吐、催眠作用,用于各种手术前后或妇女分娩前后的催眠止痛。
氢氰酸被广泛地用于治疗癌症和治疗其他一些疾病,但是这些治疗方法却存在着致命的风险。
2003年,日本药物评价委员会认定氢氰酸为第二类致癌物。
氢氰酸容易穿透皮肤、粘膜和消化道,而且可以通过胎盘屏障。
母亲或准妈妈对氰化氢的敏感性增加,尤其是怀孕后期。
这是因为体内可利用的甲状腺激素的减少引起的。
不论氰化物进入体内多少,都是直接影响DNA。
一旦血液中的浓度达到1mg/L,就能够致人死亡。
3.氢氰酸有三个同分异构体:氢氰酸的危害氰化物对机体的危害很大,吸入氰化物后会出现流涎、多汗、头晕、头痛、乏力、恶心、呕吐等症状,严重时可致呼吸困难、心力衰竭而死亡。
氰化物主要经呼吸道侵入人体并在局部组织细胞内蓄积,使组织细胞内外窒息。
由于无色无味,吸入高浓度氰化物可能没有明显的感觉,但对呼吸中枢的危害很大。
2.MgSO4(aq)+2H2Cl=Na2CO3(aq)+H2O(aq)亚硝酸钠与氰化钠溶液加热煮沸,然后冷却结晶,析出的固体加热至熔融再重新结晶,
可得纯品。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
氢氰酸生产工艺
1、氢氰酸的用途
氰化氢HCN亦名无水氢氰酸。
是一种剧毒化学品在常温常压下极易扩散。
这种性质使它在运输和使用中受到限制,甚至还可能被恐怖分子用来危害人类。
鉴
于这些,主要的氢氰酸生产国家开始对氢氰酸的生产和使用进行了严格的限制。
在美国一些主要道路上已被禁止运输氢氰酸,一些出口商必须从相关政府获得出口
证书,同时保证它的合法使用才可以出口。
氢氰酸的用途很广,可用于制造尼龙、杀虫剂、丙烯腈和丙烯酸树脂、金银铜等的
电镀、金银等的采矿业、制药灭鼠药、有机合成等离子蚀刻等。
尤其是已二醇和甲基丙烯酸酯树脂,对氢氰酸的需求就显示出很大的市场强劲。
仅
在美国2007年对氢氰酸的需求量将达84.8万吨,就世界范围来说全世界氢氰酸年产量
约120万吨左右,且每年以1~1.5的速度递增,其中74%来源于直接法生产,其余来
自丙烯腈的副产。
为了确保使用安全、减少对环境的影响、提高生产效率、合理利用资源,必须加快
对氢氰酸合成技术与生产工艺的研究,以满足不断增长的市场需求。
2、氢氰酸生产工艺
生产HCN的传统工艺主要有Andrussow法以及由它引出的一系列氨氧化法、BMA 法、丙烯腈副产法、轻油裂解法。
在国外主要使用直接法,也就是Andrussow法。
我国主要采取丙烯腈副产法生产氰化氢。
主要氢氰酸生产企业有上海石化股份有限
公司、大庆石化总厂、抚顺石化公司、河北诚信、安徽曙光等。
2.1、安氏法
氨氧化法就是在氨氧化催化剂的存在下,将氨源和氧源以及可氨氧化的有机物高温
转化为氰化物的方法。
最传统的氨氧化法是Andrussow法,是由德国I.G公司安德罗索夫(L.Andrussow)提出,并在德国首先实现工业化生产氢氰酸的一种方法。
Andrussow法亦称安氏法或直接法,采用的主要原料是甲烷、氨气和氧气,故又叫
甲烷氨氧化法。
它是20世纪50年代完成的工业生产方法,是生产氢氰酸的主要方法。
该法是在常压、1000℃以上的条件下,将原料混合气通入由铂、铑合金催化剂(铂
和铑按9:1制成直径为0.076 mm的丝网)或由铂铱合金制成的丝网状催化剂床,进行
的氨氧化反应,其反应式为:
2CH4+2NH3+3O2→2HCN+6H2O
需要注意的是,该法的转化率一般为60~70%,且为保证产率,生产过程要求较高的温度和较短的时间,使反应速度达到平衡。
直接法程序较简单,这也是现在该法仍为主要生产方法的原因之一。
但在这样高的
温度下产率并不是很高,而且在该法中也存在着其他方面的很多不足之处,如:考虑到
反应过程中的放热性和爆炸极限问题,必须使反应物的浓缩相对稀释以避免反应物过热
而使产率下降,那么对大量的尾气处理就会加大投资。
除此之外反应温度很高,加热和
冷却的时间太长,同时该法对氨的利用率只有60-70%,所以对剩余氨的循环利用也是必须解决的问题。
为了解决这些不足之处,人们已经从不同角度对直接法进行了改进以
求获得更高的产率。
在原料路线上的改进有甲醇(醛)氨氧化法,该法甲醇原料充足,价格上有竞争力,安全方面也具有优势。
丙烯和甲醇(醛)同时氨氧化法:由于丙烯氨氧化与甲醇氨氧化的机理相似,所以
甲醇的加入不仅不会影响丙烯的反应,反而可使氢氰酸产量增加2倍多,同时还可得到一种用途很广的副产品丙烯腈。
氧化氮和甲烷制备法:主要解决直接法尾气残余氨含量较高,以致残余的氨与HCN 聚合,因而必须除去的问题,同时引入一种可增加寿命的新型催化剂,它是将铂、钴等
涂在二氧化硅基体上制成的网状催化剂。
甲醇氨氧化和甲醛分解同时反应制备氰化氢的方法:由于甲醇氨氧化放热而甲酰胺分解吸热,如在该法中合理选择反应物比例,就可避免在直接法和甲醇氨氧化法中由于
反应放热而必须使反应物相对稀释带来的麻烦。
铵盐水溶液或有机溶液取代气体氨源的氨氧化法:因溶液分散得很细,可与氨氧化
催化剂充分接触,在溶剂蒸发后,可氨氧化的有机物和氧在催化剂表面发生氨氧化反应
生成氢氰酸,该法明显提高了反应物的利用率。
还有乙腈氨氧化法、丙烯和乙腈同时氨氧化法等。
催化剂方面,如甲醇(醛)氨氧化法中Fe—Mo氧化物催化剂的研究、磷一矾氧化
物催化剂的使用、铂床催化剂以及铂一铑催化剂的研究等,这些都不同程度地增加了催
化剂的寿命和活性。
当然这些改进并没有使直接法中的所有不足得到弥补,但这充分说明了氨氧化法制备氢氰酸的潜力所在,它有待于进行更深层次的研究。
2.2、BMA法
BMA法也是一种传统的工艺方法,它产生于与20世纪50年代末。
它是对Andrussow法的改进,即在BMA法中不需要氧气参加反应。
是甲烷和氨气在常压、l3000C以上的条件下进行的反应,使用的催化剂是管状的铂固定反应床,长约2m,内径约16 ~l8 mm。
该反应是在铂床的内表面进行的,为了保证反应温度,一般在管状催化剂的周围充
入可燃性气体。
反应过程是将甲烷和氨气的混合气体通入反应床,并迅速加热到
1300℃。
需要注意为了避免催化剂生碳,甲烷和氨气最好按分子数比为 1.08:l.001反应。
反应式为NH3+CH4=HCN+3H2。
该法的产率为80~85%,很显然与直接法相比产率有所提高,而且生成的氢气还可
以循环利用,但使用该法生产氢氰酸投资很大,而且与安氏法相比反应时间较长,造成
更多的NH3和CH4分解为N2和焦炭,从而影响了产率。
为改进该法,在原料方面Car Voigt等人通过加氢使碳、氮、氢的摩尔比为1:1.33:13,以避免炭黑的形成。
在催化剂方面为避免催化剂生碳,在铂催化剂中掺杂0.01~20mol的铜、银、金、钯、钨等元素,使催化剂的寿命增长,活性增加。
Al2O3催化剂在BMA法中的使用也可改善催化剂提高产率。
设备方面,Friedrich Bittner等人则通过在原反应管中放入有小孔的导气管,加速
混合反应气的速度来提高产率。
2.3、丙烯晴副产法
丙烯腈副产法是20世纪60年代开发的索亥俄工艺,它是用丙烯氨氧化法制丙烯腈副产氢氰酸的方法。
世界丙烯脂生产约90%采用该工艺。
该法以石油气中丙烯、氨和空气为原料,丙烯与氨按一定比例混合送入氧化反应器,由分布器均匀分散到催化剂床层中,空气按一定比例从反应器底部进入经分布板向上流。
