氟化氢 密度
氟化氢[无水]-理化性质及危险特性表
![氟化氢[无水]-理化性质及危险特性表](https://img.taocdn.com/s3/m/74350008fbd6195f312b3169a45177232f60e489.png)
吸入:立即脱离现场,吸氧,保持呼吸道通畅。用2%~4%碳酸氢钠溶液洗鼻、漱口、雾化吸入。
皮肤接触:立即用大量清水彻底冲洗,至少20~30min,可适当应用中和剂,如3%氢氧化钙溶液冲洗、浸泡或湿敷。眼睛接触:立即用大量清水或生理盐水冲洗至少15min。就医。食入:立即给服6片葡萄糖酸钙或碳酸钙(事先化在水中),不要催吐。就医。根据临床表现和血钙情况,可适当补充钙剂。
储运条件
储存注意事项:储存于阴凉、通风的库房。远离火种、热源。库温不宜超过30℃。应与易(可)燃物、食用化学品分开存放,切忌混储。储区应备有泄漏应急处理设备。应严格执行极毒物品“五双”管理制度。运输注意事项:铁路运输时应严格按照铁道部《危险货物运输规则》中的危险货物配装表进行配装。起运时包装要完整,装载应稳妥。运输过程中要确保容器不泄漏、不倒塌、不坠落、不损坏。严禁与易燃物或可燃物、食用化学品等混装混运。运输时运输车辆应配备泄漏应急处理设备。运输途中应防曝晒、雨淋,防高温。公路运输时要按规定路线行驶,勿在居民区和人口稠密区停留。
燃烧爆炸危险性
燃烧性
不燃
燃烧分解物
无资料
闪点(℃)
无资料
爆炸上限(v%)
无资料
引燃温度(℃)
无资料
爆炸下限(v%)
无资料
危险特性
氟化氢为反应性极强的物质,能与各种物质发生反应。腐蚀性极强。
建规火险分级
戊类
稳定性
稳定
聚合危害
不聚合
禁忌物
易燃物、可燃物,并与大部分物质禁配。
灭火方法
消防人员须佩戴空气呼吸器,穿全身耐酸碱消防服,在上风向灭火。尽可能将容器从火场移至空旷处。喷水保持火场容器冷却,直至灭火结束。
泄漏处理
耐氢氟酸防腐涂料

耐氢氟酸防腐研究论述氟化氢(化学式:HF),由于氟原子电负性很大,所以会与氢原子形成氢键的化合物。
氟化氢是一种极强的腐蚀剂,有剧毒。
它是无色的气体,但是在空气中,只要超过3ppm就会产生刺激的味道。
氟化氢是一种无色透明的发烟液体,为氟化氢气体的水溶液。
相对密度为1.128(40%),有刺激性气味。
为一中等强度的酸。
在稀溶液中氢氟酸微离解成离子,在较浓的溶液中,氢氟酸发生聚合作用而生成H2F2分子,它离解为H2F2=H+HF2-腐蚀性极强,能腐蚀玻璃和硅酸盐而生成气态的四氟化硅,极易挥发,与金属盐类、氧化物、氢氧化物作用生成氟化物,不腐蚀聚乙烯及白金,氢氟酸即不能进行氧化反应,也不能进行还原反应。
有剧毒!触及皮肤则溃烂最浓时的密度1.14g/cm3,沸点393.15K(120℃)。
具有弱酸性,但浓时的电离度比稀时大而与一般弱电解质有别。
现在北京志盛威华化工有限公司研发科技人员,经过五年的市场跟踪调查和试验室不断反复试验,推出的耐氢氟酸特种防腐涂料,ZS-1033耐氢氟酸防腐涂料选用酚醛树脂、重晶石、纳米铬粉、防介质固体填料等特种材料精加工而成,涂层致密稳定,耐强酸腐蚀,特别是耐氢氟酸(HF)腐蚀效果好,涂料也能防住氢离子渗透,能好的保护金属和其他材质不被腐蚀。
经过专家和工况的具体使用,材料的特性和应用效果特到专家和现场人员的一致好评氢氟酸之水溶液是一种弱酸。
由于H-F共价键高度极性以及氟化氢具有分子间氢键,使得氟化氢具有高度能学稳定性,离解度非常低。
因此,离解生成之水合氢离子浓度较低,使酸度常数Ka较低。
由此氟化氢为弱酸。
HF(aq) + H2O(l)←→ H3O+(aq)+ F-(aq)Ka=7X10-4 mol dm-3其他卤化氢于水中浓度增加,酸度会下降。
HA(aq) + H2O(l)←→ H3O+(aq)+ A-(aq)对于一般氢卤酸,卤化氢浓度上升至某个程度,每单位体积溶液中之含水量急剧下降,令此反应之平衡位置趋向左边,使离解度下降,酸性下降。
碳酰氟和氟化氢

碳酰氟和氟化氢全文共四篇示例,供读者参考第一篇示例:碳酰氟和氟化氢是两种重要的氟化学品,它们在有机合成、医药、材料科学等领域拥有广泛的应用。
本文将对碳酰氟和氟化氢的物理性质、化学性质、用途及安全性等方面进行详细的介绍,希望能为大家对这两种化学品有更深入的了解。
碳酰氟(Carbonyl fluoride,化学式为COF₂)是一种无色、具有刺激性气味的液体,密度为1.876 g/cm³,沸点为8.77℃。
碳酰氟在常温下易挥发,极易与水反应生成碳酸氟化氢并释放氟化氢气体。
碳酰氟是一种有机合成中的重要试剂,它可以用于合成酸酐、酰胺、酯等化合物。
碳酰氟还可用于金属表面处理、医药中间体的制备等领域。
碳酰氟和氟化氢都是有毒化学品,对人体有一定的危害。
碳酰氟的蒸气可引起呼吸道刺激、头晕、咳嗽等症状,长期接触可引起中毒。
而氟化氢对眼睛、皮肤和呼吸道有强烈的刺激性,接触过量可导致化学灼伤。
在使用这两种化学品时,必须严格按照操作规程进行,并保证充分的通风条件。
第二篇示例:要的应用价值。
本文将详细介绍碳酰氟和氟化氢的性质、制备方法以及应用领域。
碳酰氟(Carbonyl fluoride)是一种无色气体,化学式为COF2,分子量为66.01g/mol,其结构中包含一个碳原子和两个氟原子。
碳酰氟在室温下为液态,熔点为-124°C,沸点为-85°C。
碳酰氟是一种有机氟化合物,具有刺激性气味,易燃易爆,对皮肤、眼睛和呼吸道有刺激作用。
碳酰氟主要用于有机合成中的氟化反应,例如可以将碱性氨基团转化为氟取代基团。
碳酰氟还可以作为氟代试剂,用于氟取代反应中的催化剂。
碳酰氟和氟化氢的制备方法主要有以下几种:1.碳酰氟的制备方法:(1)从氟甲酸铅盐和五氧化二磷反应制得。
(2)从六氟丙酸和亚磷酸酐反应制得。
(3)从氟和二氧化碳气体在高温下反应制得。
碳酰氟和氟化氢在化学领域具有广泛的应用价值。
碳酰氟可以用于有机合成中的氟化反应,可以将化合物中的碱性氨基团转化为氟取代基团,从而改变分子的性质和活性。
化学危害因素简介——氟化氢

氟化氢品名氟化氢; Hydrogen fluoride; CAS:7664-39-3理化性质无色气体或液体。
空气中冒烟。
有强刺激性气味。
分子式H-F。
分子量20.01。
相对密度 1.27(34℃)。
凝固点-83.55℃。
沸点19.5℃。
蒸气压53.32kPa(400 mmHg 2.5℃)。
纯度为99~99.97 % 。
易溶于水、醇; 溶于许多有机溶剂; 微溶于乙醚。
溶于水,生成氢氟酸并放出热量。
腐蚀性很强,能侵蚀玻璃、混凝土、某些含二氧化硅的金属,如铸铁、天然橡胶、皮革、粗陶瓷制品、许多有机物质。
不易燃,但与某些金属反应生成可燃性氢气。
高热能引起钢并爆炸。
加热放出高毒和腐蚀性氟化物。
不易受氧化剂氧化。
消防措施消防人员必须在有防爆掩蔽处操作,穿戴防毒面具和全身防护服用水保持火场中容器冷却。
储运须知包装标志:腐蚀品和毒害品。
包装方法:(I)类。
用特殊钢瓶装。
储运条件:储存于通风良好的不燃库房。
与其他仓库隔离。
放置容器须防碰损。
远离热源和火源。
工作人员必须穿戴全身防护服(包括长袖工作服、氧气防毒面具、安全帽和橡胶手套、脚套)。
泄漏处理对钢瓶漏出气处理必须戴好全身防护服,用排风机排送至水洗塔或与塔相连的通风橱内。
接触机会参见氢氟酸。
侵入途径经呼吸道吸收。
毒理学简介人吸入TCLo: 100 mg/m3/1M; LCLo: 50 ppm/30M。
大鼠吸入LC50: 1276 ppm/1H。
小鼠吸入LC50: 342 ppm/1H; 经皮LDLo: 500 mg/kg。
经呼吸道吸收后,约75%与白蛋白结合,由尿、粪排出。
溶于体内的水分形成氢氟酸而起作用。
人在25mg/m^3下已感到刺激; 26mg/m^3下耐受数分钟; 在50mg/m^3时引起眼和鼻粘膜刺激症状,流泪、流涕、喷嚏、鼻塞, 感皮肤刺痛; 100mg/m^3浓度下只能耐受1分钟; 400~430mg/m^3 浓度下,急性中毒致死。
急性毒性主要表现为眼、粘膜和上呼吸道刺激,呼吸困难,尸检可见肺部充血、出血、水肿,以及肝、肾损害。
氟化氢HF

氟化氢HF1.别名·英文名(无水)氢氟酸;Hydrogen fluoride、Anhydrous hydrofluoricacid.2.用途制备氟里昂气及其它氟化物,乙醇、乙醛、乙醚的溶剂(液态氟化氢),聚合、烃化等反应的催化剂,玻璃雕刻,杀菌剂,清洗金属,清洗铸件,电镀,滤纸的处理,矿石类的分析,锗、硅的蚀刻剂。
3.制法(1)萤石和浓硫酸作用:CaF2+H2SO4→2HF+CaSO4(2) CaF2+2HNO3→Ca(NO3)2+2HF(3) Fz+H2→2HF4.理化性质分子量:20.0064熔点(三相点):-83.4℃沸点(101.325kPa):19.5℃液体密度(20℃,103.453kPa):968kg/m3气体密度(25℃,101.325kPa): 2.201kg/m3相对密度(气体,空气=1,25℃,101.325kPa):1.858比容(21.1℃,101.325kPa): 1.2048m3/kg临界温度:188.0℃临界压力:6485kPa临界密度:290kg/m3压缩系数:熔化热(-83.4℃):196.355 kJ/kg气化热(19.51℃,101.325kPa):374.72 kJ/kg比热容(气体,30℃,101.325kPa):Cp=40355.3J/(kg·K)Cv=2383 J/(kg·K)比热比(气体,30℃,101.325kPa):Cp/Cv=16.93蒸气压(-20℃):21.5kPa(0℃):52.5kPa(30℃):155kPa粘度(1~100kPa,0℃):0.0114mPa·S(液体,0℃):0.256mPa·S表面张力(0℃):10.1mN/m导热系数(1~100kPa,0℃):0.02353W/(m·K)折射率(气体,25℃,5893?): 1.1574毒性级别: 4易燃性级别:0易爆性级别:0氟化氢是具有刺鼻恶臭和强烈刺激性的无色有毒腐蚀性气体。
氟化氢

1、物质的理化常数国标编号: 81015 CAS: 7664-39-3中文名称: 氟化氢英文名称: Hydrogen fluride别名: 氢氟酸;氟氢酸分子式: HF 分子量: 20.01熔点: -83.7℃密度: 相对密度(水=1)1.15;蒸汽压: 易溶于水溶解性: 溶于水,微溶于醇稳定性: 稳定外观与性无色液体或气体状:危险标记: 20(酸性腐蚀品)用途: 用于蚀刻玻璃,以及制氟化合物2.对环境的影响:一、健康危害侵入途径:吸入、食入。
健康危害:对呼吸道粘膜及皮肤有强烈的刺激和腐蚀作用;吸入高浓度的氟化氢可引起支气管炎和肺炎;吸收后可产生全身的毒作用,还可导致氟骨症。
急性中毒:接触高浓度氟化氢,可引起眼及呼吸道粘膜刺激症状,严重者可发生支气管炎、肺炎,甚至产生反射性窒息。
慢性中毒:引起鼻、咽、喉慢性炎症,严重者可有鼻中隔穿孔。
骨骼损害可引起氟骨病。
氟化氢能穿透皮肤向深层渗透,形成坏死和溃疡,且不易治愈。
二、毒理学资料环境行为急性毒性:LC501276ppm,1小时(大鼠吸入);人在氟化氢400~430mg/m3浓度下,可引起急性中毒致死;100mg/m3浓度下,能耐受1分多钟,50mg/m3下感到皮肤刺痛、粘膜刺激,26mg/m3下能耐受数分钟,嗅觉阈值为0.03mg/m3。
亚急性和慢性毒性:家兔吸入33~41mg/m3,平均20mg/m3,经过1~5.5个月,可出现粘膜刺激,消瘦,呼吸困难,血红蛋白减少,网织红细胞增多,部分动物死亡。
致突变性:DNA损伤:黑胃果蝇吸入1300ppb(6周)。
性染色体缺失和不分离:黑胃果蝇吸入2900ppb。
生殖毒性:大鼠吸入最低中毒浓度(TCL0):4980ug/m3(孕1~22天),引起死胎。
皮肤损害:氢氟酸对皮肤有强烈的腐蚀性,渗透作用强,并对组织蛋白有脱水及溶解作用。
接触皮肤后可迅速穿透角质层,渗入深部组织,溶解细胞膜,引起组织液化、坏死,形成较难愈合的溃疡。
氟化氢

(1)化学品及企业标识化学品中文名:氟化氢化学品英文名: hydrogen fluoride分子式:HF相对分子量:20.01(2)成分/组成信息成分:纯品CAS No:7664-39-3(3)危险性概述危险性类别:第8.1类酸性腐蚀品侵入途径:吸入、食入健康危害:对呼吸道粘膜及皮肤有强烈的刺激和腐蚀作用。
急性中毒:吸入较高浓度氟化氢,可引起眼及呼吸道粘膜刺激症状,严重者可发生支气管炎、肺炎或肺水肿,甚至发生反射性窒息。
眼接触局部剧烈疼痛,重者角膜损伤,甚至发生穿孔。
氢氟酸皮肤灼伤初期皮肤潮红、干燥。
创面苍白,坏死,继而呈紫黑色或灰黑色。
深部灼伤或处理不当时,可形成难以愈合的深溃疡,损及骨膜和骨质。
本品灼伤疼痛剧烈。
慢性影响:眼和上呼吸道刺激症状,或有鼻衄,嗅觉减退。
可有牙齿酸蚀症。
骨骼X线异常与工业性氟病少见。
环境危害:对环境有危害燃爆危险:本品不燃,高毒,具强腐蚀性、强刺激性,可致人体灼伤。
(4)急救措施皮肤接触:立即脱去污染的衣着,用大量流动清水冲洗至少15分钟。
就医。
眼睛接触:立即提起眼睑,用大量流动清水或生理盐水彻底冲洗至少15min。
就医吸入:迅速脱离现场至空气新鲜处。
保持呼吸道通畅。
如呼吸困难,给输氧。
如呼吸停止,立即进行人工呼吸。
就医食入:用水漱口,给饮牛奶或蛋清。
就医(5)消防措施危险特性:氟化氢为反应性极强的物质,能与各种物质发生反应。
腐蚀性极强。
有害燃烧产物:氟化氢灭火方法:消防人员必须穿特殊防护服,在掩蔽处操作。
喷水保持火场容器冷却,直至灭火灭火注意事项及措施:消防人员必须穿全身耐酸碱消防服、佩戴空气呼吸器灭火。
尽可能将容器从火场移至空旷处。
喷水保持火场容器冷却,直至灭火结束。
(6)泄漏应急处理应急行动:迅速撤离泄漏污染区人员至安全区,并立即隔离150m,严格限制出入。
建议应急处理人员戴自给正压式呼吸器,穿防酸碱工作服。
尽可能切断泄漏源。
防止流入下水道、排洪沟等限制性空间。
氟化氢性质
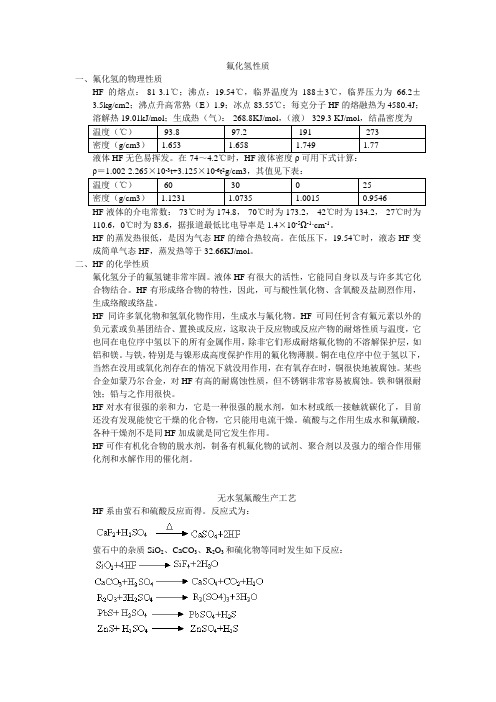
氟化氢性质一、氟化氢的物理性质HF的熔点:-81-3.1℃;沸点:19.54℃,临界温度为188±3℃,临界压力为66.2±3.5kg/cm2;沸点升高常熟(E)1.9;冰点-83.55℃;每克分子HF的熔融热为4580.4J;溶解热19.01kJ/mol;生成热(气):-268.8KJ/mol,(液)-329.3 KJ/mol,结晶密度为温度(℃)-93.8 -97.2 -191 -273密度(g/cm3) 1.653 1.658 1.749 1.77液体HF无色易挥发。
在-74~4.2℃时,HF液体密度ρ可用下式计算:ρ=1.002-2.265×10-3t+3.125×10-6t2g/cm3,其值见下表:温度(℃)-60 -30 0 25密度(g/cm3) 1.1231 1.0735 1.0015 0.9546HF液体的介电常数:-73℃时为174.8,-70℃时为173.2,-42℃时为134.2,-27℃时为110.6,0℃时为83.6,据报道最低比电导率是1.4×10-5Ω-1·cm-1。
HF的蒸发热很低,是因为气态HF的缔合热较高。
在低压下,19.54℃时,液态HF变成简单气态HF,蒸发热等于32.66KJ/mol。
二、HF的化学性质氟化氢分子的氟氢键非常牢固。
液体HF有很大的活性,它能同自身以及与许多其它化合物结合。
HF有形成络合物的特性,因此,可与酸性氧化物、含氧酸及盐剧烈作用,生成络酸或络盐。
HF同许多氧化物和氢氧化物作用,生成水与氟化物。
HF可同任何含有氟元素以外的负元素或负基团结合、置换或反应,这取决于反应物或反应产物的耐熔性质与温度,它也同在电位序中氢以下的所有金属作用,除非它们形成耐熔氟化物的不溶解保护层,如铝和镁。
与铁,特别是与镍形成高度保护作用的氟化物薄膜。
铜在电位序中位于氢以下,当然在没用或氧化剂存在的情况下就没用作用,在有氧存在时,铜很快地被腐蚀。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
氟化氢密度
介绍
氟化氢(化学式HF)是氢和氟的化合物,是一种无色、剧毒的气体。
它具有很强
的腐蚀性,能够溶解许多常见的物质,甚至包括玻璃。
本文将详细探讨氟化氢的密度及其相关内容。
氟化氢的化学性质
氟化氢是一种极其强酸,在水中离解成氟离子和氢离子,其酸性比硫酸还要强。
这使得氟化氢在实验室和工业上有着广泛的应用。
除了其强酸性外,氟化氢还是一种非常有用的溶剂,在有机合成反应中能够起到催化剂的作用。
氟化氢的物理性质
1.密度:氟化氢是一种气体,在标准温度和压力下,其密度约为0.95 g/cm³。
这使得氟化氢比空气要轻,具有上升的趋势。
2.沸点和熔点:氟化氢的沸点为19.5°C,熔点为-8
3.6°C。
由于其低沸点和
熔点,氟化氢常常以液体形式存储。
3.溶解度:氟化氢在水中有良好的溶解度,能够形成氢键。
这使得氟化氢在
实验室和工业上被广泛应用。
4.气味:氟化氢有一种刺鼻的酸味,极小的浓度就能被人类感知到,这也是
其剧毒性的体现。
氟化氢的制备方法
1.从氧化物制备:最常见的制备氟化氢的方法是通过将金属与矿石中的氧化
物反应得到金属氟化物,再与稀硫酸反应生成氟化氢气体。
2.从氟化物制备:另一种制备氟化氢的常见方法是将氟化物与稀酸反应,然
后通过蒸馏得到氟化氢气体。
氟化氢的应用
1.腐蚀剂:氟化氢是一种极其强酸,因此常用作腐蚀剂,用于蚀刻金属、石
英和玻璃等材料。
例如,在集成电路制造过程中,氟化氢通常用于去除金属
表面的氧化层。
2.催化剂:氟化氢能催化很多有机反应,如酯的加水分解、酮的脱水氟化和
芳香烃的烷基化等。
这使得氟化氢在有机合成中担任着重要角色。
3.冷却剂:由于氟化氢具有低沸点,可以用作制冷剂。
它在若干特定领域,
例如核工业中的离子交换剂制冷装置,具有广泛应用。
氟化氢的安全注意事项
1.剧毒性:氟化氢对人体有很高的毒性。
短时间暴露于高浓度氟化氢下可能
引起头晕、恶心、呼吸不畅甚至危及生命。
因此,在接触氟化氢时需要佩戴
适当的防护设备,保证充分通风,并尽量避免皮肤与氟化氢接触。
2.腐蚀性:氟化氢是一种极强的腐蚀剂,可以与许多物质发生激烈反应。
因
此,在处理氟化氢时需要注意防护设备,并确保合理的操作方法。
3.易燃性:氟化氢能与一些物质发生燃烧反应,产生剧烈的火焰。
因此,在
储存和使用氟化氢时需要注意避免与易燃物质接触,并采取适当的防火措施。
小结
氟化氢是一种具有极高酸性和腐蚀性的化合物,其密度约为0.95 g/cm³。
氟化氢
在实验室和工业上有着广泛的应用,包括作为腐蚀剂、催化剂和冷却剂等。
然而,由于其剧毒性和腐蚀性,处理氟化氢需要严格遵守安全操作规程,确保人身安全和环境保护。
参考文献
1.Emeleus, H.J. and Sharpe, A.G. (2004). “Fluorine”. Inorganic
chemistry. Elsevier Butterworth-Heinemann. pp. 91–96.
2.Cotton, F.A.; Wilkinson, G.; Murillo, C.A.; Bochmann, M. (1999).
Advanced Inorganic Chemistry. New York: Wiley.
3.Housecroft, C.E.; Sharpe, A.G. (2008). “Acidity and basicity”.
Inorganic Chemistry. Pearson.
附录
氟化氢的制备方法
1.从氧化物制备氟化氢:
–将金属与氧化物反应,得到金属氟化物。
–金属氟化物与稀硫酸反应,产生氟化氢气体。
2.从氟化物制备氟化氢:
–将氟化物与稀酸反应。
–通过蒸馏得到氟化氢气体。
氟化氢的应用
•腐蚀剂:用于蚀刻金属、石英和玻璃等材料。
•催化剂:催化有机反应。
•冷却剂:用作制冷剂,例如核工业中的离子交换剂制冷装置。
氟化氢的安全注意事项
•佩戴适当的防护设备,保证充分通风。
•避免皮肤与氟化氢接触。
•注意防护设备,并确保合理的操作方法。
•避免与易燃物质接触,并采取适当的防火措施。
