新药生产的申报与审批流程图
新药和仿制药的申报与审批流程图

药检所注册检验
国家局审批(20d)
申请人 4 个月内一次性补充资料 不符合规定,发给《审批意见通知件》。
符合规定,发给《临床试批件》
符合规定,发给《药品批准证书》
申请人完成临床试验。
认证中心 现场核查
申请人提出现场检查
国家局审批,30d 批准临床试验
申请生产
认证中心 动态抽样 1 批 药检所检验 30d
CDE 进行技术审评
国家局审批 30d
批准生产
仿制药的申报与审批流程图
申请人提著申请
省局受理(5d),现场核查,抽取 3 批样品,资料初审。
国家局 CDE 技术审评(160d),补充资料审评(40d)
新药注册申报程序
IND(申报临床程序)
NDA(申报生产程序)
新药报批程序(28 号令)
申请临床
省局对临床试验情况及原始资料进行现 场核查(抽样 3 批),30d
受理判断
省局对研制情况和原始资料进行现 场核查(不抽样),30d
CDE 进行技术审评,90d
药检所复核,30d CDE 进行技术审评,150d
新药(原料)申报流程
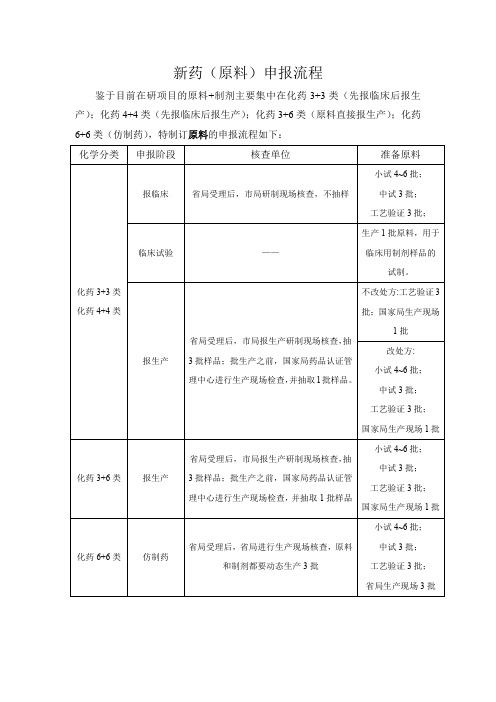
生产现场检查
国家局认证中心通知申请生产现场核查时,准备好一批工艺验பைடு நூலகம்规模用起始 物料,以迎接国家局认证中心的现场核查,核查同时抽取一批样品。
注:化药 3+6 类,原料直接报生产, 制剂要看具体品种:如果是口服固体制剂,制剂国家局临
床批件,做 18-24 例的生物等效性实验,做完临床,把临床部分提交,如果通过,制剂和原料
制剂实验室做质量研究、稳定性研究和生产三批中试规模制剂。 撰写中试记录。 6.中试规模做完 6 个月加速和长期试验以后,可到车间进行工艺验证。 7.若步骤较短或起始物料为关键起始物料,要提供起始物料的工艺流程图和过程 控制标准。 8.工艺验证三批需要分析中心全检,出具检验报告(上报资料需要)后入库,供 制剂做三批工艺验证。 9.若工艺验证三批原料扣除分析中心留样量和制剂工艺验证领取量,所剩余的原 料还能够满足动态核查时做三批制剂,则不需要再准备原料,仅仅备够生产三批 原料所用的起始物料即可;若剩余的原料量不能满足动态核查时做三批制剂,则 还要为制剂准备足够的原料,全检合格后入库,同时备够生产三批原料所用的起 工艺验证 始物料。 阶段 项目组需撰写原料工艺部分的 CTD 资料 3.2.S.2.2~3.2.S.2.6 部分,工艺验证批的 批记录,协同车间完成工艺验证方案和工艺验证报告。
③将小试记录,中试批生产记录和车间批生产记录等交给制剂实验室核对,
以迎接市局研制现场核查。
临床试验用原料 (跟需要做临床 或生物等效性试 验的制剂同时申
报时需要)
国家局收到申报资料后,经审查符合规定,发给《药物临床试验批件》的, 则需要提供一批原料,供生产临床用样品使用(可以用不过期、有剩余的工
艺验证原料)。
中试原料用途:原料的质量研究、稳定性考察;三批中试规模制剂;如资
新药临床申请审批流程图

现在有三种申报方法一.申报1.1类药进口(进口药)(1)方法:a.等药品在国外上市后,不在国内生产。
申请分包进口(类似于代理)。
b.等药品在国外上市后,完善国内厂房技术,在国内生产。
(2)费用:临床实验37.6万,生产59.39万。
(3)难点:a.需要等药物在国外上市后才可以进行,延长周期。
b.如果在国内生产,需要完善国内厂房技术,延长周期、增加费用。
c.如果国外生产,分包进入国内时可以申请免除临床实验,但是不能确定可以申请成 功。
d.需要所有的临床资料,包括所有的实验数据。
二.申报1.1类新药临床试验(国产药)(1)方法:直接在国内申报1类新药,相关药理毒理研究资料由国外进行,提供相关证明,然后工艺研究、质量研究跟稳定性研究在国内进行,等国内药厂达到生产要求后,将药品在国内生产,按照国内药来报。
(2).费用:申请临床实验19.2万,申请生产43.2万。
(3)难点:a.需要等国内工厂具备相关生产条件后才可以进行申报。
b.无法申请避免临床。
三.申报国际多中心临床试验(1)基本流程+费用+时间:主要临床基地伦理委员会审(费用...,时间...)+临床审批(费用37.6万,时间205天)+药品清关(费用...+时间...)(时间相对较短)(2)方法:申报程序与国内1.1类化学新药临床试验申报大致相同,但是需要更多的临床资料和证明性文件。
(3)申请地点:国家药监局 北京市西城区宣武门西大街28号大成广场3门一层(总局办公大楼 西侧),邮编100053(4)流程图:注:斜线前为一般审批时限,斜线后为特殊审批时限,均为工作日。
(5)申报资料列表:(一)概要部分1. 药品名称通用名:替拉扎明汉语拼音:Ti La Zha Ming英文名:Tirapazamine (TPZ)化学名:3-amino-1,2,4-benzotriazine 1,4-di-N-oxide)化学结构式:分子式:C 7H 6N 4O 2分子量:178.14812. 证明性文件 已有资料已整理至“申报资料2_证明性文件_20161203”,其余需根据实际情况请申办人提供国家局药审中心接受审查意见、核查报告、申报资料 药检所检验样品,复核标准(60/30/90日) 药审中心技术审评(90/80) 申请人在4个月内1次性补充资料 药审中心对补充资料的审评(30/20日) 国家局审批(20日) 不批准或退审,发给《审批意见通知件》(10日) 批准进行药物临床试验,发给《药物临床试验批件》(205/195) 临床试验方案及参加单位报国家局、省局备案 实施药物临床试验•申请国际多中心临床试验的,应提供其临床试验用药物在符合药品生产质量管理规范的条件下制备的情况说明。
最新中药新药研发申报流程及相关材料说明

中药新药研发申报流程及相关材料说明中药新药研发申报流程及相关申报材料说明一、中药新药的注册分类及说明1.1注册分类中药新药注册按审批管理的要求分以下几类:1.未在国内上市销售的从植物、动物、矿物等物质中提取的有效成份及其制剂。
2.新发现的药材及其制剂。
3.新的中药材代用品。
4.药材新的药用部位及其制剂。
5.未在国内上市销售的从植物、动物、矿物等物质中提取的有效部位及其制剂。
6.未在国内上市销售的中药、天然药物复方制剂。
7.改变国内已上市销售中药、天然药物给药途径的制剂。
8.改变国内已上市销售中药、天然药物剂型的制剂。
9.仿制药。
1.2说明注册分类1-6的品种为新药,注册分类7、8按新药申请程序申报,注册分类9的品种为已有国家标准的药品。
二、中药新药的研发及申报流程中药新药的研发申报一般按以下程序进行:选题立项——临床前研究——临床研究——申报审批——正式生产,其中,新药临床前及临床研究的主要内容及注意事项分别列举如下:2.1 新药的临床前研究(一)主要内容:新药的临床前研究主要包括制备工艺(中药制剂包括原药材的来源、加工及炮制)、理化性质、纯度、检验方法、处方筛选、剂型、稳定性、质量标准、药理、毒理、动物药代动力学等研究。
新发现中药材还应包括来源、生态环境、栽培(养殖)技术、采收处理、加工炮制等研究。
(二)注意事项:从事新药安全性研究的实验室应符合国家药品监督管理局《药品非临床研究质量管理规范》(GLP)的相应要求,实验动物应符合国家药品监督管理局的有关要求,以保证各项实验的科学性和实验结果的可靠性。
2.2 新药的临床研究(一)主要内容:新药的临床研究包括临床试验和生物等效性试验。
新药的临床试验分为Ⅰ、Ⅱ、Ⅲ、Ⅳ期。
Ⅰ期临床试验:初步的临床药理学及人体安全性评价试验。
观察人体对于新药的耐受程度和药物代谢动力学,为制定给药方案提供依据。
Ⅱ期临床试验:随机盲法对照临床试验。
对新药有效性及安全性作出初步评价,推荐临床给药剂量。
中药新药研发申报流程及相关材料说明

中药新药研发申报流程及相关申报材料说明一、中药新药的注册分类及说明1.1注册分类中药新药注册按审批管理的要求分以下几类:1.未在国内上市销售的从植物、动物、矿物等物质中提取的有效成份及其制剂。
2.新发现的药材及其制剂。
3.新的中药材代用品.4.药材新的药用部位及其制剂.5.未在国内上市销售的从植物、动物、矿物等物质中提取的有效部位及其制剂。
6.未在国内上市销售的中药、天然药物复方制剂。
7.改变国内已上市销售中药、天然药物给药途径的制剂。
8.改变国内已上市销售中药、天然药物剂型的制剂。
9.仿制药。
1.2说明注册分类1—6的品种为新药,注册分类7、8按新药申请程序申报,注册分类9的品种为已有国家标准的药品.二、中药新药的研发及申报流程中药新药的研发申报一般按以下程序进行:选题立项-—临床前研究——临床研究--申报审批——正式生产,其中,新药临床前及临床研究的主要内容及注意事项分别列举如下:2.1 新药的临床前研究(一)主要内容:新药的临床前研究主要包括制备工艺(中药制剂包括原药材的来源、加工及炮制)、理化性质、纯度、检验方法、处方筛选、剂型、稳定性、质量标准、药理、毒理、动物药代动力学等研究。
新发现中药材还应包括来源、生态环境、栽培(养殖)技术、采收处理、加工炮制等研究。
(二)注意事项:从事新药安全性研究的实验室应符合国家药品监督管理局《药品非临床研究质量管理规范》(GLP)的相应要求,实验动物应符合国家药品监督管理局的有关要求,以保证各项实验的科学性和实验结果的可靠性.2。
2 新药的临床研究(一)主要内容:新药的临床研究包括临床试验和生物等效性试验.新药的临床试验分为Ⅰ、Ⅱ、Ⅲ、Ⅳ期。
Ⅰ期临床试验:初步的临床药理学及人体安全性评价试验。
观察人体对于新药的耐受程度和药物代谢动力学,为制定给药方案提供依据。
Ⅱ期临床试验:随机盲法对照临床试验.对新药有效性及安全性作出初步评价,推荐临床给药剂量.Ⅲ期临床试验:扩大的多中心临床试验。
药物申报流程ppt课件

3.2.P.6 对照品 3.2.P.7 稳定性
3.2.P.7.1 稳定性总结 3.2.P.7.2 上市后的稳定性研究 方案及承诺 3.2.P.7.3 稳定性数据
可编辑课件
15
质量控制及稳定性资料CTD格式分析 新药申报
1.CTD质量控制、稳定性研究资料对应《药品注册管理办法》 附件2的资料10、11、12、14,但是,CTD的撰写不能 机械地套用附件2的内容,应注意理清研究思路,注意研 究内容编排的逻辑性;陈述内容的全面性;图表、数据清 晰、明确、可追溯。
报临床不提供综述资料综述资料16新药申报可编辑课件可编辑课件1111药学研究资料ctd部分药物质量控制体系原辅料控制包材控制生产过程控制终产品控制工艺参数环境控制过程检测中间体控制ctd格式申报资料撰写要求确立和固化了系统的药品质量控制理念新药申报可编辑课件可编辑课件1212药学研究资料药学研究资料ctdctd部分部分新药申报制剂处方工艺资料32p1剂型及产品组成32p2产品开发32p21处方组成32p211原料药32p212辅料32p22制剂研究32p221处方开发过程32p222制剂相关特性32p23生产工艺的开发32p24包装材料容器32p24相容性32p3生产32p31生产商32p32批处方32p33生产工艺和工艺控制32p34关键步骤和中间体的控制32p35工艺验证和评价32p4原辅料的控制可编辑课件可编辑课件1313制剂处方工艺资料制剂处方工艺资料ctdctd格式分析格式分析申报资料更体现研究逻辑性研究脉络更清晰研究过程研究结果ctd体现研究过程不同研究阶段批次样品的质量比较附件二研究信息罗列容易忽视不同研究阶段样品的比较新药申报可编辑课件可编辑课件1414制剂处方工艺资料制剂处方工艺资料ctdctd格式分析格式分析更加强调质量控制体系通过处方和生产工艺开发对药品关键质量特征进行研究和确认对关键参数环节进行研究建立关键工艺参数控制进而说明大生产条件下工艺是否能够稳定持续生产出质量符合要求的药品通过药品研究质量控制体系证明建立系统有效的药品生产质量控制体系
新药审批流程及标准
新药审批流程及标准随着医疗技术的不断提高和发展,越来越多的新药问世,这些新药对于人类健康的保障起到了非常重要的作用。
然而,新药的审批流程并不是一件简单的事情。
一款新药首先需要进行大量的实验,证明其安全性和有效性,然后才能被纳入药品审批流程之中。
在我国,新药审批流程也是十分严格和规范的。
本篇文章将介绍我国新药审批流程及标准的相关内容。
一、新药的核查在我国,任何一款新药的上市,都需要经过严格的核查和审批程序。
新药上市申报的基础资料包括:新药申报表、制剂申报表、质量规格书、药品制造规程、药品检验规范等文件。
这些文件需要包括药品的详细信息、制剂的成分、药品的生产工艺、药品的质量控制和检测标准等信息。
新药的申报材料还需要提交一份合法的生产厂家营业执照、医疗机构执业许可证、质量管理体系认证证书以及药品广告批准号等基础资料。
如果申报的资料不完整或存在问题,缺少重要信息,审批管控人员会拒绝其申请,直到返工完善。
二、临床试验阶段一款新药通过核查后,还需要进行临床试验。
新药的临床试验主要分为三个阶段。
第一阶段是小规模试验,主要是验证药品对人的耐受性、安全性。
第二阶段是中规模试验,主要是验证药品的疗效和安全性。
第三阶段是大规模试验,主要是验证药品的疗效、安全性以及是否具有可持续的有效性。
在临床试验阶段,药品的疗效、安全性以及质量控制等都是非常重要的。
这其中,药品质量控制问题是临床试验中首要解决的问题,因为只有质量得到保证,才能保证试验结果的准确性和可信性。
三、药品获批上市经过多年的研究和调查后,一款新药终于获得了审批机构的批准,获得了上市的资格。
新药上市后还需要进行安全风险监测和防控。
对于上市后出现的药品安全问题,相关部门会及时进行调查和处理。
对于新药的营销和推广,也需要按照国家相关的规定执行,否则一旦涉嫌不规范行为,将会受到法律的严惩。
总的来说,我国新药的审批流程及标准非常严格,药品所需的资质、相关证明以及临床试验等都需要仔细把关,确保新药上市后能够真正的保障人类健康。
新药申报流程
物料名称 质量标准 生产商 使用步骤
提供以上物料的质量控制信息,明确引用标准,或提供内控 标准(包括项目、检测方法和限度),并提供必要的方法学
验证资料。
注:化药6+6类,原料仿制, 制剂要看具体品种:如果是口服固体制 剂,制剂国家局临床批件,做18-24例的生物等效性实验,做完临 床,把临床部分提交,如果通过,制剂和原料一起批生产。如果是注 射剂,原料+制剂直接报生产,如果通过,直接批生产,(高风险注 射剂除外,高风险注射剂要做临床)。 注:国家局有因核查品种替加环素(化药3+6类)、恩替卡韦(化药6+6 类)省局生产现场核查完毕后,等申报资料和省所的检验报告汇总到审 评中心后,国家局认证中心择日进行一批样品的生产现场核查。
科研部
2011-10-10
核查,原料和制剂都要动态生产 3批
工艺验证3批;
省局生产现场3 批
(一)
化药3+3类(包括化药4+4类)新药申报程序
报临床:
阶段
准备的实验内容
备料 小试
备齐小试、中试、工艺验证所需物料(根据需要小 试、中试、工艺验证可分开备料),进厂后,经分析 中心检验并出检验报告后,开领料单领取。 原料工艺需要一般4~6批左右的工艺摸索,最后的一个 小试工艺为最终的确定工艺(尽量跟中试、大生产工 艺一致,只是设备、规模的大小差异),其中需要的 中间体、粗品检验按当天的时间真实检验,同时撰写 相关记录(仪器使用记录、设备使用记录等)。
中试原料用途:原料的质量研究、稳定性考察;三批 中试规模制剂;如资料所需,还需提供部分原料做药 效、药代、药理等相关实验。 物料:厂家的发票、供货协议、起始物料的合成工艺 (要不到所用溶剂也可)、厂家检验报告。进厂后, 经分析中心检验并出检验报告后,开领料单领取。
中药新药研发申报流程及相关材料说明
中药新药研发申报流程及相关申报材料说明一、中药新药的注册分类及说明1.1注册分类中药新药注册按审批管理的要求分以下几类:1.未在国内上市销售的从植物、动物、矿物等物质中提取的有效成份及其制剂。
2.新发现的药材及其制剂。
3.新的中药材代用品。
4.药材新的药用部位及其制剂。
5.未在国内上市销售的从植物、动物、矿物等物质中提取的有效部位及其制剂。
6.未在国内上市销售的中药、天然药物复方制剂。
7.改变国内已上市销售中药、天然药物给药途径的制剂.8.改变国内已上市销售中药、天然药物剂型的制剂.9.仿制药。
1.2说明注册分类1—6的品种为新药,注册分类7、8按新药申请程序申报,注册分类9的品种为已有国家标准的药品。
二、中药新药的研发及申报流程中药新药的研发申报一般按以下程序进行:选题立项-—临床前研究-—临床研究——申报审批——正式生产,其中,新药临床前及临床研究的主要内容及注意事项分别列举如下:2.1 新药的临床前研究(一)主要内容:新药的临床前研究主要包括制备工艺(中药制剂包括原药材的来源、加工及炮制)、理化性质、纯度、检验方法、处方筛选、剂型、稳定性、质量标准、药理、毒理、动物药代动力学等研究。
新发现中药材还应包括来源、生态环境、栽培(养殖)技术、采收处理、加工炮制等研究.(二)注意事项:从事新药安全性研究的实验室应符合国家药品监督管理局《药品非临床研究质量管理规范》(GLP)的相应要求,实验动物应符合国家药品监督管理局的有关要求,以保证各项实验的科学性和实验结果的可靠性.2。
2 新药的临床研究(一)主要内容:新药的临床研究包括临床试验和生物等效性试验。
新药的临床试验分为Ⅰ、Ⅱ、Ⅲ、Ⅳ期.Ⅰ期临床试验:初步的临床药理学及人体安全性评价试验.观察人体对于新药的耐受程度和药物代谢动力学,为制定给药方案提供依据.Ⅱ期临床试验:随机盲法对照临床试验.对新药有效性及安全性作出初步评价,推荐临床给药剂量。
Ⅲ期临床试验:扩大的多中心临床试验.应遵循随机对照原则,进一步评价有效性、安全性。
中药新药研发申报流程及相关材料说明
中药新药研发申报流程及相关材料说明Revised by Jack on December 14,2020中药新药研发申报流程及相关申报材料说明一、中药新药的注册分类及说明1.1注册分类中药新药注册按审批管理的要求分以下几类:1.未在国内上市销售的从植物、动物、矿物等物质中提取的有效成份及其制剂。
2.新发现的药材及其制剂。
3.新的中药材代用品。
4.药材新的药用部位及其制剂。
5.未在国内上市销售的从植物、动物、矿物等物质中提取的有效部位及其制剂。
6.未在国内上市销售的中药、天然药物复方制剂。
7.改变国内已上市销售中药、天然药物给药途径的制剂。
8.改变国内已上市销售中药、天然药物剂型的制剂。
9.仿制药。
1.2说明注册分类1-6的品种为新药,注册分类7、8按新药申请程序申报,注册分类9的品种为已有国家标准的药品。
二、中药新药的研发及申报流程中药新药的研发申报一般按以下程序进行:选题立项——临床前研究——临床研究——申报审批——正式生产,其中,新药临床前及临床研究的主要内容及注意事项分别列举如下:新药的临床前研究(一)主要内容:新药的临床前研究主要包括制备工艺(中药制剂包括原药材的来源、加工及炮制)、理化性质、纯度、检验方法、处方筛选、剂型、稳定性、质量标准、药理、毒理、动物药代动力学等研究。
新发现中药材还应包括来源、生态环境、栽培(养殖)技术、采收处理、加工炮制等研究。
(二)注意事项:从事新药安全性研究的实验室应符合国家药品监督管理局《药品非临床研究质量管理规范》(GLP)的相应要求,实验动物应符合国家药品监督管理局的有关要求,以保证各项实验的科学性和实验结果的可靠性。
新药的临床研究(一)主要内容:新药的临床研究包括临床试验和生物等效性试验。
新药的临床试验分为Ⅰ、Ⅱ、Ⅲ、Ⅳ期。
Ⅰ期临床试验:初步的临床药理学及人体安全性评价试验。
观察人体对于新药的耐受程度和药物代谢动力学,为制定给药方案提供依据。
Ⅱ期临床试验:随机盲法对照临床试验。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
项目名称:新药生产的申报与审批
许可依据:《药品管理法》、《药品管理法实施条例》、《药品注册管理办法》
申报资料:
1、提交〈药品注册申请表〉纸质原件一式四份及电子版一份
按〈药品注册管理办法〉附件一、附件二和附件三的要求提交申报资料四套,包括原件二套,复印件一套及综述资料复印件一套。
办理程序:申请人向省局药品注册处提出注册申请,按要求提交〈药品注册申请〉及申报资料;省局进行形式审查并决定是否受理;省局对受理的注册申请进行现场核查、抽取3批样品注册检验并进行初步资料审查,符合要求的上报国家局药审中心进行技术审评;经审评符合要求的,由药审中心通知国家局药品认证中心进行生产现场检查,并抽取1批样品(生物制品抽取3批)进行检验。
均符合要求的,国家局发给新药证书。
申请人已持有《药品生产许可证》并具备生产条件的,同时发给药品批准文号。
办理时限:205(175)日,其中:
省局受理、现场核查及资料初审:35日
国家局技术审评:150日,获准进入特殊审批程序的品种:120日
国家局审批:20日
收费标准:3500元
新药生产的申报与审批流程图。
