邻氯苯甲醛
邻氯苯甲醛生产及副产品的回收技术分析

邻氯苯甲醛生产及副产品的回收技术分析邻氯苯甲醛是一种重要的有机合成中间体,广泛应用于医药、染料和农药等领域。
邻氯苯甲醛的生产及副产品的回收技术对于提高产品质量、降低生产成本具有重要意义。
本文将对邻氯苯甲醛的生产及副产品的回收技术进行分析。
邻氯苯甲醛的生产主要有两种方法,一种是邻氯苯的氯化制备法,另一种是芳香烃的氯化方法。
其中邻氯苯的氯化制备法是较为常用的方法。
该方法的主要步骤为:首先将邻氯苯与氯代碱金属或氯代碱土金属在酸性条件下进行氯化反应,生成邻氯苯甲醛;然后通过蒸馏、结晶等方法对反应产物进行分离纯化,得到纯度较高的邻氯苯甲醛产品。
这种制备方法工艺简单、成本低廉,但由于该方法的氯化反应是发生在液相,存在废水处理问题。
邻氯苯甲醛生产过程中,会伴随着一些副产品的产生,如间苯二甲酸酯、对-氯苯甲醛等。
对这些副产品的回收和利用对于提高生产效率和资源利用率有着重要意义。
对副产品的回收技术主要有以下几种:一是蒸馏技术。
对于副产品的回收,可采用蒸馏技术进行分离纯化。
蒸馏技术是通过升温使混合物中组分按照其沸点由液态转化为气态,再通过冷凝使其沉淀成液态的分离方法。
通过蒸馏技术,可以将副产品从反应混合物中分离出来,得到纯度较高的副产品。
二是结晶分离技术。
结晶分离技术是通过溶解度差异来实现物质的分离。
对于副产品的回收,可以通过改变温度和溶剂种类等条件使其溶解度发生变化,通过结晶的方法将副产品从反应混合物中分离出来。
三是萃取技术。
萃取技术是利用不同物质在不同溶剂中的亲和性差异实现物质的分离。
对于副产品的回收,可以利用合适的溶剂系统和适当的条件进行萃取,从而将副产品与主产品进行分离。
四是反应工艺优化。
在邻氯苯甲醛生产过程中,通过优化反应条件、控制反应时间等方法,可以减少副产品的生成,降低副产品对主产品产率的影响。
含GHS的邻氯苯甲醛安全数据单(安全技术说明书)SDS.doc

邻氯苯甲醛安全数据单(化学品安全技术说明书)SDS第一部分化学品名称及企业标识化学品中文名:2-氯苯甲醛化学品英文名:O-Chlorobenzaldehyde化学品俗名或商品名:邻氯苯甲醛第二部分危险性概述GHS危险性类别:物理危害:健康危害:环境危害:化学危险性信息:象形图、信号词、标识符名称危害警示:危害防范措施:第三部分成分/组成信息第四部分急救措施皮肤接触:脱去被污染的衣着,用肥皂水和清水彻底冲洗皮肤。
就医。
眼睛接触:提起眼睑,用流动清水或生理盐水冲洗。
就医。
吸入:迅速脱离现场至空气新鲜处。
保持呼吸道通畅。
如呼吸困难,给输氧。
如呼吸停止时,立即进行人工呼吸。
就医。
食入:饮足量温水,催吐。
就医。
第五部分消防措施灭火方法:喷水冷却容器,可能的话将容器从火场移至空旷处。
灭火剂:雾状水、泡沫、干粉、二氧化碳、砂土。
救火时,须戴防毒面具、防止中毒。
第六部分泄漏应急处理作业人员防护措施、防护装置和应急处置程序:迅速撤离泄漏污染区人员至安全区,并进行隔离,严格限制出入。
切断火源。
建议应急处理人员戴自给正压式呼吸器,穿消防防护服。
尽可能切断泄漏源。
防止进入下水道、排洪沟等限制性空间。
环境保护措施:废水禁止进入下水道、排洪沟等限制性空间以及水体环境。
泄漏化学品的收容、消除方法及所使用的处置材料:小量泄漏:用砂土或其它不燃材料吸附或吸收。
也可以用不燃性分散剂制成的乳液刷洗,洗液稀释后放入废水系统。
大量泄漏:构筑围堤或挖坑收容;用泡沫覆盖,降低蒸气灾害。
用防爆泵转至槽车或专用收集器内,回收或运至废物处理场所处置。
防止发生次生危害的预防措施:处理现场禁止一切火源。
第七部分操作处置与储存操作注意事项:处理:仅在良好的通风处使用。
空容器保存残留产品渣(液体和烟雾),可能是危险的。
保持容器密闭,与热源,火星和火焰隔离。
不要弄到皮肤和眼睛上。
不要摄取和吸入。
在惰性气体下处理,与空气隔离储存。
不允许与水接触。
丢掉被污染的鞋。
邻氯苯甲醛清洁生产工艺

氯一 氯 苄 与氯 气反 应生 成 邻 氯二 氯苄 的 反应 速 度较 慢 。 因此 ,反 应 后 期 时 ,通 人反 应 器 中的 氯气 ,常来 不及 全 部参 与 反应 ,部 分 氯气从 尾气 中逸 出污 染环境 。 2 高 浓度废 水 . 2 邻 氯 甲苯侧 链 光氯 化产 物 主要 为邻 氯二 氯 苄和 邻氯 三氯 苄 , 在水解过程中邻氯二氯苄与水反应生成邻氯苯甲醛 ,邻氯三氯苄 与水反应生成邻氯苯 甲酸,邻苯甲酸在碱洗水洗过程 中生产邻氯 苯 甲酸 钠 转 移 到 水 相 中 ,该 碱 洗 废 水 含 有 高 浓 度 邻 氯 苯 甲 酸 , C D O 含量 高达 2 万毫 克, ,强酸性 ,处 理难 度大 ,处理 成本 高 。 升
2 .邻氯苯甲醛工艺流程及存在主要环境 问题
邻 氯 苯 甲醛 的合 成 ,有 许 多 文献 报 道 “,有 工 业生 产 价 值 的 路 线 主 要 是 以邻 氯 甲苯 为 原料 的 直 接 氧化 法 和 侧链 氯 化 水 解法 。 目前 国内邻 氯苯 甲醛 的生 产都 采用 邻氯 甲苯 侧链 氯化 水解 工艺 路 线 ,其 合成路 线如 下 :
一
3 .清 洁生产 改造
丹 阳中超 化 工有 限 公司 总结 多年 生 产经 验 ,不 断优 化生 产 工 艺 ,实施 了邻 氯苯 甲醛 清洁 化生 产 工艺 ,在解 决废 气 废水 污 染 问 题 的 同时 变废 为 宝 ,利 用尾 气 中的 余氯 生 产对 邻 氯 甲苯 ,回收废 水 中的邻 氯苯 甲酸 及盐 ,为企 业创 造 出一定 的经济 效益 。 31 .甲苯 吸收 尾气 中的氯 气 为 了不使 氯 气排 到大 气 中污染 环境 ,可 以采 用碱 吸收 法 洗涤 尾 气 ,但 这样 不仅 要 消耗 碱 ,而 且 吸收 后 的碱 液产 生 新 的污 染 。 我们 采 用 甲苯 催化 吸 收尾 气 中 的氯 气 。 甲苯在 催化 剂 作用 下 与 氯 气 反应 ,生成 对邻 氯 甲苯 ,该 反应 速度 很 快 ,能够 全 部 吸收 尾 气 的 氯 气 ,产生 的对 邻 氯 甲苯供 对 邻氯 生 产用 ,这样 既解 决 了 氯气 污染 问题 ,氯 气又得 到充 分的利 用 ,且不 产生新 的 污染 。 工 艺过程 如 下 : 邻 氯 甲苯 从塔 式 反应 器底 部加 入塔 内 ,塔 夹 套 内通入 蒸汽 加 热至 反 应温 度 ,开 启 塔光 照灯 ,从塔 底 通 入氯 气 ,邻 氯 甲苯 与氯 气反应后产生的氯化氢尾气经塔顶冷却器冷却后进人吸收系统 。 反应 的 前期 因为邻 氯 甲苯 含量 高 ,塔 顶 出 来的 氯化 氢 气体 中 不含 有氨 气 ,所 以 此时 氯 化氢 气体 直 接 进入 水 吸收 制盐 酸 系统 。 当 反 应液 中邻氯甲苯含量小于1%时,尾气中含有氯气 ,此时将尾气 0 切人 加 有 甲苯 和催 化 剂的 吸收 釜 ,尾气 中 的氯 气与 甲苯 反应生 成 对邻 氯 甲苯和 氯化 氢 气体 ,两部 分 氯化 氢 气体 经 吸收 釜冷 凝 器冷 却后 进入 水吸 收制盐 酸 系统 。 邻 氯 一 氯 苄 与 氯 气 反 应 生 成 邻 氯 二 氯 苄 的 化学 反应 速 度 较 慢 ,反 应后 期 通入 的 氯 气往 往来 不 及反 应便 随 着尾 气逸 出。 为尽 量减 少氯 气逸 出 ,本 工艺采 用塔 式氯 化反 应器 ,塔 的径 长 比为 1 : 1 ,塔 内物 料 高度 约 8 ,是 同 样容 积 反应 釜 内物 料高 度 的4 , O 米 倍 大大 增加 了氯 气与物 料的 接触 时 间,减少 氯 气逸 出量 。 该 工艺 有 以下 几个优 点 :() 1甲苯与 氯气 在路 易斯 酸催 化剂 作 用下 发生 的环 氯 化 反应速 度快 ,氯 气吸 收较 干净 。() 2吸收 后 的产 物 为 对邻 氯 甲苯 ,当 吸收 釜 中氯化液 甲苯含 量低 于5 %时 ,就将 此 氯化 液送 至 对邻 氯 甲苯 车 间 ,用于 生 产对 邻 氯 甲苯 ,氯 气 得到 充 分 利 用 。() 收工 艺清 洁 无污 染 。 目前 许 多工 厂普 遍采 用 碱液 吸 3吸 法 ,不仅 要消 耗 碱 ,而且 吸 收后 的碱 液 又变 成 了新 的污 染源 。() 4 吸收过 程不 仅不 增加 费用 ,而且 还产 生一 定的 经济效 益 。 3 碱 洗废 水 回收邻 氯苯 甲酸 . 2 碱洗 废 水 中含 有高 浓 度邻 氯苯 甲酸 ,有文 献报 导可 提 取邻 氯 苯 甲酸 ,采用 加 入 水溶 助 剂 的溶 解 萃取 结 晶 分 离技 术 ,水 溶 助 剂可 以 采 用丁 基单 甘 醇 硫 酸酯 钠 盐 或哌 嗪 等 。该 方 法 存在 的 问 题 是 难 以 从 水溶 助 剂 与邻 氯 苯 甲酸 形 成 的复 合物 中 回收 水溶 助 剂 ,造 成提 取成 本高 。 我 们 经 过 大 量 实 验 ,提 出一 种低 成 本 、高 品质 的 邻 氯 苯 甲
邻氯苯甲醛气相含量测定

邻氯苯甲醛气相含量测定
邻氯苯甲醛气相含量测定可以借助气相色谱-质谱联用仪器(GC-MS)来完成。
具体操作步骤如下:
1. 取适量待测样品,加入适量的内标溶液进行混合。
2. 将混合液转移到样品瓶中,通过气相色谱-质谱联用仪器进行测定,选择合适的柱子及柱温程序进行分离。
3. 使用电离源将待测物质分解成离子,并利用质谱检测器进行测量,得到待测物质的质谱谱图。
4. 通过对质谱谱图进行解析,可以得到待测物质的含量。
需要注意的是,这个方法需要专业的仪器和操作技能,建议在相关专业人士的指导下进行操作。
邻氯苯甲醛生产

• 早在二十世纪二十年代,美国关注食品中残留得杀虫 剂并作出相应的要求规定。在二十世纪六十年代,在 世界范围内不断增加的兴趣与环保化学杀虫剂成为科 学的大众的抗议的对象。批评者指控化学杀虫剂是危 险的,也是有违自身利益。发展目标害虫抗药性令人 烦恼,破坏生态系统以及中毒人员和其它生物以及环 境,作为回应,政府已经限制或禁止许多危险的杀虫 剂,包括许多氯化烃药品:DDT、 六氯化苯、林丹、 艾氏剂、狄氏剂、七氯、异狄氏剂和毒杀芬,强大,广 泛接触和胃毒。
• 与此同时,化学家发明了替代杀虫剂,选择性 攻击而不是盲目的分解成无毒物质的环境,有 机磷酸昆虫神经系统的攻击,就像氯化磷氢化 合物,但是更快的分解成无毒物质。包括有机 磷酸酯类庞大的集团之一,水平最高的哺乳动 物的毒性。为有机磷杀虫剂最低之一。氨基甲 酸类杀虫剂酸酯的甲酸酯杀虫幼虫的少女和成 人在接触,有获得青睐,因为他们分解得更快, 比有机磷酸酯类的危害比较小,在醇是西维因 或胺甲奈,氨基甲酸酯类氮-甲基芳香酯。
化学杀虫剂的责任是鼓励对生物的控制,反过来 自然过程和机制性对害虫有副作用。生物控制包括使 用食肉动物寄生虫和病原体杀死昆虫,而没有对其他 生物体造成伤害。另一种策略,是大量绝育雄性昆虫 与能繁殖的雄性求偶发布竞争,来使下一代的人口减 少。在他们增长中使用合成的昆虫激素来扰乱害虫的 重要过程,如生长,合成信息素,大量的昆虫性引诱 剂,监测害虫的种群,破坏害虫的繁殖,引诱害虫进 入陷阱。然而,在实践中,有些在环保吸引力功能生 物杀虫剂,他们有缓慢的作用和有选择性活动,他们 严格管理的要求,可以使他们在经济上没有吸引力。 因此,越来越多的在综合害虫的管理方案,生物和化 学方法正在用来协调发展。
项目相关参数
• • • • • • • • 中文名称:邻氯苯甲醛 别名:2-氯苯甲醛 英文名:O-chlorobenzonic aldehyde 分子式:C7H5ClO 分子量:140.56 外观:无色或浅黄色透明液体 含量:>=99% 水分:<=0.2% 熔点:12.39摄氏度 闪点:87摄氏度 沸点:84.3摄氏度 折光率:1.5662
邻氯苯甲醛生产及副产品的回收技术分析

邻氯苯甲醛生产及副产品的回收技术分析邻氯苯甲醛是一种重要的有机化工产品,广泛应用于染料、药物、化妆品和聚合物等领域。
在邻氯苯甲醛的生产过程中,产生了一些副产品,这些副产品可以通过回收技术得到利用,减少资源浪费并降低环境污染。
对邻氯苯甲醛生产及副产品的回收技术进行分析具有重要意义。
一、邻氯苯甲醛的生产工艺邻氯苯甲醛的生产主要是通过氯苯和甲醛在碱性条件下反应而成,其反应方程式如下所示:C6H5Cl + CH2O + NaOH → C6H4ClCHO + NaCl + H2O在反应过程中,产生了邻氯苯甲醛以及氯化钠和水。
经过反应生成的混合物需要经过一系列的分离和纯化工艺,最终得到高纯度的邻氯苯甲醛产品。
二、邻氯苯甲醛生产过程中产生的副产品在邻氯苯甲醛生产过程中,除了目标产品外,还会产生一些副产品,主要包括氯苯、甲苯、二氯苯和氯化钠等。
这些副产品在传统工艺中往往被视为废弃物,直接排放或处理,造成了资源的浪费和环境的污染。
近年来,随着环保意识的提高和资源利用的重要性,邻氯苯甲醛生产副产品的回收技术备受关注。
主要包括以下几种技术:1. 氯苯的回收氯苯是邻氯苯甲醛生产过程中的重要副产品之一,通过精馏、萃取、结晶等工艺可以将氯苯从反应产物中分离出来。
经过纯化处理后,氯苯可以用作溶剂或者是再生利用,降低了化工产品的生产成本和资源消耗。
甲苯是邻氯苯甲醛生产过程中的另一个副产品,可以通过蒸馏、萃取等方法进行回收。
回收的甲苯可以用于再生产其他化工产品或者作为溶剂使用,有效减少了对新鲜原料的需求。
氯化钠是邻氯苯甲醛生产过程中的无机盐副产物,可以通过结晶、沉淀等实现对氯化钠的回收。
回收的氯化钠可以用于制备其他化工产品,或者是用于工业废水处理等方面,节约了资源并降低了排放物的污染。
邻氯苯甲醛生产副产品的回收技术具有重要的应用价值。
通过副产品的回收利用,可以减少资源的浪费,提高生产效率,降低生产成本。
副产品的回收利用有利于环境保护,减少了对自然资源的消耗,降低了对环境的负面影响。
24二氯苯甲醛及邻氯苯甲醛、对氯苯甲醛合成工艺述评
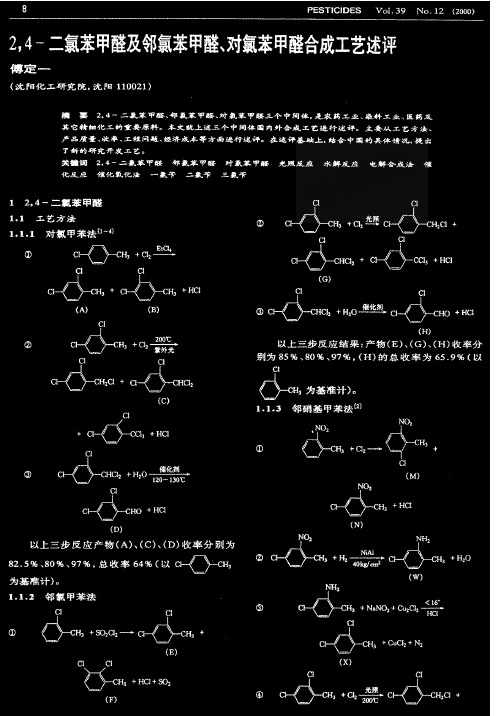
22.5%(以g—卜c地为基准计)。
1.1.4 4,6一二氯邻硝基甲苯法
9
相同。 1.1.6戊二酮法【5】
伽州删
了 c:心c哪 H.。 卜.。
CHO
一步法工艺,收率75%~65%。 1.1.7 3一氯一4一甲基苯胺法(沈阳化工研究院研 究)
① c鸭a杏m—m景 a
①
②
a
Cl
@ 。a咎Qa删…z+嗪c(扣ac,l9…一
鑫re br璐dly娃辩d魏tk i砖站stry of毽g∞ehemic建s'dyestu弧鞠d pkr瓣8·
ceuticals.The proce鹞study all over the world of the aboVe three inter—
mediates wa3 b“efly reviewed in this paper by comparing with the syn— thes.s method,p∞_duct qu8嚣锣,yie黼,engineering,e。st and others.下he
new proce蟠was pr∞ented based on the reView.
Key啪嘲s:群∞e骚,豫vi尊w,2。4一dic鞋。曲麟蒜aldeh嫡e,2一chlo∞ben—
zaldehyde,4一chloroben∽ldehyde.
收稿日期:2000.1.26
2,4-二氯苯甲醛及邻氯苯甲醛、对氯苯甲醛合成工艺述评
美键谰2,4一二氟辇甲臻邯氯笨甲醛峙瓤笨甲醛兜腻葳魔承解魔应 电解合成汝催 %。反应催m氧*汝一氯苄。氯带i氯苄
l 2。4一=氯苯单醛
1.1 工艺穷法
l。1.1 对氯甲苯法(1~∞
o c卜(>屿+%旦
邻氯苯甲醛生产及副产品的回收技术分析

邻氯苯甲醛生产及副产品的回收技术分析邻氯苯甲醛是一种重要的有机合成中间体,广泛应用于农药、染料、医药和香料等领域。
邻氯苯甲醛生产过程中会产生一些副产品,如果不加以有效回收和利用,不仅会浪费资源,还会对环境造成污染。
开展邻氯苯甲醛生产及副产品的回收技术分析具有重要的现实意义。
邻氯苯甲醛的生产常用的方法是邻氯化苯与甲醇反应,通常采用氯化铁作为催化剂。
该反应生成的主要副产品为邻氯苯甲醇和对氯苯甲酸。
邻氯苯甲醇是邻氯苯甲醛的重要中间体,在医药和染料行业有广泛应用;对氯苯甲酸则可以通过氧化反应进一步转化为邻氯苯甲醛。
回收这些副产品对提高资源利用效率和降低生产成本具有重要意义。
1. 邻氯苯甲醇的回收:邻氯苯甲醇可通过蒸馏或萃取进行回收。
蒸馏是常用的分离技术,可将邻氯苯甲醇和甲醇分离,然后通过冷凝回收邻氯苯甲醇。
萃取是通过溶剂提取的方法,将邻氯苯甲醇从反应体系中提取出来,然后通过脱水或其他方法将其纯化。
2. 对氯苯甲酸的回收:对氯苯甲酸可以通过蒸馏或酸性条件下进行还原反应回收。
蒸馏是通过加热将对氯苯甲酸分离出来,然后通过冷凝回收。
还原反应是将对氯苯甲酸与还原剂(如亚硫酸盐)反应,还原为邻氯苯甲醛。
3. 废水处理:邻氯苯甲醛生产过程中会产生废水,其中含有有机物和有毒物质。
废水处理主要包括物理和化学处理。
物理处理方法包括沉淀、过滤、吸附等,用于去除悬浮固体和悬浮液。
化学处理方法通常采用氧化、还原、中和等方法,用于去除废水中的有机污染物和有毒物质。
邻氯苯甲醛生产及副产品的回收技术分析是一个涉及多个方面的综合问题。
通过合理选择和组合上述回收技术,可以达到提高资源利用效率、降低生产成本和减少环境污染的目的。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
向带有温度计、搅拌器、氯气吹入管、回流冷凝器和高压水银灯光照装 置的 600mL 光反应器中,加入邻氯甲苯 380g(3.0mol),加热至 130℃, 在光照下吹入氯气 106g/h(1.5mol/h),通入时间 3.6h。共通入 5.4mol 氯气。反应毕,向反应液通入干燥的氮气,以赶出氯化氢和氯气,得反 应液共 558g,其中邻氯甲苯 0.5%(mol),邻氯苄基氯 28%,邻氯二氯甲 苯 67%,邻氯三氯甲苯 3%,邻氯一氯甲苯的平均氯化度为 1.8。 向带有温度计、搅拌器、回流冷凝器的 2 L 三口烧瓶中,加入上述邻氯 甲苯的氯化混合物 64.7g(0.343mol)、3%(质量分数)的硝酸 1440g 和五 氧化二钒 2.0g,搅拌下加热回流 6h。反应毕,冷却,加入 200mL 甲苯, 分离出油相,水溶液层加入 100mL 甲苯抽提 2 次。合并油相和抽提液,
蒸出甲苯,剩余物进行蒸馏,收集 107~110℃(4.0kPa)馏分,可得产品 邻氯苯甲醛 36g,以邻氯甲苯计,收率为 73.5%。 (3)邻氯二氯甲苯水解法 由邻氯二氯甲苯催化水解制得。
生产 方法
制备实例 1 邻氯二氯甲苯 97.7g 中加入氧化锌 0.034g(1mol 原料为 0.00084mol),搅拌下加热至 110℃,然后缓慢加入 9.45mL 水,于 110~ 120℃下反应 1.9h。经分析确认原料邻氯二氯甲苯完全消失之后,于氮气 流下进行减压蒸馏,收集 97.1~98.3℃(2.8kPa)馏分,得产品邻氯苯甲 醛 68.6g,收率 97.6%,含量 99.8%。 制备实例 2 向反应器中滴加邻氯二氯甲苯 0.3g/min,水蒸气 3g/min, 反应器中事先加入 100mL 水,水温 110℃。将生成的邻氯二氯甲苯和水 蒸气的混合物通过已加热至 118℃的 5~10 目三氧化铝 50g 的反应管层, 冷却生成的气体,得悬浮液,用乙醚抽提,干燥,蒸出乙醚,氮气流下 减压蒸馏,收集 96~98℃(2.93kPa)馏分,得邻氯苯甲醛 68.8g,收率 95.7%,含量 97.8%。 由邻氯甲苯侧链经氯气和三氯化磷氯化工艺,催化水解,蒸馏精制而成。
生产 其制备方法是以苯甲醛为原料,在溶剂二氯乙烷中再加少量三氯化铝为 方法 催化剂进行氯化,反应温度 25~30℃,即得产品。
也可用间氯甲苯氯化、水解而制得本品。
ቤተ መጻሕፍቲ ባይዱ
类别 有毒物质
毒性 中毒 分级
急性 毒性 可燃 性危 险特 性
口服-大鼠 LD50: 2160 毫克/公斤; 口服-小鼠 LD50: 1900 毫克/公斤 热分解排出有毒氯化物烟雾
中文 名称: 中文 同义 词: 英文 名称: 英文 同义 词:
CAS 号: 分子 式: 分子 量: EINE CS 号: 相关 类别:
Mol 文件:
邻氯苯甲醛
2-氯苯甲醛;邻氯苯甲醛;2-氯苯甲醛,98%;2-氯苯甲醛,97%;邻氯苯甲 醛,2-氯苯甲醛
2-Chlorobenzaldehyde
2-chloorbenzaldehyde;2-Chlorbenzaldehyd;2-chloro-benzaldehyd;2-C lorobenzaldeide;Benzaldehyde, o-chloro-;Benzaldehyde,2-chloro-;-Chloroformylbenzene;o-Chloorben zaldehyde 89-98-5
和果树上的螨虫。邻氯苯甲醛肟化可得邻氯苯甲肟,进一步氯化可得邻
氯苯甲肟,都是药物中间体。
用途 镀锌光亮剂
用途 用作染料、农药、医药中间体
用途 用作染料中间体,也用于有机合成
用途 邻氯苯甲醛又名 2-氯苯甲醛,是合成杀螨剂四螨嗪的原料,也可用于合 成另一杀螨剂新品种氟螨嗪(flutenzine),还可用作医药、染料中间体。
生产 邻氯苯甲醛有以下 3 种合成方法。
方法 (1)邻氯甲苯氯化、水解法 由邻氯甲苯经氯化、水解而得。
①氯化 将邻氯甲苯、三氯化磷、氯化亚砜加热至 150℃,在紫外线照射 下通氯气至理论量,得邻氯亚苄基二氯。 ②冰解 将邻氯亚苄基二氯、氯化锌混合物加热保持在 120~130℃,搅 拌滴加 1%三氯化铁水溶液,滴加完毕,加热,带水回流,分出油层即为 精制邻氯苯甲醛。 此外,水解操作也可在硫酸存在下进行。将邻氯亚苄基二氯和工业浓硫 酸一起搅拌,至温度自动降低、氯化氢逸出减缓时,再慢慢加热 12h, 使温度保持在 30~40℃;反应毕,经用冷水分层,分取油状物,再经洗 涤、水蒸气蒸馏即得成品。 (2)邻氯甲苯氯化、氧化法 将邻氯甲苯中的甲基氯化后再用硝酸氧化制得。
邻氯苯甲醛 性质
熔点 沸点 密度 蒸气密度 蒸气压 折射率 闪点 储存条件 水溶解性 敏感性
BRN
9-11 °C(lit.) 209-215 °C(lit.) 1.248 g/mL at 25 °C(lit.) 4.84 (vs air) 1.27 mm Hg ( 50 °C) n20/D 1.566(lit.) 190 °F -20?C Freezer 0.1-0.5 g/100 mL at 24 ºC Air Sensitive 385877
C7H5ClO
140.57
201-956-3
Aromatic Aldehydes & Derivatives (substituted);C7Alphabetic;Aldehydes;C;Carbonyl Compounds;CH;C7;植物生长调节剂中间体;农药中间体;杀螨剂中间 体;Aromatics 89-98-5.mol
8 III 29130000
储运 库房低温通风干燥 特性
灭火 水,二氧化碳, 泡沫, 干粉 剂
安全信息
危险品标志 危险类别码 安全说明 危险品运输编号
C,Xi 34 26-45 UN 3265 8/PG 3
WGK Germany 1
RTECS 号
CU5075000
F
8-9-23
Hazard Note
Irritant
HazardClass PackingGroup 海关编码
稳定性
Stable. Combustible. Incompatible with strong oxidizing
agents, strong bases, iron, strong reducing agents.
CAS 数据库 NIST 化学物质信息 EPA 化学物质信息
Moisture and light-sensitive. 89-98-5(CAS DataBase Reference) Benzaldehyde, 2-chloro-(89-98-5) Benzaldehyde, 2-chloro-(89-98-5)
邻氯苯甲醛 用途与合成方法
化学 本品为无色液体,m.p.17~18℃,b.p.213~214℃,n20D 1.5640,相对 性质 密度 1.241,f.p.88℃,不溶于水,溶于苯、醇、醚。
用途 间氯苯甲醛是植物生长调节剂吲熟酯的中间体。
用途 用作医药、染料中间体。用邻氯苯甲醛生产的农药螨死净可防治旱作物
