各种元素周期表
化学元素周期表读音完整版

化学元素周期表读音完整版化学元素周期表读音01号元素:氢[化学符号]H,读qīng第02号元素:氦[化学符号]He,读hài第03号元素:锂[化学符号]Li,读lǐ第04号元素:铍[化学符号]Be,读pí第05号元素:硼[化学符号]B,读péng第06号元素:碳[化学符号]C,读tàn第07号元素:氮[化学符号]N,读dàn第08号元素:氧[化学符号]O,读yǎng第09号元素:氟[化学符号]F,读fú第10号元素:氖[化学符号]Ne,读nǎi第11号元素:钠[化学符号]Na,读nà第12号元素:镁[化学符号]Mg,读měi第13号元素:铝[化学符号]Al,读lǚ第14号元素:硅[化学符号]Si,读guī第15号元素:磷[化学符号]P,读lín第17号元素:氯[化学符号]Cl,读lǜ第18号元素:氩[化学符号]Ar,A,读yà第19号元素:钾[化学符号]K,读jiǎ第20号元素:钙[化学符号]Ca,读gài 第21号元素:钪[化学符号]Sc,读kàng 第22号元素:钛[化学符号]Ti,读tài 第23号元素:钒[化学符号]V,读fán 第24号元素:铬[化学符号]Cr,读gè第25号元素:锰[化学符号]Mn,读měng 第26号元素:铁[化学符号]Fe,读tiě第27号元素:钴[化学符号]Co,读gǔ第28号元素:镍[化学符号]Ni,读niè第29号元素:铜[化学符号]Cu,读tóng 第30号元素:锌[化学符号]Zn,读xīn 第31号元素:镓[化学符号]Ga,读jiā第32号元素:锗[化学符号]Ge,读zhě第33号元素:砷[化学符号]As,读shēn 第34号元素:硒[化学符号]Se,读xī第36号元素:氪[化学符号]Kr,读kè第37号元素:铷[化学符号]Rb,读rú第38号元素:锶[化学符号]Sr,读sī第39号元素:钇[化学符号]Y,读yǐ第40号元素:锆[化学符号]Zr,读gào 第41号元素:铌[化学符号]Nb,读ní第42号元素:钼[化学符号]Mo,读mù第43号元素:碍[化学符号]Tc,读dé第44号元素:钌[化学符号]Ru,读liǎo 第45号元素:铑[化学符号]Rh,读lǎo 第46号元素:钯[化学符号]Pd,读bǎ第47号元素:银[化学符号]Ag,读yín 第48号元素:镉[化学符号]Cd,读gé第49号元素:铟[化学符号]In,读yīn 第50号元素:锡[化学符号]Sn,读xī第51号元素:锑[化学符号]Sb,读tī第52号元素:碲[化学符号]Te,读dì第53号元素:碘[化学符号]I,读diǎn第55号元素:铯[化学符号]Cs,读sè第56号元素:钡[化学符号]Ba,读bèi 第57号元素:镧[化学符号]La,读lán 第58号元素:铈[化学符号]Ce,读shì第59号元素:镨[化学符号]Pr,读pǔ第60号元素:钕[化学符号]Nd,读nǚ第61号元素:钷[化学符号]Pm,读pǒ第62号元素:钐[化学符号]Sm,读shān 第63号元素:铕[化学符号]Eu,读yǒu 第64号元素:钆[化学符号]Gd,读gá第65号元素:铽[化学符号]Tb,读tè第66号元素:镝[化学符号]Dy,读dī第67号元素:钬[化学符号]Ho,读huǒ第68号元素:铒[化学符号]Er,读ěr第69号元素:铥[化学符号]Tm,读diū第70号元素:镱[化学符号]Yb,读yì第71号元素:镥[化学符号]Lu,读lǔ第72号元素:铪[化学符号]Hf,读hā第74号元素:钨[化学符号]W,读wū第75号元素:铼[化学符号]Re,读lái 第76号元素:锇[化学符号]Os,读é第77号元素:铱[化学符号]Ir,读yī第78号元素:铂[化学符号]Pt,读bó第79号元素:金[化学符号]Au,读jīn 第80号元素:汞[化学符号]Hg,读gǒng 第81号元素:铊[化学符号]Tl,读tā第82号元素:铅[化学符号]Pb,读qiān 第83号元素:铋[化学符号]Bi,读bì第84号元素:钋[化学符号]Po,读pō第85号元素:砹[化学符号]At,读ài第86号元素:氡[化学符号]Rn,读dōng 第87号元素:钫[化学符号]Fr,读fāng 第88号元素:镭[化学符号]Ra,读léi 第89号元素:锕[化学符号]Ac,读ā第90号元素:钍[化学符号]Th,读tǔ第91号元素:镤[化学符号]Pa,读pú第93号元素:镎[化学符号]Np,读ná第94号元素:钚[化学符号]Pu,读(bù第95号元素:镅[化学符号]Am,读méi第96号元素:锔[化学符号]Cm,读jū第97号元素:锫[化学符号]Bk,读péi第98号元素:锎[化学符号]Cf,读kāi第99号元素:锿[化学符号]Es,读āi第100号元素:镄[化学符号]Fm,读fèi 第101号元素:钔[化学符号]Md,读mén 第102号元素:锘[化学符号]No,读nuò第103号元素:铹[化学符号]Lw,读láo 第104号元素:鐪[化学符号]Rf,读第105号元素:钅杜[化学符号]Db,读dù第106号元素:钅喜[化学符号]Sg,读xǐ第107号元素:钅波[化学符号]Bh,读bō第108号元素:钅黑[化学符号]Hs,读hēi 第109号元素:钅麦[化学符号]Mt,读mài 第110号元素:鐽[化学符号]Ds,读dá第111号元素:钅仑[化学符号]Rg,读lún第112号元素:uub(112)第113号元素:uut(113)第114号元素:uuq(114)第115号元素:uup(115)第116号元素:uuh(116)巧记化学元素周期表口诀先用2分钟时间看一个不伦不类的小故事:侵害:从前,有一个富裕人家,用鲤鱼皮捧碳,煮熟鸡蛋供养着有福气的奶妈,这家有个很美丽的女儿,叫桂林,不过她有两颗绿色的大门牙(哇,太恐怖了吧),后来只能嫁给了一个叫康太的反革命。
化学必修元素周期表ppt课件

ppt课件.
41
总结:
碱金属的原子结构
Li Na K Rb Cs
1.相似性:
最外层上都只 有一个电子
化学性质相似
1) 都易失电子表现强还 原性
2) 化合物中均为+1价
核电荷数
2.递变性: 电子层数
原子半径
核对最 外层电 子的引 力
失电 子能 力
还原 性
金 属 性
(电子层数的影响大于核电荷数的影响)
很好 逐渐增大(K特殊) 单质的熔沸点逐渐降低
ppt课件.
40
通过比较碱金属单质与氧气、水的反应, 我们可以看出,元素性质与原子结构有密 切关系,主要与原子核外电子的排布,特 别是 最外层电子数 有关。原子结构相 似的一族元素,它们在化学性质上表现出
相似性 和递变性 。
在元素周期表中,同主族元素从上到下原 子核外电子层数依次 增多 ,原子半径逐 渐 增大 ,失电子能力逐渐 增强 ,金 属性逐渐 增强 。
通过大量实验和研究,人们得出了如下结论:
碱金属元素原子的最外层都有1个电子,它们的化学性
质彼此相似 ,它们都能与 水 等非金属单质以及氧气 反应,表现出金属性(还原性).
4Li+O2=2Li2O
2Na+O2=Na2O2 2Na+2H2O=2NaOH +H2↑
2K+2H2O=2KOH +H2↑
上述反应的产物中,碱金属元素的化合价都是 +1 。
49
卤族元素: 氟(F)
F +9 2 7
氯(Cl)
Cl + 1 7 2 8 7
溴(Br)
Br +35 2 8 18 7
碘(I)
I +53 2 8 1818 7
最新元素周期表注音版

最新元素周期表注音版化学元素周期表是化学学科中最重要的工具之一,它按照原子序数递增的顺序排列,展示了元素的周期性规律。
对于学习化学的人来说,熟悉元素周期表是至关重要的。
为了帮助大家更好地学习和记忆元素周期表,我们特地为您带来了最新元素周期表的注音版。
首先,让我们来了解一下元素周期表的基本结构。
元素周期表由横行和纵列组成。
横行称为周期,纵列称为族。
周期表共有 7 个周期,18 个族。
其中,1、2、3 周期称为短周期,4、5、6 周期称为长周期,第 7 周期尚未填满,称为不完全周期。
接下来,我们按照原子序数的顺序来介绍一下元素的名称和注音。
第 1 号元素是氢(qīng),它是宇宙中最常见的元素之一,也是构成许多有机化合物的重要成分。
第 2 号元素是氦(hài),氦气是一种惰性气体,常用于气球和飞艇中。
第 3 号元素是锂(lǐ),锂在电池技术中有着重要的应用。
第 4 号元素是铍(pí),铍是一种具有高硬度和高强度的金属。
第 5 号元素是硼(péng),硼在玻璃制造和农业等领域有一定的用途。
第 6 号元素是碳(tàn),碳是生命的基础元素,存在于有机物和许多无机化合物中。
第 7 号元素是氮(dàn),氮气在空气中占很大比例,也是许多化肥的重要成分。
第 8 号元素是氧(yǎng),氧气是维持生命所必需的气体。
第 9 号元素是氟(fú),氟气是一种具有强氧化性的气体,含氟化合物在牙膏等产品中有应用。
第 10 号元素是氖(nǎi),氖气常用于霓虹灯中。
第 11 号元素是钠(nà),钠在日常生活中常见于食盐中。
第 12 号元素是镁(měi),镁是一种轻金属,在航空航天等领域有应用。
第 13 号元素是铝(lǚ),铝是一种广泛使用的金属,具有良好的导电性和延展性。
第 14 号元素是硅(guī),硅是半导体材料的重要组成部分。
第 15 号元素是磷(lín),磷在火柴和化肥生产中起着重要作用。
元素周期(原始)表

练习: 1、完成下列表格:
2、已知某主族元素的原子结构示意图如下,判 断其位于第几周期,第几族?
.
3.已知碳元素、镁元素和溴元素的原子结构示意图:
它们分别位于第几周期?为什么? 回答: 碳有两个电子层,位于第二周期,镁有三个电 子层,位于第三周期;溴有四个电子层,位于第 四周期。
.
4、下列各表为周期表的一部分(表 中为原子序数),其中正确的是( D)
(A)
(B)
234
11
19
2 10 11 18 19
(C) 6 (D)
11 12 13 24
67 14 31 32
.
祝同学们学习进步 再见
.
具有相同的最外层电子数的列主族类别周期序包括元素种数核外电子层数短周期kkr18rbxe18csrn32不完全周期非金属元素金属元素过渡元素元素周期表1元素周期表的编制原则周期
元素周期表
.
1869年门捷列夫在继承和分析了前 人工作的基础上,对大量实验事实进 行了订正、分析和概括,成功地对元 素进行了科学分类。将化学性质相似 的元素放在一个纵行制出了第一张元 素周期表,揭示了化学元素的内在联 系,使其构成一个完整的体系成为化 学发展史上重要的里程碑之一。
元素种数 周期分类
288 短周期
18 18 32 长周期
26
不完全 周期
.
• 3.本节的基本规律: • 原子序数=核电荷数=质子数=核外电子
数 • 周期数=电子层数 • 主族序数=最外层电子数 • 各周期的元素数目:2,8,8,18,
18,32,32 • 稀有气体的原子序数:2,10,18,
36,54,86. • 记住1~20号元素的名称和符号
第一节元素周期表(共40张PPT)
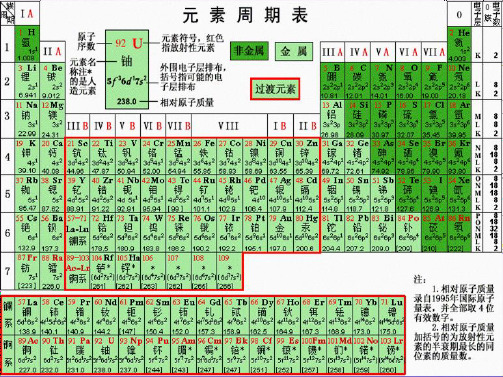
第ⅦA 族
与水缓慢反应
(2)原子结构特点 Cl2+H2O=HCl+HClO
静置后,液体分为两层。
通一过个以 12上C相质比量较同×,1点/思12考:钠和钾最的外性质层有 7个电子
静置后,液体分为两层。
和递变性。 (氧化性:Cl2 >I2)
核电荷数依次增多
不同点: 电子层数依次增多 上层无色,下层分别呈橙红色、紫红色
第一章 物质结构、元素周期律
第一节 元素周期表 一、元素周期表的结构
原子序数:依原子核电荷数由小到大的顺序给元素编号,这种
编号叫原子序数。
原子序数=核电荷数=质子数=核外电子数 (一)元素周期表的编排原则
1、横行: 把电子层数相同的各种元素按原子序数递增顺序
从左到右排列。
2、纵行: 把最外层电子数相同的各种元素按电子层数递增顺序 从上而下排成。
性逐渐增强,非金属性逐渐减弱。
2. 元素性质与原子结构有有密切的关系,主要与原子
核外的排布,特别是最外层电子数有关。原子结构
相似的一族元素,它们在化学性质上表现出相似性 和递变性。
1、砹(At)原子序数85,与F、Cl、Br、I同族,推测砹或
砹的化合物不可能具有的性质是( B)
A、砹易溶于某些有机溶剂 B、砹能与水剧烈反应
应越来越
,剧生烈成的氧化物越来越
。
最高复价杂氧化物对应水化物的碱性越来越 。
强
讨论1:Li与K 应如何保存? Li封存于固体石蜡中, 少量K保存于煤油中。
讨论2:碱金属与盐酸: 2R+2H+= 2R++H2 ↑ 讨论3:碱金属与盐溶液: 先与水反应
讨论4:Li+、Na+、K+、Rb+、Cs+也具有强还原性吗? 没有。 有较弱的氧化性。 氧化性: Li+ > Na+ > K+ > Rb+ > Cs+
化学元素周期表前二十

以下为前20号元素,1到20号按照从左至右的顺序依次排开:H氢,He氦,Li锂,Be铍,B硼,C碳,N氮dao,O氧,F氟,Ne氖内,Na钠,Mg镁,Al铝,Si硅,P 磷,S硫,Cl氯,Ar氩,K钾,Ca钙扩展数据:化学元素周期表是根据原子序数从小到大排序的化学元素的列表。
该列表通常是矩形的,某些具有类似特征的元素归为同一组,例如碱金属元素,碱土金属,卤化元素,稀有气体等。
这使得元素周期表中的元素分为七个主要元素组,七个子组,VIII族和0组。
由于元素周期表可以准确预测各种元素的特性及其相互关系,因此它在化学和其他科学领域中被广泛用作分析化学行为的非常有用的框架。
俄罗斯化学家德米特里·门捷列夫(Dmitri Mendeleev)于1869年发明了元素周期表。
从那时起,已经有170多种元素周期表可以归纳为:短表(由门捷列夫代表),长表(由Werner代表)。
类型),超长表(由polta类型表示);平面螺旋工作台和圆形工作台(由damchev类型表示);三维元素周期表(由莱西的圆锥柱实心表表示)。
中国教学上长期习用的是长式周期表。
化学元素周期表是从小到大核电荷分类的化学元素的列表。
该列表通常是矩形的,某些具有类似特性的元素归为同一组,例如碱金属元素,碱土金属,卤化元素,稀有气体,非金属,过渡元素等。
元素周期表分为七个主要组,七个子组,VIII族和0组。
由于元素周期表可以准确预测各种元素的特性及其相互关系,因此它在化学和其他科学领域中被广泛用作分析化学行为的非常有用的框架。
俄国化学家德米特里·门捷列夫(Dmitri Mendeleev)于1869年发布了此元素周期表,此后,已经有170多种元素周期表,可以将其总结如下:短表(以门捷列夫表示),长表(以Werner类型表示)。
,超长表(以polta类型表示);平面螺旋工作台和圆形工作台(以damkiev型表示);三维元素周期表(由莱西的圆锥柱实心表表示)表。
元素周期表(全面版)
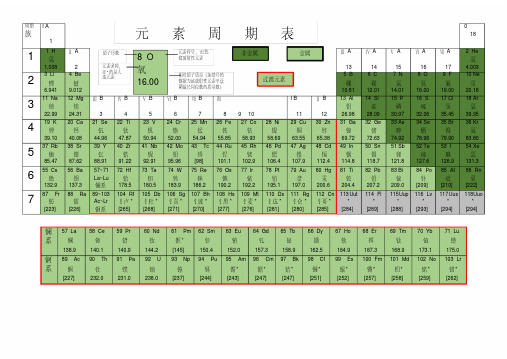
周期族I A1 0181 1 H 氢1.008 Ⅱ A2Ⅲ A13Ⅳ A14Ⅴ A15Ⅵ A16Ⅶ A172 He氦4.0032 3 Li 锂6.941 4 Be铍9.0125 B硼10.816 C碳12.017 N氮14.018 O氧16.009 F氟19.0010 Ne氖20.183 11 Na 钠22.99 12 Mg镁24.31Ⅲ B3Ⅳ B4Ⅴ B5Ⅵ B6Ⅶ B7Ⅷ8 9 10I B11Ⅱ B1213 Al铝26.9814 Si硅28.0915 P磷30.9716 S硫32.0617 Cl氯35.4518 Ar氩39.954 19 K钾39.10 20 Ca钙40.0821 Se钪44.9622 Ti钛47.8723 V钒50.9424 Cr铬52.0025 Mn锰54.9426 Fe铁55.8527 Co钴58.9328 Ni镍58.6929 Cu铜63.5530 Zn锌65.3831 Ga镓69.7232 Ge锗72.6333 As砷74.9234 Se硒78.9635 Br溴79.9036 Kr氪83.805 37 Rb 铷85.47 38 Sr锶87.6239 Y钇88.9140 Zr锆91.2241 Nb铌92.9142 Mo钼95.9643 Tc锝[98]44 Ru钌101.145 Rh铑102.946 Pd钯106.447 Ag银107.948 Cd镉112.449 In铟114.850 Sn锡118.751 Sb锑121.852 Te碲127.653 I碘126.954 Xe氙131.36 55 Cs 铯132.9 56 Ba钡137.357~71La~Lu镧系72 Hf铪178.573 Ta钽180.574 W钨183.975 Re铼186.276 Os锇190.277 Ir铱192.278 Pt铂195.179 Au金197.080 Hg汞200.681 Ti铊204.482 Pb铅207.283 Bi铋209.084 Po钋[209]85 At砹[210]86 Rn氡[222]7 87 Fr钫[223] 88 Ra镭[226]89~103Ac~Lr锕系104 Rf钅卢*[265]105 Db钅杜*[268]106 Sg钅喜*[271]107 Bh钅波*[270]108 Hs钅黑*[277]109 Mt钅麦*[276]110 Ds钅达*[281]111 Rg钅仑*[280]112 Cn钅哥*[285]113Uut*[284]114 Fl*[289]115Uup*[288]116 Lv*[293]117Uus*[294]118Uuo*[294]镧系57 La镧138.958 Ce铈140.159 Pr镨140.960 Nd钕144.261 Pm钷*[145]62 Sm钐150.463 Eu铕152.064 Gd钆157.365 Tb铋158.966 Dy镝162.567 Ho钬164.968 Er铒167.369 Tm铥168.970 Yb镱173.171 Lu镥175.0锕系89 Ac锕[227]90 Th钍232.091 Pa镤231.092 U铀238.093 Np镎[237]94 Pu钚[244]95 Am镅*[243]96 Cm锯*[247]97 Bk锫*[247]98 Cf锎*[251]99 Es锿*[252]100 Fm镄*[257]101 Md钔*[258]102 No锘*[259]103 Lr铹*[262]金属非金属过渡元素8 O氧16.00原子序数元素符号,红色指放射性元素元素名称,注*的是人造元素相对原子质量(加括号的数据为该放射性元素半衰期最长同位数的质量数)元素周期表元素周期表有关知识一、部分酸、碱和盐的溶解性表(室温)说明:“溶”表示那种物质可溶于水,“不”表示不溶于水,“微”表示微溶于水,“挥”表示挥发性,“-”表示那种物质不存在或遇水就分解了。
元素周期表

元素周期表元素周期表主族元素类金属▪硼 ( 5 ) ▪硅 ( 14 ) ▪锗 ( 32 ) ▪砷 ( 33 ) ▪锑 ( 51 )▪碲 ( 52 ) ▪钋 ( 84 )金属元素碱金属▪锂 ( 3 ) ▪钠 ( 11 ) ▪钾 ( 19 ) ▪铷 ( 37 ) ▪铯 ( 55 )▪钫 ( 87 )碱土金属▪铍 ( 4 ) ▪镁 ( 12 ) ▪钙 ( 20 ) ▪锶 ( 38 ) ▪钡 ( 56 )▪镭 ( 88 )其他金属▪铝 ( 13 ) ▪铟 ( 49 ) ▪镓 ( 31 ) ▪锡 ( 50 ) ▪铊 ( 81 )▪铅 ( 82 ) ▪铋 ( 83 )▪ Uut( 113 )▪ Uuq( 114 )▪ Uup( 115 )▪ Uuh( 116 )▪ Uus( 117 )非金属元素稀有气体▪氦 ( 2 ) ▪氖 ( 10 ) ▪氩 ( 18 ) ▪氪 ( 36 ) ▪氙 ( 54 )▪氡 ( 86 )▪ Uuo( 118 )卤族元素▪氟 ( 9 ) ▪氯 ( 17 ) ▪溴 ( 35 ) ▪碘 ( 53 ) ▪砹 ( 85 )其他元素▪氢 ( 1 ) ▪碳 ( 6 ) ▪氮 ( 7 ) ▪氧 ( 8 ) ▪磷 ( 15 )▪硫 ( 16 ) ▪硒 ( 34 )副族元素金属元素镧系▪镧 ( 57 ) ▪铈 ( 58 ) ▪镨 ( 59 ) ▪钕 ( 60 ) ▪钷 ( 61 )▪钐 ( 62 ) ▪铕 ( 63 ) ▪钆 ( 64 ) ▪铽 ( 65 ) ▪镝 ( 66 )▪钬 ( 67 ) ▪铒 ( 68 ) ▪铥 ( 69 ) ▪镱 ( 70 ) ▪镥 ( 71 )锕系▪锕 ( 89 ) ▪钍 ( 90 ) ▪镤 ( 91 ) ▪铀 ( 92 ) ▪镎 ( 93 ) ▪钚 ( 94 ) ▪镅 ( 95 ) ▪锔 ( 96 ) ▪锫 ( 97 ) ▪锎 ( 98 ) ▪锿 ( 99 ) ▪镄 ( 100 ) ▪钔 ( 101 ) ▪锘 ( 102 ) ▪铹 ( 103 )过渡金属▪钪 ( 21 ) ▪钛 ( 22 ) ▪钒 ( 23 ) ▪铬 ( 24 ) ▪锰 ( 25 ) ▪铁 ( 26 ) ▪钴 ( 27 ) ▪镍 ( 28 ) ▪铜 ( 29 ) ▪锌 ( 30 ) ▪钇 ( 39 ) ▪锆 ( 40 ) ▪铌 ( 41 ) ▪钼 ( 42 ) ▪锝 ( 43 ) ▪钌 ( 44 ) ▪铑 ( 45 ) ▪钯 ( 46 ) ▪银 ( 47 ) ▪镉 ( 48 ) ▪铪 ( 72 ) ▪钽 ( 73 ) ▪钨 ( 74 ) ▪铼 ( 75 ) ▪锇 ( 76 ) ▪铱 ( 77 ) ▪铂 ( 78 ) ▪金 ( 79 ) ▪钅卢( 104 )▪钅杜( 105 )▪钅喜( 106 )▪钅波( 107 )▪钅黑( 108 )▪钅麦( 109 )▪鐽 ( 110 ) ▪錀 ( 111 ) ▪鎶 ( 112 ) ▪汞 ( 80 )目录发展史概述发明者生平简介大学期间的探索攀登科学高峰正式发现元素周期表119号元素元素周期表简介IUPAC元素系统命名法元素的位置碱金属性质发展史概述发明者生平简介大学期间的探索攀登科学高峰正式发现元素周期表119号元素元素周期表简介IUPAC元素系统命名法元素的位置碱金属性质展开编辑本段发展史◆诞生:1869年,俄国化学家门捷列夫编制出第一张元素周期表◆依据:按照相对原子质量由小到大排列,将化学性质相似的元素放在同一纵行◆意义:揭示了化学元素之间的内在联系,成为化学发展史上的重要里程碑之一◆发展:随着科学的发展,元素周期表中未知元素留下的空位先后被填满。
