物体是由大量分子组成的典型例题
高中物理-物体是由大量分子组成的练习5

高中物理-物体是由大量分子组成的练习1.(河北省邢台市第一中学高二下学期月考)空调在制冷过程中,室内空气中的水蒸气接触蒸发器(铜管) 液化成水,经排水管排走,空气中水分越来越少,人会感觉干燥.某空调工作一段时间后,排出液化水的体积为V ,水的密度为ρ,摩尔质量为M ,阿伏加德罗常数为N A ,则液化水中分子的总数N 和水分子的直径d 分别为( C )A .N =M ρVN A ,d =36M πρN AB .N =ρVN A M ,d =3πρN A 6MC .N =ρVN A M ,d =36M πρN AD .N =M ρVN A ,d =3πρN A 6M解析:水的摩尔体积 V mol =M ρ;水分子数N =V V mol N A =ρVN A M ;将水分子看成球形,由V mol N A =16πd 3,解得水分子直径为d =36M πρN A,故选C.2.(江苏徐州市高二下学期期末)在“用油膜法估测油酸分子大小”的实验中:(1)下列实验操作正确的是CA .水槽中倒入的水越深越好B .水面上多撒痱子粉比少撒好C .待水面稳定后再将痱子粉均匀地撒在水面上D .滴入液滴时要使滴管离水面尽可能高一些 (2)现有按酒精与油酸的体积比为m n 配制好的油酸酒精溶液,用滴管从量筒中取体积为V 的该种溶液,让其自由滴出,全部滴完共N 滴,把一滴这样的溶液滴入盛水的浅盘中,正确描绘出油膜的形状如图所示,已知坐标纸上每个小方格面积为S .根据以上数据可估算出油酸分子直径为d =nV 8m +n NS. (3)在测量溶液体积时,滴数多数了几滴,会使得测量结果比真实值偏小.解析:(1)根据实验要求,易判选项C 正确,ABD 错误.(2)根据坐标纸上油酸薄膜的轮廓,数出轮廓范围内正方形的个数为8(不足半个的舍去,多于半个的算一个),又因为坐标纸上每个方格面积为S ,则油膜面积为S 0=8S .设油酸的体积为V 酸,油酸酒精溶液的浓度为V 酸V 液=n m +n1滴油酸酒精溶液的体积V 滴=V N1滴油酸酒精溶液中纯油酸的体积为V 0=nm +n ×V N则估算油酸分子直径的表达式为 d =V 0S 0=nV 8NS m +n. (3)由上式可知,滴数多数了几滴,N 变大,d 变小.3.(南京市溧水高中高二下学期期中)已知潜水员在岸上和海底吸入空气的密度分别为 1.3kg/m 3和 2.1kg/m 3,空气的摩尔质量为0.029kg/mol,阿伏加德罗常数N A=6.02×1023mol-1.若潜水员呼吸一次吸入2L空气,试估算潜水员在海底比在岸上每呼吸一次多吸入空气的分子数.(结果保留一位有效数字)答案:3×1022个解析:设空气的摩尔质量为M,在海底和岸上的密度分别为ρ海和ρ岸,一次吸入空气的体积为V,则有Δn=ρ海-ρ岸VMN A,代入数据得Δn=3×1022.。
物体是由大量分子组成的(原创)

第1节 物体是由大量分子组成的
• 什么叫分子? • 分子是什么形状? • 油水分子结构
用油膜法估测分子的大小
• 在做“用油膜法测分子的大小”实验时,油酸酒精溶液 的浓度为每104ml溶液中有纯油酸6mL,用注射器测得 1mL上述溶液有液滴75滴.把1滴该溶液滴入盛水的浅盘 里,待水面稳定后,将玻璃板放在浅盘上,在玻璃板上 描出油酸膜的轮廓,随后把玻璃板放在坐标纸上,其形 状和尺寸如图所示,坐标中正方形小方格的边长为1cm, 问:
(1)每一滴油酸酒精溶液中含有纯油酸的体 积是多少? (2) 油酸膜的面积是多少cm2 ? (3)按以上数据,估测出油酸分子的直径是 多少?
分子的大小
• 多数分子尺寸的数量级为10-10m
课堂练习
• 课课练第3页第12题。
分子的数目
• 1mol的任何物质都含有相同的粒子数,这 个数量用阿伏加德罗常数。 • NA=6.02×1023mol-1
高二物理物体是由大量分子组成的 人教版

Байду номын сангаас
固体、液体
ddd
d
小球模型
气体
立方体模型
d
d
d
巩固练习: 1.体积是10-4cm3的油滴滴于水中,若展开成一单分子油膜, 则油膜面积的数量级是_________
A.102cm2 B.104cm2 C.106cm2 D.108cm2
2.若已知铁的原子量是 56,铁的密度是7.8×103kg/m3, 试求:①质量是1g的铁块中铁原子的数目? ②是否可以计算出铁原子的直径d是多少m? (结果保留1位有效数字)
第11章 分子热运动 能量守恒
1、物体是由大量分子组成的
单分子油膜法实验装置
已知体积V=1mm3的一滴油,在水面上形成面积S=3.5m2 的油膜,那么这种油分子的直径d为多少m?
油酸分子
d
油膜法估算分子直径公式 d V S
扫描隧道显微镜装置示意图
扫描隧道显微镜拍摄的石墨表面原子排布图
例题1.已知金刚石的密度ρ= 3.5×103 kg/m3 , 碳的摩尔质量为1.2×10-2 kg/mol。现有一块体 积V = 5.7×10-8 m3的金刚石,则: ①它含有多少个碳原子?
物体是由大量分子组成的

l
d
微观量的估算方法
3、物质分子所含分子数的估算: 物质分子所含分子数的估算:
关键为求出分子的摩尔数, 关键为求出分子的摩尔数,便可以利用阿佛加德罗 常数求出含有的分子数
例题: 例题:
MA = 29×10−3 kg/m ol 已知空气的摩尔质量是, 已知空气的摩尔质量是,
则空气中气体分子的平均质量多大? 则空气中气体分子的平均质量多大?成年人 做一次深呼吸,约吸入450cm3的空气,则做 的空气, 做一次深呼吸,约吸入 一次深呼吸所吸入的空气质量是多少? 一次深呼吸所吸入的空气质量是多少?所吸 入的气体分子数量是多少?( ?(按标准状况估 入的气体分子数量是多少?(按标准状况估 算) VA=22.4l
23
−1
微观量的估算方法
1、固体或者液体分子的估算方法: 固体或者液体分子的估算方法: 对固体或液体来说, 对固体或液体来说,分子间隙数量级远小于分子大小的 数量级,所以可以近似认为分子紧密排列, 紧密排列 数量级,所以可以近似认为分子紧密排列,据这一理想 化模型, 任何固体或液体都含有N 化模型,1mol任何固体或液体都含有 A个分子,其摩 任何固体或液体都含有 个分子, 尔体积N 可以认为是N 个分子体积的总和。 尔体积 mol可以认为是 A个分子体积的总和。
解析 :
1.空气分子的平均质量为: 空气分子的平均质量为:
29×10−3 MA m= = = 4.82×10−26 kg NA 6.02×1023
2.成年人做一次深呼吸所吸入的空气质量为: 成年人做一次深呼吸所吸入的空气质量为:
m′ =
×29×10−3 kg = 5.8×10−4 kg 22.4×10−3
45ቤተ መጻሕፍቲ ባይዱ×10−6
物质是由大量分子组成的(含答案)

物质是由大量分子组成的基础练习题1、1g 氢气中含有氢分子的个数是____,在标准状况下它的体积是_____m 3。
2、已知阿伏伽德罗常数为N ,固态或液态物质的摩尔体积为V mol ,物质的摩尔质量为M ,密度为ρ,则每一个分子的体积V =_____,每一个分子的质量m =__,若物质的总质量为M 总,则物质的分子数n =_____,物质的密度ρ=_____。
3、水分子的质量等于_____kg ,已知阿伏伽德罗常数为6.02×1023/mol4、已知金属铅的密度是11.34×103kg /m 3 ,它的摩尔质量是0.2027kg /mol ,那么1cm 3的铅块中含有_______个铅原子,每个铅原子的质量是_____kg (阿伏伽德常数N =6.022×1023/mol )5、体积是2×10-3cm 3的一滴油,滴在湖面上,最终扩展成面积为6 m 2的油膜,由此可以估算出该种油分子直径的大小是______m .(要求一位有效数字)6、在标准状况下,1mol 任何气体的体积都是22.4L ,那么,在标准状况下,11.2L 氢气中的分子数是____个(阿伏伽德罗常数N A =6.02×1023/mol )7、已知物质的密度为ρ,该物质的摩尔质量为μ,估算分子的直径为______8、1mol 某种物质的质量是Mkg ,若用N A 表示阿伏伽德罗常数,则这种物质每个分子的质量是_____kg .9、阿伏伽德罗常数是N /mol ,铜的摩尔质量为Mkg /mol ,铜的密度是ρkg /m 3,那么以下说法正确的是( ).(A)1kg 铜所含原子的数目是ρN(B)1m 3铜所含原子的数目是ρN /M(C)1个铜原子的质量是ρ/Nkg(D)1个铜原子占有的体积是M /ρNm 310、对容积为0.831L 的容器中的空气进行抽气,抽气过程中温度保持为27°C 不变,当容器内的空气压强降为1.0×10-8Pa 时,则容器中空气的分子数为( ).(A)2.0×109个 (B)2.0×1010个(C) 2.0×1011个 (D) 2.0×1012个11、已知铜的密度为8.9×103kg ∕m 3,原子量为64.通过估算可知铜中每个铜原子所占的体积为( ).(A)7×10-6m 3 (B)1×10-29 m 3(C)1×10-26 m 3 (D)8×10-24 m 312、将体积为V 的一滴油,滴在水面上扩展成单分子油膜,油膜面积为S ,已知油的密度为ρ,油的摩尔质量为M ,假定每个油分子都是等大的球形,并认为油分子是一个挨着一个紧密排列的,那么根据这些数据可以列出阿伏伽德罗常数计算式为_____。
高中物理选修3-3-物体是由大量分子组成的
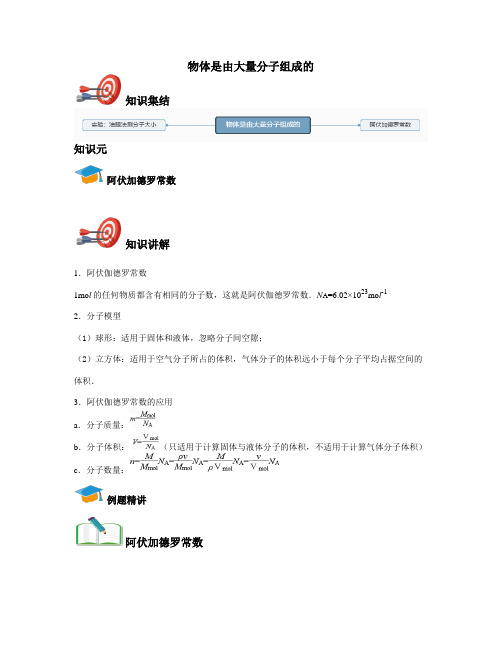
物体是由大量分子组成的知识集结知识元阿伏加德罗常数知识讲解1.阿伏伽德罗常数1mo l的任何物质都含有相同的分子数,这就是阿伏伽德罗常数.N A=6.02×1023mo l-12.分子模型(1)球形:适用于固体和液体,忽略分子间空隙;(2)立方体:适用于空气分子所占的体积,气体分子的体积远小于每个分子平均占据空间的体积.3.阿伏伽德罗常数的应用a.分子质量:b.分子体积:(只适用于计算固体与液体分子的体积,不适用于计算气体分子体积)c.分子数量:例题精讲阿伏加德罗常数例1.'已知气泡内气体的密度为1.29kg/m3,平均摩尔质量为0.29kg/mol。
阿伏加德罗常数N A=6.02×1023mol-1,取气体分子的平均直径为2×10-10m,若气泡内的气体能完全变为液体,请估算液体体积与原来气体体积的比值。
(结果保留以为有效数字)'例2.'水是生命之源,保护水源需要人类共同努力,使用完毕后应及时关闭开关水龙头。
某水龙头打开1秒钟就有50ml水流出,已知水的摩尔质量为M=1.8×10-2kg/mol,水的密度ρ=1.0×103kg/m3,阿伏加德罗常数N A=6.0×1023mol-1(结果保留一位小数字)。
(i)若将水分子视为立方体,估算水分子的质量及其边长大小;(ii)估算1s内流出的水分子个数。
'例3.'科技人员测得钙钛单晶的体积为V,密度为ρ,摩尔质量为M,阿伏伽德罗常数为N A,求:①该晶体所含的分子数;②估算该晶体分子直径D(球的体积V)'例4.'成年人在正常状态下1分钟呼吸18次,每次吸入的空气约为500mL,空气中氧气的含量约为21%,氧气的密度约为1.4kg/m3、摩尔质量为3.2×10-2kg/mol,阿伏加德罗常数N A取60×1023mol-1.求成年人在1分钟的时间内:(结果均保留一位有效数字)(1)吸入氧气的质量(2)吸入氧气的分子数'例5.'目前,环境污染已非常严重,瓶装纯净水已经占领柜台,再严重下去,瓶装纯净空气也会上市,设瓶子的容积为500mL,空气的摩尔质量M=29×10-3kg/mol按标准状况计算,N A=6.0×1023mol-1,气体的摩尔体积V m=22.4L,试估算:(1)空气分子的平均质量;(2)一瓶中气体分子的个数(结果均保留两位有效数字)。
高中物理第七章分子动理论1物体是由大量分子组成的练习含解析新人教版选修3311301139

高中物理第七章分子动理论1物体是由大量分子组成的练习含解析新人教版选修3311301139物体是由大量分子组成的[A 组 素养达标]1.为了减小“用油膜法估测分子的大小”的实验误差,下列方法可行的是( ) A .用注射器取1 mL 配制好的油酸酒精溶液,共N 滴,则每滴中含有油酸1NmLB .把浅盘水平放置,在浅盘里倒入一些水,使水面离盘口距离小一些C .先在浅盘中撒些痱子粉,再用注射器把油酸酒精溶液多滴几滴在水面上D .实验时先将一滴油酸酒精溶液滴入水中,再把痱子粉洒在水面上解析:1NmL 是一滴油酸酒精溶液的体积,乘以其中油酸的浓度才是油酸的体积,A 错误,B 正确;多滴几滴能够使测量形成油膜的油酸体积更精确些,但多滴以后会使油膜面积增大,可能使油膜这个不规则形状的一部分与浅盘的壁相接触,这样油膜就不是单分子油膜了,故C 错误;为了使油酸分子紧密排列,实验时先将痱子粉均匀洒在水面上,再把一滴油酸酒精溶液滴在水面上,D 错误.答案:B2.(多选)下列说法中正确的是( ) A .很小的物体也是由大量分子组成的B .无论是无机物质的分子,还是有机物质的分子,其分子大小的数量级都是10-10mC .本节中所说的“分子”,包含化学中的分子,也包括原子和离子D .分子的质量是很小的,其数量级为10-10kg解析:物体是由大量分子组成的,故A 项正确;一些有机物质的大分子其分子大小的数量级超过10-10m ,故B 项错误;本节中把化学中的分子、原子、离子统称为分子,故C 项正确;分子质量的数量级一般为10-26kg ,故D 错误.答案:AC3.下列哪一组数据可以算出阿伏加德罗常数( ) A .水的密度和水的摩尔质量 B .水的摩尔质量和水分子的体积 C .水分子的体积和水分子的质量 D .水分子的质量和水的摩尔质量解析:对于水有:M A =N A ·m 0①,V A =N A ·V 0②,可以看出只有D 项可由①式求出N A =M A m 0,故D 正确,A 、B 、C 错误.答案:D4.纳米材料具有很多优越性,有着广阔的应用前景.边长为1 nm 的立方体,可容纳液态氢分子(其直径约为10-10m)的个数最接近于( )A .102个 B .103个 C .106个D .109个解析:1 nm =10-9m ,则边长为1 nm 的立方体的体积V =(10-9)3m 3=10-27m 3;将液态氢分子看成边长为10-10m 的小立方体,则每个氢分子的体积V 0=(10-10)3m 3=10-30m 3,所以可容纳的液态氢分子的个数N =V V 0=103个.液态氢分子可认为分子是紧挨着的,其空隙可忽略,对此题而言,建立立方体模型比球形模型运算更简洁.答案:B5.已知在标准状况下,1 mol 氢气的体积为22.4 L ,氢气分子间距约为( ) A .10-9m B .10-10mC .10-11 m D .10-8m解析:在标准状况下,1 mol 氢气的体积为22.4 L ,则每个氢气分子占据的体积V 0=V N A=22.4×10-36.02×1023 m 3≈3.72×10-26 m 3.按立方体估算,则每个氢气分子占据体积的边长:L =3V 0=33.72×10-26 m≈3.3×10-9m .故选A.答案:A6.若以M 表示水的摩尔质量,V m 表示在标准状态下水蒸气的摩尔体积,ρ为在标准状态下水蒸气的密度,N A 为阿伏加德罗常数,m 0、V 0分别表示每个水分子的质量和体积,下面四个关系式:①N A =V m ρm 0 ②ρ=M N A V 0 ③m 0=M N A ④V 0=V mN A其中正确的是( ) A .①和② B .①和③ C .③和④D .①和④解析:对于气体,宏观量M 、V m 、ρ之间的关系式仍适用,有M =ρV m ,宏观量与微观量之间的质量关系也适用,有N A =Mm 0,所以m 0=M N A ,③式正确;N A =M m 0=ρV mm 0,①式正确;由于气体的分子间有较大的距离,V mN A求出的是一个气体分子平均占有的空间,一个气体分子的体积远远小于该空间,所以④式不正确.气体密度公式不适用于单个气体分子的计算,故②式也不正确.答案:B7.已知水银的摩尔质量为M ,密度为ρ,阿伏加德罗常数为N A ,则水银分子的直径是( )A. B.C.6MπρN AD.M ρN A解析:1 mol 水银的体积V =M ρ,1个水银分子的体积V 0=V N A =MρN A,把水银分子看成球体,则V 0=16πd 3,所以d =,故选项A 正确.答案:A8.已知地球到月球的平均距离为384 400 km ,金原子的直径为3.48×10-9m ,金的摩尔质量为197 g/mol.若将金原子一个接一个地紧挨排列起来,筑成从地球通往月球的“分子大道”,试问:(1)该“分子大道”需要多少个原子? (2)这些原子的总质量为多少?解析:(1)地球到月球的平均距离为384 400 km ,金原子的直径为3.48×10-9m ,故“分子大道”需要的原子数N =s d =384 400×1033.48×10-9≈1.10×1017. (2)单个原子的质量m 0=M N A这些原子的总质量m =m 0N联立解得m =NM N A =1.10×1017×0.1976.02×1023kg≈3.6×10-8kg. 答案:(1)1.10×1017个 (2)3.6×10-8kg[B 组 素养提升]9.已知地球表面空气的总质量为m ,空气的平均摩尔质量为M ,阿伏加德罗常数为N A ,若把地球表面的空气全部液化且均匀分布在地球表面,则地球的半径将增加ΔR ,为估算ΔR ,除上述已知量之外,还需要下列哪一组物理量( )A .地球半径RB .液体密度ρC .地球半径R ,空气分子的平均体积V 0D .液体密度ρ,空气分子的平均体积V 0解析:若把空气全部液化且均匀分布在地球表面时,形成一个更大的球体,液化后的空气形成球壳的体积:V =43π(R +ΔR )3-43πR 3又:V =m MN A V 0联立可求ΔR 的值,故C 正确. 答案:C10.在“用油膜法估测分子的大小”实验中,按照酒精与油酸体积比m ∶n 配制油酸酒精溶液.现用滴管滴取油酸酒精溶液,N 滴溶液的总体积为V .(1)用滴管将一滴油酸酒精溶液滴入浅盘,待稳定后将油酸薄膜轮廓描绘在坐标纸上,如图所示.已知坐标纸上每个小方格面积为S ,则油膜面积为________.(2)估算油酸分子直径的表达式为________(用题目中物理量的字母表示).解析:(1)根据坐标纸上油酸薄膜的轮廓,数出轮廓范围内正方形的个数为115(不足半个的舍去,多于半个的算一个),又因为坐标纸上每个方格面积为S ,则油膜面积为S 0=115S .(2)设油酸的体积为V 酸,油酸酒精溶液的浓度为 V 酸V 液=n m +n1滴油酸酒精溶液的体积为V 滴=V N1滴油酸酒精溶液中纯油酸的体积为V 0=nm +n ·V N则估算油酸分子直径的表达式为d =V 0S 0=nV 115NS (m +n ). 答案:(1)115S (114S 或116S 均可) (2)nV115NS (m +n )11.2015年2月,美国科学家创造出一种利用细菌将太阳能转化为液体燃料的“人造树叶”系统,使太阳能取代石油成为可能.假设该“人造树叶”工作一段时间后,能将1.0×10-6g 的水分解为氢气和氧气.已知水的密度ρ=1.0×103 kg/m 3、摩尔质量M =1.8×10-2kg/mol ,阿伏加德罗常数N A =6.0×1023 mol -1.试求:(结果均保留1位有效数字)(1)被分解的水中含有水分子的总数N ; (2)一个水分子的体积V .解析:(1)水分子数N =mN A M =1×10-6×6.0×10231.8×10-2×103≈3×1016. (2)水的摩尔体积V m =M ρ水分子体积V =V m N A =M ρN A=3×10-29 m 3.答案:(1)3×1016(2)3×10-29m 3[C 组 学霸冲刺]12.已知银的密度为ρ=10.5×103 kg/m 3,摩尔质量为M =107.83×10-3kg/mol ,阿伏加德罗常数为N A =6.02×1023mol -1.假设银导线中银原子的最外层电子全部变成自由电子,那么直径为2 mm 的导线中,每米中含有自由电子数目的数量约为多少?解析:每立方米的银导线中物质的量为10.5×103×1107.83×10-3 mol≈0.97×105mol ,原子的数目为n =6.02×1023×0.97×105个≈5.84×1028个,因为V =LS ,所以长为1 m 、直径为2 mm 的银导线中的原子数目即自由电子数目(因银原子最外层只有1个电子)n 1=nV =n ·L ·S =n ·L ·πr 2=5.84×1028×1×3.14×(1×10-3)2个≈1.83×1023个.答案:1.83×1023个。
第十一章:分子热运动 能量守恒典型例题

第一节 物体是由大量分子组成的例题1:已知铜的密度为8.9×103kg/m 3,原子量为64,通过估算可知铜中每个铜原子所占的体积为:A 、7×10-6m 3B 、1×10-29m 3C 、1×10-26m 3D 、8×10-24m 3答案: B评析:本题为95年高考题,是一个典型的微观量计算题.由原子量知每摩尔铜的质量,再除以密度,得摩尔体积,最后用摩尔体积除以阿弗加德罗常数即可估算出每个铜原子所占的体积.本题还可以根据分子直径的数量级10-10m ,猜出答案.例题2:已知碳的摩尔质量为12g ,阿伏加德罗常数为6.02×1023mol -1,求每个碳原子的质量.解:每个碳原子的质量为kg kg N m A 2623310995.11002.61012--⨯=⨯⨯==μ例题3:某教室长m 10,宽m 7,高m 3,试在标准状态下估算空气分子间的平均距离,并比较这个距离和分子直径的数量级.选题目的:理解阿伏伽德罗常数和摩尔体积的运用.解析:教室内空气的体积332103710m m V =⨯⨯=空气的物质的量mol mol n 33104.9104.22210⨯=⨯=- 空气的分子数为 27233106.5106104.9⨯=⨯⨯⨯==A nN N 个每个空气分子平均占有空间为326327108.3106.5210m m N V v -⨯=⨯==把每个分子占有的空间看成立方体,每个分子中心间的距离等于立方体的边长,用d 表示 m m v d 93263104.3108.3--⨯=⨯==分子直径的数量级为m 1010-,由上面计算可知,气体分子间距离的数量级为m 910-,约为分子直径的10倍.例题4:一滴水的体积为35102.1cm -⨯,如果放在开口容器中,由于蒸发每分钟能跑出的水分子数为8100.6⨯个,需要多长时间跑完?选题目的:理解阿伏伽德罗常数和摩尔体积的运用.解析:水的摩尔体积为mol m V /108.135-⨯=这一滴水含水分子数为 1723565100.41002.6108.110102.1⨯=⨯⨯⨯⨯⨯==---A N V v N 个 水分子跑完的时间为min 107.6100.6100.48817⨯=⨯⨯==n N t 我们知道,在开口容器中蒸发掉一滴水,根本不需要min 107.68⨯的时间,原因在于实际当中每分钟跑出的水分子数比8107.6⨯个还要多得多.例题5:从下列哪一组数据可以算出阿伏加德罗常数( )A .氧气的摩尔质量和氧分子的体积B .氧分子的质量和氧分子的体积C .氧分子的质量和氧气的摩尔质量D .氧气的密度和氧气的摩尔质量选题目的:理解推导阿伏加德罗常数所需的物理量.解析: 要算出阿伏伽德罗常数,首先要知道1 mol 物质的质量M 或体积V ,设分子质量为m ,分子体积v ,则阿伏伽德常数. m M N A =,对固体和液体还有:vV N A = 在(A )、(D )选项中不知氧分子质量,不能算出阿伏伽德罗常数,故不能选(A )、(D )项;在(B )项中不知氧气摩尔质量,不能算出阿伏伽德罗常数,故不能选(B )项.值得注意的是在(A )、(B )选项中如果知道氧气的摩尔体积也不能算出阿伏伽德罗常数,因为气体分子间距离很大,不能忽略.正确选项(C )例题6:已知金的密度为33/103.19m kg ⨯,体积为31cm 的金中含有多少个金原子?(取2位有效数字)选题目的:练习阿伏加德罗常数的应用.解析:设金的密度为ρ,体积为V ,质量为m ,则:金的质量为kg kg V m 2631093.1101103.19--⨯=⨯⨯⨯==ρ金的摩尔质量为kg M 197.0=金原子个数为:22232109.51002.6197.01093.1⨯=⨯⨯⨯==-A N M m N 个 第二节 分子的热运动例题1:在观察布朗运动的实验过程中,每隔5秒记录下颗粒的位置,最后将这些位置用直线依次连接,如图所示,则下列说法错误的是A 、由图可以看出布朗运动是无规则的B 、图中轨迹就是颗粒无规则运动的轨迹C 、若对比不同温度下的轨迹,可以看出温度高时布朗运动显著D 、若对比不同颗粒大小时的轨迹,可以看出颗粒小时布朗运动显著答案:B评析:由于是每隔5秒记录下颗粒的位置,最后将这些位置用直线依次连接,但并不知道这5秒时间内颗粒的运动轨迹(其实这5秒内的轨迹也是无规则的),所以记录下的并不是颗粒的实际运动轨迹.典型例题2:课本中画出了三个颗粒运动位置的连线图,这些连线是颗粒的运动轨迹吗?出题目的:理解分子运动的无规则性.解析:三颗粒运动位置的连线图,是显微镜下追踪三个悬浮颗粒的运动,每隔30S 把观察到的颗粒位置记录下来,然后用直线把这些位置依次连接起来所得到的连线图,从图中可以看出颗粒的运动是无规则的.在30S之间颗粒的运动也是很不规则的,不是沿直线运动,颗粒的实际运动情况比图中记录的还要复杂,因此,图中的连线不是颗粒运动的轨迹.例题3:在较暗的房间里,从射进来的阳光中,可以看到悬浮在空气中的微粒在不停地运动,这些微粒的运动是()A.布朗运动B.曲线运动C.自由落体运动D.无法确定选题目的:理解微粒做布朗运动的条件.解析:能用肉眼直接看得到的微粒是很大的颗粒,在同一时刻它们受到来自各个方向的空气分子撞击的合力几乎为零,微小的作用不能使这么大的颗粒作布朗运动,(A)错;微粒的运动是由于空气对流和在重力作用下的结果,微粒作曲线运动,(C)、(D)错。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
物体是由大量分子组成的典型例题
[例1]试从分子动理论的观点,说明物质三态(固态、液态、气态)为什么有不同的宏观特征?
[分析]可以根据分子间距的不同,使得分子间相互作用力也不同的特点去解释.
固体分子间的距离非常小,分子之间的作用力很大,其分子只能在平衡位置附近作范围很小的无规则振动.因此,固体不但具有一定的体积,还具有一定的形状.
液体分子间的距离比较小,分子之间的作用力也相当大,但与固体分子相比,液体分子可以在平衡位置附近作范围较大的无规则振动,而且液体分子的平衡位置不是固定的,是在不断地移动.因而液体虽然具有一定的体积,却没有固定的形状.
气体分子间距离很大,彼此间的作用力极为微小,其分子除了在与其他分子或器壁碰撞时有相互作用外是不受其他作用力的.因而气体分子总是作匀速直线运动,直到碰撞时才改变方向.所以气体没有一定的体积,也没有一定的形状,总是充满整个容器.
[说明]
分子之间相互作用力,就其本质来说是属于电性的,是由构成分子的带电粒子(电子、质子)的相互作用引起的.
通常情况下分子呈电中性,当两个分子相互接近时,每个分子的表面电荷(负)密度重新分布,在分子的某一部分上,电荷的平均距离变小,而在另一部分上则变大.这样,在两个分子上就形成带相反电荷的区域,从而产生分子间的吸引力.如果分子靠得更近,以致分子的外层电子开始叠合,由于同种电荷作用,分子便相互推斥了.[例2]已知下列物理量:M(摩尔质量)、m(分子质量)、ρ(物质密度)、V(摩尔体积)、v(分子体积)、N A(阿伏加德罗常数),由这些量组成以下关系式中,对固体、液体、气体都成立的是 [ ]
分析这六个物理量在国际单位制中的单位如下表所示:
通过对题中各式的单位验算,立即可先排除A、D、F三个关系式.
对固体和液体,可设想它们的分子一个紧挨一个排列的,因此阿伏加德罗常数与摩尔体积、分子体积的关系式如B所示,但对气体不成立.只有C、E两式对固体、液体、气体都能成立.
答 C,E.
【例3】已知金刚石的密度ρ=3500kg/m3。
现有一块体积V=5.7×10-8m3的金刚石,它含有多少个碳原子?假如金刚石中碳原子是紧密地堆在一起的,试估算碳原子的直径。
[分析]
在利用阿伏伽德罗常数沟通微观世界与宏观世界时,主要体现在如下宏观量与微观量的关系上:摩尔体积与分子体积的关系是V N=N·V0;摩尔质量与分子质量的关系是M=N·m。
这类问题主要不在“数”而在“理”,不追求数据精确而追求方法正确。
例如在估算碳原子的直径时,首先要建立起一个理想化的物理模型;把碳原子看成是紧密排列的,将碳的摩尔体积分成N个等分,每个等分就是一个碳原子。
若把分子看成小球,则这一等分就是一个小球。
这样就能很快估算出碳原子的体积和直径来。
[解法1]碳的摩尔体积
每个碳原子的体积
金刚石所含碳原子数
碳原子的直径约为
[解法2]金刚石的质量
m=ρV=3500×5.7×10-8≈2.0×10-4kg
碳的摩尔数
金刚石所含碳原子数
n'=nN=1.7×10-2×6.02×1023=1.02×1022(个)
一个碳原子的体积
子直径约为
[例4]普通一个房间的面积S=15m2,高h=3m,已知空气的平均摩尔质量M=2.9×10-2kg/mol,这个房间内空气的质量约为[ ] A.几g
B.几kg
C.几十kg
D.几百kg
[分析]房间的空气体积
V=Sh=15×3m3=45m3
把这些空气看成在标准状况下,因为标准状况下1mol气体积的体积V0=22.4×10-3m3,因此这些空气的摩尔数为:
由空气的平均摩尔质量得空气质量为:
[答]C.
[说明]如要作较准确的计算,需测出空气的温度和压强,根据气体定律折算成标准状况下的体积,然后得出空气的摩尔数.[例5]在标准状况下,水蒸气分子的间距约是水分子直径的[ ]
A.1倍
B.10倍
C.100倍
D.1000倍
[分析]在标准状况下,水蒸气的摩尔体积V汽=22.4×10-3m3/mol,含有分子数为N=6.02×1023(个),每个水蒸气分子所占体积
把每个蒸气分子所占体积看成一个小立方体,分子的平均间距可以看成是相邻两个小立方体的中心间距,它等于每个小立方体的边长,即
水的摩尔体积V水=18cm3/mol=18×10-6m3/mol,把水分子看成紧挨着的一个个小球,因此,其直径为
[答]B.
[说明]应该记住固体、液体分子的间距与分子直径的数量级相同,均为10-10m,通常情况下,气体分子间距的数量级约为10-9m.[例6]将1cm3的油酸溶于酒精,制成200cm3的油酸酒精溶液.已知1cm3溶液有50滴,现取1滴油酸酒精溶液滴到水面上.随着酒精溶于水,油酸在水面上形成一单分子薄层,已测出这一薄层的面积为0.2m2.由此可估测油酸分子的直径为______m.
[分析]1滴油酸酒精溶积的体积为
式中N=50,为总的滴数.
中油酸的体积为
已知油酸薄层的面积为S=0.2m2,所以油酸分子的直径为
[答]5×10-10m
[说明]油酸溶液滴入后,由于有油酸区域的表面张力系数小于周围清水区域的表面张力系数,于是,就在水的表面张力的作用下使油滴很快散开成薄膜.当油膜的面积不再增大时,就可以认为它是一层单分子薄膜了,薄膜的厚度等于分子的直径.
实验中为了较方便地确定油膜的面积,在油滴滴入水面之前,先在水面上撒一薄层松花粉(或滑石粉),油膜面积的大小,可由松花粉(或滑石粉)围成的闭合边界确定.
待油膜不再扩散时,可用一片玻璃盖在水盘上,用笔按照松花粉的边界描出油膜的边缘,然后将描有油膜范围的玻璃片放在方格纸上,根据每一小方格的面积(l2cm2)和油膜所占的格数n(占大半格的算作1格,不足半格的舍去),即可算出油膜的面积s=nl2cm2.。
