紫外吸收光谱的基本原理
紫外吸收光谱分析

单色器是将光源发出的复合光分解为单色光的装置。在紫外吸收光谱分析中,常 用的单色器有棱镜单色器和光栅单色器。棱镜单色器分辨率较低,适用于宽波段 扫描;光栅单色器分辨率较高,适用于窄波段扫描和定量分析。
样品池设计与使用注意事项
样品池设计
样品池是承载样品的装置,其设计应考虑到样品的性质、浓度以及分析波长等因素。常 用的样品池有石英比色皿和玻璃比色皿,前者适用于紫外区域的分析,后者适用于可见 光区域的分析。此外,样品池的光程长也是需要考虑的因素,一般根据分析需求选择合
03 样品前处理与实验条件 优化
样品溶解与稀释方法
选择合适溶剂
根据样品的性质选择合适的溶剂 ,确保样品在溶剂中完全溶解, 避免产生浑浊或沉淀。
稀释倍数确定
根据样品的浓度和仪器的检测范 围,确定合适的稀释倍数,使样 品在检测时处于线性范围内。
pH值调整及缓冲液选择
pH值调整
根据样品的性质和实验需求,使用酸或碱调整样品的pH值,确保样品在合适 的pH值下进行实验。
多组分体系同时测定策略探讨
1 2 3
多波长测定法
利用不同组分在紫外光谱中的特征吸收峰,选择 多个波长进行同时测定,实现多组分体系的分析 。
差分光谱法
通过比较样品与参比溶液在特定波长下的吸光度 差异,消除背景干扰,提高多组分体系测定的准 确性。
化学计量学方法
结合化学计量学算法,对多组分体系的紫外吸收 光谱数据进行解析,实现各组分浓度的同时测定 。
应用举例
在药物分析中,利用紫外光谱法可以 快速识别原料药或制剂中的主成分, 以及可能的杂质或降解产物。
导数光谱法在Biblioteka 合物鉴定中应用原理导数光谱法通过对原始紫外光谱进行数学处理(求导),可 以突出光谱的细微特征,提高混合物中各组分的分辨率。
紫外吸收光谱的基本原理.

n →π* 丙酮:280nm,15)ε≤100
饱和烃 σ→σ* ; 烯烃、炔烃 σ→σ*、π→π*; 脂肪醚σ→σ*、n →σ*; 醛酮 π→π* 、 n →σ* 、σ→ σ* 、 n → π*)
四、紫外光谱中常用的几个术语 1、发色基团和助色基团
发色基团:凡是能导致化合物在紫外及可见光区产 生吸收的基团,不论是否显示颜色都称 为发色基团。
§2 紫外吸收光谱的基本原理
一、紫外吸收光谱的产生
物质
电磁波1
电磁波 2
能量
n2
n1
ΔE=En2-En1=hν
二、紫外光谱的表示方法
A=log(I0/I1)
T= I1/I0 A=log(1/T)
A=εbc ε 为 摩 尔 吸 光 系 数 , 它 是 浓 度 为 1mol/L 的 溶 液 在 1cm宽的吸收池中,在一定波长下测得的吸光度; c为物质的浓度,单位为mol/L; b为液层厚度,单位为cm。
三、分子轨道与电子跃迁的类型
1、分子轨道
分子轨道
成键分子轨道 反键分子轨道
分子轨道
σ 轨道 π 轨道 n轨道
σ 电子 π 电子 n电子
2、电子跃迁的类型
分子轨道能级高低次序: σ* > π* > n > π > σ
σ*
σ*
π*
π*
E
n
E
n
π σ
π
σ
(1)、σ→σ* λ< 150nm 、环丙烷 190nm
abcabcd变化增色减色3吸收带ar吸收带跃迁所产生bk吸收带k吸收带波长大于200nm吸收强度强10含有氧硫氮等杂原子的发色基团羰基硝基乙醛290nm17吸收波长长吸收强度低共轭双键跃迁所产生cb吸收带吸收波长长吸收强度低苯256nm215闭合环状共轭双键的跃迁所产生的在非极性溶剂中或气态时b吸收大带会出现精细结构但有一些芳香化合物的b吸收带往往没有精细结构极性溶剂的使用会使精细结构消失
紫外光谱分析基本原理

TYPES OF TRANSITIONS
提示 分子轨道理论:一个成键轨道必定有一 个相应的反键轨道。通常外层电子均处 于分子轨道的基态,即成键轨道或非键 轨道上。
v Not
all transitions that are possible will be observed. Some electronic transitions are "forbidden" by certain selection rules. However, even forbidden transitions can be observed, but these are usually not very intense.
to *
Chromophore
lmax
Alkanes ~ 150 v__________________________
_____________________________
to *
Chromophore lmax ______________________ Alkenes ~ 175 Alkynes ~ 170 Carbonyls ~ 188 ________________________
真空 紫外区
近紫外区
可见光区
100nm
200nm
400nm
800nm
真空紫外区——波长范围在200nm以下的区域。 真空紫外区对普通有机物的结构分析的用处不大。 近紫外区——波长范围在200nm-400nm之间的区域。 近紫外区对有机物结构分析的用处最大。共轭体系以及 芳香族化合物在此区域内有吸收,是紫外光谱讨论的主要对 象。 可见光区——波长范围在400nm-800nm之间的区域。 可见光区与近紫外区基本上没有太大的差别, 只是光源不同,普通紫外区用氢灯,可见光区用钨丝灯。
紫外可见光吸收光谱仪的原理

紫外可见光吸收光谱仪的原理
紫外可见吸收光谱仪的原理主要是由于分子(或离子)吸收紫外或者可见光(通常在200-800纳米)后,发生价电子的跃迁,这种跃迁同时伴随着振动和转动能级间的跃迁,因此紫外可见光谱呈现宽谱带。
紫外可见吸收光谱的横坐标为波长(纳米),纵坐标为吸光度。
紫外可见吸收光谱有两个重要的特征:最大吸收峰位置(λmax)以及最大吸收峰的摩尔吸光系数(κmax)。
最大吸收峰所对应的波长代表着化合物在紫外可见光谱中的特征吸收,而其所对应的摩尔吸收系数是定量分析的依据。
紫外可见吸收光谱基本原理
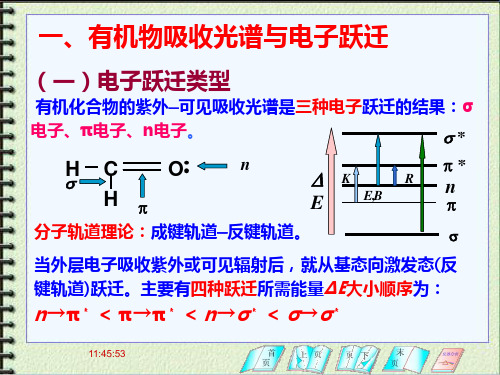
n→π* < π→π* < n→σ* < σ→σ*
11:51:47
2
σ→σ*跃迁
所需能量最大;σ电子只有吸收远紫外光的能量
才能发生跃迁;
饱和烷烃的分子吸收光谱出现在远紫外区; 吸收波长λ <200 nm; 例:甲烷的λ max为125nm , 乙烷λ max为135nm 。 只能被真空紫外分光光度计检测到; 作为溶剂使用;
max(甲醇) max(水) max(氯仿)
n → p*跃迁:蓝移; ;
max(正己烷)
p → p* n → p*
230 329
11:51:47
238 315
237 309
243 305
溶剂的影响
苯 酰 丙 酮 1 1:乙醚 2:水
2
250
300
极性溶剂使精细结构 消失;
11:51:47
11:51:47
11:51:47
精品课件!
11:51:47
精品课件!
11:51:47
(三) 金属离子影响下的配位体内π→π*跃迁 金属离子的微扰,将引起配位体吸收波长和 强度的变化。变化与成键性质有关,若共价 键和配位键结合,则变化非常明显。 茜素磺酸钠: 弱酸性介质:黄色(λ max=420nm) 弱碱性介质:紫红色(λ max=560nm )
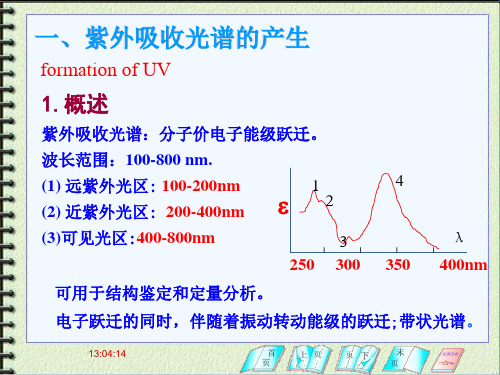
一、有机物吸收光谱与电子跃迁
(一)电子跃迁类型
有机化合物的紫外—可见吸收光谱是三种电子跃迁的结果: σ电子、π电子、n电子。 s*
E p 分子轨道理论:成键轨道—反键轨道。
s
H
C H
OnKR Nhomakorabeap*
E,B
n
p
s
当外层电子吸收紫外或可见辐射后,就从基态向激发态(反 键轨道)跃迁。主要有四种跃迁所需能量ΔΕ大小顺序为:
紫外光谱的基本原理

噻吩 231nm ( ε 7400)
精选可编辑ppt
29
2.5 空间结构对紫外光谱的影响
2.5.1 空间位阻的影响
直立键 λmax ﹥平伏键 λmax
精选可编辑ppt
30
2.5.2 顺反异构
双键或环上取代基在空间排列不同而形成的异构体。 反式 λmax ﹥ 顺式 λmax
精选可编辑ppt
31
2.5.3 跨环效应
精选可编辑ppt
10
2.2.2 烯、炔及其衍生物
非共轭 *跃迁, λmax位于190nm以下的远紫外区。
例如:乙烯 165nm(ε 15000),乙炔 173nm
C=C与杂原子O、N、S、Cl相连,由于杂原子的助色 效应, λmax红移。
小结:C=C,C≡C虽为生色团,但若不与强的
助色团N,S相连, *跃迁仍位于远
(2)220-250nm内显示强的吸收(近10000或更大),这 表明K带的存在,即存在共轭的两个不饱和键(共轭二烯 或、 不饱和醛、酮)
(3)250-290nm内显示中等强度吸收,且常显示不同程度 的精细结构,说明苯环或某些杂芳环的存在。
(4)250-350nm内显示中、低强度的吸收,说明羰基或共
9
同一碳原子上杂原子数目愈多, λmax愈向长波移动。
例如:CH3Cl 173nm,CH2Cl2 220nm, CHCl3237nm ,CCl4 257nm
小结:一般的饱和有机化合物在近紫外区无吸收, 不能将紫外吸收用于鉴定; 反之,它们在近紫外区对紫外线是透明的, 所以可用作紫外测定的良好溶剂。
精选可编辑ppt
3
2.1.3紫外光谱表示法
1.紫外吸收带的强度 吸收强度标志着相应电子能级跃迁的几率,
紫外吸收光谱基本原理
13:04:14
注:当出现几个发色团共轭,则几个发色团所产生的 吸收带将消失,代之出现新的共轭吸收带,其波 长将比单个发色团的吸收波长长,强度也增强
2) 助色团:本身无紫外吸收,但可以使生色团吸收 峰加强同时使吸收峰长移的基团
13:04:14
1) σ→σ*跃迁
所需能量最大;σ电子只有吸收远紫外光的能量才能发 生跃迁;
饱和烷烃的分子吸收光谱出现在远紫外区;
吸收波长λ<200 nm;
s*
例:甲烷的λmax为125nm ,
乙 烷λmax为135nm。 只能在真空环境被真空紫外
E K
R
E, B
p*
n
p
分光光度计检测到;
s
常作为溶剂使用
收强度发生变化:
λmax向长波方向移动称
为红移,向短波方向移动称 为蓝移 (或紫移)。如图所示
13:04:14
4) 增色效应和减色效应 吸收强度即摩尔吸光系数ε增大或减小 的现象分别称为: 增色效应(吸收强度增强的效应)或 减色效应(吸收强度减小的效应)。 如图所示:
5) 强带和弱带 εmax>105 → 强带 εmin<103 → 弱带
13:04:14
2.物质对光的选择性吸收及吸收曲线
M + h → M *
M +热
基态
激发态
M + 荧光或磷光
E1 (△E) E2
E = E2 - E1 = h 量子化 ;选择性吸收
吸收曲线与最大吸收波
紫外吸收光谱的基本原理

紫外吸收光谱的基本原理
紫外吸收光谱的基本原理是基于物质对紫外光的吸收特性。
当一束紫外光照射到被测物质上时,物质中的电子会吸收能量跃迁到高能级,形成激发态。
然后,电子会以辐射或非辐射的形式返回到基态,释放出吸收光的能量。
根据表达式A = log(I0/I),其中A是吸光度,I0是入射光的强度,I是透射光的强度,可以得知吸光度与溶液中物质的浓度
成正比。
因此,可以通过测量吸光度的变化来确定物质的浓度。
在紫外吸收光谱中,常用的检测器是光电二极管或光电倍增管。
这些检测器可以测量透射光的强度,并将其转换为电信号进行处理。
紫外吸收光谱通常在200-400纳米的波长范围内进行测量。
这
个范围对应着紫外光的波长,因为紫外光的能量较高,能够引起物质中电子的激发跃迁。
通过测量样品在不同波长下的吸光度,可以得到紫外吸收光谱图。
从光谱图中可以得知物质在不同波长下的吸收峰,进而可以确定物质的分子结构、浓度以及反应动力学等信息。
总之,紫外吸收光谱是一种常用的分析方法,它通过测量物质对紫外光的吸收特性来分析物质的成分和性质。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
紫外吸收光谱的基本原理,应用与其特点
紫外吸收光谱的基本原理
吸收光谱的产生
许多无色透明的有机化合物,虽不吸收可见光,但往往能吸收紫外光。
如果用一束具有连续波长的紫外光照射有机化合物,这时紫外光中某些波长的光辐射就可以被该化合物的分子所吸收,若将不同波长的吸收光度记录下来,就可获的该化合物的紫外吸收光谱.
紫外光谱的表示方法
通常以波长λ为横轴、吸光度A(百分透光率T%)为纵轴作图,就可获的该化合物的紫外吸收光谱图。
吸光度A,表示单色光通过某一样品时被吸收的程度A=log(I0/I1), I0入射光强度,I1透过光强度;
透光率也称透射率T,为透过光强度I1与入射光强度I0之比值,T= I1/I0透光率T与吸光度A的关系为A=log(1/T)
根据朗伯-比尔定律,吸光度A与溶液浓度c成正比A=εbc ε为摩尔吸光系数,它是浓度为1mol/L的溶液在1cm的吸收池中,在一定波长下测得的吸光度,它表示物质对光能的吸收强度,是各种物质在一定波长下的特征常数,因而是检定化合物的重要数据;c为物质的浓度,单位为mol/L;b为液层厚度,单位为cm。
在紫外吸收光谱中常以吸收带最大吸收处波长λmax和该波长下的摩尔吸收系数εmax来表征化合物吸收特征。
吸收光谱反映了物质分子对不同波长紫外光的吸收能力。
吸收带的许多无色透明的有机化合物,虽不吸收可见光,但往往能吸收紫外光。
如果用一束具有连续波长的紫外光照射有机化合物,这时紫外光中某些波长的光辐射就可以被该化合物的分子所吸收,若将不同波长的吸收光度记录下来,就可获的该化合物的紫外吸收光谱.
通常以波长λ为横轴、吸光度A(百分透光率T%)为纵轴作图,就可获的该化合物的紫外吸收光谱图。
吸光度A,表示单色光通过某一样品时被吸收的程度A=log(I0/I1), I0入射光强度,I1透过光强度;
透光率也称透射率T,为透过光强度I1与入射光强度I0之比值,T= I1/I0透光率T与吸光度A的关系为A=log(1/T)
根据朗伯-比尔定律,吸光度A与溶液浓度c成正比A=εbc ε为摩尔吸光系数,它是浓度为1mol/L的溶液在1cm的吸收池中,在一定波长下测得的吸光度,它表示物质对光能的吸收强度,是各种物质在一定波长下的特征常数,因而是检定化合物的重要数据;c为物质的浓度,单位为mol/L;b为液层厚度,单位为cm。
在紫外吸收光谱中常以吸收带最大吸收处波长λmax和该波长下的摩尔吸收系数εmax来表征化合物吸收特征。
吸收光谱反映了物质分子对不同波长紫外光的吸收能力。
吸收带的形状、λmax和εmax与吸光分子的结构有密切的关系。
各种有机化合形状、λmax 和εmax与吸光分子的结构有密切的关系。
各种有机化合物的λmax和εmax都有定值,同类化合物的εmax比较接近,处于一个范围。
紫外吸收光谱是由分子中价电子能级跃迁所产生的。
由于电子能级跃迁往往要引起分子中核的运动状态的变化,因此在电子跃迁的同时,总是伴随着分子的振动能级和转动能级的跃迁。
考虑跃迁前的基态分子并不是全是处于最低振动和转动能级,而是分布在若干不同的
振动和转动能级上;而且电子跃迁后的分子也不全处于激发态的最低振动和转动能级,而是可达到较高的振动和转动能级,因此电子能级跃迁所产生的吸收线由于附加上振动能级和转动能级的跃迁而变成宽的吸收带。
此外,进行紫外光谱测定时,大多数采用液体或溶液试样。
液体中较强的分子间作用力,或溶液中的溶剂化作用都导致振动、转动精细结构的消失。
但是在一定的条件下,如非极性溶剂的稀溶液或气体状态,仍可观察到紫外吸收光谱的振动及转动精细结构。
分子轨道基本原理
根据分子轨道理论,当2个原子形成化学键时,原子轨道将进行线性组合形成分子轨道。
分子轨道具有分子的整体性,它将2个原子作为整体联系在一起,形成的分子轨道数等于所组合的原子轨道数。
例如两个外层只有1个S电子的原子结合成分子时,两个原子轨道可以线性组合形成两个分子轨道,其中一个分子轨道的能量比相应的原子轨道能量低,称为成键分子轨道;另一个分子轨道的能量比相应的原子轨道能量高,称为反键分子轨道(反键轨道常用*标出)。
分子轨道中最常见的有σ轨道和π轨道两类。
σ轨道是原子外层的S轨道与S轨道、或Px轨道与Px轨道(沿χ轴靠近时)线性组合形成的分子轨道。
成键σ分子轨道的电子云分呈圆柱型对称,电子云密集于两原子核之间;而反键σ分子轨道的电子云在原子核之间的分布比较稀疏,处于成键σ轨道上的电子称为成键σ电子,处于反键σ轨道上的电子称为反键σ电子。
π轨道是原子最外层Py轨道或Pz轨道(沿χ轴靠近时)线性组合形成的分子轨道。
成键π分子轨道的电子云分不呈圆柱型对称,但有一对对称,在此平面上电子云密度等于零,而对称面的上下部空间则是电子云分布的主要区域。
反键π分子轨道的电子云也有一对称面,但2个原子的电子云互相分离,处于成键π轨道的电子称为成键π电子,处于反键π轨道的电子称为反键π电子。
含有氧、氮、硫等原子的有机化合物分子中,还存在未参与成键的电子对,常称为孤对电子。
孤对电子是非键电子,也称为n电子。
例如甲醇分子中的氧原子,其外层有6个电子,其中2个电子分别与碳原子和氢原子形成2个σ键其余4个电子并未参与成键,仍处于原子轨道上,称为n电子。
而n电子的原子轨道称为n轨道。
紫外吸收光谱的应用
1.定性分析
紫外吸收光谱在化合物定性鉴定方面的应用主要有以下几方面。
(1) 把样品光谱图与被测物质的标准光谱图进行比较,判别是否为同一化合物。
(2) 确定混合物中某一特定的组分是否存在或鉴定一个纯样品中是否含有其他杂质。
(3) 推断化合物的骨架结构。
(4) 判别顺反异构体、互变异构体.。
2.定量分析
与定性鉴定相比,紫外光谱法在定量分析领域有着更为重要和广泛的用途,其定量分析的依据是朗伯-比尔定律。
含芳环的化合物以及带有共轭双键的化合物在紫外可见区有较强吸收,并且吸光度与化合物的浓度成正比,因而可用来进行定量分析。
对于在紫外或可见区本身无吸收的化合物,可采用适当的化学反应,使其转化为在紫外或可见区有吸收的化合物进行测定。
紫外光谱分析对纯样品或含有其他不影响被测物分析的成分都有效,常用的分析测定方
法有工作曲线法、标准对照法等。
紫外吸收光谱的特点
1.灵敏度高
紫外一可见吸收光谱法是测量物质微量组分(1%~O.001%)的常用方法。
其测定下限可达10-6mol/L的痕量组分。
2.准确度高
可见吸收光谱法的相对误差一般为2%~5%,采用精密的分光光度计测量,其相对误差可低于l%。
用于常量组分的分析,紫外一可见吸收光谱法的准确性不及重量法和滴定分析法,但对于微量组分的分析,则完全可以满足要求。
3.适用范围
几乎所有的无机离子和许多有机物都可以直接或间接地采用紫外一可见吸收光谱法进行分析测定。
4.操作简便,快捷。
