电极电势与电池电动势的计算
化学反应中的电极电势与电池电动势实例

化学反应中的电极电势与电池电动势实例在化学反应中,电极电势和电池电动势是两个重要的概念。
电极电势指的是在电化学反应中,电极与溶液中某种溶质之间建立的电势差。
而电池电动势则是指整个电池中两个电极之间的电势差。
本文将结合实例介绍化学反应中的电极电势与电池电动势的概念与相关原理。
实例一:铜与铁电池在铜与铁电池中,铜离子是从铜电极溶解产生的,这个反应可以表示为:Cu(s) → Cu²⁺(aq) + 2e⁻而在铁电极上,则是铁离子发生还原反应:Fe²⁺(aq) + 2e⁻ → Fe(s)根据这两个半反应的标准电极电势可以计算出它们之间的电势差。
在标准状态下,铜电极的标准电极电势为+0.34V,而铁电极的标准电极电势为-0.44V。
所以,在这个铜与铁电池中,电池电动势可以计算为:Ecell = E(铜) - E(铁) = +(0.34V) - (-0.44V) = +0.78V这个正值表示铜与铁电池是一个可行的电池反应,并且产生正向的电势差。
这意味着当铜与铁电池连接成电路时,电子会从铁电极流向铜电极,而离子则会在溶液中迁移,从而产生电流。
实例二:锌与铜电池在锌与铜电池中,锌离子会溶解,并且金属锌会被氧化为锌离子,这个反应可以表示为:Zn(s) → Zn²⁺(aq) + 2e⁻与之相对应的是铜电极上的还原反应:Cu²⁺(aq) + 2e⁻ → Cu(s)通过比较这两个半反应的标准电极电势,可以计算出锌与铜电池的电动势。
在标准状态下,锌电极的标准电极电势为-0.76V,而铜电极的标准电极电势为+0.34V。
因此,锌与铜电池的电动势可以计算为:Ecell = E(锌) - E(铜) = (-0.76V) - (+0.34V) = -1.1V这个负值表示锌与铜电池是一个不可行的电池反应,不能产生正向的电势差。
因此,在锌与铜电池中,电子从铜电极流向锌电极,但离子却会在溶液中迁移,从而产生反向的电流。
电极势与电池电动势之间的关系

电极势与电池电动势之间的关系电极势是指在电池中两个电极上的电势差,即正极与负极之间的电位差。
而电池电动势则是指电池在无负载情况下产生的电压。
电极势和电池电动势之间存在着密切的关系。
首先,我们来了解一下电极势。
电极势是由电池内部的化学反应引起的,在电池内完成氧化还原反应的正极和负极上会形成电势差。
对于一般的电池,正极电势相对于负极电势更高,从而形成了电势差。
这个差值正好等于电池电动势。
电池电动势是指在没有负载时,电池正负极之间产生的电压。
正常情况下,正极的势高于负极,形成了一个电势差。
这种电势差是电池内部化学反应所产生的,能够推动电荷在电池中自由流动,从而产生电流。
电池电动势通常以伏特(V)为单位。
电极势和电池电动势之间的关系可以用下式来表示:电池电动势 = 正极电势 - 负极电势根据这个关系,我们可以看出电池电动势的大小取决于正极和负极电势的差值。
如果正极电势和负极电势之间的差值越大,那么电池电动势就会越大。
相反,如果差值较小,电池电动势也会相应地减小。
正常情况下,电池的电动势是一个恒定的值。
然而,在实际应用中,电池的电动势往往会随着使用时间的增加而降低。
这是因为电池内部的化学反应会导致电极材料的消耗和损耗,从而使得正极和负极之间的电势差减小。
最后,还需要注意的是,电极势和电池电动势是两个不同的概念。
电极势是针对单个电极来讨论的,而电池电动势是针对整个电池来讨论的。
在一个完整的电池中,正极和负极之间形成的电势差就是电池电动势。
总结起来,电极势和电池电动势之间有着密切的关系。
电池电动势是由正极和负极之间的电势差引起的,而这个差值可以被称为电极势。
电极势和电池电动势的大小取决于正极和负极之间的电势差。
通过研究和了解这个关系,我们能够更好地理解电池的工作原理,并有效地应用于各种电子设备和能源系统中。
化学反应中的电极电势与电池电动势

化学反应中的电极电势与电池电动势化学反应是一种涉及原子和分子之间重组的过程,而电池则是利用化学反应产生电能的装置。
电极电势和电池电动势是描述电化学反应中电子转移能力的重要参数。
本文将介绍电极电势和电池电动势的概念、影响因素以及它们之间的关系。
一、电极电势的概念与测量电极电势是指电极与溶液或气体之间的电势差。
在电化学反应中,电极上电子的转移产生电势差,进而影响反应的进行。
电极电势能够反映电子在电极上的活动程度,是判断电极是氧化还是还原的参数。
电极电势通常用标准电极电势(E°)来表示,单位为伏特(V)。
测量电极电势的方法有很多种,其中最常用的方法是通过比较电池。
比较电池由两个半电池组成,可以产生一个已知电势差的电池。
通过将待测电极与比较电池相连,测量它们之间的电势差,从而确定待测电极的电势差。
二、电极电势的影响因素1. 温度:电极电势随温度的变化而变化。
温度升高会导致电极电势升高或降低,具体取决于反应的热力学性质。
2. 浓度:电极电势与参与反应的物质浓度有关。
当参与反应的物质浓度发生改变时,电极电势也会发生变化。
3. 压力:对于气体电极,电极电势随气体的分压变化而变化。
增大气体分压会导致电极电势升高。
4. pH 值:对于溶液电极,电极电势会受到 pH 值的影响。
改变溶液pH 值能够改变电极电势。
三、电池电动势的概念与计算电池电动势是指电池两个电极之间的电势差,表征了电化学反应产生的电能。
电池电动势通常用电池电动势(Ecell)来表示,单位为伏特(V)。
计算电池电动势的方法是通过测量两个电极的电极电势,并利用Nernst 方程进行计算。
Nernst 方程是描述电极电势与反应物浓度之间关系的数学方程。
Ecell = E°cell - (RT/nF)ln(Q)其中,E°cell 是标准电动势,R 是气体常数,T 是温度,n 是电子转移的摩尔数,F 是法拉第常数,Q 是反应物的活度积。
电池电动势与电极电势

4)电极的类型及符号
四种电极
(1)金属-金属离子电极 如: Zn2+/Zn, Cu2+/Cu 等
电极符号: Zn|Zn2+ (c)
Cu|Cu2+ (c)
(2)气体-离子电极 如: H+/H2 Cl2/Cl需用一个惰性固体导体如铂(Pt)和石墨。
Pt,H2(p)|H+(c) Pt,Cl2(p)|Cl-(c) Pt与H2之间用逗号隔开,p 为气体的压力。 (3)离子电极 如 Fe3+/Fe2+ 等体系
将惰性电极插入到同一种元素不同氧化态的两种离子的溶液中 所组成的电极。
Pt|Fe2+(c1), Fe3+(c2)
(4)金属-金属难溶盐电极 如 Hg2Cl2/Hg 由金属及其难溶盐浸在含有难溶盐负离子溶液中组成的电极。 如甘汞电极: Hg2Cl2 + 2e = 2 Hg + 2 Cl- Pt,Hg,Hg2Cl2(s)|Cl-(c)
Cl2
Cl- +
ClO2e
OH- Cl-
改正: 碱性介质中(容易进行,实际上常用的方法):
2 Cr(OH)3 + 3Cl2 + 10 OH- = 2CrO42- + 6Cl- + 8 H2O
酸性介质中( Cl2的氧化性大于Cr2O72- 的,但差别较小): 2 Cr3+ + 3Cl2 + 7 H2O = Cr2O72- + 6Cl- + 14 H+
氧化态、还原态的共轭关系
2 氧化数与电子转移
Fe + Cu2+ = Fe2+ + Cu H2 + 0.5 O2 H 2 O
电动势和电极电势的关系

电动势和电极电势的关系引言:在电学领域中,电动势和电极电势是两个重要的概念。
电动势是指电源推动单位正电荷沿闭合回路移动所做的功,而电极电势则是指电池两极之间的电位差。
本文将探讨电动势和电极电势之间的关系,并介绍它们在电路中的应用。
一、电动势的定义和特点电动势是电源内能量转化为电能的能力,通常用字母E表示。
电动势的单位是伏特(V),它的大小与电池内部化学反应的能量转化有关。
电动势可以通过以下公式计算:E = W / q其中,E代表电动势,W代表电源对电荷做的功,q代表单位正电荷。
二、电极电势的定义和特点电极电势是指电池两极之间的电位差,通常用字母V表示。
电极电势是电荷在电路中移动时,由于电场力做功而使电位能发生变化的结果。
电极电势的大小与电池内部电化学反应有关,它可以通过以下公式计算:V = W / q其中,V代表电极电势,W代表电场力对电荷做的功,q代表单位正电荷。
三、电动势与电极电势的关系电动势和电极电势之间存在着密切的关系。
在理想情况下,电动势等于电极电势之和。
也就是说,电动势E等于正极电势V+和负极电势V-之差。
这个关系可以用以下公式表示:E = V+ - V-这个公式表明了电动势和电极电势之间的直接联系。
电动势可以看作是电池内部化学反应的驱动力,而电极电势则是电池两极之间的电压差。
四、电动势和电极电势在电路中的应用电动势和电极电势在电路中起着至关重要的作用。
电动势可以决定电流的大小和方向,它是电路中电流的驱动力。
电极电势则决定了电路中各个元件之间的电压差,它是电路中电压的来源。
在闭合电路中,电动势源通过电极电势差推动电荷的流动,从而产生电流。
而在开路电路中,电动势和电极电势之间的差别会导致电场力的存在,这个力使电荷在电路中产生电场,但不会导致电流的流动。
电动势和电极电势还可以用于判断电池的正负极。
根据电动势的定义,正极电势大于负极电势时,电流从正极流向负极;反之,电流从负极流向正极。
这个规律被广泛应用于电路设计和电池的连接。
第9节 由电极电势计算电池电动势

三、单液浓差电池
Pt | Cl 2 ( p1 ) | HCl(aq) | Cl 2 ( p2 ) | Pt
2Cl-(a-) →Cl2(p1)+2e-
Cl2(p2)+2e- →2Cl-(a-) Cl2(p2)→ Cl2(p1)
四、双液浓差电池
Ag|AgCl(s)|Cl- (a1 )||Cl- (a2 )|AgCl(s)|Ag
§7.9
由电极电势计算电池电动势
一、单液化学电池
Pt,H2(p1) | H+(a+)|O2(p2),Pt 2H2(p1) - 4e- → 4H+(a+) O2(p2) + 4H+(a+) + 4e- → 2H2O 2H2(p1) + O2(p2) → 2H2O
二、双液化学电池 Pt,H2(p1) | H+(a+) OH-(a-)|O2(p2),Pt 2H2(p1) - 4e- → 4H+(a+) O2(p2)+2H2O+4e- →4OH-(a-) 2H2(p1) + O2(p2) → 4H+(a+) +4OH-(a-) -2H2O
θ
三、求化学反应的平衡常数
AgCl Ag Cl
设计一个电池:
Ag(s) Ag (aq) Cl (aq) AgCl(s) Ag(s)
Ag(s) →Ag (a+)+ e-
AgCl(s)+e- →Ag(s)+Cl-(a2)
AgCl Ag Cl
四、求离子平均活度系数
(Pt)H 2 (p θ ) HCl( m) AgCl(s) Ag(s)
电池电动势与电极电势

电极电势的计算方法
Nernst方程
电极电势可以通过Nernst方程计算,该方程描述了电极电势与溶液中离子浓度 的关系。
线性关系
电极电势与反应物和产物的浓度之间存在线性关系,可以利用这一关系求出电 极电势。
影响电极电势的因素
物质性质
电极电势与参与反应的物质性质有关,如氧化还原能力、离子迁 移率等。
温度
温度对电极电势产生影响,温度升高会导致电极电势降低。
物质浓度
参与反应的物质浓度也会影响电极电势,浓度变化会导致电极电 势相应发生变化。
03 电池电动势与电极电势的 关系
电动势与电极电势的差异
定义不同
电池电动势是指电池在开路状态 下正负极之间的电位差,而电极 电势是指电极与其周围溶液之间
的电位差。
决定电池性能
电池电动势和电极电势共同决定了电池的性能,如能量密度、功率 密度、充放电效率等。
平衡状态
在一定条件下,电池电动势和电极电势可以达到平衡状态,此时电 池性能达到最优。
电动势与电极电势在实际应用中的重要性
1 2
能源存储
电池电动势和电极电势是决定电池能量存储和释 放的关键因素,对于电动汽车、移动设备等领域 具有重要意义。
电池电动势与电极电势
目录
• 电池电动势 • 电极电势 • 电池电动势与电极电势的关系 • 电化学反应与电极过程 • 电池性能的优化与改进
01 电池电动势
定义与性质
定义
电池电动势是指在标准温度和压 力下,电池正负极之间的电势差 。
性质
电池电动势是衡量电池能量转换 效率的重要参数,具有方向性, 即电流从正极流向负极。
电极反应的可逆性
可逆电极反应在正向和逆向反应中均能进行, 且正向和逆向反应速率相等。
无机化学-电池电动势和电极电势
标准甘汞电极(NCE) 1.0 mol / L +0.2828
饱和甘汞电极(SCE) 饱和溶液 +0.2438
温度校正,对于SCE,t ℃时的电极电势为:
t= 0.2438- 7.6×10-4(t-25) (V)
电池符号: (-) Hg,Hg2Cl2(s)︱KCl (1 mol·dm-3) Mn+ (1 mol·dm-3 ) M (+)
氧化半反应: H2 - 2e = 2H+ 还原半反应: Cl2 + 2 e = 2Cl– 总反应: H2 + Cl2 = 2H+ + 2Cl–
2. 题中给出总反应方程式,要能够写出电池符号和半反应
例题:试以中和反应 H+ (aq) + OH–(aq) = H2O(l)为电池反应, 设计成一种原电池反应(用电池符号表示),分别写出电极半 反应,并求出它在25℃时的标准电动势。
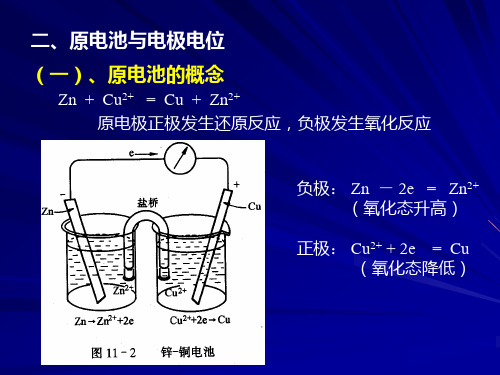
二、原电池与电极电位 (一)、原电池的概念
Zn + Cu2+ = Cu + Zn2+ 原电极正极发生还原反应,负极发生氧化反应
负极: Zn - 2e = Zn2+ (氧化态升高)
正极: Cu2+ + 2e = Cu (氧化态降低)
盐桥(Salt bridge)
通常内盛饱和 KCl 溶液或 NH4NO3 溶液(以琼胶 作成冻胶)。
作用: ● 让溶液始终保持电中性 ,使电极反应得以继续进行 ● 消除原电池中的液接电势(或扩散电势)
(二)、原电池的表达式
(-) Zn|Zn2+ (C1) ‖ Cu2+ (C2)|Cu (+)
1、负极写在左边,正极写在右边 2、用∣表示电极与离子溶液之间的物相界面 3、不存在相界面,用,分开。 4、用表示盐桥 5、在有气体参加的电池中还要表明气的压力,溶液要表 明浓度。
