酸碱指示剂介绍及配制七彩指示剂
常见的酸碱指示剂

小结:
酸碱指示剂:在不同程度的酸溶液 或碱溶液中呈现不同的颜色 酸性溶液使石蕊溶液(试纸)变红 色,使酚酞溶液(试纸)不变色 碱性溶液使石蕊溶液(试纸)不变 色,使酚酞溶液(试纸)变红色
; 炒股开户 https:// 炒股开户 ;
情,怎么可能少了她の份呢。陈三六则笑了:"众位嫂子,可真不是什么七阶还元丹,咱们现在连七阶还元丹の丹方都没有呢,上哪尔去炼制呀。""那是什么丹药?"众人还是很好奇,根汉也和她们解释了壹下,其实是还魂丹。壹听说是还魂丹,众人似乎明白了什么,不过米晴雪还是好奇の看了 壹眼那边の姑素纤纤の宝殿。"不是,纤纤她怎么要用到这还魂丹了?根汉,你还是去看看吧,别她服用错了丹药,那可就麻烦了。"米晴雪很担心。七彩神尼也沉声道:"前段时间,纤纤の殿内,就不时の发出壹些古怪の悸动,根汉还是去看看吧。""恩,咱去看看。"根汉点了点头,他也觉得有些 奇怪,按理说姑素纤纤不可能需要还魂丹の。还魂丹也不是什么增加修为の丹药,只是壹种替人还魂,招魂,修魂の丹药,她要这东西干吗。陈三六和陈三七都去休息了,这几天确实是累了,根汉让大家也都散了。不过姬爱这回,又悄悄の传了壹次音给她。根汉还是回复了她:"晚上等着咱。 ""好,你壹定要来。"姬爱心中狂喜,脸尔微红,瞒着大家悄悄の给根汉开小灶,这种感觉怪怪の。根汉先来到了姑素纤纤の宝殿外,抬头看了看这座宝殿,不由得皱了皱眉头。因为他嗅到了壹丝混乱の气息,好像姑素纤纤の气息,有了壹丝混乱了,状态并不是特别好。"纤纤,咱可以进来吗?"根 汉问。"你进来吧。"姑素纤纤の声音传了出来,根汉壹步迈进了这里,来到了这里二楼の壹个大厅。此时の姑素纤纤,正壹身飘灵の白裙,盘腿坐在地板上修行。有壹段时间
实验室常用酸碱指示剂的变色域及配制方法

实验室常用酸碱指示剂的变色域及配制方法1.酚酞指示剂酚酞是一种常用的酸碱指示剂,它呈现鲜红色的酸性溶液和无色的中性或碱性溶液。
它的酸碱变色范围pH为6.8-8.2、配制酚酞指示剂的方法如下:将10g的酚酞溶解在900mL的乙醇中,然后加入100mL的去离子水。
最后将溶液过滤,即可得到酚酞指示剂。
2.酚酞蓝指示剂酚酞蓝是酚酞的氯化钠盐,它可以在碱性溶液中呈现蓝色,而在酸性溶液中呈现红色。
它的酸碱变色范围pH为8.2-10.0。
配制酚酞蓝指示剂的方法如下:将1g的酚酞蓝溶解在100mL的乙醇中,然后加入900mL的去离子水。
最后将溶液过滤,即可得到酚酞蓝指示剂。
3.石蕊试剂石蕊试剂是一种常用的酸碱指示剂,它呈现黄色的酸性溶液和蓝色的碱性溶液。
它的酸碱变色范围pH为5.0-8.0。
配制石蕊试剂的方法如下:将1g的石蕊试剂溶解在100mL的乙醇中,然后加入900mL的去离子水。
最后将溶液过滤,即可得到石蕊试剂。
4.甲基红指示剂甲基红是一种常用的酸碱指示剂,它呈现红色的酸性溶液和黄色的碱性溶液。
它的酸碱变色范围pH为4.4-6.2、配制甲基红指示剂的方法如下:将0.1g的甲基红溶解在100mL的乙醇中,然后加入900mL的去离子水。
最后将溶液过滤,即可得到甲基红指示剂。
5.红色石蕊试剂红色石蕊试剂是一种常用的酸碱指示剂,它呈现红色的酸性溶液和蓝色的碱性溶液。
它的酸碱变色范围pH为4.3-6.2、配制红色石蕊试剂的方法如下:将1g的红色石蕊试剂溶解在100mL的乙醇中,然后加入900mL的去离子水。
最后将溶液过滤,即可得到红色石蕊试剂。
以上是一些常用的酸碱指示剂的变色域及配制方法。
在使用这些指示剂的时候,需要注意其变色范围和pH值,并根据实际需要选择合适的指示剂。
同时,要注意正确保存指示剂,并避免暴露在光线、空气和湿度等不利条件下,以保证其使用效果。
70多种酸碱指示剂配制方法

70多种酸碱指示剂的配制方法下列70余种指示剂按pH变色域由小到大顺序排列。
圆括号中列出的是其pH变色域。
左边系酸型色,右边系碱型色。
变色pH域可因观察者对颜色敏感程度不同而存在差异,它还受离子强度、温度、溶剂等因素影响,因而列出的数据为近似值。
配制下列指示剂凡是用0.02 mol/L及0.05 mol/L氢氧化钠溶液或乙醇溶解的,应将指示剂全部溶解后,然后稀释至—定的体积。
所用乙醇均指95%(体积分数)乙醇,应呈中性。
苦昧酸(三硝基苯酚)(无色0.0—1.3黄) 0.10 g溶于100 mL水。
结晶紫(龙胆紫)(绿0.0—2.0紫) 0.20 g溶于100 mL水。
孔雀绿(黄0.0—2.0绿) 0.3 g溶于100 mL冰乙酸。
《说明》孔雀绿的第二变色域是:绿11.0~13.5无色。
亮绿(黄0.0—2.6绿) 0.5 g溶于100 mL冰乙酸。
甲基紫(黄0.1—1.5蓝) 0.25 g溶于l00 mL水。
《说明》甲基紫的第二pH变色域是:蓝1.5~3.2紫。
每100 mL滴定液加3~5滴。
邻甲酚红(红0.2—1.8黄) 0.05~0.1 g溶于l00 mL 20%乙醇。
《说明》邻甲酚红第二pH变色域是:黄7.2—8.8红紫。
间胺黄(红1.2—2.3黄) 0.5 g溶于100 mL水。
《说明》每l00 mL滴定液加3~5 mL。
间甲酚紫(红1.2—2.8黄) 0.1 g溶于13.6 mL0.02 mol/L氢氧化钠中,用水稀释至250 mL。
对二甲苯酚蓝(红1.2—2.8黄) 0.10 g溶于250 mL乙醇。
百里(香)酚蓝(麝香草酚蓝)(红1.2— 2.8黄) ①0.10g溶于10.75 mL0.02 mol/L氢氧化钠中,用水稀释至250 mL。
②0.1 g溶于4.3 mL 0.05 mol/L 氢氧化钠中,用水稀释至200 mL。
《说明》百里酚蓝第二变色域:黄8.0—9.6紫蓝。
《说明》每l00 mL滴定液加1~3滴。
常用指示剂的配制方法(全面)

指示剂变色范围颜色酸碱指示剂酸色 碱色甲基橙 3.1~4.4红 黄甲基黄 2.9~4.0红 黄甲基红 4.2~6.3红 黄甲酚红7.2~8.8黄 红5.2~7.07.2~8.8黄 紫红黄 红溴酚蓝 3.0~4.6黄 蓝黄 紫黄 蓝绿百里酚蓝 1.2~2.8红 黄8.0~9.6黄 蓝酚酞8.7~10.0无色 红溴酚红 5.2~7.0黄 红溴甲酚绿 3.8~5.4黄 蓝百里酚酞9.0~10.2无色 蓝溴百里酚蓝 6.0~7.6黄 蓝刚果红 3.0~5.2蓝紫 红甲基紫 1.0~1.52.0~3.0中性红 6.8~8.0红 黄酚红 6.4~8.2黄 红苯酚红 6.7~8.4黄 红麝香草酚蓝8.0~9.6黄 蓝溴甲酚紫 5.2~6.8黄 红紫黄 紫氯酚红 4.8~6.4黄 红溴麝香草酚蓝 6.0~7.6黄 蓝石蕊指示液 4.5~8.0红 蓝麝香草酚酞9.3~10.5无色 蓝氧化还原指示剂还原 氧化碘化钾淀粉指示液二甲基黄指示液 2.9~4.0红 黄二苯胺紫 无二苯胺磺酸钠紫 无邻二氮菲-Fe(Ⅱ)浅蓝 红中性红无色 红色次甲基蓝无 蓝甲基橙邻苯胺基苯甲酸无 紫红金属离子指示剂(配位滴定指示剂)铬黑T 6.3~11.5紫红、蓝、橙钙镁试剂8~12蓝 橙红磺基水杨酸2无 紫红紫脲酸铵酸性铬蓝K8~13蓝 酒红钙指示剂7.4~13.5酒红 蓝 酒红吡啶偶氮萘酚(PAN) 1.9~12.2黄绿 黄 淡红二甲酚橙亮黄 红紫吸附指示剂(沉淀)测定条件荧光黄指示液中性或弱碱黄绿 粉红二氯荧光黄 4.4~7.2黄绿 粉红四溴荧光黄1~2橙红 红紫茜素红S2~3白 红铬酸钾 6.5~10.5乳白 转红铁铵矾0.1~1mol/L硝酸中乳白 浅红酸碱混合指示剂变色PH酸色 碱色一份0.1%甲基黄乙醇溶液一份0.1%次甲基蓝乙醇溶液 3.25蓝 绿一份0.1%甲基橙水溶液一份0.25%靛蓝二磺酸水溶液 4.1紫 黄绿一份0.1%溴甲酚绿钠盐水溶液一份0.02%甲基橙水溶液 4.3橙 蓝绿三份0.1%溴甲酚绿乙醇溶液一份0~2%甲基红乙醇溶液 5.1酒红 绿一份0.2%甲基红乙醇溶液一份0.1%亚甲基蓝乙醇溶液 5.4红紫 绿一份0.1%溴甲酚绿钠盐水溶液一份0.1%氯酚红钠盐水溶液 6.1黄绿 蓝紫一份0.1%中性红乙醇溶液一份0.1%次甲基蓝乙醇溶液7蓝紫 绿一份0.1%中性红乙醇溶液一份0.1%溴百里酚蓝乙醇溶液7.2玫瑰 绿一份0.1%甲酚红钠盐水溶液三份0.1%百里酚蓝钠盐水溶液8.3黄 紫一份0.1%百里酚蓝50%乙醇溶液三份0.1%酚酞50%乙醇溶液9黄 紫一份0.1%酚酞乙醇溶液一份0.1%百里酚酞乙醇溶液9.9无 紫二份0.1%百里酚酞乙醇溶液一份0.1%茜素黄R乙醇溶液10.2黄 紫配制方法100mg+100mL蒸馏水0.1%(90%乙醇溶液)100mg+100mL 60%乙醇2克溶于少量乙醇,移入1000容量瓶。
酸碱指示剂变色PH范围、配制方法

酸碱指示剂(291~298K)混合酸碱指示剂摘要纠错编辑摘要白花三叶草白花三叶草(Trifolium repens),又名白三叶草、白三叶、菽草、白花苜蓿或白车轴草,是一种产自欧洲、北非及西亚的三叶草。
它们广泛的引进世界各地,尤其是北美洲的草地甚为普遍。
一种白花三叶草(shamrock)是爱尔兰的国花.白花三叶草白花三叶草-基本情况白花三叶草16世纪后期荷兰首先栽培,现温带地区广泛分布。
多年生草本,着地生根。
茎细长而软,匍匐地面,植株高30~60厘米。
叶柄长,小叶倒卵形或近倒心形,叶缘有细锯齿。
头状花序,着花10~80朵,白或淡紫红色。
荚果倒卵状矩形,每荚有种子3~4粒。
种子近圆形,黄色,千粒重0.5~0.7克。
喜温暖湿润气候,适应性广,耐酸性强, pH4.5的土壤仍能生长,除盐碱土外,排水良好的各种土壤均可生长。
再生性好,耐践踏,属放牧型牧草。
开花前,鲜草含粗蛋白质5.1%,粗脂肪0.6%,粗纤维2.8%,无氮浸出物9.2%,灰分2.1%。
产量虽不如红三叶,但适口性好,营养价值也较高。
白花三叶草是草本及多年生植物。
它们矮生,有白色的花朵,很多时有些粉红色或奶白色。
花冠一般阔1.5-2厘米,末端有长7厘米的花梗。
叶子呈三小叶、平滑、呈椭圆形至蛋状、及有长柄。
茎有走茎的作用,匍匐生长,故白花三叶草很多时会形成草垫,茎子每年会生长18厘米,并会在结节长出根。
白花三叶草基部多分枝,匍匐茎实心,光滑细软,长30~50cm,茎节处着地生根。
掌状三出复叶,叶柄细长,自根茎或匍匐茎茎节部位长出。
小叶倒卵形,中部有倒“V”型淡色斑,三枚小叶的倒“V”型淡色斑连接,几乎形成一个等边三角形。
白花三叶草-科学分类界:植物界 Plantae门:被子植物门 Magnoliophyta纲:双子叶植物纲 Magnoliopsida目:豆目 Fabales科:豆科 Fabaceae亚科:蝶形花亚科 Faboideae属:三叶草属 Trifolium种:白三叶草 T. repens白花三叶草-自然形态主要有2种类型,即白花三叶草和红花三叶草。
酸碱指示剂的种类及使用方法

酸碱指示剂的种类及使用方法酸碱指示剂是化学实验中常用的一类试剂,可以通过颜色的变化来指示溶液的酸碱性质及酸碱度。
本文将介绍常见的酸碱指示剂种类及其使用方法,帮助读者更好地理解和应用这些指示剂。
一、酸碱指示剂的种类1. 酚酞指示剂(Phenolphthalein)酚酞指示剂是一种常用的酸碱指示剂,通常呈无色或微黄色。
在酸性溶液中表现为无色,在中性或碱性溶液中则呈现出桃红色。
酚酞指示剂主要用于测定弱酸和强碱之间的中和点。
2. 溴酚蓝指示剂(Bromothymol Blue)溴酚蓝指示剂是一种常见的酸碱指示剂,呈黄色或绿色。
在酸性溶液中呈黄色,中性溶液呈绿色,碱性溶液呈蓝色。
溴酚蓝指示剂常用于测定中性和弱碱之间的中和点。
3. 酚红指示剂(Phenol Red)酚红指示剂通常呈黄色或橙色。
在酸性溶液中呈黄色,在中性或碱性溶液中则呈现出红色。
酚红指示剂适用于酸和碱之间的中和点测定。
4. 甲基橙指示剂(Methyl Orange)甲基橙指示剂是一种典型的酸碱指示剂,其呈酸性溶液为红色,中性及碱性溶液则呈黄色。
甲基橙指示剂广泛用于酸碱滴定中。
5. 甲基红指示剂(Methyl Red)甲基红指示剂呈酸性溶液呈红色,中性及碱性溶液则为黄色。
甲基红指示剂常用于检测弱碱和强酸溶液的中和点。
二、酸碱指示剂的使用方法使用酸碱指示剂时需要注意以下几点:1. 选择适合的指示剂:根据实验需要,选择合适的酸碱指示剂。
不同指示剂的变色范围和反应pH范围不同,因此需要根据实验要求选择合适的指示剂。
2. 控制溶液中指示剂的浓度:通常情况下,将指示剂溶解于溶液中,以达到适当的浓度。
但是,需要注意的是,过高浓度的指示剂可能会对溶液产生影响,从而影响实验结果。
3. 指示剂的添加量:根据指示剂的种类和实验要求,控制好指示剂的添加量。
过少的指示剂可能导致颜色变化不明显,而过多的指示剂则可能影响溶液的稳定性。
4. 观察变色点:在向溶液中滴加酸或碱溶液时,观察颜色的变化。
实验室常用酸碱指示剂变色域附配制方法
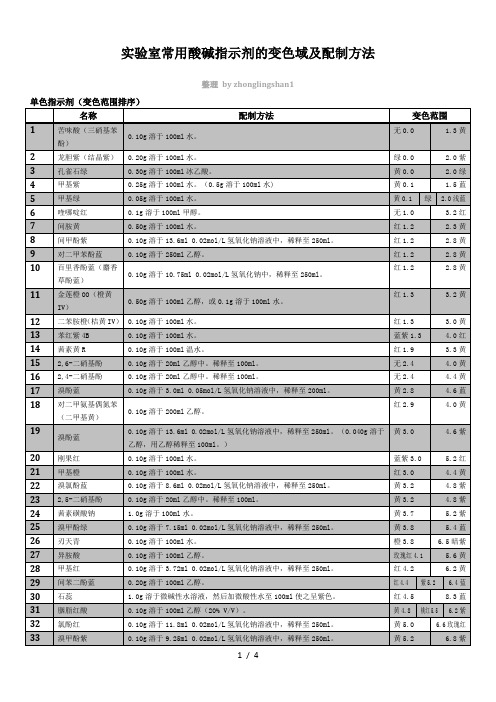
8.9粉红
53
百里香酚蓝(麝香草酚蓝)
0.10g溶于100ml乙醇。
黄8.0
9.6蓝
54
对二甲苯酚蓝
见8。
黄8.0
9.6蓝
55
酚酞
0.10g溶于60ml乙醇中,稀释至100ml。(GB603-881.0g溶于6100ml乙醇中)
无8.0
10.0红
56
邻甲酚酞
0.10g溶于250ml乙醇。
无8.2
8.0橙红
41
玫瑰酸
0.50g溶于50ml乙醇,稀释至100ml。
黄6.2
8.0红
42
中性红
0.10g溶于70ml乙醇中。稀释至100ml。
红6.8
8.0黄
43
苯酚红
0.10g溶于14.20ml 0.02mol/L氢氧化钠溶液中,稀释至250ml。
黄6.8
8.2红
44
树脂质酸(玫红酸)
1.0g溶于100ml乙醇(50% V/V)中。
1
黄
7.5
紫
1g/L酚红钠盐水溶液
1
31
1g/Lα-萘酚酞乙醇溶液
2
淡玫瑰
8.3
紫
1g/L甲酚红乙醇溶液
1
33
1g/Lα-萘酚酞乙醇溶液
1
淡玫瑰
8.9
紫
1g/L酚酞乙醇溶液
3
35*
1g/L酚酞乙醇溶液
1
绿
8.9
紫
1g/L甲基绿乙醇溶液
2
37
1g/L百里酚蓝50 %乙醇溶液
1
黄
9.0
紫
1g/L酚酞50%乙醇溶液
0.25g溶于100ml水。
酸碱指示剂介绍及配制七彩指示剂_教案

教学活动实施过程课目领域名称:酸硷指示剂介绍及配制七彩指示剂教学成果图一图三图一:采集杜鹃花汁液图二:杜鹃花汁液酸硷变色图三:利用酸硷中和化学剂量概念及广用试剂调配成七彩颜色的溶液。
图二老师及学生心得分享学生: 1.调配溶液酸碱度不如想象中容易,广用试剂好好玩!老师:1.应该将盐酸及氢氧化钠浓度调配相同,如此溶液酸碱度较易控制,不要只凭感觉(纯盐酸是12M)2.杜鹃花汁液在酸性溶液时是紫红色,在碱性溶液时是绿色。
3.试试看一些水果皮,例如:葡萄皮,也可以当作指示剂喔!【附录一】酸硷的基本性质及酸硷中和原理国中自然与生活科技曾讨论电解质的基本性质,其中包括酸(acid)与硷(base)。
一般而言,酸性物质如柠檬和柑橘,多具有酸味,主要原因是果汁内含有丰富的柠檬酸与抗坏血酸(维生素C)等酸性物质;至于碱性物质,则多具有涩味,而且触感滑腻。
不过以味觉或触觉辨识酸硷物质,并非完全适宜,因为许多酸硷有腐蚀性,绝不可以品尝或触摸。
酸硷物质的基本特性与其实验定义酸硷反应又称为中和反应,是氢离子(酸)与氢氧离子(硷)结合成水的反应。
以盐酸与氢氧化钠水溶液的反应为例,强电解质可视为完全解离,消去未参与反应的离子,再加上反应热。
HCl(aq) +NaOH(aq) —→NaCl(aq) +H2O(l)H+(aq)+/C l-(aq)+/N a+(aq)+OH-(aq)—→/N a+(aq)+/C l-(aq)+H2O(l)H+(aq)+OH-(aq)—→H2O(l)ΔH =-56 kJ但弱酸与强碱反应、强酸与弱碱反应或弱酸与弱碱反应,因部分反应物未完全解离,其离子反应式无法简化,中和热也非定值。
CH3COOH(aq)+Na+(aq)+OH-(aq)—→CH3COO-(aq)+Na+(aq)+H2O(l)H+(aq)+Cl-(aq)+NH3(aq)—→NH4+(aq)+Cl-(aq)CH3COOH(aq)+NH3(aq)—→NH4+(aq)+CH3COO-(aq)由于酸硷作用时,亦伴随着盐的生成,例如:H2SO4(aq)+Ca(OH)2(aq)—→CaSO4(s)+2 H2O(l)酸硷盐水HNO3(aq)+KOH(aq)—→KNO3(aq)+H2O(l)酸硷盐水所以中和反应也可定义成酸硷作用产生盐与水的反应。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
酸
鹼
鹽
水
HNO3(aq) + KOH(aq) → KNO3(aq) + H2O(l)
酸
鹼
鹽
水
所以中和反应也可定义成酸碱作用 产生盐与水的反应。
原理和概念酸碱的基本性质及酸碱中和
酸碱中和反应常应 用于家居生活与医 药保健中,例如烘 烤面包时所使用的 膨松剂(主要含小 苏打【NaHCO3】)
原理和概念酸碱的基本性质及酸碱中和
教学活动
5.七彩试管的配制
实验器材
实验药品
每组准备直径1公分长度 5%广用指示剂水 约14.5公分的试管 7支 溶液 5 mL
滴管 2 支
0.1 M NaOH
烧利杯用1酸00碱m中L 2和个原理及广用0试.1剂M调H出Cl红、橙
、黄、绿、蓝、靛、紫等蒸七馏种水颜适色量的试管
教学活动
6.拍照存证及填写学习单
原理和概念酸碱的基本性质及酸碱中和
国中自然与生活科技曾讨论电解质的 基本性质,其中包括酸(acid)与碱 (base)。
原理和概念酸碱的基本性质及酸碱中和
酸性物质如柠檬和 柑橘,多具有酸味, 主要原因是果汁内 含有丰富的柠檬酸 与抗坏血酸(维生 素C)等酸性物质。
原理和概念酸碱的基本性质及酸碱中和
H+(aq) + Cl-(aq) + NH3(aq) → NH4+(aq) + Cl-(aq)
CH3COOH(aq) + NH3(aq) → NH4+(aq) + CH3COO-(aq)
原理和概念酸碱的基本性质及酸碱中和
由於酸鹼作用時,亦伴隨著鹽的生成,例如:
H2SO4(aq) + Ca(OH)2(aq) → CaSO4(s) + 2 H2O(l)
• 一般实验室中常用的酸、碱试剂有: 盐酸、硝酸与硫酸,以及氢氧化钠与 氢氧化钾等。
• 然而,由于潮解或挥发等因素,多数 酸碱试剂的标示成分或浓度常与实验 情况有异,因此利用这些试剂之前, 必须施以浓度校正(或标定)。
原理和概念酸碱的基本性质及酸碱中和
• 例如,以已知浓度的 NaOH 水溶液 标定盐酸,或以邻苯二甲酸氢钾 (简称 KHP)标定氢氧化钠水溶液。
海藻酸钠性质 • 海藻酸(Alginic acid)是由单糖醛酸线性
聚合而成的多糖,单体为 β-D-甘露醛酸 (M)和 α-L-古罗糖醛酸(G)。 • M和G单元以 M-M,G-G 或 M-G 的组 合方式通过 1,4 糖苷键相连成为嵌段 共聚物。海藻酸的实验式为(C6H8O6)n, 分子量范围从 1 万到 60 万不等。
甲
蓝
无沉淀 无沉淀
乙
黄
无沉淀 无沉淀
丙
偏绿
白色沉淀 无沉淀
丁
偏绿
无沉淀 白色沉淀
课后学习单
2.取0.05 M的 HCl 20 mL与 0.05 M 的 NaOH 30 mL混合后,溶液中 的 pH 值为多少?
课后学习单
3.是否完成七彩试管,并交由老 师检查?请简述自己在实验 过程中所运用的实验技巧为 何?
市售某些发粉分为 A、B 两包,混合后 静置产生二氧化碳,而使得面团变得松 软可口。便是利用下述酸碱反应:
HCO3-(aq) + H+(aq) → H2O(l) + CO2(g)
原理和概念酸碱的基本性质及酸碱中和
• 胃乳为胃药 的一种,可 以抑制胃酸 过多时所引 起的身体不 适。
原理和概念酸碱的基本性质及酸碱中和
原理和概念酸碱的基本性质及酸碱中和
• 滴定终点(end point):当滴定至 指示剂变色时,此点即为各种酸碱 指示剂均有其适用范围,而且实验 操作者对颜色的辨识敏感度也常因 人而异,因此利用酸碱指示剂所获 得的滴定终点并不真正代表当量点, 二者之间不尽相同。
原理和概念酸碱的基本性质及酸碱中和
• 事实上,除了上述酸碱指示剂外, 许多常见花卉、蔬菜,如紫色高丽 菜、波斯菊甚至葡萄皮,其所含的 色素可在不同 pH 值下显现不同颜 色,因此也可作为简易酸碱指示剂, 辨识酸碱度。
原理和概念酸碱的基本性质及酸碱中和
• 植物若长期暴露于酸性环境中,树叶将 无法顺利进行光合作用而逐渐枯萎死亡 。
• 酸雨可与土壤中的氧化铝进行酸碱反应 而生成铝离子:
Al2O3(s) + 6 H+(aq) → 2 Al3+(aq) + 3 H2O(l)
原理和概念酸碱的基本性质及酸碱中和
• 如果树木吸收过多铝离子时,根部将 逐渐萎缩,而丧失水土保持功能。
酸碱指示剂介绍 及 配制七彩指示剂
淡淡的三月天 杜鹃花开在山坡上
疑,发现上当了吗?
杜鹃花分布非常广泛…。
70%的杜鹃花种类生长在海拔 1700~3700 米的 地区。
杜鹃花的花期依气候和各种而不同,低山暖热地 带多在 2 ~ 3 月开放,中山温凉地带多在 4 ~ 6 月开放,高山冷凉地带多在 7 ~ 8 月开放。
实验步骤
( 4 ) 取 5 个 100mL 烧 杯 , 分 别 倒 入 20mL海藻酸钠溶液。
(5)利用酸碱中和原理及广用试剂, 配制至少五种不同颜色的溶液, 各 取 5mL 倒 入 步 骤 ( 4 ) 的 溶 液 中。
延伸实验:「膜」球的威力
实验步骤
(6)以滴管吸取溶有各种色素的海藻 酸钠溶液滴入氯化钙溶液中观察 半透膜的形成。
原理和概念酸碱的基本性质及酸碱中和
弱酸与强碱反应、强酸与弱碱 反应或弱酸与弱碱反应,因部 分反应物未完全解离,其离子 反应式无法简化,中和热也非 定值。
原理和概念酸碱的基本性质及酸碱中和
CH3COOH(aq) + Na+(aq) + OH-(aq) → CH3COO-(aq) + Na+(aq) + H2O(l)
课后学习单
4. ◎回家所使用的天然指示剂为
,
本身颜色为
,
◎加入碳酸氢钠(小苏打)后颜色,溶
液颜色为
,
◎加入醋酸后,溶液颜色为
。
老师及学生心得分享
碱性物质,则多具有涩味,而且触感 滑腻。不过以味觉或触觉辨识酸碱物 质,并非完全适宜,因为许多酸碱有 腐蚀性,绝不可以品尝或触摸。
原理和概念酸碱的基本性质及酸碱中和
酸碱物质的基本特性与其实验定义
酸
碱
有酸味
有涩味﹐具有滑腻感
可使蓝色石蕊试纸变 可使红色石蕊试纸变
为红色
为蓝色
水溶液会导电
水溶液会导电
原理和概念酸碱的基本性质及酸碱中和
• 现在以 0.100 M 的盐酸与 0.100 M 的氢氧化钠为例,说明酸碱滴定的 一般原理与应用。
原理和概念酸碱的基本性质及酸碱中和
• 当 NaOH 水溶液逐滴加入 HCl 溶液, 一般溶液中的氢离子浓度将逐渐降 低,其 pH 值逐渐增高。
原理和概念酸碱的基本性质及酸碱中和
• 当量点(equivalence point):滴定过 程中,当酸和碱剂量相等时,也就是 H+的总莫耳数等于 OH-的总莫耳数 称之。
以台湾为例,在合欢山东峰北峰也有高山杜鹃的 生长, 每年 5 月~ 6 月期间开满整个山谷,但是 花期只有 2 周左右。
疑?跑错教室?
请留步!!
跨学科跨领域, 以生物观点论述完, 来探讨在化学上的运用唷~~
教学活动
1.介绍酸碱指示剂及呈色原理 2.讲解酸碱中和反应 3.教师教导盐酸及氢氧化钠溶液配制 4.教导学生进行实验操作时应注意事项
中呈黄色;在碱性中呈蓝色;在
中性中呈绿色。现有四种未知物
溶液经分析性质,得结果如下页
附表。已知其分别为下列试药中
的 一 种 : HCl 、 BaCl2 、 NaOH 、
Na2SO4,则甲为 ,乙为 ,
丙为 ,丁为
。
课后学习单
未 以溴瑞香草酚蓝 加入 加入
知 检验所呈的颜色 Ba(OH)2 H2SO4 物
延伸实验:「膜」球的威力
海藻酸钠性质
延伸实验:「膜」球的威力
实验步骤
(1)取海藻酸钠(Sodium Alginate) 约2克,放入烧杯子中,再加水 100 mL。
(2)持续搅拌使海藻酸钠充分溶解。 (3)取氯化钙(CaCl2)7克,放置于
杯子中,再加水一公升,并搅拌 充分溶解。
延伸实验:「膜」球的威力
酸碱反应又称为中和反应,是氢离子 H(+(酸aq) )+与/C氢l-(氧aq) 离+子/N(a+碱(aq) )+结O合H-成(aq水) 的反 应。以→盐/N酸a+与(aq氢)+氧C化l-(a钠q) 水+H溶2O液(l)的反应为 H例+(,aq) 强+电O解H-质(aq可) →视H为2O完(l) 全解ΔH离=,消-去56未kJ 参与反应的离子,再加上反应热。 HCl(aq) + NaOH(aq) → NaCl(aq) + H2O(l)
延伸实验:七彩魔法池
如何闯关?
• 闯关者使用氢氧化钠和盐酸在适 当比例下,利用不同的指示剂下 调配出七彩颜色。
• 并会解释指示剂颜色变化的原理 即为过关!
延伸实验:七彩魔法池
此外学生对于「彩虹泉之水」觉得很新 奇,虽然原理很简单,利用酸性及碱性 溶液让各种不同指示剂变色,百闻不如 一见,觉得可以看到课本叙述的指示剂 变色情形重现,觉得非常开心
原理和概念酸碱的基本性质及酸碱中和
• 由于酸碱溶液多不具有颜色,因此滴 定是否达到当量点通常无法以视觉直 接判断,而必须仰赖 pH 仪或是酸碱指 示剂(acid-base indicator)的变பைடு நூலகம்予以 识别。
• 指示剂是会因 pH 值变化而改变颜色 的色素。
原理和概念酸碱的基本性质及酸碱中和
广用指示剂在不同pH值会呈现 多种不同的颜色变化
• 事实上,胃乳或胃酸抑制锭之能有效 减轻胃部不适,主要是利用氢氧化镁、 氢氧化铝等碱性物质经由酸碱反应以 中和胃酸。
(反应如下页方程式)
原理和概念酸碱的基本性质及酸碱中和
