8 溶液酸碱性的检验实验报告
溶液ph值的测定实验报告

溶液pH值的测定实验报告实验目的本实验旨在通过测定溶液的pH值,了解溶液的酸碱性质,并学习使用pH试纸和pH计测定溶液pH值的方法。
实验器材和试剂•pH试纸或pH计•不同浓度的酸碱溶液(如盐酸、硫酸、氢氧化钠、氨水等)•蒸馏水实验步骤1. 实验前的准备工作•确保实验台面整洁干净。
•准备所需的试剂和器材。
2. pH试纸的使用1.取一张pH试纸,并将其浸入待测溶液中。
2.等待片刻,直至试纸颜色稳定。
3.根据试纸的颜色变化与对照色卡进行比较,确定溶液的pH值范围。
3. pH计的使用1.打开pH计并校准。
根据pH计的说明书进行校准操作。
2.将pH计的电极插入待测溶液中。
3.等待数秒,直到pH计显示的数值稳定。
4.记录pH计显示的数值,即为溶液的pH值。
4. 清洗和储存1.每次使用完pH试纸后,将其丢弃。
2.使用完pH计后,将电极清洗干净,并储存在盐桶中。
结果与讨论本次实验中,我们使用了pH试纸和pH计两种方法来测定不同浓度的酸碱溶液的pH值。
通过使用pH试纸,我们可以根据试纸的颜色变化对比对照色卡,大致确定溶液的pH值范围。
然而,由于试纸的颜色变化区间较宽,无法给出具体的pH值。
而使用pH计则可以直接读取溶液的pH值。
pH计的使用相对较为准确和精确,可以给出更具体的数值结果。
在实验过程中,我们发现溶液的pH值与溶液的酸碱性质有关。
当pH值小于7时,溶液为酸性;当pH值大于7时,溶液为碱性;当pH值等于7时,溶液为中性。
结论通过本次实验,我们学会了使用pH试纸和pH计来测定溶液的pH值。
通过测定溶液的pH值,我们可以了解溶液的酸碱性质,并对不同浓度的酸碱溶液进行分类。
需要注意的是,在进行实验时,要严格遵守实验室安全操作规范,正确使用和处理化学试剂,以避免任何意外发生。
参考文献无。
溶液的酸碱度实验报告

溶液的酸碱度实验报告一、实验目的1、学习使用 pH 试纸和 pH 计测量溶液的酸碱度。
2、了解常见溶液的酸碱性,探究不同溶液酸碱度的差异。
3、培养实验操作能力和观察分析能力。
二、实验原理溶液的酸碱度通常用 pH 值来表示。
pH 值的范围为 0 14,其中 pH< 7 的溶液呈酸性,pH = 7 的溶液呈中性,pH > 7 的溶液呈碱性。
pH 值越小,溶液的酸性越强;pH 值越大,溶液的碱性越强。
pH 试纸是一种广泛使用的测定溶液酸碱度的工具,它通过颜色变化来指示溶液的 pH 范围。
pH 计则是一种更精确的测量仪器,能够直接显示溶液的 pH 值。
三、实验仪器和药品1、仪器:pH 试纸、玻璃棒、表面皿、pH 计、烧杯、量筒、胶头滴管。
2、药品:盐酸溶液、氢氧化钠溶液、氯化钠溶液、白醋、柠檬汁、肥皂水、碳酸钠溶液、蒸馏水。
四、实验步骤1、 pH 试纸的使用(1)用玻璃棒分别蘸取少量的盐酸溶液、氢氧化钠溶液、氯化钠溶液、白醋、柠檬汁、肥皂水、碳酸钠溶液和蒸馏水,滴在 pH 试纸上。
(2)半分钟后,将 pH 试纸与标准比色卡对照,读出溶液的 pH 值,并记录下来。
2、 pH 计的使用(1)将 pH 计的电极用蒸馏水冲洗干净,并用滤纸吸干。
(2)分别量取 20 mL 的盐酸溶液、氢氧化钠溶液、氯化钠溶液、白醋、柠檬汁、肥皂水、碳酸钠溶液和蒸馏水,倒入不同的烧杯中。
(3)将 pH 计的电极插入溶液中,待读数稳定后,记录溶液的 pH 值。
五、实验数据与结果|溶液名称|pH 试纸测量值|pH 计测量值||||||盐酸溶液|____|____||氢氧化钠溶液|____|____||氯化钠溶液|____|____||白醋|____|____||柠檬汁|____|____||肥皂水|____|____||碳酸钠溶液|____|____||蒸馏水|____|____|六、实验分析与讨论1、比较 pH 试纸和 pH 计测量结果的差异通过对比两种测量方法得到的数据,可以发现 pH 计的测量结果更加精确。
溶液的ph值实验报告

溶液的ph值实验报告
《溶液的ph值实验报告》
实验目的:通过测定不同溶液的ph值,探究溶液的酸碱性质及其影响因素。
实验材料:盖有标尺的ph试纸、酸碱指示剂、玻璃棒、试管、盖有ph值标尺
的ph计。
实验步骤:
1. 准备不同浓度的酸碱溶液,分别倒入试管中。
2. 用ph试纸或酸碱指示剂将溶液浸泡一段时间,观察颜色变化并记录下来。
3. 使用ph计测量溶液的精确ph值,并记录下来。
实验结果:
通过实验我们发现,不同浓度的酸碱溶液在ph试纸或酸碱指示剂下呈现不同
的颜色变化,且通过ph计测量得出的ph值也有明显的差异。
根据实验结果,
我们可以初步判断溶液的酸碱性质,并进一步探究溶液的ph值受溶质浓度、
温度、溶解度等因素的影响。
实验分析:
溶液的ph值是衡量其酸碱性质的重要指标,ph值越低表示溶液越酸,ph值越
高表示溶液越碱。
在实验中,我们发现溶液的酸碱性质受溶质浓度的影响较大,浓度越高的溶液通常具有更低的ph值。
此外,溶液的温度、溶解度等因素也
会对ph值产生一定影响,这需要进一步的实验研究来验证。
结论:
通过本次实验,我们初步了解了溶液的ph值对溶液酸碱性质的影响,并初步
探究了影响ph值的因素。
通过进一步的实验研究,我们可以更深入地了解溶
液的酸碱性质及其影响因素,为相关领域的研究提供更多的实验数据和理论支持。
溶液的酸碱度实验报告

溶液的酸碱度实验报告一、实验目的1、学习使用 pH 试纸测定溶液的酸碱度。
2、了解常见溶液的酸碱性,以及酸碱度对化学反应和生活中的影响。
二、实验原理溶液的酸碱度可以用 pH 来表示,pH 的范围通常在 0 14 之间。
pH=7 时,溶液呈中性;pH <7 时,溶液呈酸性,pH 越小,酸性越强;pH > 7 时,溶液呈碱性,pH 越大,碱性越强。
pH 试纸是一种广泛应用的检测溶液酸碱度的工具,其原理是基于试纸中的指示剂在不同 pH 溶液中会显示不同的颜色。
通过与标准比色卡对比,可确定溶液的 pH 值。
三、实验用品1、仪器:玻璃棒、表面皿、点滴板、pH 试纸。
2、药品:稀盐酸、稀硫酸、氢氧化钠溶液、氢氧化钙溶液、氯化钠溶液、蒸馏水。
四、实验步骤1、准备工作将 pH 试纸剪成小块,备用。
用蒸馏水清洗玻璃棒和点滴板。
2、测定稀盐酸的 pH用玻璃棒蘸取少量稀盐酸,滴在点滴板的一个凹槽中。
取一小片 pH 试纸,放在表面皿上,用玻璃棒蘸取点滴板中的稀盐酸,滴在 pH 试纸上。
半分钟后,将 pH 试纸的颜色与标准比色卡对照,读出 pH 值,并记录。
3、按照同样的方法,分别测定稀硫酸、氢氧化钠溶液、氢氧化钙溶液、氯化钠溶液和蒸馏水的 pH 值,并记录。
五、实验记录|溶液名称| pH 值||::|::||稀盐酸| 2 ||稀硫酸| 1 ||氢氧化钠溶液| 13 ||氢氧化钙溶液| 11 ||氯化钠溶液| 7 ||蒸馏水| 7 |六、实验结果分析1、稀盐酸和稀硫酸的 pH 值均小于 7,说明它们呈酸性,且稀硫酸的酸性比稀盐酸更强。
2、氢氧化钠溶液和氢氧化钙溶液的 pH 值均大于 7,说明它们呈碱性,且氢氧化钠溶液的碱性比氢氧化钙溶液更强。
3、氯化钠溶液和蒸馏水的 pH 值均为 7,说明它们呈中性。
七、实验讨论1、在测定溶液 pH 值时,为什么要将 pH 试纸放在表面皿上?答:将 pH 试纸放在表面皿上可以避免溶液直接滴在实验台上,保持实验环境的整洁,同时也便于观察和对比试纸的颜色变化。
九年级化学实验活动7溶液酸碱性的检验实验报告单

实验报告实验名称:溶液酸碱性的检验一、实验目的1.掌握酸碱指示剂的使用和分类方法;2.了解酸碱溶液的鉴别方法;3.学习溶液酸碱性检验的操作技巧。
二、实验原理酸和碱是化学中两种常见的物质,它们的性质不同。
通过酸碱指示剂,能够很好地判断溶液是酸性、中性还是碱性。
常见的酸碱指示剂有苏丹红、酚酊、酚酞、甲基橙和甲基红等。
不同的酸碱指示剂对酸、碱的变色范围不同,所以我们要根据指示剂的性质选择适当的指示剂。
三、实验器材和试剂器材:试管、滴管、显微镜。
试剂:酸碱试剂、酸碱指示剂。
四、实验步骤1.在试管中分别加入待测溶液10滴;2.滴加少许酸碱指示剂;3.观察试管内的颜色变化;4.使用显微镜观察溶液中的小细胞。
五、实验数据记录和处理1.观察到的颜色变化:-对于苏丹红:酸性溶液变红,中性溶液橙黄,碱性溶液黄色。
-对于酚酊:酸性溶液变红,中性溶液橙黄,碱性溶液无变化。
-对于酚酞:酸性溶液颜色无变化,中性溶液橙红,碱性溶液变黄。
-对于甲基橙:酸性溶液变红,中性溶液橙黄,碱性溶液变黄。
-对于甲基红:酸性溶液变红,中性溶液橙黄,碱性溶液变黄。
2.显微镜观察结果:-酸性溶液下显微镜观察到的小细胞属于酸性小细胞;-碱性溶液下显微镜观察到的小细胞属于碱性小细胞;-中性溶液下显微镜观察到的小细胞属于中性小细胞。
六、实验结果和结论通过实验可以得到以下结论:1.根据不同酸碱指示剂的变色范围可以判断溶液的酸碱性;2.酸性溶液对应的是酸性小细胞,碱性溶液对应的是碱性小细胞,中性溶液对应的是中性小细胞;3.运用酸碱指示剂和显微镜观察小细胞的方法可以鉴别溶液的酸碱性。
七、实验心得通过这个实验,我学习到了酸碱指示剂的使用方法,并且掌握了一些常用的酸碱指示剂的变色范围。
我还知道了如何使用显微镜观察溶液中的小细胞来鉴别酸碱性。
这个实验不仅培养了我的观察力,还提高了我的实验操作技巧。
我相信这些知识和技能在以后的学习中会有很大的帮助。
实验08 溶液酸碱性的检验(解析版)
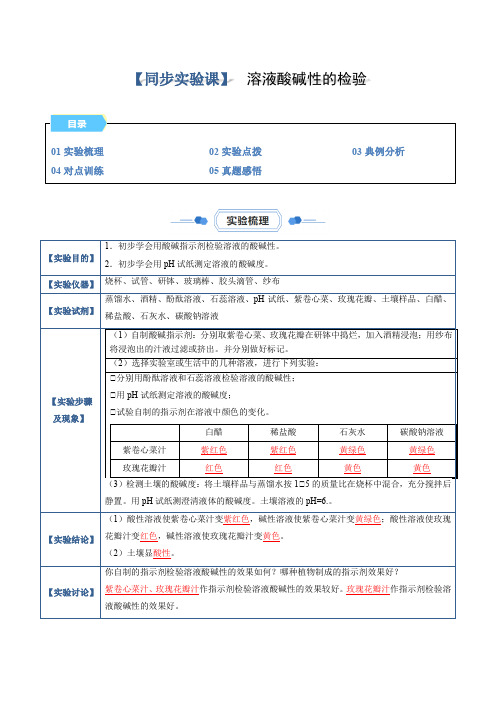
【同步实验课】溶液酸碱性的检验【实验目的】1.初步学会用酸碱指示剂检验溶液的酸碱性。
2.初步学会用pH试纸测定溶液的酸碱度。
【实验仪器】烧杯、试管、研钵、玻璃棒、胶头滴管、纱布【实验试剂】蒸馏水、酒精、酚酞溶液、石蕊溶液、pH试纸、紫卷心菜、玫瑰花瓣、土壤样品、白醋、稀盐酸、石灰水、碳酸钠溶液【实验步骤及现象】(1)自制酸碱指示剂:分别取紫卷心菜、玫瑰花瓣在研钵中捣烂,加入酒精浸泡;用纱布将浸泡出的汁液过滤或挤出。
并分别做好标记。
(2)选择实验室或生活中的几种溶液,进行下列实验:①分别用酚酞溶液和石蕊溶液检验溶液的酸碱性;①用pH试纸测定溶液的酸碱度;①试验自制的指示剂在溶液中颜色的变化。
白醋稀盐酸石灰水碳酸钠溶液紫卷心菜汁紫红色紫红色黄绿色黄绿色玫瑰花瓣汁红色红色黄色黄色(3)检测土壤的酸碱度:将土壤样品与蒸馏水按1①5的质量比在烧杯中混合,充分搅拌后静置。
用pH试纸测澄清液体的酸碱度。
土壤溶液的pH=6.。
【实验结论】(1)酸性溶液使紫卷心菜汁变紫红色,碱性溶液使紫卷心菜汁变黄绿色;酸性溶液使玫瑰花瓣汁变红色,碱性溶液使玫瑰花瓣汁变黄色。
(2)土壤显酸性。
【实验讨论】你自制的指示剂检验溶液酸碱性的效果如何?哪种植物制成的指示剂效果好?紫卷心菜汁、玫瑰花瓣汁作指示剂检验溶液酸碱性的效果较好。
玫瑰花瓣汁作指示剂检验溶液酸碱性的效果好。
01实验梳理02实验点拨03典例分析04对点训练05真题感悟1. 利用酸碱指示剂检验溶液酸碱性的一般步骤【典例01】某同学用火龙果皮自制酸碱指示剂,并用于检验苏打水的酸碱性,部分操作如图,其中错误的A.研磨果皮B.浸取色素C.取用苏打水D.滴入自制指示剂【答案】D【解析】A、将果皮放到研钵中用杵慢慢研碎,选项正确;B、将研磨好的果皮放到液体中,用玻璃棒搅拌,加快溶解,选项正确;C、倾倒液体时,取下瓶塞倒放在桌面上,标签朝向手心持瓶,瓶口紧靠试管口缓缓倒入液体,选项正确;D、向试管中滴加液体时,胶头滴管垂悬于试管口上方,不能将胶头滴管伸进试管内,选项错误。
溶液ph的测定实验报告

溶液ph的测定实验报告溶液pH的测定实验报告引言:pH是溶液酸碱性强度的量度,它是指溶液中氢离子(H+)的浓度。
在化学实验中,准确测定溶液的pH值对于了解溶液的性质和酸碱反应的进行至关重要。
本实验旨在通过使用酸碱指示剂和pH计两种方法来测定溶液的pH值,并对实验结果进行分析和比较。
实验材料和方法:1. 实验材料:- 酸碱指示剂:酚酞、溴蓝、甲基橙- pH计- 酸和碱溶液:稀盐酸、稀氢氧化钠溶液2. 实验方法:1) 酸碱指示剂法:a) 取三个试管,分别加入少量的酚酞、溴蓝和甲基橙。
b) 用滴管分别向三个试管中滴加待测溶液,观察颜色变化。
c) 根据颜色变化,判断溶液的酸碱性质。
2) pH计法:a) 打开pH计,将电极插入待测溶液中。
b) 等待数秒,直到pH计显示的数值稳定下来。
c) 记录下pH计显示的数值。
实验结果:1. 酸碱指示剂法:- 酚酞:红色表示酸性,无色表示中性或弱碱性。
- 溴蓝:黄色表示中性,蓝色表示碱性。
- 甲基橙:红色表示酸性,黄色表示中性,橙色表示碱性。
2. pH计法:- 待测溶液1:pH值为2.5- 待测溶液2:pH值为7.0- 待测溶液3:pH值为11.2讨论和分析:通过酸碱指示剂法,我们可以初步判断出溶液的酸碱性质。
然而,由于酸碱指示剂的颜色变化范围有限,对于pH值较接近中性的溶液,很难准确判断其酸碱性。
因此,使用pH计进行测定可以提供更准确的结果。
从实验结果可以看出,待测溶液1的pH值为2.5,属于酸性溶液;待测溶液2的pH值为7.0,属于中性溶液;待测溶液3的pH值为11.2,属于碱性溶液。
实验中的误差主要来自于实验操作的不精确和仪器的误差。
在使用酸碱指示剂时,由于颜色变化的主观判断,可能会导致一定的误差。
而pH计的误差则来自于仪器本身的精度以及电极的使用和校准等方面。
结论:本实验通过酸碱指示剂法和pH计法两种方法测定了不同溶液的pH值。
结果表明,pH计提供了更准确的测量结果,可以准确判断溶液的酸碱性质。
溶液的酸碱度实验报告

溶液的酸碱度实验报告实验报告:溶液的酸碱度1. 实验目的通过实验探究不同物质溶液的酸碱度,并了解酸碱度的测试方法。
2. 实验原理酸碱度可以用PH值来表示,PH值越小表示溶液越酸,越大表示溶液越碱。
本实验使用酸碱指示剂和PH试纸来测定溶液的酸碱性。
3. 实验材料和设备- 硫酸- 盐酸- 纯净水- 醋酸- PH试纸- 酸碱指示剂- 实验容器(试管或烧杯)- 实验台或工作台4. 实验步骤步骤1:将实验容器清洗干净,并确保表面干燥。
步骤2:准备四个实验容器,分别加入硫酸、盐酸、醋酸和纯净水。
步骤3:将PH试纸的一端浸入每个溶液中,等待片刻后,观察试纸颜色变化,并与PH值指南对照,记录结果。
步骤4:将酸碱指示剂滴入每个溶液中,观察颜色的变化,并与酸碱指示剂颜色对照表对照,记录结果。
步骤5:整理实验容器和实验台。
5. 实验结果与数据分析通过PH试纸测试,硫酸的PH值为1,盐酸的PH值为2,醋酸的PH值为4,纯净水的PH值为7。
由此可见,PH值越小表示溶液越酸。
通过酸碱指示剂测试,硫酸呈红色,盐酸呈橙黄色,醋酸呈橙色,纯净水无明显变化。
根据酸碱指示剂颜色对照表,可以得出相应的酸碱度。
6. 实验讨论实验结果表明,硫酸是一种强酸,盐酸是一种中等强度的酸,醋酸为一种弱酸。
纯净水呈中性,既不酸也不碱。
实验中的酸碱指示剂在不同PH值下产生颜色变化,从而可用于鉴别溶液的酸碱度。
7. 实验结论利用PH试纸和酸碱指示剂可以测试溶液的酸碱度。
通过实验得出硫酸为强酸,盐酸为中等强度的酸,醋酸为弱酸,纯净水呈中性。
8. 实验注意事项- 操作时要戴上安全手套和护目镜。
- 实验后要彻底清洁和收拾实验容器和实验台。
- 酸碱溶液应小心操作,避免接触皮肤或溅入眼睛。
- 酸碱指示剂和PH试纸应妥善保存,避免阳光直射。
本实验给出了一种简单的测试溶液酸碱度的方法,可以通过测试结果判断溶液的酸碱性。
在实际应用中,了解溶液的酸碱度对于化学实验和其他领域的研究都具有重要意义。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1、选择植物的花瓣或果实,在研钵中捣烂,加入酒精浸泡;
2、用纱布将浸泡出的汁液过滤或挤出
实验现象
选择实验室或生活中的几种溶液,进行试验:
1、分别用酚酞溶液和石蕊溶液检验溶液酸碱性;
2、用pH试纸测定溶液酸碱度;
3、试验自制指示剂在溶液中的颜色变化。
使石蕊使酚酞
使石蕊使酚酞
实验现象
指示剂在酸中变
在碱中变
实验结论
在校园或农田里取少量土壤样品,将其与蒸馏水按质量比1:5在烧杯中混合,充分搅拌后静置。用pH试纸测澄清液的酸碱度。
实验现象
实验结论
问题与讨论
溶液酸碱性的检ห้องสมุดไป่ตู้实验报告
班级姓名日期合作者
实验目的:
1、学会用酸碱指示剂检验溶液的酸碱性。
2、初步学会用pH值试纸测定溶液的酸碱度。
实验用品:
烧杯、玻璃棒、试管、研钵、胶头滴管、纱布
蒸馏水、酒精、酚酞溶液、石蕊溶液、pH试纸、植物的花瓣或果实、土壤
实验过程,现象,结论:
步骤及实验操作过程
实验现象
结论和解释
