臭氧层的形成和化学破坏
臭氧层破坏的机理

臭氧层破坏的机理一、引言臭氧层是地球大气层中非常重要的一部分,它能够吸收太阳紫外线,保护地球上的生物免受紫外线的危害。
然而,随着人类活动的不断增加,臭氧层破坏问题也越来越严重。
本文将从机理方面介绍臭氧层破坏的原因。
二、臭氧层的形成和作用1. 臭氧层形成臭氧层是由大量高能量紫外线辐射作用于大气中的氧分子(O2)形成的。
这种辐射会将O2分子分解为单个氧原子(O),随后这些单个氧原子会与其他O2分子结合形成臭氧(O3)。
2. 臭氧层作用臭氧层能够吸收太阳紫外线中最短波长(200-290纳米)的部分,这部分紫外线对生物体伤害最大。
如果没有臭氧层存在,这些紫外线将直接照射到地球表面,并对生物体造成伤害。
三、臭氧层破坏的原因1. 氯氟烃类物质氯氟烃类物质是臭氧层破坏的主要原因之一。
这些物质包括氯氟烷(CFCs)、卤代甲烷(Halons)和溴化物(Bromides)等。
这些物质在大气中会逐渐分解,释放出氯、溴等化学元素,这些元素会与臭氧反应,形成一系列的化合物,最终导致臭氧层的破坏。
2. 氮氧化物二氧化氮和一氧化二氮等氮氧化物也是臭氧层破坏的原因之一。
这些物质会与臭氧发生反应,生成一种叫做亚硝基过程的反应链,最终导致大量的臭氧被消耗掉。
3. 紫外线辐射紫外线辐射也是导致臭氧层破坏的原因之一。
紫外线能够将O3分解为O2和单个O原子,从而降低了臭氧层中O3的浓度。
4. 温室效应温室效应也可能对臭氧层产生影响。
随着温室气体的增加,大气层中的温度也会上升,这可能会导致臭氧层的下降。
四、结论臭氧层破坏是一个非常严重的问题,它对地球上的生物体造成了巨大的危害。
目前,国际社会已经采取了一系列措施来减缓臭氧层破坏问题。
这些措施包括限制和禁止使用氯氟烃类物质、减少二氧化碳等温室气体排放等。
我们应该认识到保护臭氧层是我们每个人都应该承担的责任。
臭氧层破坏的原因危害及措施

臭氧层破坏的原因危害及措施人类过多地使用氯氟烃类化学物质(用CFCs表示)是臭氧层被破坏的主要原因。
氯氟烃是一种人造化学物质。
在第二次世界大战后,尤其是进入20世纪60年代以后,氯氟烃大量用作气溶胶、制冷剂、发泡剂、化工溶剂等。
人类过多地使用氯氟烃类化学物质(用CFCs表示)是臭氧层被破坏的主要原因。
氯氟烃是一种人造化学物质,1930年由美国的杜邦公司投人生产。
在第二次世界大战后,尤其是进入20世纪60年代以后,氯氟烃大量用作气溶胶、制冷剂、发泡剂、化工溶剂等。
另外,哈龙类物质(用于灭火器)、氮氧化物也会造成臭氧层的损耗。
而CFCs物质的非同寻常的稳定性使其在大气同温层中很容易聚集起来,其影响将持续一个世纪或更长的时间。
在强烈的紫外辐射作用下,它们光解出Cl原子和Br原子,成为破坏臭氧的催化剂。
1、对人类免疫系统造成损害,使得免疫机制减退;对人类健康危害严重,可引发和加剧眼部疾病、皮肤癌、传染疾病;导致白内障眼疾和皮肤癌发病率上升。
2、破坏生态系统,减慢农作物的生长速度,减低农作物的质量和产量,甚至会造成绝收。
50%以上的陆生植物,如土豆、瓜类、番茄、甜菜等,产量会急剧下降;森林草地衰退,危及生态平衡和生物多样性。
3、对水生生态系统产生影响,使浮游生物受到危害,导致海洋食物链中基础食物数量减少,使生活在浅水里的鱼类和贝类很难生存,减少海洋生物数量,大量鱼类死亡,同时可能导致生物物种变异。
4、造成全球气候变暖与温室效应。
同时,它还会引起新的环境问题,过量的紫外线能使塑料等高分子材料更加容易老化和分解,结果又带来光化学大气污染。
1、冻结和削减氟利昂与哈龙的生产及消耗量既然破坏臭氧层的物质均为人造化学品,那么完全禁止生产和应用这些物质是可能的。
但是,由于氟里昂在工农业生产上的重要地位,立即禁止生产和使用是有难度的,因此,国际上采用的办法是逐步禁止生产和使用这些破坏臭氧层的物质。
即将氟利昂的生产及使用冻结在1986年的水平上,1994年停止生产和使用哈龙。
臭氧层破坏及其原因
臭氧层破坏及其原因约10亿年前,随着生物的进化,地球上由于好氧生物的产生和光自养生物(主要是绿色植物)的增多,加速了大气中游离氧的含量,在平流层中逐渐形成了臭氧层。
O2+光(波长为242纳米)—→2OO2+O—→O3臭氧层主要分布在距地球表面25~40千米的平流层中,但即使在那里,10万个气体分子中也只有1个臭氧分子,总的累积厚度平均也仅0.3厘米左右,然而就是这一层薄薄的臭氧层成了生命的防线,能强烈地吸收太阳光中90%波长为220-330纳米的紫外线辐射:O3+紫外线—→O2+OO+O—→O2+热量如果没有臭氧层的保护,所有紫外线会落到地面上,那么,日光晒焦的速度将比夏天的烈日下快50倍,几分钟内地球上的树木全被烧焦,所有生物都将被杀死,生机勃勃的世界就会变成荒漠及焦土。
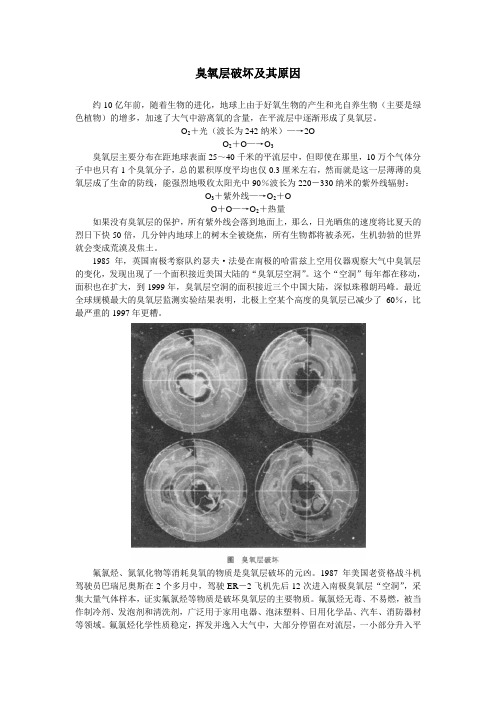
1985年,英国南极考察队约瑟夫·法曼在南极的哈雷兹上空用仪器观察大气中臭氧层的变化,发现出现了一个面积接近美国大陆的“臭氧层空洞”。
这个“空洞”每年都在移动,面积也在扩大,到1999年,臭氧层空洞的面积接近三个中国大陆,深似珠穆朗玛峰。
最近全球规模最大的臭氧层监测实验结果表明,北极上空某个高度的臭氧层已减少了60%,比最严重的1997年更糟。
氟氯烃、氮氧化物等消耗臭氧的物质是臭氧层破坏的元凶。
1987年美国老资格战斗机驾驶员巴瑞尼奥斯在2个多月中,驾驶ER-2飞机先后12次进入南极臭氧层“空洞”,采集大量气体样本,证实氟氯烃等物质是破坏臭氧层的主要物质。
氟氯烃无毒、不易燃,被当作制冷剂、发泡剂和清洗剂,广泛用于家用电器、泡沫塑料、日用化学品、汽车、消防器材等领域。
氟氯烃化学性质稳定,挥发并逸入大气中,大部分停留在对流层,一小部分升入平流层。
在对流层相当稳定的氟氯烃上升进入平流层后,在一定气象条件和紫外线的照射下会分解生成一种氯自由基(Cl·)。
这种氯自由基的反应能力极强,导致臭氧迅速分解。
CF3Cl+紫外线—→CF3·+Cl·Cl·+O3—→ClO·+O2在平流层中的自由氧原子还会与ClO·自由基反应:O+ClO·—→Cl+O2反应产生的Cl·又会进一步破坏臭氧。
对流层臭氧的形成和破坏

对流层臭氧的形成和破坏对流层是地球大气层中的最低一层,其中包含了我们生活所需的氧气、氮气等气体。
其中,臭氧是非常重要的一种气体,它能够吸收宇宙射线,起到保护生命的作用。
然而,随着人类活动的增加和自然因素的变化,对流层臭氧的形成和破坏也变得更加复杂和关键。
本文将对对流层臭氧的形成和破坏进行探讨。
一、对流层臭氧的形成对流层臭氧是一种同氧气分子相比多了一个氧原子的物质,其化学式为O3。
对流层臭氧的形成主要是通过光解作用和化学反应两种途径实现的。
1.光解作用在对流层中,高能量的太阳紫外线辐射会将氧分子分解为两个氧原子,即O2 + 光子 = 2O。
这个过程需要光子有充足的能量才能发生,所以它只会发生在紫外线波段,即波长低于290纳米的光线上。
分解出来的氧原子很容易与其他氧分子结合,形成臭氧分子:O + O2 + M = O3 + M(其中M代表的是一种稳定基元分子)。
这个过程是一个自由基反应,需要有足够的氧气存在才能进行。
通过这个途径,对流层臭氧便得以形成。
2.化学反应在对流层中,臭氧还可以通过化学反应的方式形成。
大气中存在着一些含氮化合物,比如NO和NO2。
这些氮气化合物会受到太阳光的影响,生成一些高能量的分子,导致它们能够与臭氧反应,形成NO2和O2。
这个反应必须在高能量的紫外线下才能发生。
此外,NO2和O2还可以反应生成臭氧和一个氧原子,形成一种局部的臭氧循环。
二、对流层臭氧的破坏尽管对流层臭氧在保护地球生命方面发挥着重要作用,但它也会因为人类活动和自然因素而遭到破坏。
对流层臭氧破坏主要有两种途径:化学消耗和物理损失。
1.化学消耗当人类活动释放出来的含氯或溴物质进入大气层中时,它们会通过化学反应与臭氧反应,降解臭氧分子。
比如,CFCl3(也称为CFC-11)就是一种广泛使用的氯氟碳化合物,它在臭氧分子中起到催化分解的作用。
这一过程称为氯化臭氧反应,化学式如下:CFCl3 + O3 = CFCl2O + O2CFCl2O + O = CFCl2 + O2CFCl2 + O3 = Cl + CFCl2O2Cl + O3 = ClO + O2ClO + O = Cl + O2因此,氯化臭氧作用将臭氧分子分解为氧气和一个氯自由基。
第二章 大气环境化学 (10)臭氧层的形成与耗损

十、臭氧层的形成与耗损1.臭氧层破坏的化学机理平流层中的臭氧来源于平流层中O2 的光解:O2 + hν(λ≤243nm) → O + OO + O2 + M → O3 + M平流层中的臭氧的消除途径有两种①臭氧光解:O3 + hν → O2 + O②能够使平流层的O3 真正被清除的反应为O3 与O 的反应:O3 + O → 2O2由于人类活动的影响,水蒸气、氮氧化物、氟氯烃等污染物进入了平流层,在平流层形成了HO x、NO x 和ClO x 等活性基团,从而加速了臭氧的消除过程,破坏了臭氧层的稳定状态。
(1)平流层中NO x对臭氧层破坏的影响平流层中NO x 主要存在于25km 以上的大气中,其数量约为10μL/m3。
在25km 以下的平流层大气中所存在的含氮化合物主要是HNO3。
①平流层中NO x的来源(a)N2O 的氧化N2O 是对流层大气中含量最高的含氮化合物,主要来自于土壤中硝酸盐的脱氮和铵盐的硝化。
因此,天然来源是其产生的主要途径。
由于N2O 不易溶于水,在对流层中比较稳定,停留时间较长,因此,可通过扩散作用进入平流层。
进入平流层的N2O 有90%会通过光解形成N2:N2O+ hν(λ≤243nm) →N2+O有2%会氧化形成NO:N2O + O → 2NO因此,N2O 在平流层的氧化是平流层中NO 和NO2 的主要天然来源。
(b)超音速和亚音速飞机的排放(c)宇宙射线的分解这个来源所产生的NO x 数量较少。
②NO x清除O3的催化循环反应NO + O3 → NO2 + O2NO2 + O• → NO + O2总反应:O3 + O• → 2O2该反应主要发生在平流层的中上部。
如果是在较低的平流层,由于O•的浓度低,形成的NO2 更容易发生光解,然后与O•作用,进一步形成O3:NO2 → NO + O•O• + O2 + M → O3因此,在平流层底部NO 并不会促使O3 减少。
③NO x的消除(a)由于NO 和NO2 都易溶于水,当它们被下沉的气流带到对流层时,就可以随着对流层的降水被消除,这是NO x 在平流层大气中的主要消除方式。
臭氧层的认识

臭氧层的认识臭氧层是大气中的一个重要组成部分,它对地球上的生物和环境起着至关重要的保护作用。
本文将从臭氧层的定义、形成、破坏以及保护等方面进行阐述。
一、臭氧层的定义臭氧层是大气中含有较高浓度臭氧分子的一层,位于地球的平流层中,大约在15至35公里的高度范围内。
臭氧层是由于太阳紫外线照射下,大气中的氧分子发生光化学反应而形成的。
二、臭氧层的形成臭氧层的形成主要是通过紫外线的照射作用下,氧分子发生光化学反应而产生的。
太阳的紫外线主要分为UVA、UVB和UVC三种,其中UVC被大气层中的氧气和臭氧吸收,不会到达地球表面。
而UVA和UVB会透过大气层到达地球表面,UVB对生物体的伤害更大。
当太阳的紫外线照射到大气中的氧分子时,一部分氧分子会发生光解作用,将一个氧分子分解为两个自由氧原子。
这些自由氧原子与其他氧分子结合,形成臭氧分子(O3)。
因此,臭氧层的形成是由于紫外线的照射下,氧分子发生光化学反应而生成的。
三、臭氧层的破坏然而,由于人类活动和自然因素的影响,臭氧层正在遭受破坏。
其中最主要的原因是人类活动产生的氯氟烃类化合物(CFCs)和卤代碳化合物(HCFCs)。
这些化合物在大气中逐渐上升到平流层,然后被紫外线分解,释放出氯原子和溴原子。
氯原子和溴原子是臭氧分子的破坏者。
它们与臭氧分子发生反应,导致臭氧分子被分解成氧分子和单质氧。
这就造成了臭氧层的破坏,从而减少了对紫外线的屏蔽作用。
四、臭氧层的保护为了保护臭氧层,国际社会采取了一系列措施。
1987年,联合国环境规划署和世界气象组织共同发起了《蒙特利尔议定书》,约定逐步减少和禁止使用对臭氧层具有破坏作用的物质。
这些物质包括CFCs 和HCFCs等。
随着国际社会的共同努力,禁止使用CFCs的措施已经取得了显著成效。
目前,许多国家已经实现了完全停止使用CFCs,并取得了明显的臭氧层恢复效果。
然而,仍然需要持续努力,继续减少和禁止使用对臭氧层有破坏作用的化学物质,以保护臭氧层的完整性和稳定性。
大气化学中的臭氧层损耗机制

大气化学中的臭氧层损耗机制臭氧层是指大气中一层浓度更加稠密的臭氧分子团,它可以吸收一部分紫外线,保护地球上的生物免受辐射的伤害。
然而,随着人类工业化和技术进步的不断发展,大气中的一些化学物质开始威胁到臭氧层的稳定性,导致臭氧层的损耗加剧并对人类健康和环境造成威胁。
本文将探讨大气化学中的臭氧层损耗机制,旨在增强对该问题的认识和理解。
第一部分:臭氧层的形成在普通大气中,氧气分子是最为常见的组分之一。
但是当大气中存在足够强的紫外线时,氧气分子可以自发地发生核反应,生成自由基氧分子(O)和原子氧(O)。
这些自由基之后又可以和氧气反应,形成臭氧分子(O3)。
臭氧分子对紫外线具有很强的吸收能力,并且在大气中能够稳定存在,形成了臭氧层。
臭氧层的稳定性取决于大气中臭氧分子的生成和损耗速率之间的平衡。
第二部分:臭氧层的损耗机制臭氧层的损耗主要分为自然损耗和人为损耗两种。
1. 自然损耗臭氧分子的自然损耗主要涉及到大气中的各种化学反应。
例如,氧自由基和氮氧自由基(NOx)等反应都可以导致臭氧分子的损耗。
其中最为重要的反应式如下所示:O3 + O → 2O2O3 + NO → NO2 + O2以上反应中,氧自由基促使臭氧分子分解为氧气;而NOx可以促进臭氧分子与其他氧气或自由基反应,导致臭氧分子的消耗。
这些反应既可以在平流层内,也可以在对流层内发生。
2. 人为损耗与自然损耗相比,人为损耗对臭氧层的安全性产生了更大的威胁。
人类活动中产生的一些化学物质可以比自然情况下更快地将臭氧分子分解,导致臭氧层的稳定性下降。
以下是最为严重的几种臭氧层破坏物质:(1)氯氟烃(CFCs):这些物质被广泛使用于制冷、喷雾剂和泡沫等方面。
它们的主要危害在于它们中的氯原子可以与臭氧反应,产生氯氧自由基,导致大量臭氧分子消耗,从而破坏臭氧层。
(2)卤代甲烷(如氯甲烷、溴甲烷等):这些物质通常由人类活动中的焚烧、排放和使用过程中产生。
这些化学物质都具有制造CFCs相同的原因:它们能够产生卤素自由基,从而破坏臭氧分子。
臭氧层的形成和耗损

臭氧空洞旳成因
❖ 臭氧层损耗是臭氧空洞旳真正成因。
❖ 臭氧层是怎样耗损旳呢?是什么原因造成臭氧层旳 破坏呢?科学家以为,臭氧急剧耗损不是由已知旳 自然现象引起旳,而是人为旳活动起决定性旳作用。 是某些人类活动所散发旳物质进入臭氧层,引起臭 氧旳损耗。
❖ 这些物质有含氯氟烃类、有机溴化合物、氧化亚氮 及超音速飞机排放氮氧化物、甲烷、水汽和二氧化 碳等。
❖ 1991年成立了保护臭氧层领导小组,开始 编制并完毕了《中国消耗臭氧层物质逐渐 淘汰国家方案》
❖ 1999年7月1日冻结了氟利昂旳生产,并将
❖ 从这里我们不但能够看到人类日益紧迫旳步伐,而 且也发觉,虽然如此努力地弥补我们上空旳“臭氧 洞”,但因为臭氧层损耗物质从大气中除去十分困 难.估计采用哥本哈根修正案,也要在2050年左 右平流层氯原子浓度才干下降到临界水平下列,到 那时,我们上空旳“臭氧洞”可望开始恢复。臭氧 层保护是近代史上一种全球合作十分经典旳范例, 这种合作机制将成为人类旳财富,并为处理其他重 大问题提供借鉴和经验。
❖ 2023年1-3月期间,北极上空臭氧层耗损曾经 到达60%,是历史上该地域臭氧层耗损旳最 高水平。
❖ 当南极旳春季来临(九月下旬),阳光照射 冰云,冰晶融化,释放吸附旳氯氟烃类物质。 在紫外线旳照射下,分解产生氯原子,与臭 氧反应,形成季节性旳“臭氧空洞”。
❖ 因为北极没有极地大陆和高山,仅有一片海 洋冰帽,形不成大范围旳强烈旳“极地风 暴”,所以不易产生象南极那样大旳臭氧洞。 但是,北极上空旳臭氧在不断地降低。
大气中臭氧层现状及发展
❖ 这是美国航空航天局用卫星 测绘出旳南极臭氧层空洞, 左图是去年9月24日旳臭氧 层空洞图像,虽然只有一种, 但其面积比北美洲还大。右 图是今年9月24日旳图像, 科学家首次发觉臭氧层空洞 居然一分为二,但总面积比 去年降低了40%,科学家以 为这要归因于南极洲气温旳 上升。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
臭氧层的形成和化学破坏
摘要:臭氧层的破坏,是人类面临的三大环境问题之一.臭氧层担当着防止高能紫外
线辐射直接照到地球表层大气的作用,因而臭氧层的存在是与人类健康及生态平衡关系密
切的问题.随着现代工业的发展,平流层大气受到污染,臭氧层遭到破坏.自从二十世纪70年代Crutzen发现臭氧层遭到破坏以来,世界各国对此问题非常重视,做了大量研究,已
基本弄清臭氧层的形成、作用及被破坏机理等问题,并制定了保护臭氧层的一系列国际公约,使臭氧层被破坏的速度得以减缓.
关键词:形成;机理;保护
作者简介:王国栋(1985-),男,本科,中学二级教师,陕西户县人,研究方向:
高中化学教学研究. 一、臭氧层的形成
在平流层中,氧气吸收波长为180nm-240nmUV(紫外线)光而使氧气分子分解:
O2+hν→O+O
自由的O原子和其它的O2分子形成臭氧,该反应被认为是平流层中臭氧的唯一来源:O2+O+M → O3+M
但臭氧也会发生光解而遭到破坏:O3+O → O2+O2
可见,平流层中同时存在着臭氧的产生和臭氧的分解两种光化学过程,这两种过程在
光的作用下会达到动态平衡.最终,在离地面25km-30km的高空,就形成一浓度相对较大
和稳定的臭氧层,阻挡了对人类有害的高能紫外线. 二、臭氧层化学破坏的机理
目前,人类认为直接破坏臭氧层的物质有:氮氧化物、氢氧自由基和卤代烷烃等.
1.氮氧化物对臭氧层的破坏作用
存在于大气中的氮氧化物有:N2O、NO、NO2. N2O是自然界微生物活动的产物,大气中含量很少,活性较小,在低层大气中被认为是非污染性气体,当其扩散至平流层后,
可被转化为一氧化氮: N2O+O → NO+NO N2O+hν→ NO+N
平流层中破坏臭氧的污染物为NO:O3+NO → NO2+O2
NO2也能与平流层中较丰富的氧原子反应:NO2+O → NO+O2
该反应速率较快,生成的一氧化氮再次破坏臭氧,可以认为是在一氧化氮催化下加速
了臭氧与氧原子的反应:
O3+ONOO2+O2
据研究,一个N2O分子产生的NO引发上述链式反应,可破坏105个臭氧分子.
一氧化氮来源有两种方式,自然来源由一氧化二氮产生,人工源主要来自于平流层下
部飞行的超音速飞机排放的废气.其排放的废气中所含的氮氧化物及水气均可破坏臭氧.
2.氢氧自由基对臭氧层的破坏
平流层中HO?自由基的来源主要来自喷气机排放的废气中的水气,其与臭氧的反应:HO?+O3 → O2+HO2? HO2?+O → O2+HO?
HO?自由基反复产生,其实质是在HO?自由基催化作用下臭氧与氧原子反应生成氧分子:O3+OHO?O2+O2
3.卤代烷烃对臭氧层的破坏(1)氟利昂
氟利昂是含氟氯饱和烃类的总称.Rowland和Molina于1974年提出了CFCs理论,阐
明了氟利昂影响臭氧层厚度的机理.以CCl2F2为例:CCl2F2+hν→ CF2Cl?+Cl
光解产生的Cl原子与臭氧发生作用,使臭氧遭到破坏:O3+Cl → ClO?+O2
ClO?+O → Cl+O2 ClO?+O3 → ClO2?+O2 ClO2?+hν → Cl+O2 … …
其实质是在Cl原子催化下,臭氧与氧原子反应,生成氧分子:
O3+O Cl O2+O2
科学家证实,随着大气层高度的增加,氯原子对臭氧的破坏作用增强,当处于平流层时,一个氯原子可以分解掉105个O3分子.因此,氟利昂对平流层中的臭氧有巨大的破坏
作用.
(2)哈隆
哈隆是一类含溴卤代甲、乙烷的商品名,主要用做灭火器.哈隆破坏臭氧层的机理与
氟利昂类似,实质是在溴原子催化作用下,臭氧与氧原子反应: O3+O Br O2+O2
研究结果表明,在平流层中,哈隆比氟利昂破坏更大. (3)其它卤代烷烃
工农业生产中应用的氯仿(CHCl3)、甲基氯仿(CH3CCl3)等其它氯代烷?N也同样分解破坏臭氧.
综上所述,氮氧化物、HO?自由基、氟氯代烃等破坏臭氧层的机理是:这些物质分别
产生的NO、HO?自由基、氯或
溴原子等作为催化剂,加速了臭氧与氧原子的反应. 几种破坏臭氧层的物质中,
主要危害物为氮氧化物,约占破坏总量的65%,其次为HO?自由基,约为20%,卤代烷烃类约占10%,自然破坏仅占5%左右. 三、臭氧层的保护
1987年,联合国26个会员国在加拿大蒙特利尔签署了环境保护公约《蒙特利尔破坏
臭氧层物质管制议定书》,又称《蒙特利尔议定书》.该议定书禁止或淘汰使用耗蚀臭氧
层的化学品,其中包括曾广泛用于冰箱和喷雾器中的氟氯碳化物,自1989年1月1日起
生效,开始了全球保护臭氧层的行动.
1995年联合国大会决定,每年的9月16日为国际保护臭氧层日.
联合国组织300名科学家对大气臭氧水平进行持续监测,每4年为一个评估期.
随着世界各国的努力,臭氧层在2000年�D2021年间变厚了4%,南极洲上空的臭氧
空洞也停止扩大.臭氧层虽然有所恢复,但离痊愈还很遥远,人类的保护行动依然任重道远. 参考文献:
[1]成广兴,邵军.臭氧层的化学破坏及其对策.化学通报,1999,(9):44~47.
[2]汪桂斌.环境化学的回顾与展望.化学通报,1999,(11):
14~15.
[3]龚书椿,陈应新,韩玉莲,张静贞.环境化学,上海:华东师范大学出版社,1991:133~137.
[4]大连理工大学无机化学教研室编.无机化学(第4版),北京:高等教育出版社,2001:14~15.
感谢您的阅读,祝您生活愉快。
