有机化学之醇醛醚
大学化学《有机化学-醇和醚》课件

稀酸,反应条件温和, 不饱和键不受影响
反应式
ROH + HX 醇的活性比较: 苯甲型, 烯丙型 > 3oROH > 2oROH > 1oROH > CH3OH HX的活性比较: HI > HBr > HCl RX + H2O
浓盐酸和无水氯化锌的混合物称为卢卡斯试剂。
用卢卡斯试剂可鉴别六碳和六碳以下的一级、二级、三级醇。
将三种醇分别加入盛有卢卡斯试剂的试管中,经振荡后可发现: 三级醇立刻反应(烯丙型及苯甲型的醇也可以很快地发生反 应),生成油状氯代烷,它不溶于酸中,溶液呈混浊后分两层, 反应放热;
H3C CH3 + Br- + C O P Br Br H CH3
Br (CH3)3C OH + Br P Br
SN2
SN1
(CH3)3C+ + HOPBr2
Br -
(CH3)3CBr
10.6.3 与亚硫酰氯反应 (1) 反应方程式
ROH + SOCl2
b.p. 79oC
RCl + SO2
+ HCl
酸性条件
醇各类氧化反应的总结-2
氧化剂 新制 MnO2*1 沙瑞特试剂 CrO3吡啶 一级醇 醛 醛 二级醇 三级醇 酮 酮 特点和说明 中性 不饱和键不受影响 弱碱,反应条件温和, 不饱和键不受影响。
琼斯试剂
CrO3+稀H2SO4 费兹纳-莫发特试剂
醛(产率不高, 不用。)
醛(产率很高)
酮 酮
乙二醇二硝酸酯
2 磷酸酯的制备
3C4H9OH +
Cl Cl Cl P=O
C4H9O C4H9O C4H9O
有机化学—醇的合成

有机化学——醇的合成前言有机化学主要是介绍化学物质的科学。
目前有机化学物质的分类主要是按照其决定性作用,能代表化学物质的基团也就是官能团的不同来进行分类的。
可分为:烷烃,烯烃,炔烃,芳香烃(以上为烃类);卤代烃,醇,酚,醚,醛,酮,羧酸,羧酸衍生物,胺类,硝基化合物,腈类,含硫有机化合物(如硫醇,硫醚,硫酚,磺酸,砜与亚砜等),含磷有机化合物等元素有机化合物,杂环化合物等。
具体主要是介绍这些化学物质的系统命名,化学反应,反应机理,制备方法。
其中化学反应基本上为基团的取代,能否进行一个反应,取决于热力学和动力学两个方面的因素。
而制备方法主要是通过无机物,石油提取物,以及容易制备或成本低的物质制得难以得到的物质。
反应机理也为基团之间的进攻和离去倾向之间的竞争。
有机合成方面主要研究比较简单的化合物或元素经化学反应合成有机化合物。
19世纪30年代合成了尿素;40年代合成了乙酸。
随后陆续合成了葡萄糖酸、柠檬酸、琥珀酸、苹果酸等一系列有机酸;19世纪后半叶合成了多种染料;20世纪40年代合成了DDT和有机磷杀虫剂、有机硫杀菌剂、除草剂等农药;20世纪初,合成了606药剂,30~40年代,合成了一千多种磺胺类化合物,其中有些可用作药物。
醇醇是脂肪烃分子中的氢原子或芳香烃侧链上的氢原子被羟基所取代后的化合物,羟基(—OH)是醇的官能团。
一、醇的分类、命名和结构(1)醇的分类根据醇分子中所含羟基的数目,可以分为一元醇、二元醇及三元醇等,同时二元醇以上的醇称为多元醇;在一元醇分子中,根据羟基所连接的碳原子的不同级数,可分为一级醇(伯醇)、二级醇(仲醇)和三级醇(叔醇);根据醇分子中烃基的类别,又可分为脂肪醇、脂环醇,或饱和醇、不饱和醇。
伯醇(RCH2OH): CH3CH2OH仲醇(R2CHOH):(CH3)2CHOH叔醇(R3 COH): (CH3)3C-OH注:羟基和碳碳双键直接相连的醇叫烯醇。
在一般情况下,烯醇式互变—烯醇是不稳定,容易互变成为比较稳定的醛或酮。
有机化学课后答案第十章醇和醚
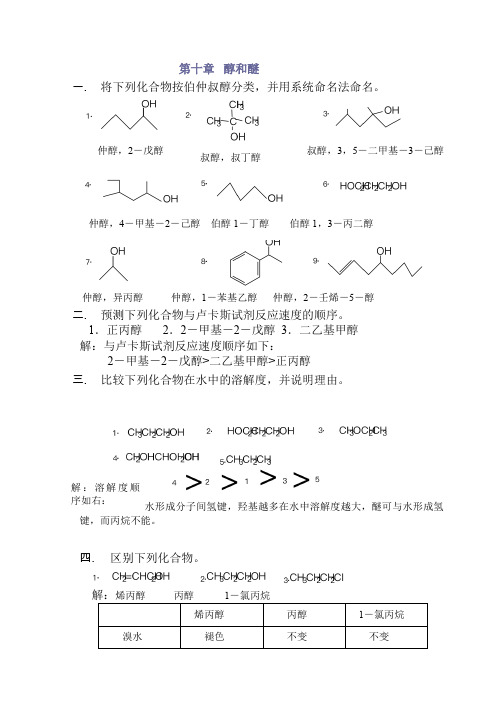
第十章 醇和醚一. 将下列化合物按伯仲叔醇分类,并用系统命名法命名。
仲醇,异丙醇 仲醇,1-苯基乙醇 仲醇,2-壬烯-5-醇二. 预测下列化合物与卢卡斯试剂反应速度的顺序。
1.正丙醇 2.2-甲基-2-戊醇 3.二乙基甲醇 解:与卢卡斯试剂反应速度顺序如下:2-甲基-2-戊醇>二乙基甲醇>正丙醇 三. 比较下列化合物在水中的溶解度,并说明理由。
四. 区别下列化合物。
仲醇,2-戊醇叔醇,叔丁醇叔醇,3,5-二甲基-3-己醇仲醇,4-甲基-2-己醇 伯醇1-丁醇 伯醇 1,3-丙二醇3.α-苯乙醇β-苯乙醇解:与卢卡斯试剂反应,α-苯乙醇立即变浑,β-苯乙醇加热才变浑。
五、顺-2-苯基-2-丁烯和2-甲基-1-戊烯经硼氢化-氧化反应后,生成何种产物?解:六、写出下列化合物的脱水产物。
七、比较下列各组醇和溴化氢反应的相对速度。
1.苄醇,对甲基苄醇,对硝基苄醇解:反应速度顺序:八、1、 3-丁烯-2-醇与溴化氢作用可能生成那些产物?试解释之。
解:反应产物和反应机理如下:2、 2-丁烯-1-醇与溴化氢作用可能生成那些产物?试解释之。
解:反应产物和反应机理如下:九、反应历程解释下列反应事实。
解:反应历程如下:十、用适当的格利雅试剂和有关醛酮合成下列醇(各写出两种不同的组合)。
1.2-戊醇4.2-苯基-2-丙醇十一、合成题1.甲醇,2-丁醇合成2-甲基丁醇解:2.正丙醇,异丙醇2- 甲基-2-戊醇2.2-甲基-2-丁醇3.1-苯基-1-丙醇3.甲醇,乙醇正丙醇,异丙醇解:4.2-甲基-丙醇,异丙醇 2,4-二甲基-2-戊烯解:5.丙烯甘油三硝酸甘油酯6.苯,乙烯,丙烯3-甲基-1-苯基-2-丁烯十二、完成下面转变。
1.乙基异丙基甲醇 2-甲基-2-氯戊烷解:。
解:2.3-甲基-2-丁醇 叔戊醇解:3.异戊醇 2-甲基-2-丁烯解:解: (2)十四、某醇C5H12O氧化后生成酮,脱水则生成一种不饱和烃,将此烃氧化可生成酮和羧酸两种产物的混合物,推测该化合物的结构。
有机化学之醇醛醚

丙三醇(三元醇)
用途
酚
酚是重要的化工原料,可制造染料、药物、酚醛 树脂、胶粘剂等。 苯酚及其类似物可制做杀菌防腐剂。 邻苯二酚、对苯二酚可作显影剂 对人体的危害
酚侵入人体,会与细胞原浆中蛋白质结合形成不溶性 蛋白,使细胞失去活性。 酚对神经系统、泌尿系统、消化系统均有毒害作用。
酚
羟基直接和芳环相连的化合物为酚,通式为Ar-OH。酚可 按照分子中所含羟基的数目分为一元酚、二元酚、三元酚 等,二元以上的酚统称为多元酚。酚也可以按照分子中酚 羟基所连接的母体不同分为苯酚、萘酚等,苯酚是酚类最 简单也是最重要的酚。例如:
O O O O O
O O
O O O O
O
O
12-冠-4
15-冠-5
18-冠-6
制作PPT小组成员:黄禹、李敏、李 燕、张祯祯、何琪玥、彭迪。
醇的用途: 1、用作燃料、溶剂、防冻液 2、重要的化工原料
醇
醇可以看做烃分子中的氢原子被羟基(-OH)取代后的产 物,一元醇也可看做水分子中的氢原子呗烃基(-R)所取 代。 (-OH)是醇的官能团,又称醇烃基。饱和一元醇的 通式是CnH2n+1OH,或简写为ROH。
1、按烃基的所连烃基的饱和程度不同,醇可分为饱和醇 和不饱和醇。例如:饱和醇
一元酚:
OH
OH
CH3
OH
苯酚
2-甲基苯酚
2-萘酚
二元酚:
OH
OH
OH
OH
OH
OH
1,2-苯二酚 三元酚:OH源自1,3-苯二酚OH
1,4-苯二酚
OH
OH
HO
OH
OH
HO
OH
1,2,4-苯三酚
有机化学相关知识点

有机化学相关知识点有机化学相关知识点(1) 难溶于水:各类烃、卤代烃、硝基化合物、酯、绝大多数高聚物、高级的醇、醛、羧酸等。
(2) 易溶于水:低级[n(C)≤4]醇、(醚)、醛、(酮)、羧酸及盐、氨基酸及盐、单糖、二糖。
(都能与水形成氢键)。
(3) 具有特殊溶解性的:①乙醇是一种很好的溶剂,既能溶解许多无机物,又能溶解许多有机物,所以常用乙醇来溶解植物色素或其中的药用成分,也常用乙醇作为反应的溶剂,使参加反应的有机物和无机物均能溶解,增大接触面积,提高反应速率。
例如,在油脂的皂化反应中,加入乙醇既能溶解NaOH,又能溶解油脂,让它们在均相(同一溶剂的溶液)中充分接触,加快反应速率,提高反应限度。
②苯酚:室温下,在水中的溶解度是 9.3g (属可溶),易溶于乙醇等有机溶剂,当温度高于65℃ 时,能与水混溶冷却后分层,上层为苯酚的水溶液,下层为水的苯酚溶液,振荡后形成乳浊液。
苯酚易溶于碱溶液和纯碱溶液,这是因为生成了易溶性的钠盐。
③乙酸乙酯在饱和碳酸钠溶液中更加难溶,同时饱和碳酸钠溶液还能通过反应吸收挥发出的乙酸,溶解吸收挥发出的乙醇,便于闻到乙酸乙酯的香味。
④ 有的淀粉、蛋白质可溶于水形成胶体。
蛋白质在浓轻金属盐(包括铵盐)溶液中溶解度减小,会析出(即盐析,皂化反应中也有此操作)。
但在稀轻金属盐(包括铵盐)溶液中,蛋白质的溶解度反而增大。
⑤线型和部分支链型高聚物可溶于某些有机溶剂,而体型则难溶于有机溶剂。
⑥氢氧化铜悬浊液可溶于多羟基化合物的溶液中,如甘油、葡萄糖溶液等,形成绛蓝色溶液。
有机物的密度(1) 小于水的密度,且与水(溶液)分层的有:各类烃、一氯代烃、酯(包括油脂)(2) 大于水的密度,且与水(溶液)分层的有:多氯代烃、溴代烃(溴苯等)、碘代烃、硝基苯3. 有机物的状态[常温常压(1个大气压、20℃ 左右)](1) 气态:① 烃类:一般N(C)≤4的各类烃注意:新戊烷[C(CH3)4]亦为气态② 衍生物类:一氯甲烷(CH3Cl,沸点为 -24.2℃ ) 氟里昂(CCl 2F 2,沸点为 -29.8℃ )氯乙烯(CH2=CHCl,沸点为 -13.9℃ ) 甲醛(HCHO,沸点为 -21℃ )氯乙烷(CH3CH2Cl,沸点为12.3℃ ) 一溴甲烷(CH3Br,沸点为 3.6℃ )四氟乙烯(CF2=CF2,沸点为 -76.3℃ ) 甲醚(CH3OCH3,沸点为 -23℃ )甲乙醚(CH3OC2H5,沸点为10.8℃ ) 环氧乙烷( ,沸点为13.5℃ )(2) 液态:一般N(C)在5~16的烃及绝大多数低级衍生物。
有机化学基础知识点整理醇醛酮和羧酸

有机化学基础知识点整理醇醛酮和羧酸有机化学基础知识点整理醇醛酮和羧酸是有机化学中非常重要的化合物类别,它们在化学合成、生物化学和药物研发等领域中扮演着关键的角色。
本文将对醇醛酮和羧酸的基本概念、性质及其在有机化学中的应用进行整理和归纳,以帮助读者全面理解和掌握这些重要的有机化合物。
一、醇的基本概念和性质1. 醇的定义:醇是一类化合物,其分子中含有一个或多个羟基(-OH)。
醇按照羟基的位置可以分为不同的类型,如一元醇、二元醇和多元醇等。
2. 醇的命名:对于一元醇,命名时通常以烃根名称加上后缀-醇。
例如,乙醇(ethyl alcohol)是由乙烷基上的一个羟基组成。
对于二元醇和多元醇,命名时需标明羟基的位置和数量,如乙二醇(ethylene glycol)和甘油(glycerol)。
3. 醇的性质:醇是无色液体或结晶物质,具有特征性的气味。
它们可以与水形成氢键,并且具有一定的溶解性。
醇还可以发生氧化反应,生成相应的醛或羧酸。
二、醛和酮的基本概念和性质1. 醛的定义:醛是一类化合物,其分子中含有一个羰基(C=O),羰基位于分子的末端。
醛的通式为RCHO,其中R代表有机基团。
2. 酮的定义:酮是一类化合物,其分子中含有一个羰基(C=O),羰基位于分子的中间。
酮的通式为R₂CO,其中R代表有机基团。
3. 醛和酮的命名:醛的命名通常以烃根名称加上后缀-醛,酮的命名通常以烃根名称加上后缀-酮。
在命名时,需要标明羰基的位置和有机基团的名称。
4. 醛和酮的性质:醛和酮通常是无色液体或结晶物质,具有较强的气味。
它们具有较高的沸点和熔点,可以与水形成氢键。
醛和酮的化学反应中,羰基碳上的氢可以进行取代反应、加成反应和氧化反应等。
三、羧酸的基本概念和性质1. 羧酸的定义:羧酸是一类化合物,其分子中含有一个羧基(-COOH)。
羧酸的通式为RCOOH,其中R代表有机基团。
2. 羧酸的命名:羧酸的命名通常以烃根名称加上后缀-酸。
醇醚醛酮和羧酸的命名与性质
醇醚醛酮和羧酸的命名与性质醇醚醛酮和羧酸是有机化学中常见的功能性化合物,它们具有不同的命名方法和独特的化学性质。
本文将介绍醇醚醛酮和羧酸的命名规则,以及它们的性质和一些重要的应用。
一、醇醚醛酮的命名醇是含有羟基的有机化合物,醚是含有氧原子连接两个有机基团的化合物,醛是含有羰基的化合物,酮是含有两个有机基团连接在碳氧化学键上的化合物。
醇醚醛酮的命名依据它们的结构和功能基团的数量和位置。
1. 醇的命名对于直链醇,命名方法是将它们的碳链数目用希腊字母表示,并在末端加上“醇”二字。
例如,甲醇是一种含有一个碳原子的醇,乙醇是含有两个碳原子的醇。
对于支链醇,需用数字表示支链所连接的碳原子位置编号。
例如,2-甲基丙醇中,甲基是连接在第二个碳原子上的。
2. 醚的命名醚的命名方法是按照它们两个有机基团的命名来表示。
首先列出较长的有机基团,接着写上“氧”,最后写上较短的有机基团。
例如,乙醚是由乙基和甲基组成的化合物。
3. 醛的命名醛的命名使用代表碳链的希腊字母加上“醛”二字。
对于直链醛,按照碳原子编号命名。
例如,甲醛是最简单的醛,它只含有一个碳原子和一个羰基。
对于支链醛,使用数字表示支链所连接的碳原子位置。
4. 酮的命名酮的命名方法与醛类似,但表示酮的代表碳链的希腊字母中间没有羰基,只有两个有机基团。
例如,丙酮是一种由两个甲基连接在一个碳上的酮。
二、羧酸的命名羧酸是一类含有羧基(–COOH)的化合物,羧基以羧的形式存在。
羧酸的命名方法根据它们的碳链数目和取代基的位置。
1. 直链羧酸的命名对于直链羧酸,先按照醇的命名方法表示碳链数量,接着在最末端加上“酸”一词。
例如,甲酸是一种只含有一个碳原子的羧酸,乙酸是含有两个碳原子的羧酸。
2. 支链羧酸的命名支链羧酸的命名需要使用数字表示支链所连接的碳原子位置,并在其前面列出支链的名称。
例如,3-甲基丙酸是一种具有三个碳原子并且甲基连接在第三个碳原子上的羧酸。
三、醇醚醛酮和羧酸的性质1. 醇醚醛酮的性质醇醚醛酮在化学反应中常表现出亲电性,与许多亲核试剂反应,如水合、氧化还原等。
有机化学——第7章醇酚醚
25
6、氧化脱氢反应
在有机化合物的分子中加入氧或脱去氢的反应都叫做氧化反应。
1) 伯醇氧化生成醛,醛进一步氧化生成酸。
CH3 CH2 CH2OH
K2CrO7-H2SO4
CH3 CH2CHO
[O]
CH3 CH2 COOH
2) 仲醇氧化生成酮,酮不易被继续氧化 。
H3 C CH OH CH3 [O] CH3 C O CH3
烯丙位 苯甲位 一级醇
}
醛
弱碱,反应条件温和, 不饱和键不受影响。
琼斯试剂 CrO3+稀H2SO4
费慈纳-莫法特试剂
醛(产率不高, 不用。)
醛(产率很高)
稀酸,反应条件温和, 不饱和键不受影响。 酸性 (H3PO4) , 其它基团不受影响。 碱性,可逆,分子内 双键不受影响。 28
反应机理 1oROH (SN2)
SN2
SN2
BrCH2CH3 +
2oROH , 3oROH (SN1)
SN2
SN1
(CH3)3C+ + HOPBr2
Br -
(CH3)3CBr
18
ROH + SOCl2
b.p. 79oC
RCl + SO2 + HCl
该反应的特点是:反应条件温 和,反应速率快,产率高,没 有副产物。
13
2、与氢卤酸反应
发生亲核取代反应,生成卤代烃和水,是制取卤代烃的重要方法。
R OH + HX
R X + H2O
氢卤酸的活性次序:HI > HBr > HCl; 醇的活性次序:烯丙式醇,苄基醇 > 3º 醇 > 2º 醇 > 1º 醇。 烯丙醇、叔醇、大多数仲醇及空间位阻大的伯醇,反应是按SN1
有机化学-醇
涉及 α H的反应 的 α R C H
::
O
碱 性 H 酸 性 羟基被取代
1,醇与活泼金属反应 , C2H5OH + Na ROH + Na C2H5ONa +
1 RONa + 2 H2
1 2
H2
ROH的反应活性 1°>2°> 3° 的反应活性: ° 的反应活性 ° °
2,与氢卤酸反应 , R — OH + HX R — X + H2O
(三)乙二醇 (HOCH2CH2OH) ) 无色粘稠有甜味的液体,沸点 无色粘稠有甜味的液体,沸点197.2℃,能与水,乙醇,丙 ℃ 能与水,乙醇, 酮等混溶.其水溶液的凝固点很低,可作为防冻剂和致冷剂. 酮等混溶.其水溶液的凝固点很低,可作为防冻剂和致冷剂. (四)丙三醇 俗称甘油
无色带有甜味的粘稠液体,沸点290℃,具有强烈的吸湿 无色带有甜味的粘稠液体,沸点 ℃ 性,可与水以任意比例混溶,其水溶液的凝固点很低. 可与水以任意比例混溶,其水溶液的凝固点很低. 甘油具有微弱的酸性,能与新制的氢氧化铜反应, 甘油具有微弱的酸性,能与新制的氢氧化铜反应,生成 能溶于水的深蓝色甘油铜.乙二醇也有类似的反应, 能溶于水的深蓝色甘油铜.乙二醇也有类似的反应,此反应 可用于鉴别多元醇. 可用于鉴别多元醇.
第十二章 有机化学基础 基础课时3 醇、酚、醛
解析:芳香醇是指分子里碳链上连接有苯环的醇,A错误;含碳碳双键,能发
生加成反应,含—OH能发生取代反应,B错误;异香天竺葵醇分子中含有饱
和碳原子,与之相连的原子具有类似甲烷四面体的结构,一定不会共面,所
以该分子中的所有碳原子不可能都处在同一平面上,C正确;含碳碳双键,
与溴发生加成反应,与高锰酸钾发生氧化反应,所以两者都能使酸性高锰
名称
甲醛
结构简式
HCHO .
颜色
无色 .
状态
气态
乙醛
CH3CHO .
无色 .
液态
气味
刺激性 .
气味
溶解性
易溶 于水
与水、乙
醇等互溶
2.醛的化学性质
醛类物质既有氧化性又有还原性,其氧化、还原关系为:醇
(1)氧化反应
①银镜反应:
CH3CHO+2Ag(NH3)2OH
CH3COONH4+3NH3+2Ag↓+H2O
D.苯甲醛分子中所有原子可能位于同一平面内
)。下列
解析:肉桂醛含碳碳双键可发生加成、加聚反应,含醛基可发生加成反应,
苯环上H可发生取代反应,苯甲醛含醛基可发生加成反应,苯环上H可发生
取代反应,苯甲醛也会发生聚合反应和氧化反应,A正确;含—CHO的物质可
与新制氢氧化铜反应生成红色沉淀,则可用新制氢氧化铜检验肉桂醛分子
酸钾溶液褪色,也能使溴的四氯化碳溶液褪色,D错误。
2.下列四种有机物的分子式均为 C4H10O。
①
②
③
④
(1)能被氧化成含相同碳原子数的醛的是
(2)能被氧化成酮的是
。
。
(3)能发生消去反应且生成两种产物的是
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
醚
醚是两个烃基通过氧原子连接起来的化合物,醚可以看作 是水分子中的两个氢原子被烃基取代后的生成物,也可以 看作是醇羟基中的氢原子被烃基取代后的生成物。烃基可 以是烷基、烯基或芳基。其通式为R-O-R(Ar)。醚分子 中的-O-叫做醚键。
醚可以分为单醚和混醚,即醚键两端连接的烃基相同(即 R=R)叫单醚,两个烃基不同(即R ≠R)叫混醚,醚键两 端连接的都是饱和烃基的叫饱和醚;两个烃基中有一个是 不饱和烃基的叫不饱和醚。醚键两端连接的都是脂肪烃基 的叫脂肪醚,其中有一段连接的是芳基的叫芳醚。如果烃 基与氧原子连接成环状的叫环醚,多氧的大环叫冠醚
O
O
O
O
O
15-冠-5
O
O
O
O
O
O
18-冠-6
制作PPT小组成员:黄禹、李敏、李 燕、张祯祯、何琪玥、彭迪。
饱和醇:
H2 C
HO
CH3
乙醇
CH3
HO
CH
C H2
异丁醇
CH3
OH
环己醇
不饱和醇:
H2 HC C OH
2-丙烯醇
H2 H2 HC C C C OH
H2 C OH
3-丁炔-1-醇
苯甲醇
(2)按烃基的结构不同,醇可分为脂肪醇和芳香醇。 例如:甲醇、乙醇、异丁醇都是脂肪醇,苯甲醇为芳香 醇。
(3)按烃基所连烃基碳原子的不同,醇可分为伯醇(一 级)、仲醇(二级)、叔醇(三级)
用途
酚
酚是重要的化工原料,可制造染料、药物、酚醛 树脂、胶粘剂等。
苯酚及其类似物可制做杀菌防腐剂。
邻苯二酚、对苯二酚可作显影剂 对人体的危害
酚侵入人体,会与细胞原浆中蛋白质结合形成不溶性 蛋白,使细胞失去活性。
酚对神经系统、泌尿系统、消化系统均有毒害作用。
酚
羟基直接和芳环相连的化合物为酚,通式为Ar-OH。酚可 按照分子中所含羟基的数目分为一元酚、二元酚、三元酚 等,二元以上的酚统称为多元酚。酚也可以按照分子中酚 羟基所连接的母体不同分为苯酚、萘酚等,苯酚是酚类最 简单也是最重要的酚。例如:
醇的用途:
1、用作燃料、溶剂、防冻液 2、重要的化工原料
醇
醇可以看做烃分子中的氢原子被羟基(-OH)取代后的产 物,一元醇也可看做水分子中的氢原子呗烃基(-R)所取 代。 (-OH)是醇的官能团,又称醇烃基。饱和一元醇的 通式是CnH2n+1OH,或简写为ROH。
1、按烃基的所连烃基的饱和程度不同,醇可分为饱和醇 和不饱和醇。例如:饱和醇
一元酚: OH OH
CH3
OH
苯酚
2-甲基苯酚
2-萘酚
二元酚: OH
OH
OH
OH
1,2-苯二酚
三元酚:
OH
OH
1,3-苯二酚
OH
OH
OH
1,4-苯二酚
OH
OH
1,2,4-苯三酚
HO
OH
HO
OH
1,3,5苯三酚
1,2,3-苯三酚
乙醚的用途:
主要用作油类、染料、生物碱、脂肪、天然 树脂、合成树脂、硝化纤维、碳氢化合物、 亚麻油、石油树脂,松香脂、香料、非硫化 橡胶等的优良溶剂.药物生产的萃取剂和医 疗上的麻醉剂.油污洁净剂.制造无烟火药.
H2 H2 H3C C C OH
伯醇(10)
H
H3C
C
CH3
OH
仲醇(20)
CH3H3CCCH3OH叔醇(30)
(4)按分子中所含烃基的数目不同,醇可分为一元醇和 多元醇(二元或二元以上的醇)
H2
H2 H2
H3C C OH HO C C OH
H2C OH
H C OH
CH2 OH
乙醇(一元醇) 乙二醇(二元醇) 丙三醇(三元醇)
脂肪醚:
H2
H2
H3C C O C CH3
乙醚
H2
H3C
O
C
C H
CH2
甲基烯丙基醚
芳香醚:
O
O CH3
二苯醚
苯甲醚
其中乙醚和二苯醚是单醚,甲基烯丙基醚和苯甲醚是混醚
环醚:
H2C CH2
O
环氧乙烷
冠醚:
O
O
O
O
12-冠-4
H H3C C CH2
O
1,2-环氧丙烷
CH2
CH2
H2C
CH2 O
1,4-环氧丁烷
