循环伏安法实验报告
循环伏安法判断电极过程实验报告

循环伏安法判断电极过程实验报告循环伏安法判断电极过程实验报告引言:循环伏安法是一种常用的电化学测试方法,用于研究电极材料的电化学行为。
本实验旨在通过循环伏安法测定电极材料的氧化还原反应特性,并分析实验结果,探讨其在电化学领域的应用前景。
实验材料与方法:实验所用材料为铂电极和铜电极,实验仪器为循环伏安仪。
首先,将铂电极和铜电极分别清洗并抛光,以确保电极表面的纯净度和光滑度。
然后,将电极插入电解质溶液中,并设置循环伏安仪的扫描速度和电位范围。
接下来,进行循环伏安法测试,记录电流与电位之间的关系曲线。
实验结果与分析:通过循环伏安法测试,我们得到了铂电极和铜电极的电流-电位曲线。
根据曲线的形状和特点,我们可以得到以下结论和分析:1. 铂电极的电流-电位曲线呈现出典型的双电极峰形状,其中一个峰对应氧化反应,另一个峰对应还原反应。
这说明铂电极在测试条件下发生了氧化还原反应,具有良好的电化学活性。
这一特性使得铂电极在催化剂、电池等领域有着广泛的应用前景。
2. 铜电极的电流-电位曲线呈现出单峰形状,没有出现双电极峰。
这说明铜电极在测试条件下只发生了一种氧化还原反应,具有较低的电化学活性。
然而,铜电极在电化学合成、电镀等领域仍然有着重要的应用,其特殊的电化学行为可以被利用。
3. 通过对电流-电位曲线的分析,我们可以得到电极反应的动力学参数,如峰电位、峰电流等。
这些参数可以进一步用于计算电极的表面积、电荷转移速率等重要参数,为电极材料的性能评价提供参考。
结论:本实验通过循环伏安法测试了铂电极和铜电极的电流-电位曲线,并对实验结果进行了分析。
通过曲线的形状和特征,我们可以了解电极材料的氧化还原反应特性和电化学活性。
这对于电化学领域的研究和应用具有重要意义。
循环伏安法作为一种常用的电化学测试方法,具有广泛的应用前景,可以用于研究各种电极材料的性能,并为相关领域的发展提供支持。
总结:循环伏安法是一种重要的电化学测试方法,通过测定电流-电位曲线,可以研究电极材料的氧化还原反应特性和电化学活性。
实验报告_96
三电化学实验循环伏安法测定铁氰化钾的电极反应过程及定量分析【实验目的】了解CHI660电化学工作站的基本操作。
掌握循环伏安方法的基本原理和实验技术。
了解循环伏安法的基本应用。
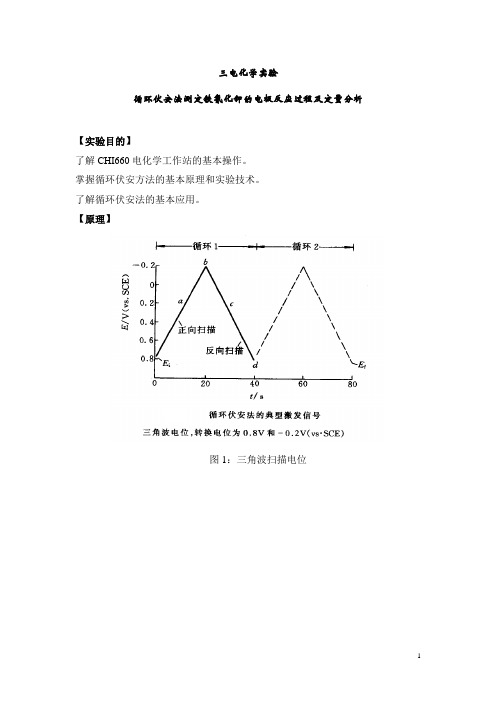
【原理】图1:三角波扫描电位图2:循环伏安曲线循环伏安法是在固定面积的工作电极和参比电极之间加上对称的三角波扫描电压,记录工作电极上得到的电流与施加电位的关系曲线,即循环伏安图,见图1。
在三角波的前半部分,工作电极上如发生氧化反应(阳极过程),记录到一个峰形的阳极波;而在三角波的后半部分,工作电极上发生则发生的是还原过程(阴极过程),记录得到一个峰形的还原波。
一次三角波电位扫描完成,电极上完成了一个氧化还原循环。
从循环伏安图的波形,阴阳极峰的峰电流的数值和比值,阴阳极峰的峰电位数值可判断电极反应的机理。
电极反应的可逆性主要取决于电极反应的速率常数k s 的大小,也与电位扫描的速率有关。
可逆性判据【仪器和试剂】1. CHI 660A 电化学系统,玻碳电极(d = 3mm )为工作电极,Ag/AgCl 电极为参i —E 曲线比电极,铂丝电极为辅助电极;2. 固体铁氰化钾、氯化钾;3. 250 mL 容量瓶、50 mL 烧杯、玻璃棒。
【实验步骤】1.铁氰化钾试液的配置配置1 mM的铁氰化钾溶液250 mL (1.0 M)。
2.将玻碳电极在抛光布上用氧化铝粉抛光,并用蒸馏水冲洗净。
3. 将三个电极安装于盛有铁氰化钾试液的电解池里。
4.开启电化学系统及计算机电源开关,启动CHI660操作程序,在Setup下拉菜单中(或快捷方式中)选择“Technique”,然后在“Technique”菜单选择“Cyclic V oltammetry”,按“OK”键返回主菜单,然后在“Parameters”菜单下选择参数。
Init E(V)-0.2High E(V)0.5Low E(V)-0.2Scan rate(V/s)xSweep Segments 2Quiet Time (sec) 2Sensitivity (A/V)按“OK”。
物理化学实验报告可逆体系的循环伏安研究自动保存的

物理化学试验汇报可逆体系旳循环伏安研究1.试验目旳(1)掌握循环伏安法研究电极过程旳基本原理。
(2)学习使用CHI660电化学综合分析仪。
(3)测定K3Fe(CN)6体系在不一样扫描速率时旳循环伏安图。
2.试验原理(1)循环伏安法概述:循环伏安法(Cyclic Voltammetry)旳基本原理是:根据研究体系旳性质, 选择电位扫描范围和扫描速率, 从选定旳起始电位开始扫描后, 研究电极旳电位按指定旳方向和速率随时间线性变化, 完毕所确定旳电位扫描范围抵达终止电位后, 会自动以同样旳扫描速率返回到起始电位。
在电位进行扫描旳同步, 同步测量研究电极旳电流响应, 所获得旳电流-电位曲线称为循环伏安曲线或循环伏安扫描图。
通过对循环伏安扫描图进行定性和定量分析, 可以确定电极上进行旳电极过程旳热力学可逆程度、得失电子数、与否伴随耦合化学反应及电极过程动力学参数, 从而确定或推断电极上所进行旳电化学过程旳机理。
(2)循环伏安扫描图:循环伏安法研究体系是由工作电极、参比电极、辅助电极构成旳三电极系统, 工作电极和参比电极构成电位测量, 工作电极和辅助电极构成旳回路测量电流。
工作电极可选用固态或液态电极, 如: 铂、金、玻璃石墨电极或悬汞、汞膜电极。
常用旳参比电极有: 饱和甘汞电极(SCE)、银-氯化银电极, 因此, 循环伏安曲线中旳电位值都是相对于参比电极而言。
辅助电极可选用固态旳惰性电极, 如: 铂丝或铂片电极、玻碳电极等。
电解池中旳电解液包括: 氧化还原体系(常用旳浓度范围: mmol/L)、支持电解质(浓度范围: mol/L)。
循环伏安测定措施是: 将CHI660电化学综合分析仪与研究体系连接, 选定电位扫描范围E1~E2和扫描速率υ, 从起始电位E1开始扫描, 电位按选定旳扫描速率呈线性变化从E1抵达E2, 然后持续反方向再扫描从E2回到E1, 如图C17.1所示, 电位随时间旳变化展现旳是等腰三角波信号。
最新实验4 循环伏安法

实验4循环伏安法华南师范大学实验报告学生姓名学号专业新能源材料与器件年级、班级 2014课程名称电化学实验实验项目循环伏安法测定电极反应参数实验类型□√验证□设计□综合实验时间2016/4 / 25实验指导老师吕东生实验评分一.实验目的1.了解循环伏安法的基本原理以及应用2.掌握循环伏安法的实验技术和有关参数的测定方法二.实验原理循环伏安法(CV)是重要的电分析化学研究方法之一。
该方法使用的仪器简单,操作方便,图谱解析直观,在电化学,无机化学,有机化学,生物化学等许多领域被广泛应用。
循环伏安法通常使用三电极系统,一支工作电极(被研究物质起反应的电极),一支参比电极,一支辅助(对)电极。
外加电压加在工作电极与辅助电极之间,反应电流通过工作电极与辅助电极。
对可逆电极反应(电荷交换速率很快,反应由扩散控制的过程),如一定条件下的VO2+/VO2+还原体系,当电压负向扫描时,VO2+在电极上还原,反应为:VO2++e-+2H+——VO2++H2O,得到一个还原峰。
当电极正向扫描时,VO2+在电极上氧化,反应为VO2++H2O- e-—— VO2++2H+,得到一个氧化峰。
循环伏安法能迅速提供电活性物质电极反应的可逆性,化学反应历程,电活性物质的吸附等许多信息。
三.实验器材CHI电化学工作站;玻碳电极;铂电极;Hg/Hg2SO4电极;0.1mol/L VO2++0.1mol/L VO2++3mol/L H2SO4,三口电解槽四.实验步骤1.准备好配置好的0.1mol/L VO2+,0.1mol/L VO2+,3mol/L H2SO4溶液。
2.预处理电极:1)用去离子水润湿玻碳电极,用砂纸打磨至玻碳电极的表面至光滑,用去离子水冲洗之后用滤纸擦干。
2)用去离子水润湿玻碳电极,用砂纸打磨至电极表面光滑,有光泽,用去离子水冲洗之后用滤纸擦干。
3.将溶液倒入三口槽之后连接好电极,打开CHI电化学工作站,选择“开路电压“方法,测定开路电压(0.3598V)4.选择“Cyclic Voltammetry Parameters”, Init E 为开路电压(0.3598V),Low E 设置为-2V,High E 设置为+2V, Final E 设置为开路电压(0.3598V),Sweep segments为5,扫描速率为20mV/s,循环次数2次。
常用电池材料的循环伏安法测试 实验报告
实验一常用电池材料的循环伏安法测试一.实验目的1.让学生认识电化学工作站的基本功能;2. 通过演示实验让学生更加深刻理解循环伏安法的测试方法;3.通过观察在循环伏安法测试过程中电解池内的变化,更加深刻理解循环伏安法的原理。
二.实验原理循环伏安法(Cyclic Voltammetry)是一种常用的动电位暂态电化学测量方法,是电极反应动力学、反应机理以及可逆性研究的重要手段之一,应用非常广泛。
何。
三.主要实验设备及样品1. 电化学工作站 1台;2. 电解池(包括三个电极) 1套;3. 超级电容器电极材料4. 3mol/L KOH溶液 30ml四.实验步骤1.准备好待测电极,电解液,组装好三电极电解池。
2.连接电化学工作站电源,并启动。
3. 将电化学工作站测试端和电解池中的工作电极,参比电极,辅助电极一一对应进行连接。
4. 打开电化学工作站工作菜单,点击进入测试任务选项,选择Cyclic Voltammetry项。
5. 在Cyclic Voltammetry菜单中输入测试起始电压,结束电压,扫描速度,循环次数等参数。
6. 点击“开始”进行测量。
7.测量结束后,将数据保存到指定位置。
五.注意事项1. 实验前需要检查电解池组装是否规范,有无漏液,或者短路情况;2. 连接三电极时,要一一对应。
3. 数据注意及时保存六. 数据记录及处理数据记录(取第二圈数据)Temperature('C): 25Begin Information: Cell InformationSurface Area: 1Density: 7.8Weight: 28Polarity: 0PolarityI: 0Corrosion Unit Type: 1Reference Type: 2Reference Potential: 0.241Reference User-Defined: 0Stern-Geary: 18End Information: Cell InformationBegin Experiment:Axes Type: 3End Experiment:Data Points: 604E(Volts) i(A/cm2) T(s) E(Volts) i(A/cm2) T(s)-1.29725E-03, 1.15674E-04, 4.8 -3.12376E-03, 7.04208E-05, 4.825 -5.13839E-03, 4.49166E-05, 4.85 -7.16281E-03, 2.72451E-05, 4.875 -9.18006E-03, 1.35282E-05, 4.9 -1.11773E-02, 1.72894E-06, 4.925 -1.31812E-02, -8.77842E-06, 4.95 -1.51924E-02, -1.80440E-05, 4.975 -1.72145E-02, -2.63783E-05, 5-1.92320E-02, -3.38648E-05, 5.025 -2.12576E-02, -4.10504E-05, 5.05 -2.32638E-02, -4.77369E-05, 5.075 -2.52801E-02, -5.39935E-05, 5.1 -2.72876E-02, -5.97033E-05, 5.125 -2.92965E-02, -6.49689E-05, 5.15 -3.13045E-02, -7.01868E-05, 5.175 -3.33251E-02, -7.51396E-05, 5.2 -3.53354E-02, -7.96554E-05, 5.225 -3.73440E-02, -8.37723E-05, 5.25 -3.93377E-02, -8.80374E-05, 5.275 -4.13716E-02, -9.31000E-05, 5.3 -4.33719E-02, -9.79358E-05, 5.325 -4.53954E-02, -1.02604E-04, 5.35 -4.74220E-02, -1.06148E-04, 5.375 -4.94213E-02, -1.08527E-04, 5.4 -5.14374E-02, -1.11235E-04, 5.425 -5.34525E-02, -1.15201E-04, 5.45 -5.54650E-02, -1.20622E-04, 5.475 -5.74557E-02, -1.25804E-04, 5.5 -5.94539E-02, -1.29147E-04, 5.525 -6.14807E-02, -1.30437E-04, 5.55 -6.35065E-02, -1.31034E-04, 5.575 -6.55128E-02, -1.33529E-04, 5.6 -6.75148E-02, -1.38900E-04, 5.625 -6.95103E-02, -1.46747E-04, 5.65 -7.15228E-02, -1.54890E-04, 5.675 -7.35317E-02, -1.58950E-04, 5.7 -7.55537E-02, -1.56703E-04, 5.725 -7.75602E-02, -1.51631E-04, 5.75 -7.95586E-02, -1.50664E-04, 5.775 -8.15959E-02, -1.56777E-04, 5.8 -8.36132E-02, -1.68896E-04, 5.825 -8.56436E-02, -1.83093E-04, 5.85 -8.76477E-02, -1.91786E-04, 5.875 -8.96556E-02, -1.90162E-04, 5.9 -9.16681E-02, -1.81073E-04, 5.925 -9.36699E-02, -1.73983E-04, 5.95 -9.56871E-02, -1.75475E-04, 5.975 -9.77032E-02, -1.85610E-04, 6-9.97106E-02, -1.99642E-04, 6.025 -1.01736E-01, -2.09359E-04, 6.05 -1.03757E-01, -2.10398E-04, 6.075 -1.05770E-01, -2.05230E-04, 6.1 -1.07773E-01, -2.00741E-04, 6.125 -1.09784E-01, -2.02637E-04, 6.15 -1.11792E-01, -2.10744E-04, 6.175 -1.13810E-01, -2.20225E-04, 6.2 -1.15806E-01, -2.24213E-04, 6.225 -1.17802E-01, -2.21851E-04, 6.25 -1.19821E-01, -2.19093E-04, 6.275 -1.21842E-01, -2.20991E-04, 6.3 -1.23849E-01, -2.29419E-04, 6.325 -1.25877E-01, -2.41204E-04, 6.35 -1.27888E-01, -2.50756E-04, 6.375 -1.29893E-01, -2.52991E-04, 6.4 -1.31912E-01, -2.49024E-04, 6.425 -1.33918E-01, -2.45863E-04, 6.45 -1.35921E-01, -2.47522E-04, 6.475 -1.37922E-01, -2.53552E-04, 6.5 -1.39941E-01, -2.60895E-04, 6.525 -1.41966E-01, -2.68033E-04, 6.55 -1.43975E-01, -2.75138E-04, 6.575 -1.45981E-01, -2.81994E-04, 6.6 -1.47974E-01, -2.87725E-04, 6.625 -1.49986E-01, -2.90349E-04, 6.65 -1.52008E-01, -2.89337E-04, 6.675-1.54023E-01, -2.87797E-04, 6.7 -1.56027E-01, -2.89994E-04, 6.725 -1.58050E-01, -2.98352E-04, 6.75 -1.60070E-01, -3.10672E-04, 6.775 -1.62094E-01, -3.23784E-04, 6.8 -1.64121E-01, -3.33251E-04, 6.825 -1.66112E-01, -3.36606E-04, 6.85 -1.68135E-01, -3.35388E-04, 6.875 -1.70142E-01, -3.33360E-04, 6.9 -1.72157E-01, -3.35245E-04, 6.925 -1.74162E-01, -3.43006E-04, 6.95 -1.76166E-01, -3.54898E-04, 6.975 -1.78188E-01, -3.67474E-04, 7-1.80203E-01, -3.76056E-04, 7.025 -1.82217E-01, -3.80116E-04, 7.05 -1.84221E-01, -3.82387E-04, 7.075 -1.86231E-01, -3.86506E-04, 7.1 -1.88239E-01, -3.92820E-04, 7.125 -1.90249E-01, -3.98432E-04, 7.15 -1.92269E-01, -4.02769E-04, 7.175 -1.94267E-01, -4.07363E-04, 7.2 -1.96278E-01, -4.15330E-04, 7.225 -1.98291E-01, -4.26563E-04, 7.25 -1.99572E-01, -4.15315E-04, 7.275 -1.98498E-01, -3.56641E-04, 7.3 -1.96478E-01, -3.06516E-04, 7.325 -1.94472E-01, -2.71245E-04, 7.35 -1.92470E-01, -2.45660E-04, 7.375 -1.90468E-01, -2.26902E-04, 7.4 -1.88451E-01, -2.10830E-04, 7.425 -1.86428E-01, -1.94007E-04, 7.45 -1.84431E-01, -1.76431E-04, 7.475 -1.82416E-01, -1.59545E-04, 7.5 -1.80389E-01, -1.45482E-04, 7.525 -1.78384E-01, -1.34088E-04, 7.55 -1.76385E-01, -1.23512E-04, 7.575 -1.74384E-01, -1.12250E-04, 7.6 -1.72371E-01, -9.98343E-05, 7.625 -1.70349E-01, -8.84433E-05, 7.65 -1.68324E-01, -7.88315E-05, 7.675 -1.66309E-01, -7.07480E-05, 7.7 -1.64311E-01, -6.27457E-05, 7.725 -1.62300E-01, -5.36377E-05, 7.75 -1.60277E-01, -4.46563E-05, 7.775 -1.58253E-01, -3.64773E-05, 7.8 -1.56225E-01, -2.93370E-05, 7.825 -1.54210E-01, -2.30565E-05, 7.85 -1.52216E-01, -1.64297E-05, 7.875 -1.50208E-01, -9.30140E-06, 7.9 -1.48189E-01, -2.19938E-06, 7.925 -1.46185E-01, 3.48415E-06, 7.95 -1.44180E-01, 8.58261E-06, 7.975 -1.42170E-01, 1.40273E-05, 8-1.40141E-01, 1.95318E-05, 8.025 -1.38127E-01, 2.51198E-05, 8.05 -1.36122E-01, 3.01728E-05, 8.075 -1.34107E-01, 3.50683E-05, 8.1 -1.32103E-01, 3.98205E-05, 8.125 -1.30100E-01, 4.42264E-05, 8.15 -1.28078E-01, 4.86085E-05, 8.175 -1.26082E-01, 5.26682E-05, 8.2 -1.24071E-01, 5.69308E-05, 8.225 -1.22043E-01, 6.11576E-05, 8.25 -1.20028E-01, 6.50836E-05, 8.275 -1.17999E-01, 6.88352E-05, 8.3 -1.15994E-01, 7.21760E-05, 8.325 -1.14001E-01, 7.55670E-05, 8.35 -1.11994E-01, 7.90536E-05, 8.375 -1.09984E-01, 8.24088E-05, 8.4 -1.07966E-01, 8.56087E-05, 8.425 -1.05963E-01, 8.84051E-05, 8.45 -1.03945E-01, 9.15335E-05, 8.475 -1.01935E-01, 9.45185E-05, 8.5 -9.99210E-02, 9.74295E-05, 8.525 -9.79097E-02, 1.00009E-04, 8.55 -9.58948E-02, 1.02444E-04, 8.575 -9.38916E-02, 1.05217E-04, 8.6 -9.18698E-02, 1.07880E-04, 8.625 -8.98583E-02, 1.10435E-04, 8.65 -8.78437E-02, 1.12629E-04, 8.675 -8.58405E-02, 1.14685E-04, 8.7 -8.38295E-02, 1.17085E-04, 8.725 -8.17965E-02, 1.19459E-04, 8.75 -7.97768E-02, 1.21790E-04, 8.775 -7.77620E-02, 1.23521E-04, 8.8 -7.57507E-02, 1.24966E-04, 8.825 -7.37477E-02, 1.26898E-04, 8.85 -7.17341E-02, 1.29381E-04, 8.875-6.97302E-02, 1.31961E-04, 8.9 -6.77210E-02, 1.33584E-04, 8.925 -6.57136E-02, 1.34456E-04, 8.95 -6.36961E-02, 1.35330E-04, 8.975 -6.16826E-02, 1.36868E-04, 9-5.96616E-02, 1.39626E-04, 9.025 -5.76670E-02, 1.42229E-04, 9.05 -5.56667E-02, 1.44307E-04, 9.075 -5.36540E-02, 1.45107E-04, 9.1 -5.16286E-02, 1.45228E-04, 9.125 -4.96018E-02, 1.46076E-04, 9.15 -4.76168E-02, 1.47745E-04, 9.175 -4.56091E-02, 1.50432E-04, 9.2 -4.35868E-02, 1.52631E-04, 9.225 -4.15638E-02, 1.53503E-04, 9.25 -3.95477E-02, 1.53202E-04, 9.275 -3.75341E-02, 1.53142E-04, 9.3 -3.55311E-02, 1.55124E-04, 9.325 -3.35125E-02, 1.58551E-04, 9.35 -3.14907E-02, 1.61465E-04, 9.375 -2.94863E-02, 1.61957E-04, 9.4 -2.75060E-02, 1.60283E-04, 9.425 -2.54828E-02, 1.59292E-04, 9.45 -2.34632E-02, 1.60357E-04, 9.475 -2.14543E-02, 1.63640E-04, 9.5 -1.94299E-02, 1.67363E-04, 9.525 -1.74186E-02, 1.69357E-04, 9.55 -1.54111E-02, 1.69130E-04, 9.575 -1.33996E-02, 1.67471E-04, 9.6 -1.13802E-02, 1.66886E-04, 9.625 -9.37224E-03, 1.67912E-04, 9.65 -7.36000E-03, 1.70121E-04, 9.675 -5.33892E-03, 1.72237E-04, 9.7 -3.32907E-03, 1.73133E-04, 9.725数据处理:七、实验结果的分析与讨论1、从实验数据中我们可以看出曲线没有测好,正常的CV曲线应是光滑曲线。
电化学实验报告Microsoft Word 文档

循环伏安法测定电极反应参数一、实验目的:1、学习循环伏安法测定电极反应参数的基本原理2、熟悉伏安法测定的实验技术3、学习固体电极表面的处理方法 二 实验原理:铁氰化钾离子[Fe(CN)6]3--亚铁氰化钾离子[Fe(CN)6]4-氧化还原电对的标准电极电位为[Fe(CN)6]3-+ e -= [Fe(CN)6]4- ; Ө= 0.36V(vs.NHE) 电极电位与电极表面活度的Nernst 方程式为: 峰电流与电极表面活性物质的浓度的Randles-Savcik 方程在一定扫描速率下,从起始电位( +0.8 V )负向扫描到转折电位( -0.2 V )的过程中,溶液中[Fe(CN)6]3-被还原而生成[Fe(CN)6]4-,因此产生还原电流;当正向扫描从转折电位(-0.2 V )变到原起始电位( +0.8 V )期间,在工作电极表面生成的[Fe(CN)6]4- 又被氧化生成[Fe(CN)6]3- ,从而产生氧化电流,终点又回到起始电位(+0.8V )而完成一次循环。
扫描速率可以从循环伏安法的典型激发信号图的斜率反映出来。
53/21/21/2p 2.6910i n ACD v =⨯0'Ox pa RedC RTInF C ϕϕ∆=+从循环伏安图可获得氧化峰电流ipa与还原峰电流ipc,氧化峰电位ψpa 与还原峰电位ψpc。
峰电流可表示为ip=6.25×105×n3/2Av1/2D1/2 c其中:ip为峰电流;n为电子转移数;D为扩散系数;v为电压扫描速度;A为电极面积;c为被测物质浓度。
可逆过程: △ϕp=ϕPa-ϕPc=56.5/n mV 而且iPa /iPc=1不可逆过程:△ϕp>56.5/n mV iPa /iPc<1使液相传质过程只受扩散控制的处理方法:为了使液相传质过程只受扩散控制,应在加入电解质和溶液处于静止下进行电解。
在0.1MNaCl溶液中[Fe(CN)6]的扩散系数为0.63×10-5cm.s-1;电子转移速率大,为可逆体系(1MNaCl溶液中,25℃时,标准反应速率常数为5.2×10-2cm·s-1)。
循环伏安法实验报告

循环伏安法实验报告一、实验目的1、学习并理解可逆电极反应的发生条件。
2、学习循环伏安法测定电极反应参数的基本原理和方法。
3、熟悉仪器的使用并根据所测数据验证并判断电极反应是否是可逆反应。
二、实验原理1、溶液中的电解质会离解出阴、阳离子,在外电场作用下发生定向移动产生电流使整个回路导通。
在电场的作用下,阴、阳离子分别向阳极、阴极移动,并在电极表面发生氧化或还原反应。
如果电极反应的速度足够快以致使得当离子刚移动到电极表面的反应区便立刻被反应掉,即电极表面总是处于缺少反应物的状态,这时电极表面的反应是可逆的,能量损失较小。
2、凡是能够测出电流电压关系获得I-U曲线的方法都可成为伏安法。
循环伏安法便是让电压做循环变化同时测出电流的改变的方法。
因此对于可逆的电极反应,所获得的曲线具有某种对称性,曲线会出现两个峰,电位差为:其中,Epa和Epc分别对应阴极和阳极峰电势。
对应的正向峰电流满足Randles-Savcik方程:其中ip为峰电流(A),n为电子转移数,A为电极面积(cm2),D为扩散系数(cm2/s),v1/2为扫描速度(V/s),c为浓度(mol/L)。
3、对本实验:该电极反应时可逆的。
用循环伏安法测量时,所得曲线会出现最大值和最小值,比较两个峰值所对应的电势之间的差值,若大小为0.056则说明该反应是可逆的;同时根据Randles-Savcik方程,ip 和v1/2 和浓度c都成直线关系,若两个峰电流比值接近于1,也可说明该电极反应是可逆的。
因此,本实验中,用循环伏安法测出峰电流、峰电位是关键。
三、实验试剂和仪器1、伏安仪,工作电极、辅助电极、参比电极,0.5ml移液管,50ml容量瓶,烧杯2、0.50mol/L氯化钾溶液,0.10mol/L铁氰化钾空白溶液,0.10mol/LH3PO4-KH2PO4溶液,0.10mol/L抗坏血酸溶液.四、实验步骤1、a)移取0.50mol/L氯化钾溶液20mL于50mL烧杯中,插入工作电极、对电极和参比电极,将对应的电极夹夹在电极接线上,设置好如下仪器参数:初始电位:0.60V; 开关电位1:0.60V; 开关点位2:0.0V电位增量:0.001V;扫描次数:1;等待时间:2电流灵敏度:10μA 滤波参数:50Hz; 放大倍率:1;b) 以50mV/s的扫描速度记录氯化钾空白溶液的循环伏安曲线并保存。
循环伏安法实验报告

循环伏安法实验报告循环伏安法实验报告引言:循环伏安法(Cyclic Voltammetry)是一种常用的电化学分析方法,通过测量电流与电位之间的关系,研究电化学反应的动力学和热力学性质。
本实验旨在通过循环伏安法对某种物质的电化学行为进行研究,并探讨其在实际应用中的潜力。
实验原理:循环伏安法是在电化学工作电极上施加一定的电位扫描范围,记录电流与电位的变化关系。
在实验中,我们使用了三电极系统,包括工作电极、参比电极和计时电极。
工作电极是我们感兴趣的物质所在的电极,参比电极用于提供一个稳定的参考电位,计时电极用于记录电位扫描的时间。
实验步骤:1. 准备工作:清洗和抛光电极,准备电解质溶液。
2. 装置搭建:将电解质溶液倒入电化学池中,将工作电极、参比电极和计时电极插入溶液中,连接电极和电位扫描仪。
3. 参数设置:设置扫描速率、起始电位和终止电位等参数。
4. 开始实验:启动电位扫描仪,进行电位扫描,记录电流与电位的变化关系。
5. 数据处理:根据实验结果,绘制循环伏安曲线,并进行数据分析。
实验结果与讨论:通过实验,我们得到了一组循环伏安曲线。
根据曲线的形状和特征,我们可以得到一些有关电化学反应的信息。
首先,我们可以通过观察峰值电位和峰电流的变化来确定物质的电化学反应类型。
对于可逆反应,峰电位与峰电流呈线性关系;对于不可逆反应,峰电位与峰电流之间存在一定的差异。
其次,我们可以通过计算峰电位之间的差值来确定电化学反应的电位差。
这个差值反映了反应的活化能,对于一些催化反应的研究具有重要意义。
另外,我们还可以通过循环伏安曲线的形状来研究电化学反应的速率。
如果曲线呈现出对称的波形,说明反应速率较快;如果曲线呈现出不对称的波形,说明反应速率较慢。
在实际应用中,循环伏安法可以用于研究电化学催化剂、电化学传感器和电化学能源等领域。
例如,通过研究某种催化剂的循环伏安曲线,可以评估其催化活性和稳定性,为催化剂的设计和合成提供依据。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
循环伏安法实验报告
在电化学研究中,循环伏安法是一种简单而又强大的研究方法。
通过循环伏安法,
可以对电极可逆性进行判断:反应是可逆的,则曲线上下对称,若反应不可逆,则曲线上下不对称;判断电极反应机理的判断:如电极吸附现象、电化学反应过程中产物等;更重要的是,循环伏安法能够用于实验中的定量分析。
接下来,运用实验数据来答疑解惑。
通常我们选择铁氰化钾体系(Fe(CN)63-/4-)对电化学行为中的可逆过程进行研究,它的氧化与还原峰对称,两峰的电流值相等,两峰电位差理论值为0.059V 0 通常电极表面的处理对该理论值有很大的影响,一般选择玻碳电极为工作电极、铂电极为对电极、饱和甘汞电极为参比电极。
选择AI2O3抛光粉将电极表面磨
光,然后在抛光机上抛成镜面,最后分别在1:1乙醇、1:1HNO3和蒸馏水中超
声波清洗15秒。
另外,溶液是否除氧,这个也是必须考虑的,我们选择通高纯
N2除O2 o在电解池中放入 5.00 x l0-4mol/LK3(内含0.20mol/L KNO3 ,作为支持电解质。
支持电解质的浓度实际上也对实验有影响,此处暂不考虑)。
插入工作电极、铂丝辅助电极和饱和甘汞电极。
设置电化学工作站中的参数,参数的设定需要不断的尝试,根据电化学工作站窗口显示的图形调节出合适的参数
图一的i-E曲线即为循环伏安图。
从循环伏安图中可以看出有两个峰电流和两个峰电位,阴极峰电流ipc,峰电位以Epc(jpc)表示;阳极峰电流ipa,峰电位以
Epa 表示。
ipc 或ipa 的下标的 a 代表 anode, c 代表 cathode。
我们可知道,
A Ep=Epa-Epc=56/n (单位:mV)( n为反应过程中的得失电子数),ipc与
ipa的比值越接近于1,则该体系的可逆程度就越高。
这是判断可逆体系的最直接的方法。
OOOOOOOOODOOAUOOOO 987<05
从321 12 3 4-^5-7- 从电化学工作站的工作界面,可以得出氧化峰电位为 Epa=227mV,峰电流为
ipa=-1.91 '10-6A ;还原峰电位是 Epc=170mV ,峰电流是 ipc=1.9 '10-6A 。
氧 化峰与还原峰电位差为57mV (直接比较横坐标数值即可),峰电流的比值为: ipa/ipc=1.005 "1。
由此可知,pH=7时,铁氰化钾体系(Fe (CN )63-/4-)的
电化学反应是一个可逆过程。
(通常都是借助该体系与其它体系进行比较,鉴别 电极的优劣以及反应可逆程度)。
接下来,我们来研究扫速与峰电流及峰电位的关系。
本实验室通常选择铁氰化钾 作为实验对象。
不同扫描速率 100、200、300、400mV/s ,分别记录从-200〜
+600mV 扫描的循环伏安图。
记录循环伏安曲线,观察峰电位和峰电流,判断
电极活性。
O
-
图二:不同扫描速率下铁氰化钾溶液的循环伏安曲线
将不同扫描速率100、200、300、400mV/s 的循环伏安曲线进行叠加,如上图 所示。
由图可知,随着扫描速度的增加,峰电流也增加。
且分别测量他们的峰数 据可以得到峰电流与扫描速度的关系。
根据电化学理论,对于扩散控制的电极过
程,峰电流ip 与扫描速度的二分之一次方呈正比关系,即ip 〜n1/2为一直线。
对于表面吸附控制的电极反应过程,峰电流 ip 与扫描速度呈正比关系,即ip 〜 n 为一直线。
v A
l/2ipa 关系曲线图
OCOOCDOS
Q.QOQaOOB
0 DOCX) 007
0 0000066
aaoacDos
0 DOM DM
0DCM0DO3
0 0000002
0 DGOOOOl
0 0.005 0.01 0015 D.D25 Q ・潞 O-Q35 0.04 0.045y = 0.00OQ2X 十 CLCKJEUI =0.98399 —
v A
l/2一一巾匚关系曲线图
0 0000005 0 0000007
O.DGM006
0 0000 DOS
ocwe-XM
0,0300 003
0 OOM 002
0 DOODOOl
G.0C5 0.01 0015 0.02 D.Q25 0.M 住 03 5 004
0. 妇折遽度y 七[rrwQ 1/2
图三:扫描速率与峰电流的关系曲线
以上详细介绍了循环伏安法在电化学应用中的定量分析, 如有不足,欢迎批评指 正。
最后,我针对微信留言区的问题来做解答。
一、 计算扩散系数时,n 是否取值?
答:物质的扩散系数表示它的扩散能力, 结合物理化学中谈到的菲克定律,扩散 系数是沿扩散方向,在单位时间每单位浓度梯度的条件下, 垂直通过单位面积所 扩散某物质的质量或摩尔数。
质量扩散系数D 和动量扩散系数v 及热量扩散系数 a 具有相同的单位(mT/s )或(cm A 2/s ),扩散系数的大小主要取决于扩散 物质和扩散介质的种类及其温度和压力。
二、 测试时,搅拌溶液对 CV 曲线有什么影响,峰电流与峰电位怎么变化?¥ = 0,00002x + 0.00001 心 0-9S505
答:搅拌溶液,对CV曲线是有很大的影响,人为搅拌破坏了界面扩散状态,能够及时补充电解质,使得氧化还原电流增大。
同时,溶液有波动,会影响曲线的稳定性。
但是,如果电极界面有气泡产生(比如析氢或者吸氧反应),电极界面会不断的析出气泡。
如果不搅拌,气泡就会吸附在电极表面,造成电极与溶液隔离,测出来的CV曲线就会不准,这个时候就可以通过搅拌来促进气泡快速逸出。
三、极化控制与扩散控制
极化可分为浓差极化和电化学极化。
浓差极化:可逆且快速的电极反应使电极表面液层内反应离子的浓度迅速降低
(或升高)---- > 电极表面与溶液本体之间的反应离子浓度不一样,形成一定
的浓度梯度----- > 产生浓差极化----- > 电极表面液层的离子浓度决定了电极
的电位,此电位偏离了电极的平衡电位,偏离值称为浓差过电位。
电化学极化电极的反应速度较慢———当电流密度较大时,引起电极上电荷的累积---------- > 产生电
化学极化一一极的电位取决于电极上所累积的电荷,此电位偏离了电极的平衡电位。
但是与反应活化能有关的极化都是不可消除。
扩散控制:它是化学反应速率因反应速度过快,无法由分子完成而是由扩散来控制的现象。
扩散控制是由于化学反应太快,扩散来不及供给反应以足够的分子所致。
