各种还原剂的还原能力
有机合成化学:第三章 还原反应

碳碳不饱和键: C4H9-CH=CH2
C4H9-CH2CH3
第三章 还原反应
炔烃: 2.锌与锌汞齐 ①锌的还原能力随介质的变化而变化,在弱酸性条件下:
②锌汞齐:锌汞齐(锌和汞的混合物)在酸性条件下的还原为 clemmesen还原:
第三章 还原反应
③在碱性介质中:
NaOH, Zn
Ph2CO
Ph2CHOH
CH3CHCH3 OH
HgCl2和Mg在苯中回流形成镁汞齐,它可还原酮得醇或片呐醇:
第三章 还原反应
5.铁: 铁是还原-NO2化合物的常用还原剂:
6.锡:锡及SnO2是还原-NO2化合物的常用还原剂,还原能 力比Fe强。
第三章 还原反应
二. 金属氢化物
1. LiAlH4:
LiAlH4的还原能力强,需要无质子溶剂,多为四氢呋喃,需要充分 干燥;反应物较大量时注意安全。
1.含硫还原剂: 1)硫化物还原剂:
第三章 还原反应
2)含氧硫化物:Na2SO3和NaHSO3:
PhN2Cl Na2SO3-H2O PhNHNH2
Na2S2O4+NaOH是较强还原剂,反应条件温和、快、收率高。
第三章 还原反应
2. 肼:
另一种合成方法?
C O NH2NH2
OHC N NH2
CH2
PhCH2CONH2
PhCH2CH2NH2 PhCH2CN
PhCH2CH2NH2
第三章 还原反应
⑷ NaBH4-H2SO4体系:此体系是还原氨基酸常用的方法:
3. 硼烷(BH3、B2H6) 一般为四氢呋喃溶液或二甲硫醚溶液。
第三章 还原反应
液体样品取样图 橡胶塞
第三章 还原反应
常见氧化剂和还原剂及氧化还原反应规律

常见氧化剂和还原剂及氧化还原反应的规律一、理清氧化还原反应概念及其关系1、氧化性和还原性(1)氧化性:物质中元素的原子或离子得到电子表现出来的性质,得电子能力越强,其氧化性越强,表现在反应中是化合价有降低趋势的一种表现能力(2)还原性:物质中元素的原子或离子失去电子表现出来的性质,失电子能力越强,其还原性越强,表现在反应中是化合价有升高趋势的一种表现能力2、氧化还原反应概念之间的联系口诀:升.(化合价升高)失.(失电子)氧.(被氧化,发生氧化反应)还.(作还原剂,本身具有还原性) 降.(化合价降低)得.(得电子)还.(被还原,发生还原反应)氧.(作氧化剂,本身具有氧化性) 3、中学化学常见的氧化剂和还原剂(1)常见的氧化剂①活泼性较强的非金属单质:如Cl2、O2②变价元素的高价态化合物:如KMnO4、FeCl3、HNO3③过氧化物:如Na2O2、H2O2④其他:如HClO、漂白粉、MnO2(2)常见的还原剂①活泼性较强的金属单质:如Al、Fe、Zn②某些非金属单质:如H2、S、C等③含有较低价态元素的化合物:如CO、SO2④其他:如浓盐酸、NH3【即学即练1】1、判断正误(正确的打“√”,错误的打“×”)(1)氧化剂得电子被氧化为还原产物()(2)非金属单质在反应中只作氧化剂()(3)在氧化还原反应中,金属单质作反应物时一定是还原剂()(4)还原剂失去电子具有氧化性()(5)碘化氢中碘为最低价,碘化氢只具有还原性()(6)阳离子只能得电子被还原,阴离子只能失电子被氧化()二、氧化性、还原性强弱的判断方法1、根据氧化还原反应方程式来判断氧化还原反应发生规律可用如下式子表示规律氧化性:氧化剂>氧化产物还原性:还原剂>还原产物特点:比什么性,找什么剂,产物之性小于剂【即学即练2】1、现有下列几个离子反应,下列有关性质的比较正确的是()①Cr2O2-7+14H++6Cl-===2Cr3++3Cl2↑+7H2O②2Fe2++Cl2===2Fe3++2Cl-③2Fe3++SO2+2H2O===2Fe2++SO2-4+4H+A.氧化性:Cr2O2-7>Cl2>Fe3+>SO2-4B.氧化性:Fe3+>SO2-4>Cl2>Cr2O2-7C.还原性:SO2<Fe2+<Cl-<Cr3+D.还原性:Cl->Cr3+>Fe2+>SO22、根据反应式:①2Fe3++2I-===2Fe2++I2,②Br2+2Fe2+===2Br-+2Fe3+,可判断离子的还原性从强到弱的顺序是()A.Br-、Fe2+、I-B.I-、Fe2+、Br-C.Br-、I-、Fe2+D.Fe2+、I-、Br-3、已知反应:①2FeCl3+2KI===2FeCl2+2KCl+I2,②2FeCl2+Cl2===2FeCl3,③I2+SO2+2H2O===H2SO4+2HI。
常见氧化剂还原剂和催化剂的应用
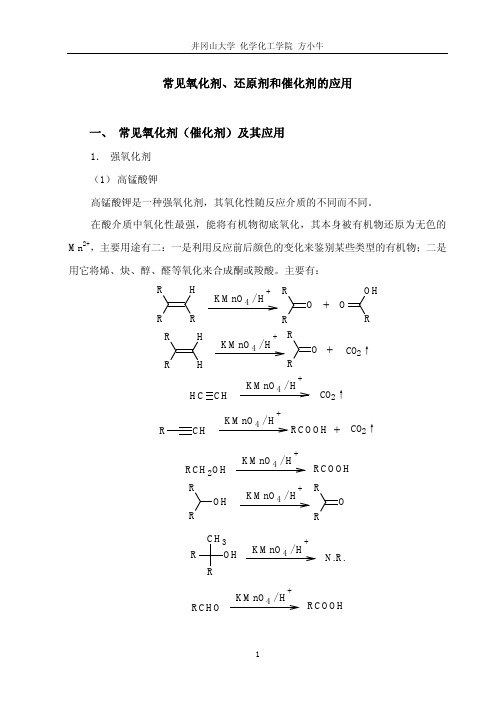
常见氧化剂、还原剂和催化剂的应用一、 常见氧化剂(催化剂)及其应用1. 强氧化剂 (1) 高锰酸钾高锰酸钾是一种强氧化剂,其氧化性随反应介质的不同而不同。
在酸介质中氧化性最强,能将有机物彻底氧化,其本身被有机物还原为无色的Mn 2+,主要用途有二:一是利用反应前后颜色的变化来鉴别某些类型的有机物;二是用它将烯、炔、醇、醛等氧化来合成酮或羧酸。
主要有:R H KMnO 4 / H+OROR OH+ R RHH KMnO 4 / H++O RRCO 2↑KMnO 4 / H+C H CH CO 2↑KMnO 4 / H++CHRCO 2↑RCOOHKMnO 4 / H+RCOOHRCH 2OHOH RRKMnO 4 / H+O RROHRR CH 3KMnO 4 / H+N.R.KMnO 4 / H+RCOOH RCHOKMnO 4 / H +N.R.RCOR' KMnO 4 / H+CO 2↑COOH COOH高锰酸钾在中性或碱性介质中的氧化性稍弱,在控制条件下可以将 π 键氧化而不断裂 σ 键,主要用于从烯烃制备邻二醇(反应的立体化学特征是顺式加成)。
四氧化锇的作用与此类似。
OO MnO(2) 重铬酸钾K 2Cr 2O 7 / H 2SO 4溶液的氧化性能与KMnO 4 / H +相似,用途也相似。
除用以氧化醇、醛等含氧衍生物外,主要用于将芳环氧化成醌。
如:O OCrO 3-H 2SO 4CrO 3-H 2SO 4OOK 2Cr 2O 7 / H 2SO 4RCH 2OHRCHO 边氧化边蒸馏(3) 稀硝酸稀硝酸具有强氧化性,它可以将芳环的侧链氧化和将醇氧化,如:Ar-CH 3Ar-COOH 稀HNO 3稀HNO 3OHO△HO 2C-(CH 2)4-CO 2H2. 温和氧化剂 (1) 二氧化锰MnO 2-H 2SO 4是一种中强氧化剂,可将甲苯氧化成苯甲醛:C 6H 5-CH 3C 6H 5-CHOMnO 2-H 2SO 4活性MnO 2则是一种温和的氧化剂,能将烯丙式醇氧化成醛而不影响C=C 双键:CH 3CH 3CH 3CHOMnO 2石油醚(2) 三氧化铬-吡啶络合物三氧化铬-吡啶络合物(CrO 3-C 5H 5N )又称为Sarett 试剂,是一种温和的氧化剂,能将醇(尤其是烯丙式的)氧化成为醛,而不影响其它基团。
纺织常用还原剂

纺织常用还原剂随着纺织工业的发展,还原剂在纺织过程中起着重要作用。
纺织常用还原剂是指在纺织工艺中用于还原染料、去除染料残留或改变纤维物质性质的化学物质。
本文将介绍几种常用的纺织还原剂及其应用。
一、硫酸亚铁硫酸亚铁是一种常用的还原剂,具有良好的还原性能。
它可以将染料还原为无色或不溶于水的物质,从而实现染料的去除或改变颜色的目的。
硫酸亚铁还可用于纺织品的漂白和脱色过程。
在染色过程中,硫酸亚铁可以与染料发生化学反应,使染料变成可溶于水的物质,从而实现染色的目的。
二、硫代硫酸钠硫代硫酸钠是一种常用的还原剂,具有较强的还原能力。
它可以将染料还原为无色或不溶于水的物质,从而实现染料的去除或改变颜色的目的。
硫代硫酸钠还可用于纺织品的漂白和脱色过程。
在染色过程中,硫代硫酸钠可以与染料发生化学反应,使染料变成可溶于水的物质,从而实现染色的目的。
三、亚硫酸钠亚硫酸钠是一种常用的还原剂,具有较强的还原能力。
它可以将染料还原为无色或不溶于水的物质,从而实现染料的去除或改变颜色的目的。
亚硫酸钠还可用于纺织品的漂白和脱色过程。
在染色过程中,亚硫酸钠可以与染料发生化学反应,使染料变成可溶于水的物质,从而实现染色的目的。
四、氢氧化钠氢氧化钠是一种常用的还原剂,具有较强的还原能力。
它可以将染料还原为无色或不溶于水的物质,从而实现染料的去除或改变颜色的目的。
氢氧化钠还可用于纺织品的漂白和脱色过程。
在染色过程中,氢氧化钠可以与染料发生化学反应,使染料变成可溶于水的物质,从而实现染色的目的。
五、硫酸硫酸是一种常用的还原剂,具有较强的还原能力。
它可以将染料还原为无色或不溶于水的物质,从而实现染料的去除或改变颜色的目的。
硫酸还可用于纺织品的漂白和脱色过程。
在染色过程中,硫酸可以与染料发生化学反应,使染料变成可溶于水的物质,从而实现染色的目的。
六、亚硫酸氢钠亚硫酸氢钠是一种常用的还原剂,具有较强的还原能力。
它可以将染料还原为无色或不溶于水的物质,从而实现染料的去除或改变颜色的目的。
还原剂

蓝绿色单斜结晶或颗粒。无气味。在干燥空气中风化。在潮湿空气中表面氧化成棕色的碱式硫酸铁。在56.6℃成为四水合物,在65℃时成为一水合物。溶于水,几乎不溶于乙醇。其水溶液冷时在空气中缓慢氧化,在热时较快氧化。加入碱或露光能加速其氧化。相对密度(d15)1.897。半数致死量(小鼠,经口)1520mG/kG。有刺激性。无水硫酸亚铁是白色粉末,含结晶水的是浅绿色晶体,晶体俗称“绿矾”,溶于水水溶液为浅绿色。用于色谱分析试剂。点滴分析测定铂、硒、亚硝酸盐和硝酸盐。还原剂。制造铁氧体。净水。聚合催化剂。照相制版。
应用在焊条及焊丝上,例如Mn,Si,Al,Ti及Zr等元素,可有效阻止氧的渗入使不致在焊道金属中形成氧化物及气孔。
种类
(1)活泼的金属单质(如 钠 , 镁 , 铝 ,等)
(2)某些非金属单质(如H2 、C等)、非金属阴离子及其化合物、低价金属离子(如Fe2+)等 还原剂实验举例:氢气还原氧化铜、氧化铁(H2+CuO=Cu+H2O ; 3H2+Fe2O3=2Fe+3H2O); 炭还原氧化铜(C+2CuO=2Cu+CO2); 一氧化碳还原氧化铜 、氧化铁(CO+CuO=Cu+CO2 ; 3CO+Fe2O3=2Fe+3CO2)
还原剂失去电子自身被氧化变成氧化产物,如用氢气还原氧化铜的反应,氢气失去电子被氧化变成水。还原剂在反应里表现 还原性 。还原能力强弱是还原剂失电子能力的强弱,如钠原子失电子数目比铝电子少,钠原子的还原能力比铝原子强。含有容易失去电子的元素的物质常用作还原剂,在分析具体反应时,常用元素化合价的升降进行判断:所含元素 化合价 升高的物质为还原剂。
氯化亚锡SnCl2,草酸,硼氢化钾KBH4,硼氢化钠NaBH4,
常用蛋白还原剂和变性剂

常用蛋白还原剂1.DTT中文名称为二硫苏糖醇(Dithiothreitol,简称为DTT),是苏糖醇的C-1及C-4位羟基置换成巯基的化合物。
在生化反应中用做还原剂,保护蛋白质或酶中的巯基不致氧化而失活。
也常用于还原蛋白质分子中的二硫键等。
DTT是一种小分子有机还原剂,化学式为C4H10O2S2。
其还原状态下为线性分子,被氧化后变为包含二硫键的六元环状结构。
二硫苏糖醇的名字衍生自苏糖(一种四碳单糖)。
DTT的异构体为二硫赤糖醇(DTE),即DTT的C3-差向异构体。
DTT也常常被用于蛋白质中二硫键的还原,可用于阻止蛋白质中的半胱氨酸之间所形成的蛋白质分子内或分子间二硫键。
但DTT往往无法还原包埋于蛋白质结构内部(溶剂不可及)的二硫键,这类二硫键的还原常常需要先将蛋白质变性(高温加热或加入变性剂,如6M 盐酸胍、8M 尿素或1% SDS)。
反之,根据DTT存在情况下,二硫键还原速度的不同,可以判断其包埋程度的深浅。
2.β-巯基乙醇英文名称:β-Mercaptoethanol,化学式:HOCH2CH2SH,分子量:78.13,是一种具有特殊臭味的无色透明液体,易燃、易溶于水和醇、醚等多种有机溶剂。
β-巯基乙醇(又称为2-巯基乙醇、1-硫代乙二醇、2-羟基乙硫醇、β-硫醇代乙醇)是一种有机化合物,其化学式为HOCH2CH2SH,英文通用缩写为ME或β-ME。
它兼具乙二醇(HOCH2CH2OH)和乙二硫醇(HSCH2CH2SH)的官能团,为挥发性液体,具有较强烈的刺激性气味。
β-ME通常用于二硫键的还原,可以作为生物学实验中的抗氧化剂。
它被广泛使用的原因是它的羟基使它能够溶解于水中,并且降低它的挥发性。
由于具有较低的蒸汽压,它的难闻的情况比起恶臭的硫醇要好得多。
2-巯基乙醇可以打开蛋白质中存在的二硫键:cysS-Scys+2HOCH2CH2SH→2cysSH+ HOCH2CH2S-SCH2CH2OH,二硫键被打开后可以使蛋白质的四级或三级结构被破坏。
5常用化学反应还原的方法及化学还原剂还原能力的比较.

C C
O C O C OH
C C
芳杂环
O O
C N
O C H
N
2、催化氢解 在催化剂存在下,含有碳杂键的有机物分子与氢气反应,发 生碳杂键断裂,分解成两部分氢化产物的反应叫做催化氢解。
催 化 剂 H2 C H + HZ
C Z
Z=X, O, S
优点:反应易于控制,产品纯度较高,收率较高,三废少,在工 业上应用广泛。 缺点:需要使用带压设备,安全措施要求高,催化剂的选择要求 严格。
还原剂用量:过量5~10% 还原温度:40~80℃ 实例:
OH NH 2
H2N OH NH 2
NO 2 NH 2
NO 2
NO 2
(一)化学还原法
4、金属复氢化合物还原 主要使用的是LiAlH4和NaBH4
特点:反应速度快,副反应少,选择性好, 产品收率高,反应条 件较温和。 主要应用:
4LiH + AlCl3 → LiAlH4 + 3LiCl
江苏高校品牌专业——石油化工技术
催化剂的类型 一般金属系:Ni、Cu、Mo、Cr、Fe、Pb 贵金属系:Pt、Pd、Rh、Ir、Os、Ru、Re
还原型纯金属粉: Pt、Pd、Ni等,如骨架镍、骨架铜
化合物型:氢氧化物、氧化物、硫化物如PtO2、MoS 载体型:如Pt/C、Pd/C
谢谢观看
课程:化工产品合成 知识点:常用化学反应还原的方法及化学还原剂还原能力的比较
课程:化工产品合成 知识点:常用化学反应还原的方法及化 学还原剂还原能力的比较
情境一:邻甲氧基苯胺的合成 任务一:邻甲氧基苯胺合成路线份析
江苏高校品牌专业——石油化工技术
常用化学反应还原的方法及化学还原剂还原能 力的比较
(完整版)金属纳米颗粒制备中的还原剂与修饰剂の总结,推荐文档

《金属纳米颗粒制备中的还原剂与修饰剂》总结一:金属纳米材料具有表面效应(比表面积大,表面原子多,表面原子可与其他原子结合稳定下来,使材料化学活性提高。
)和量子尺寸效应,因而有不同于体相材料的光学、电磁学、化学特性。
目前制备方法为液相合成(操作简便、成本低、产量高、颗粒单分散性好)。
——以金属盐或金属化合物为原料将其还原得到金属原子后聚集成金属纳米粒子。
而金属纳米粒子比表面积大、物化活性高、易氧化、易团聚,所以需要引入修饰剂来控制形貌、稳定或分散纳米颗粒。
液相还原法按照溶剂不同可分为有机溶剂合成法(结晶性好、单分散性好、形貌易控、不能直接用于生物体系、环境不友好)和水溶液合成法(水溶性、制备方法简单环保、成本低、颗粒大小不均一)。
按照还原手段不同可分为化学试剂还原法、辐射还原法、电化学还原法。
二:化学试剂还原法中常用的还原剂及其还原机理还原能力不同:1)强还原剂(硼氢化物、水合肼、氢气、四丁基硼氢化物),还原能力强、反应速率快、纳米颗粒多为球形或类球形、尺寸小。
2)弱还原剂(柠檬酸钠、酒石酸钾、胺类化合物、葡萄糖、抗坏血酸、次亚磷酸钠、亚磷酸钠、醇类化合物、醛类化合物、双氧水、DMF),反应体系一般需要加热。
例如多元羟基类化合物可做溶剂和还原剂,通过控制反应条件可制备多种形貌的材料。
柠檬酸钠、抗坏血酸做还原剂的同时可做保护剂。
(一)无机类还原剂1,硼氢化物(硼氢化钠钾、硼氢化四丁基铵TBAB),硼氢化钠化学性质活波与水反应放出氢气,与金属盐反应时所需浓度低。
2,氢化铝锂,还原性极强,应用不及硼氢化钠。
3,水合肼N2H4·H2O,应用广泛。
在碱性介质中为强还原剂。
4,双氧水。
5,有机金属化合物,二茂铁还原制备银纳米线。
6,氢气,(可以合成相当稳定无保护的可进一步修饰的银纳米颗粒。
),控制反应时间可以得到相当大尺寸跨度的纳米颗粒,进一步处理如过滤离心可以得到尺寸分布窄的颗粒。
7,次亚磷酸盐,弱还原剂,因为容易与氧气反应所以一般用3-4倍。
