晶体的常识
高中化学必修三 晶体常识
平行六 面体
3、特点:晶胞都是平 行六面体.晶胞在晶体 中是“无隙并置”而成 33 .
二﹑晶胞
1、描述晶体结构的基本单元叫做晶胞 2、三种典型立方晶体结构
简单立方
体心立方
面心立方
3、晶胞的特征: 晶胞都是平行六面体. 4、晶体和晶胞的关系:晶体可以看作是数量巨 大的晶胞“无隙并置”而成。
34
[思考] 铜晶体的一个晶胞中含有多少个铜原子?
[课堂练习]
1、下列物质有固定熔点的是 D A、水玻璃 B、塑料 C、玻璃 D、氯化钠 2、下列哪些性质不能区别晶体与玻璃体 A、各向异性 B、导电性 C、自范性 D、x-射线衍射实验
B
24
小结:晶体和非晶体的差异
固体 外观 具有规 则的几 何外形 微观结构 粒子在三 维空间周 期性有序 排列 自范性 各向 异性 各向 异性 熔点
晶体
有
固定
非晶 不具有规 粒子排列 体 则的几何 相对无序 外形
没有
各向 不固 同性 定
本质 微观粒子在三维空间是否呈现周期性有序排列 区别
25
金刚石晶体 结构示意图
26
二﹑晶胞 1.描述晶体结构的基本单元叫做晶胞
ห้องสมุดไป่ตู้
蜂巢与蜂室
铜晶体
铜晶胞
晶体与晶胞的关系可用蜂巢与峰室的关系比喻然而, 蜂巢是有形的,晶胞是无形的,是人为划定的。
1
体心:1
1
小结:立方晶胞中对质点的占有率
晶胞
立方体
顶角
棱上
面上
中心
1/8
1/4
1/2
1
顶角
棱上
面上
[思考] 铜晶体的一个晶胞中含有多少个铜原子?
第一节-晶体的常识

(3)晶体具有固定的熔点
二、晶胞
1.晶胞:描述晶体结构的基本单元 2.晶胞的结构
晶胞都是平行六面体,上下左右前后无隙 并置排列着无数晶胞。
3.确定晶胞化学式的方法——均摊法
顶点占1/8
面占1/2
棱占1/4
氯化钠晶体
一个Na+吸引多少个 Cl- ? 6个
一个Cl-吸引多少个 Na+ ? 6个 NaCl晶体中Na+ 与Cl-的离 子个数比为多少?︰1 1 与Na+等距离且距离最近的Na+为多少个? 12个
与Cl-等距离且距离最近的Cl-为多少个? 12个
二氧化碳结构模型
与二氧化碳距离最近且等距离的二氧化碳 有多少个? 12个
第一节 晶体的常识
一、晶体与非晶体
1.晶体与非晶体的本质差异 自范性 晶体 有(能自发呈现多 面体外形) 没有(不能自发呈 现多面体外形)
具有规则的几何外 形的固体叫晶体
微观结构 原子在三维空间 里呈周期性有序 排列 原子排列相对无 序
非晶 体
2.晶体呈现自范性的条件
晶体生长的速率适当Fra bibliotek3.得到晶体的一般条件
(1)熔融态物质凝固
固体粉末仍是晶体, 只因晶粒太小,肉眼 看不到而已
(2)气体物质凝华
(3)溶质从溶液中析出
4.晶体的特点
(1)晶体的外形和内部质点排列高度有序
晶体SiO2与非晶体SiO2的投影示意图
(2)晶体具有各向异性
在晶体中,不同晶面和晶面上原子排列的方式不 同和密度不同,它们之间结合力的大小也不相同, 这种性质叫做晶体的各向异性
晶体常识
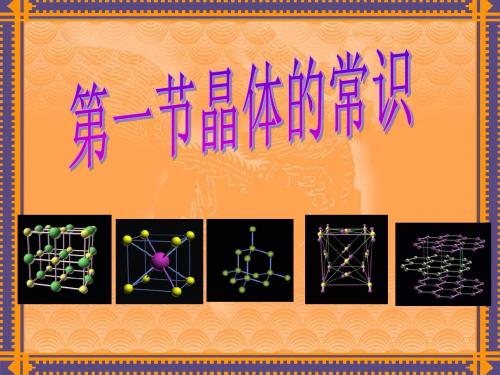
(4)X+中所有电子正好充满 K、L、M三个电子层,它与 N3-形成的晶体结构如图所 示。X的元素符号(Cu ), 与同一个N3-相连的X+有(6 ) 个。
黑球代表X+ 白球代表N3-
练习5高考链接
(2010江苏高考12分)乙炔是有机合成工业的一种 原料。工业上曾用CaC2与水反应生成乙炔。 (1)CaC2中C22-与O22+互为等电子体,O22+的电子 式可表示为____________; 1mol O22+中含有的键 数目为__________________。 (2)将乙炔通入[Cu(NH3)2]Cl溶液生成Cu2C2红 棕色沉淀。Cu+基态核外电子排布式为______。 (3)乙炔与氢氰酸反应可得丙烯腈(H2C=CH- C≡N)。丙烯腈分子中碳原子轨道杂化类型是 ____________;分子中处于同一直线上的原子数 目最多为____________。
④属于正四面体的分子构型。
CO2和SiO2的一些物理性质如下表所示, 通过比较试判断SiO2晶体是否属于分子晶 体。
二.原子晶体(共价晶体)
1.概念:相邻原子间以共价键相结合而形成空间立体
网状结构的晶体.
注:(1)构成微粒: 原子 (不存在单个分子或离子) (2)微粒之间的作用: 共价键 (3)气化或熔化时破坏的作用力:共价键
1
顶 角
棱上
面 上
小结:晶胞对质点的占有率
体心:
立方晶胞
1
面心: 1/2
棱边: 1/4
顶点: 1/8
学与问(教材64页: )
学与问答案: 2
作业:
2
8
8
教材P64 3:列式计算下图晶胞中各有多少个原子
《晶体的常识》课件

03
晶体生长与变化
晶体生长的过程
01
02
03
晶体生长的起点
晶体生长通常从一个小的 晶核开始,这个晶核可以 是自发形成的,也可以是 人为提供的。
晶体生长的机制
晶体通过吸附周围介质中 的离子、分子或原子,按 照一定的规律不断生长。
晶体生长的条件
晶体生长需要一定的温度 、压力、浓度等条件,这 些条件影响晶体的结构和 形态。
晶体的性质
01
02
03
04
晶体具有固定的熔点,加热至 熔点时开始融化,融化后温度
继续升高。
晶体具有各向异性,即在不同 方向上表现出不同的物理性质 ,如导热性、导电性和光学性
质等。
晶体具有一定的硬度,不同晶 体的硬度不同,与内部原子或
分子的排列密切相关。
晶体具有规则的几何外形,不 同晶体的外形也不同,与晶体 的内部结构和生长条件有关。
晶体分类
根据晶体内部结构特点,晶体可分为 金属晶体、离子晶体、共价晶体、分 子晶体等。
晶体性质
晶体具有固定的熔点、导电性、光学 性质等特点,在电子、光学、半导体 等领域有广泛应用。
晶体应用
晶体在生产生活中有广泛的应用,如 LED灯、太阳能电池、集成电路等。
对未来晶体研究的展望
新材料探索 随着科技的发展,人们对于新型 晶体材料的需求越来越高,未来 需要不断探索新的晶体材料,以 满足各种应用需求。
在生物组织工程中,通过控制生物材料的晶体结构, 可以调节细胞的生长和分化,促进组织的再生和修复
。
晶体在生物医学领域中也有着广泛的应用,如 药物研发、生物成像和生物组织工程等。
在生物成像中,晶体可以作为闪烁体,用于X射 线、CT等医学影像设备的探测器。
晶体结构与性质知识点

第三章晶体构造与性质第一节晶体的常识【知识点梳理】一、晶体与非晶体1、晶体与非晶体① 晶体:是内部微粒〔原子、离子或分子〕在空间按一定规律做周期性重复排列构成的物质。
② 非晶体:是内部的原子或分子的排列呈杂乱无章的分布状态的物质。
2、晶体的特征〔1〕晶体的根本性质晶体的根本性质是由晶体的周期性构造决定的。
① 自范性:a.晶体的自范性即晶体能自发的呈现多面体外形的性质。
b.“自发〞过程的实现,需要一定的条件。
晶体呈现自范性的条件之一是晶体生长的速率适当。
② 均一性:指晶体的化学组成、密度等性质在晶体中各局部都是一样的。
③ 各向异性:同一晶体构造中,在不同方向上质点排列一般是不一样的,因此,晶体的性质也随方向的不同而有所差异。
④ 对称性:晶体的外形与内部构造都具有特有的对称性。
在外形上,常有相等的对称性。
这种一样的性质在不同的方向或位置上做有规律的重复,这就是对称性。
晶体的格子构造本身就是质点重复规律的表达。
⑤ 最小内能:在一样的热力学条件下,晶体与同种物质非晶体固体、液体、气体相比拟,其内能最小。
⑥ 稳定性:晶体由于有最小内能,因而结晶状态是一个相对稳定的状态。
⑦ 有确定的熔点:给晶体加热,当温度升高到某温度便立即熔化。
⑧ 能使X射线产生衍射:当入射光的波长与光栅隙缝大小相当时,能产生光的衍射现象。
X射线的波长与晶体构造的周期大小相近,所以晶体是个理想的光栅,它能使X射线产生衍射。
利用这种性质人们建立了测定晶体构造的重要试验方法。
非晶体物质没有周期性构造,不能使X射线产生衍射,只有散射效应。
〔2〕晶体SiO2与非晶体SiO2的区别① 晶体SiO2有规那么的几何外形,而非晶体SiO2无规那么的几何外形。
② 晶体SiO2的外形与内部质点的排列高度有序,而非晶体SiO2内部质点排列无序。
③ 晶体SiO2具有固定的熔沸点,而非晶体SiO2无固定的熔沸点。
④ 晶体SiO2能使X射线产生衍射,而非晶体SiO2没有周期性构造,不能使X射线产生衍射,只有散射效应。
晶体常识

12 简单立方点阵
a=b=c,α=β=γ =90°
13 体心立方点阵
a=b=c,α=β=γ =90°
14 面心立方点阵
a=b=c,α=β=γ =90°
2.1.2 晶向指数和晶面指数
晶面(crystal plane)——晶体结构一系列原子所 构成的平面。
晶向(crystal directions)——通过晶体中任意两 个原子中心连成直线来表示晶体结构的空间的各个 方向。
距为负数则在指数上加一负号。
立方晶系中晶面指数示意图
立方晶系中两个晶面指数
晶面指数还有如下规律:
(1)某一晶面指数代表了在原点同一侧的一组想互平行且 无限大的晶面。
(2) 若晶面指数相同,但正负符号相反,则两晶面是以点 为对称中心,且相互平行的晶面。如(110)和(TT0)互相 平行。
(3) 凡晶面间距和晶面上原子分布完全相同,只是空间取 向 不 同 的 晶 面 , 可 归 为 同 一 晶 面 族 ( crystal plane group),用{hkl}表示。如{100}包括(100)、(010)、 (001)、(T00)、(0T0)、(00T)。
的
七大晶系和十四种空间格子
七大晶系:
1.三斜晶系(triclinic system):a≠b≠c,α≠β≠γ≠ 90° 2.单斜晶系(monoclinic system ):a≠b≠c,α=γ=90°≠β 3.正交(斜方)晶系(orthogonal system ):a≠b≠c,α=β=γ= 90° 4.四(正)方晶系(tetragonal system ):a=b ≠ c,α=β=γ=90° 5.立方晶系(cubic system ):a=b=c,α=β=γ=90° 6.六方晶系(hexagonal system ):a=b ≠ c,α=β=90°,γ=120° 7.菱形晶系(rhombohedral system):a=b=c, α=β=γ≠90°
晶体常识(公开课)
某些晶体具有优异的物理性能,如耐高温、高强度、高硬度 等,可用于制造建筑材料,如耐火砖、玻璃纤维等。
饰品和工艺品
水晶、宝石等晶体具有独特的色彩和光泽,常被加工成各种 饰品和工艺品,如项链、手链、吊坠、耳环等。
晶体在工业生产中的应用
电子工业
晶体是制造电子元件的重要材料,如晶体管、集成电路等,能够实现电子信号的放大、传输和处 理等功能。
在结晶过程中,原子或分子会自 发地按照一定的规律排列,形成 稳定的晶体结构。
结晶过程可以通过降温、蒸发、 化学反应等方式实现,形成的晶 体结构可以通过实验手段进行表 征和观察。
03
晶体的应用
晶体在日常生活中的应用
1 2
3
光学仪器
晶体是制造眼镜、望远镜、显微镜等光学仪器的重要材料, 能够使光线发生折射、反射、衍射等现象,用于矫正视力、 观察微观世界等。
化学研究
晶体可用于研究化学反应机理和催 化剂性能等方面,能够提供反应过 程中的物质结构和化学键信息。
材料科学
晶体可用于研究新型材料和制备技 术,如纳米材料、复合材料等,有 助于推动材料科学的发展和应用。
04
晶体合成与生长
晶体合成与生长的基本原理
晶体是由原子、离子或分子在空 间按一定规律重复排列而成的固
晶体中的胶原蛋白和透明质酸等成分具有保湿、抗衰老等功效,可用于 护肤品和美容品中,改善皮肤质量和延缓衰老。
某些晶体具有抗氧化、清除自由基等生物活性,有助于延缓衰老和维护 人体健康。
THANKS
能源工业
晶体可用于制造太阳能电池板、核反应堆控制棒等,能够实现光能、热能等能源的转换和利用。
航空航天
某些晶体具有优异的力学性能和耐高温性能,可用于制造飞机、火箭等航空航天器的零部件。
高中化学选修3:晶体结构与性质知识点总结
一.晶体常识
1 .晶体与非晶体比较
2 .获得晶体的三条途径
①熔融态物质凝固。
②气态物质冷却不经液态直接凝固(凝华)。
③溶质从溶液中析出。
3 .晶胞
晶胞是描述晶体结构的基本单元。
晶胞在晶体中的排列呈“无隙并置”。
4 .晶胞中微粒数的计算方法 —— 均摊 法
如某个粒子为n个晶胞所共有,则该粒子有1/n属于这个晶胞。
中学中常见的晶胞为立方晶胞
立方晶胞中微粒数的计算方法如下:
注意:在使用“均摊法”计算晶胞中粒子个数时要注意晶胞的形状
二.四种晶体的比较
晶体熔、沸点高低的比较方法
(1)不同类型晶体的熔、沸点高低一般规律:原子晶体>离子晶体>分子晶体。
金属晶体的熔、沸点差别很大,如钨、铂等熔、沸点很高,汞、铯等熔、沸点很低。
(2)原子晶体
由共价键形成的原子晶体中,原子半径小的键长短,键能大,晶体的熔、沸点高.如熔点:金刚石>碳化硅>硅
(3)离子晶体
一般地说,阴阳离子的电荷数越多,离子半径越小,则离子间的作用力就越强,相应的晶格能大,其晶体的熔、沸点就越高。
(4)分子晶体
①分子间作用力越大,物质的熔、沸点越高;具有氢键的分子晶体熔、沸点反常的高。
②组成和结构相似的分子晶体,相对分子质量越大,熔、沸点越高。
③组成和结构不相似的物质(相对分子质量接近),分子的极性越大,其熔、沸点越高。
④同分异构体,支链越多,熔、沸点越低。
(5)金属晶体
金属离子半径越小,离子电荷数越多,其金属键越强,金属熔、沸点就越高。
三.几种典型的晶体模型。
晶体结构与性质知识总结(完善)
3—1、晶体的常识一、晶体和非晶体1、概述——自然界中绝大多数物质是固体,固体分为和两大类.*自范性——晶体能自发地呈现多面体外形的性质.本质上,晶体的自范性是晶体中粒子在微观空间里呈现周期性有序排列的宏观表象。
*晶体不因颗粒大小而改变,许多固体粉末用肉眼看不到规则的晶体外形,但在显微镜下仍可看到。
* 晶体呈现自范性的条件之一是晶体生长的速率适当,熔融态物质凝固速率过快常得到粉末或没有规则外形的块状物。
*各向异性——晶体的许多物理性质如强度、热导性和光导性等存在各向异性即在各个方向上的性质是不同的二、晶胞1、定义——描述晶体结构的基本单元.2、特征-—(1)习惯采用的晶胞都是体,同种晶体所有的晶胞大小形状及内部的原子种类、个数和几何排列完全相同。
(2)整个晶体可以看作是数量巨大的晶胞“无隙并置"而成。
<1〉所谓“无隙”是指相邻晶胞之间没有任何间隙;〈2> 所谓“并置”是指所有晶胞都是平行排列的,取向相同。
3、确定晶胞所含粒子数和晶体的化学式——均摊法分析晶胞与粒子数值的关系(1)处于内部的粒子,属于晶胞,有几个算几个均属于某一晶胞。
(2)处于面上的粒子,同时为个晶胞共有,每个粒子有属于晶胞.(3)处于90度棱上的粒子,同时为个晶胞共有,每个粒子有属于晶胞.(4)处于90度顶点的粒子,同时为个晶胞共有,每个粒子有属于晶胞;处于60度垂面顶点的粒子,同时为个晶胞共有,每个粒子有属于晶胞;处于120度垂面顶点的粒子,同时为个晶胞共有,每个粒子有属于晶胞。
4、例举三、分类晶体根据组成粒子和粒子之间的作用分为分子晶体、原子晶体、金属晶体和离子晶体四种类型。
3—2、分子晶体和原子晶体一、分子晶体1、定义——只含分子的晶体。
2、组成粒子——。
3、存在作用—-组成粒子间的作用为(),多原子分子内部原子间的作用为。
*分子晶体中定含有分子间作用力,定含有共价键。
*分子间作用力于化学键.4、物理性质(1)熔沸点与硬度-—融化和变形只需要克服,所以熔沸点、硬度,部分分子晶体还可以升华。
高中化学-3-1晶体结构和性质(晶体常识)优秀课件
8×1/8+6×1/2+4=8
举一反三·分析 NaCl晶胞中氯离子和钠离子的个数
Cl- 顶点: ( 1/8 ) 8 = 1,
面心 : ( 1/2 ) 6 = 3 , 共4个
Na+ 棱上 : ( 1/4 ) 12 = 3 ,
体心 : 1 共4个
NaCl晶胞 ----Na+ ---- Cl-
2、推算晶体的化学式
思考与交流
1、某同学在网站上找到一张
玻璃的结构示意图,如右图,
这张图说明玻璃是不是晶体?
为什么?
玻璃的结构示意图
不是,质点不是有序排列
2、根据晶体的物理性质的各向异性的特点, 人们很容易识别用玻璃仿造的假宝石。你能列 举一些可能有效的方法鉴别假宝石吗?
(四)鉴别晶体和非晶体
〔1〕性质差异 ------外形、硬度、熔点、折光率等
顶点:1/8
位于顶点上的粒子为8个小立方体所共有,每个 立方体拥有其1/8
棱心:1/4
位于棱心上的离子为4个小立方体所 共有,每个立方体拥有其1/4
面心: 1/2
位于面心上的离子为2个小立方体所 共有,每个立方体拥有其1/2
体心:1
位于体心上的离子为1个小立方体所 有,每个立方体拥有1个离子
立方晶胞对粒子〔质点〕的占有率:
----求晶体中微粒个数最简整数比
例题1 下图所示是晶体结构中具有代表性的最小重 复单元(晶胞)的排列方式,其对应的化学式正确的
是(图中:O-X,●-Y,○-Z)( )C
XY
X3Y
XY3Z
例题 2 2001年报道的硼和镁形成的化合物刷新了金 属化合物超导温度的最高记录。如下图的是该化合物 的晶体结构单元:镁原子间形成正六棱柱,且棱柱的 上下底面还各有1个镁原子,6个硼原子位于棱柱内。 那么该化合物的化学式可表示为( )
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
【教学目标】
1、了解晶体的初步知识,知道晶体与非晶体的本质差异,学会识别晶体与非晶体的结构示意图。
2、知道晶胞的概念,了解晶胞与晶体的关系,学会通过分析晶胞得出晶体的组成。
3、培养空间想象能力和进一步认识“物质结构觉得物质性质”的客观规律。
【教学重点】晶体、晶胞的概念。
【教学难点】计算晶胞的化学式。
【教学过程】
你是否知道固体有晶体和非晶体之分?绝大多数常见的固体是晶体,只有如玻璃之类的物质属于非晶体(又称玻璃体)。
晶体与非晶体有什么本质的差异呢?今天我们开始学习…。
[板书] 第三章晶体的结构与性质
第一节晶体的常识
[投影]常见的晶体(或展示实物):
[思考]晶体规则的几何外型与组成晶体的微粒在空间的存在什么关系?
[投影]表3-1晶体与非晶体的本质差异
自范性微观结构
晶体有(能自发呈现多面体外型)原子在三维空间里呈周期性的有序排列
非晶体没有(不能自发呈现多面体外型)原子排列相对无序
[讲解] 晶体的自范性即晶体能白发地呈现多面体外形的性质。
所谓自发过程,即自动发生的过程。
不过,“自发”过程的实现,仍需要一定的条件。
例如,水能白发地从高处流向低处,但不打开拦截水流的闸门,水库里的水就不能下泻。
晶体呈现自范性的条件之一是晶体生长的速率适当。
熔融态物质冷却凝固,有时得到晶体,但凝固速率过快,常常只得到看不到多面体外形的粉末或没有规则外形的块状物。
[板书]1、晶体的自范性即晶体能白发地呈现多面体外形的性质。
[投影]图3-1天然水晶球里的玛瑙和水晶。
[讲述]最有趣的例子是天然的水晶球。
水晶球是岩浆里熔融态的si02侵入地壳内的空洞冷却形成的。
剖开水晶球,常见它的外层是看不到晶体外形的玛瑙,内层才是呈现晶体外形的水晶。
其实,玛瑙和水晶都是二氧化硅晶体,不同的是,玛瑙是熔融态si02快速冷却形成的,而水晶则是热液缓慢冷却形成的。
[讨论]除以上水晶和玛瑙是熔融态冷却得到的,根据所学知识还有那些方法得到晶体?
[汇报并板书]
2、得到晶体一般有三条途径:(1)熔融态物质凝固;(2)气态物质冷却不经液态直接凝固(凝华); (3)溶质从溶液中析出。
[投影]硫晶体、碘晶体、硫酸铜晶体的获得
[分组实验1] 在一个小烧杯里加入少量碘,用一个表面皿盖在小烧杯上,并在表面皿上加少量冷水。
把小烧杯放在石棉网上加热,观察实验现象。
[板书]3、晶体的自范性是晶体中粒子在微观空间里呈现周期性的有序排列的宏观表象。
[投影]晶体二氧化硅与非晶体二氧化硅微粒排列情况:
[自学]晶体特点自然段。
[提问]什么是晶体的各向异性?
[板书]4、晶体的特点①外形和内部质点排列的高度有序性;②各向异性;③晶体的熔点较固定。
[讲述]各向异性:像人们在观察大幅图案画时的视觉感受,对不同的图案画的感受当然是不同的,而对于同一幅图案画来说,由不同的方向审视时,也会产生不同的感受。
所以,晶体
的某些物理性质的各向异性同样反映了晶体内部质点排列的有序性,而且通过这些性质可以了解晶体的内部排列与结构的一些信息。
而非晶体则不具有物理性质各向异性的特点。
区分晶体和非晶体最可靠的科学方法是对固体进行x—射线衍射实验,有兴趣的同学可以阅读相关的科学视野。
[分组探讨]1、某同学在网站土找到一张玻璃的结构示意图如图3—5所示,这张图说明玻璃是不是晶体?为什么?
2.根据晶体物理性质的各向异性的特点,人们很容易识别用玻璃仿造的假宝石。
你能列举出一些可能有效的方法鉴别假宝石吗?
[汇报]1、不是,因为构成玻璃的微粒许多是孤立存在的,没有形成立体网状的结构。
2、(1)玻璃无固定的熔点(2)形状、硬度等。
……
[投影]蜂巢、铜晶体及铜晶胞模型:
[讲述] 为了描述晶体在微观空间里原子的排列,无须画出千千万万个原子,只需在晶体微观空间里取出一个基本单元即可。
这种描述晶体结构的基本单元叫做晶胞。
可用蜂巢和蜂室的关系比喻晶体和晶胞的关系。
[板书]二、晶胞
1、晶胞:描述晶体结构的基本单元。
[讲解]铜晶体的排列方式:整块晶体可以看作是数量巨大的晶胞“无隙并置”而成;所谓“无隙”,是指相邻晶胞之间没有任何间隙;所谓“并置”,是指所有晶胞都是平行排列的,取向相同。
[设问]铜晶胞含有4个铜原子,为什么不是14个?
[讲解] 我们在观察晶胞图时,千万不能忘记,晶胞只是晶体微观空间里的一个基本单元,在它的上下左右前后无隙并置地排列着无数晶胞,而且所有晶胞的形状及其内部的原子种类、个数及几何排列是完全相同的。
因而,晶胞的顶角原子是8个晶胞共用的,晶胞棱上的原子是4个晶胞共用的,晶胞面上的原于是两个晶胞共用的。
[投影]3-8学生探究晶胞占有原子的规律:
[学生汇报•板书]2、晶胞中原子占有率:顶点:1/8;边心:1/4;面心:1/2;体心:1。
[汇报•副板书]钠、锌晶胞都是:8×1/8+1=2;碘:(8×1/8+6×1/2)×2=8;金刚石:8×1/8+6×1/2+4=8。
[小结]略。
