原子吸收值与浓度的关系
分析化学-原子吸收与原子荧光

(二) Graphite furnace atomizer 石墨炉原子化器
1. 构造:
2. 分析过程
T
Time drying ashing atomizing cleaning
干燥-----灰化-----原子化----净化
paring with flame atomizer
原子化原理 原子化效率 试样体积 固体进样 灵敏度 重现性 背景干扰 分析速度
1. Hollow cathode lamp
2. Electrodeless discharge lamp
mg MX
400Pa Ar 3 ~ 8 cm
10mm
As, Cd, Pb, Se, Zn, Hg, P, Sn, Te, Tl…...
二、 原子化器 Atomizer
M(* 激发态原子)
MX(试样)
消除方法: 1. 稀释待测溶液 2. 采用标准加入法进行定量 3. 配制与试样溶液物理性质相似的
标准溶液
五、背景吸收 Background absorption
背景吸收包括: 分子吸收、光散射、火焰气体吸收。 背景吸收干扰主要存在于石墨炉原子化器。
减小背景吸收的方法:
减小进样量 增加灰化温度和灰化时间 增加石墨管内气流 采用基体改进剂 (增加共存物的挥发性或 降低待测元素的挥发性)
Characteristics: ☆Sensitivity ☆Selectivity ☆Analysis speed ☆Application:
determination of (metal) elements
§1. 原子吸收光谱法基本原理
一、原子吸收光谱的产生 1.原子能级跃迁 Atomic energy level transition
原子吸收分光光度法测定自来水中铜含量

点击“校正曲线和斜率重调参数设置”
选择“线性标准加入法”
设置好参数后点击“确定”
任务 原子吸收分光光度法测定自来水中铜含量
7、蒸馏水(空白)调0,标准空白测三下,吸未知样三次,再依次放入标样,等数据稳定后读数 三次,标样做完后用蒸馏水清洗。记录未知样浓度。
毛细管插入蒸馏水中
等待火焰呈现黄色
点击“调零”
打开风机
检查水封
装空心阴极灯
任务 原子吸收分光光度法测定自来水中铜含量
2、打开电脑软件,初始化通讯端口出现,打开主机电源(仪器自检),结束后按确定。仪器 参数设置(选择元素灯、灯架位置),结束后按”确定“。
打开电脑软件
初始化通讯端口
选择元素灯
选择灯架位置
任务 原子吸收分光光度法测定自来水中铜含量 3、设置:仪器参数设置,升降台设置,游标检测(前后226、上下98左右),结束后按”确定“。
• 2.2园林植物与温度
• 温度是植物生活所必须的重要环境因子, 植物的各种生理活动都是在一定温度范围内进 行的。园林植物的环境温度主要包括空气温度 和土壤温度。空气温度即是空气的冷热程度, 简称气温。土壤温度即是植物周围的土壤温度, 它是植物的重要生活因子之一,直接影响种子 的发芽和根系生长。要搞好园林生产,必须了 解和考虑空气和土壤的热状况。
• 2)水是某些代谢过程的原料
• 水是光合作用的原料,参与碳水化合物的
• 合成。水解反应和呼吸等过程中的许多反应, 也需要水分子直接参加。
• 3)水是植物体内代谢过程的介质
• 外界环境中的无机物和有机物都只能先溶 解在水中,才能被植物吸收。植物体内许多生 物化学反应都是在水介质中进行的。植物体内 的矿质元素和有机物也都是溶解在水中运往各 个部分。正是这种体内的液流活动,协调着体 内各部分的供求,从而把植物各个部分联系起 来,成为一个整体。
原子吸收光谱法
15:35
(2)谱线的热变宽 又称多普勒( Doppler )变宽,它是由于原子在空间 作热运动而引起的。
从物理学原理可知,从一个运动的原子发出的光,如果运动方 向离开观察者,则在观察者看来,其频率要比静止原子所发出 的光频率低,反之,如果原子向着观察者运动,则其频率要比 静止原子发出的光的频率高,这就是多普勒效应。 原子吸收分析法中,气体中的原子是处于无规则热运动中,有 的向着检测器方向运动,使光能增大,波长变短一点。有的背 向检测器运动,光能减弱,波长变长一点,一长一短,使谱线 变宽。这种频率分布和气体中原子的热运动的速度分布相符。
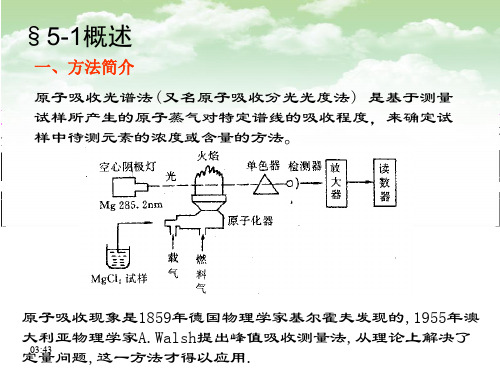
§5-1概述
一、方法简介 原子吸收光谱法 (又名原子吸收分光光度法 ) 是基于测量 试样所产生的原子蒸气对特定谱线的吸收程度,来确定试 样中待测元素的浓度或含量的方法。
原子吸收现象是1859年德国物理学家基尔霍夫发现的,1955年澳 大利亚物理学家A.Walsh提出峰值吸收测量法,从理论上解决了 15:35 定量问题,这一方法才得以应用.
1.14 10 4
从以上计算可以看出,与基态原子数相比,激发态原子数可忽 略不计。
即 N0≈N总
由此我们可以得到结论: (1)基态原子数等于总原子数。
15:35 ( 2)原子吸收法受温度影响不大。
二、吸收轮廓及变宽原因 1.吸收轮廓 从能级跃迁的观点看,吸收线与发射线应是一条严格的几何线, 但实际上是有一定宽度的。我们把吸收线或发射线的强度按频 率的分布叫谱线轮廓。如图5-2所示。 图中最大吸收对应的 频率 ν 0 称为峰值吸收
15:35
§5-2 原子吸收法的基本原理 一、基态原子数与火焰温度的关系 根据热力学原理,在一定温度下达到热力学平衡状态时,基态 和激发态的原子数之比与热力学温度的关系,可以用玻尔茨曼公 式描述: E j E0
原子吸收光谱法基本原理——原子吸收值与浓度的关系

《仪器分析测试技术》系列课程
原子吸收光谱法基本原理——原子吸收值与浓度的关系
《仪器分析测试技术》
在吸收轮廓内,将吸收系数对频率进行积分,称为积分吸收。
式中:e为电子电荷;m为电子质量;c为光速;N0为单位体积原子蒸气
中吸收辐射的基态原子数,即基态原子密度;f为振子强度。
积分吸收与单位体积基态原子数呈简单的线性关系。
峰值吸收是指基态原子蒸气对入射光中心频率线的吸收。
峰值吸收的大小以峰值吸收系数K0表示。
在一定实验条件下,基态原子蒸气的峰值吸收与待测元素的浓度N0成正比。
如何实现峰值吸光度的测量?
Ø
峰值吸收测量条件
锐线光源的必备条件
采用锐线光源实现。
锐线光源是能发射出谱线宽
度很窄的发射线的光源。
具备两个条件:发射线的中
心频率恰好与吸收线的中心频率(υ0)一致;发射线的
半宽度(△υe )远小于吸收线的半宽度(△υa )。
使用锐线光源时,吸光度与基态原子数之间的关系是:
式中:k为常数;L为光程;N0为基态原子数。
在原子吸收测量温度下,基态原子数近似等于总原子数。
因此,原子吸收测定的吸光度与吸收介质中原子总数N呈正比关系。
在原子化效率恒定、一定浓度范围及一定的吸光介质厚度的情况下,吸光度与待测元素的浓度成正比,
式中:K为与待测元素和分析条件有关的常数;
c为待测元素的浓度。
请大家查阅相关文献,寻找答案。
第十三章 原子吸收分光光度法

第十三章 原子吸收分光光度法原子吸收分光光度法(atomic absorption spectrophotometry, AAS)又称为原子吸收光谱法。
它是本世纪60年代后期迅速发展和广泛应用的一种较新型的仪器分析方法。
1955年澳大利亚物理学家瓦尔西(A.Walsh)在墨尔本展出了由他设计的第一台原子吸收分光光度计。
原子吸收分光光度法是基于物质产生的原子蒸气对特征谱线的吸收,测量原子蒸气对光辐射的吸收,即通过测量基态原子对特征谱线吸收程度,进行定量分析方法。
AAS法同UV法同属于吸收光谱法,因此在基本原理和仪器基本组成等方面有某些相似。
然而UV法研究对象是溶液中化合物的分子吸收,分子吸收的谱带较宽(在几nm以上),为带状吸收光谱,而原子吸收分光光度法研究对象是原子蒸气,气态原子吸收是窄带吸收,即线吸收,线宽仅为千分之几纳米(约为10-3 nm,极窄吸线)。
由于这种区别,致使它们的仪器装置和分析方法都有不同,由图比较,就可以看出二者的主要区别:(1)原子吸收分光光度法采用原子化器代替了吸收池;(2)用空心阴极灯(锐线光源)代替了连续光源;(3)单色器位置放在原子化系统之后。
原子吸收分光光度法具有如下特点:(1)灵敏度高。
火焰原子吸收法灵敏度高达可测到10-6~10-9g/ml,用无火焰原子吸收光谱法可没到10-9mg/ml数量级。
1(2)干扰少,且易于消除。
由于原子吸收光谱法是根据原子蒸气对待测元素特征谱线的吸收来进行分析的。
特别是同族元素,不需预分离,就可以直接测定。
(3)分析速度快。
由于选择性好,化学处理的测定操作简便。
近年来,微机的广泛应用以及智能化仪器的出现,与自动进样器、荧光显示屏的打印机等相配合,可在30分钟内分析50个样品中6元素。
(4)准确度高。
±1~3%误差。
(5)应用范围广。
几乎全部金属元素和一些准金属元素,目前用原子吸收分光光度法可测定元素已达70多种。
缺点:通常每个元素都要有自已的灯作为光源,因而附件多。
金属元素的原子吸收法原理

金属元素的原子吸收法原理
原子吸收法是一种光谱分析技术,用于测定金属元素的含量。
它的原理基于元素原子在特定波长的光照射下,原子吸收能量的量与元素的浓度成正比关系。
具体原理如下:
1. 原子化:通过加热样品或使用火焰、燃烧炉等将样品转化为气态原子。
有机物样品需要先进行矿化处理,将其转化为无机物。
2. 光谱测定:将样品送入光谱仪,使用特定波长的光照射样品。
光源通过一个窄缝发出的光束,经过物镜透镜聚焦后通过样品室中的样品,被光罩捕捉到一个条状窄缝的光栅上。
3. 吸收:样品中的金属原子在特定波长的光照射下会吸收特定的能量,导致吸收的光强度减弱。
吸收的光强度与金属元素的浓度成正比。
4. 比较:将吸收的光通过光电倍增管转化为电信号,经过放大、滤波等处理后与标准溶液进行比较。
5. 计算:通过校正曲线,将吸收的信号与标准曲线上的吸收值对应,从而确定样品中金属元素的浓度。
原子吸收法具有准确性高、灵敏度好等优点,在环境、食品、医药等领域有广泛
应用。
原子吸收法的定量关系式

原子吸收法的定量关系式原子吸收法是一种常被用于测定痕量金属元素浓度的分析技术。
它基于原子吸收光谱原理,并且可以利用光的吸收强度与待测物质浓度之间的定量关系。
在原子吸收法中,首先需要将样品原子化,通常使用火焰或电弧进行原子化。
然后,通过光源(通常是一束白炽灯或者是一束特定的原子发射光谱的气体放电灯)照射样品原子化的区域。
原子化的样品吸收光源中特定波长的光,发生吸收现象。
被吸收的光强度与待测金属元素的浓度成正比。
原子吸收光谱仪通常由光源、样品室和光探测器组成。
光源发出特定波长的光进入样品室,经过样品原子化后进入光探测器。
光探测器测量光的强度,然后将结果转化为浓度值。
原子吸收法的定量关系可以通过比尔—朗伯定律来描述。
比尔—朗伯定律表达了光强度与浓度之间的关系,它可以表示为下面的公式:A = εbc其中,A是吸光度,表示被吸收的光与入射光之间的相对减小,ε是摩尔吸光度(molar absorptivity),c是物质的浓度,b是光程(样品的物质相对于光来源之间的距离)。
摩尔吸光度(molar absorptivity)是一个常数,它表示每摩尔物质对特定波长的光的吸收程度。
是一个取决于特定物质和特定波长的常数。
根据比尔—朗伯定律,我们可以得到下面的关系式:c = A /( εb)也就是说,物质的浓度可以通过测量吸光度,并将其除以摩尔吸光度和光程来计算。
在实际应用中,我们通常使用标准曲线法来测量待测物质的浓度。
标准曲线法是通过测量一系列已知浓度的标准溶液的吸光度,构建吸光度与浓度之间的曲线。
然后,通过测量待测样品的吸光度,可以根据标准曲线找到相应的浓度值。
这样,我们可以通过测量吸光度来定量分析待测样品中金属元素的浓度。
总结起来,原子吸收法的定量关系式可以通过比尔—朗伯定律来描述。
比尔—朗伯定律表达了光强度与物质浓度之间的关系,其中摩尔吸光度是一个常数,表示每摩尔物质对特定波长的光的吸收程度。
实际应用中,我们通常使用标准曲线法来测量待测物质浓度,通过测量吸光度并利用标准曲线求取浓度值。
原子吸收分光光度法

1.溶液的配置 (1)1000 μg/mL 钙标准储备溶液 (2)1000 μg/mL镁标准储备溶液 (3)10 mg/mL 氯化镧溶液
2.仪器工作条件选择 单一变量,确定最佳流量、燃烧器高度。 3. 工作曲线法测镁含量 (1)配置系列标准镁溶液 (2)在选定的仪器条件下以去离子水为参比调零
测定各试样相应吸光度,并绘制A-c工作曲线。 (3)测水样,利用工作曲线求水中镁含量。 4.标准加入法测钙含量 (1)估测水中钙含量cx。 (2)测定水样+按比例加入标准溶液后的样品相应吸光度,并绘制A-c曲线。 (3)反向延长吸收曲线,使交于横轴,焦点数值为cx。
【注意事项】
1.仪器使用前需预热10~30 min,实验过程中注意原子吸收分光光度计使用的注意事项。 2.使用乙炔气体时注意流量与压力情况,严格按操作步骤进行,先通空气,后开乙炔。 3.水中钙镁含量较低,测定过程中应防止污染、挥发和吸收损失。 4.为保证结果准确性,试样的钙镁含量需提前初步测定,选择适宜的稀释体积及取样体积,尽
以标准加入法定量分析钙离子含量。由于自来水中含有铝、硫酸盐等化学干扰因素,测定时加入氯化 镧等金属盐可减少干扰因素对结果的影响。
【仪器和试剂】
仪器 原子吸收分光光度计(配乙炔-空气燃烧器),乙炔钢瓶,钙、镁元素空心阴极灯,容量瓶, 移液管。
试剂 自来水样品,去离子水,氧化镁(AR),无水碳酸钙(AR),氯化镧(光谱级),盐酸 (1 mol/L)。
• 整个画面是一幅静态立体风景画,观赏点是摄影和画家写生的地方。
赏景的方式
• 平视、仰视、俯视
• 平视—平静、深远、安宁,与地平线平行,如安静休息区 • 仰视—感染力强,压抑感,情绪紧张,休疗养地不宜 • 俯视:高处向远处看—鸟瞰画面,凌空感、深远;高处向下看—险峻、有征
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Iv=I0*exp(-Kvl) 2 e N0 f K d
mc
K d kN
局限性
K d mc N 0 f K d kN
由上式可见,积分吸收与基态原子数 成正比,与频率和测量条件无关。这 是原子吸收测量的重要基础,是一种 绝对测量方法;可惜的是原子吸收线 的半宽度太小(10-3 nm) ,没有这样高 的分辨率的单色仪 另一方面,即使用分辨率很高的单色 器,采用普通的分光光度法所用的连 续光源,获得0.x nm 纯度很高的光作 为原子吸收入射光,只有很少一部分 被吸收,1%左右。大部分通过,入射 光和透过光强度没有差别。
2
2 K0 Δν D
ln 2 π e N0 f π mc
可以看出,峰值吸收系数与基态原子总数N0成正比
峰值吸收:采用锐线光源,在中心频率附近很窄范围内 积分 Kν=K0
I0 A lg 0. 434KvL I 2 2 ln 2 e A 0.43 N 0 fL D mc
N0 N
原子吸收值与浓度的关系
谢文军 陆文宏 莫玉霖
一、积分吸收
原子吸收线,可以看成是基态原子对若干极 为精细、频率相差很小的光波吸收所产生的, 若求得相应波长的相应吸收系数,则可根据 吸收定律,求得吸收和-积分吸收。 根据经典色散理论,将原子蒸气对所有光波 的吸收进行积分得到:
吸收系数-频率关系曲线 e为电子电荷;N0为基态原子密度; m为电子质量,c为光速;f 为振子 强度,代表每个原子中能被入射光 激发的平均电子数,在一定条件下 对一定的元素,f 可视为一定值。
要点:
光源发射线的中心频率ν0e与吸收 线的中心频率ν0a一致
发射线的半宽度△ν0e远远小于吸 收线的半宽度△ν0a ,一般为吸收 线半宽度的1/5~1/10。
基本原理
只考虑多普勒展宽的条件下,峰值吸收系数K0 满足:
K0
2 Δ νD
ln 2 Kvdv π
e 2 K d mc N 0f
N C
原子吸收定量分析基本关系式
A Kc
即在一定条件下,峰值吸收处测得的吸光度与试样中被测元素的浓 度呈线性关系,这是原子吸收分光光度法的基础
谢谢大家
ቤተ መጻሕፍቲ ባይዱ e2
二、峰值吸收法
1955年沃尔什提出峰值吸收原理,解决了带宽和光强度的问 题,使原子吸收法成为现实。
Alan Walsh
(1916-1998)和 他的原子吸收 光谱仪在一起
在用锐线光源及温度不太高的火焰的条件下,峰值吸收系数与 火焰中待测元素基态原子的浓度存在着简单的线性关系,这样 N0值可由测定K0而得到,即峰值吸收法。
