火焰原子吸收光谱法测定水中的钙
火焰原子吸收光谱法对水中钙镁元素含量的测定

火焰原子吸收光谱法对水中钙镁元素含量的测定
1.原理
火焰原子吸收光谱法是一种常用的元素分析方法,对添加了特定试剂
的水样进行烧结分析,利用火焰中形成的原子,以吸收光谱的方式测定其
中元素的含量。
本实验以石英环氧环热烧结炉,采用火焰原子吸收光谱法,以选择性感应火焰来谱测定水中钙镁元素的含量。
2.原理描述
水样经加热烧结,在火焰中产生原子,其中的钙镁原子能够进行光离
子化(Ca+、Mg+),此时吸收器面上的检测元素中所具有的特征谱线就会
发出一定波长的回声,光谱仪可以发出特定波长的光,使检测元素产生特
征谱线,吸收器能够收集检测元素在特定波长的光线的反射,从而准确的
称出水样中的检测元素的含量。
3.分析流程
(1)将白细胞悬浮液以标定溶液的稀释倍数将其稀释至确定浓度;
(2)将稀释后的样品放入烧杯内,加入一定的烧剂,加热烧结;
(3)将火焰喷吐管插入环氧环,连接吸收器,开启光谱仪;
(4)在设定波长下测定样品中Ca、Mg吸收强度,确定测定值;
(5)重复上述步骤,完成对样品中Ca、Mg的测定;
(6)统计多次测定的结果,求出平均值,计算所求的检测元素含量。
火焰原子吸收光谱法测定水中钙
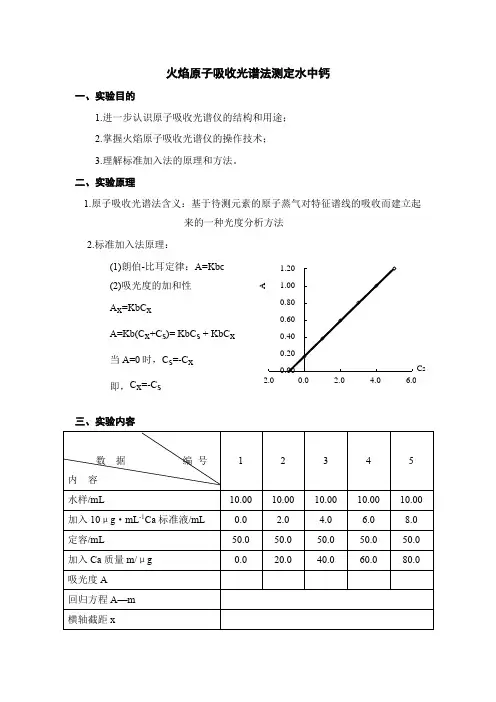
Ax=KbCx
A=Kb(Cx+Cs)= KbCs+KbCx
当A=0时,Cs=-Cx
即,Cx=-Cs
三、实验内容
数据编号
内容
1
2
3
4
5
水样/mL
10.00
10.00
10.00
10.00
10.00
加入10μg·mL-1Ca标准液/mL
0.0
2.0
4.0
6.0
8.0
定容/mL
50.0
50.0
检测器
硒光电池,将光信号转化为电信号
光电倍增管,将光信号转化为电信号
注:与可见分光光度计不同,原子吸收分光光度计单色器在吸收池后。
2.简述标准曲线法和标准加入法对样品溶液的要求有何不同?
标准曲线法适用于样品组成比较简单的批量样品的分析;标准加入法适用于样品组成比较复杂的少量样品的分析,标准加入法可以消除“基体效应”对测定结果的影响
火焰原子吸收光谱法测定水中钙
一、实验目的
1.进一步认识原子吸收光谱仪的结构和用途;
2.掌握火焰原子吸收光谱仪的操作技术;
3.理解标准加入法的原理和方法。
二、实验原理
1.原子吸收光谱法含义:基于待测元素的原子蒸气对特征谱线的吸收而建立起来的一种光度分析方法
2.标加入法原理:
(1)朗伯-比耳定律:A=Kbc
50.0
50.0
50.0
加入Ca质量m/μg
0.0
20.0
40.0
60.0
80.0
吸光度A
回归方程A—m
横轴截距x
水样含Ca量-x/μg
水样Ca含量:-x/10(μg·mL-1/mg·L-1/ppm)
火焰原子吸收光谱法对水中钙镁元素含量的测定

火焰原子吸收光谱法对水中钙镁元素含量的测定彭湘君,李银保,刘 霞,程庚金生,余 磊(赣南医学院药学系,江西 赣州 341000)摘 要:目的:本文运用火焰原子吸收光谱法直接测定了水中钙镁元素的含量。
方法:用1%KC l 和1%的SrC l 2作稀释剂,采用标准曲线法测定。
结果:所测定的水样中钙镁含量符合国家限定标准,采用此方法回收率分别为98.97%和99.39%。
结论:本方法简单、准确,结果令人满意。
关键词:火焰原子吸收光谱法;水;钙镁元素中图分类号:O 657.3 文献标识码:A 文章编号:1001-5779(2007)04-0502-02水中钙镁两种元素含量的多少是水质硬度形成的最重要的两种元素。
《生活饮用水卫生规范》[1]中规定,饮用水中以碳酸钙为总硬度的计算,其限度为450m g #l -1。
水中钙镁元素含量的测定方法主要有EDTA 络合滴定法,但该方法很难排除水中其它离子如铁、锰离子的干扰,共存离子对指示剂的指示终点也有影响。
特别是对于南方水样中水质硬度比较小的地区,往往难以使用滴定法得到准确的浓度。
本文使用火焰原子吸收法,对我校新校区井水中三份水样钙镁元素的含量进行了测定,并通过这两种元素含量计算出以碳酸钙为总硬度的水质硬度。
现报告如下。
1 材料与方法1.1 仪器 北京普析TAS -990型原子吸收分光光度计;C a 、M g 空心阴极灯[威格拉斯(北京)有限公司];N e w H um an UP 900(韩国)超纯水器(H u m an Corporati o n)。
1.2 试剂 氯化锶,优级纯(国药集团化学试剂有限公司);氯化钾,优级纯(汕头市光华化学厂)。
18.3M 8#c m 超纯水,用单蒸水经上述超纯水器制得。
Ca 、M g 标准溶液,含量均为1000L g #m l -1,国家标准物质研究中心。
1.3 实验步骤1.3.1 稀释剂及标准液的制备[2]Ca 、M g 稀释剂:称取1g 氯化锶和1g 氯化钾用超纯水配成混合溶液,作为钙镁标准溶液以及所测水样的稀释剂。
火焰原子吸收光谱法测定水中的钙实验报告

火焰原子吸收光谱法测定水中的钙实验报告《火焰原子吸收光谱法测定水中的钙实验报告》1. “嗨,小伙伴们!今天咱们要一起探索一个超酷的实验——火焰原子吸收光谱法测定水中的钙。
就像探险家在神秘的森林里寻找宝藏一样,咱们要在水里找到钙这个‘小宝藏’呢。
”例子:记得有一次我和小伙伴们去玩寻宝游戏,在公园里的小角落翻来翻去。
我兴奋地对小伙伴说:“这个小角落肯定有宝藏,就像水里肯定有钙一样。
”我们在树叶下、石头边找呀找,那股兴奋劲儿就和我现在对这个实验充满期待一样。
那时候,每一个可能藏着宝贝的地方都像是充满秘密的小世界,我们的眼睛里都闪着光。
这就像我现在对这个实验充满好奇,感觉自己即将开启一个神奇的探索之旅,充满了无限的憧憬。
2. “你们知道吗?钙在水中可不会轻易现身哦,就像躲猫猫的小朋友,得用特殊的方法把它找出来。
这火焰原子吸收光谱法就是我们的‘魔法工具’。
”例子:有天我和弟弟玩躲猫猫,弟弟躲在衣柜里,我怎么找都找不到。
后来我想了个办法,听声音才找到他。
这就像钙在水里藏着,我们得靠火焰原子吸收光谱法这个聪明的办法才能发现它。
我和弟弟从衣柜里出来后,他得意地说:“我躲得好吧。
”我笑着回答:“哼,下次我肯定一下子就找到你,就像我一定要学会用这个方法轻松找到钙一样。
”这个小游戏让我明白,不管找什么东西,都得有合适的方法,这在实验里也是很重要的道理呢。
3. “在做这个实验前,我就像个要上战场的小战士,既紧张又兴奋。
那些实验仪器就像是我的武器,得好好熟悉它们才行。
”例子:上次参加学校的跑步比赛,站在起跑线上的时候,我心里七上八下的。
旁边的同学鼓励我说:“别紧张,就把这当成平时跑步一样。
”我看着自己的运动鞋,就像看着即将帮我战斗的武器。
我对同学说:“我一定要跑好。
”在这个实验里,我看着那些仪器,也是这种感觉,我想把实验做好,就像想在比赛里跑出好成绩一样。
这让我知道,做新的事情时有点紧张是正常的,但只要准备好,就没什么可怕的。
火焰原子吸收光谱法测定自来水中的钙和镁

⽕焰原⼦吸收光谱法测定⾃来⽔中的钙和镁⽕焰原⼦吸收光谱法测定⾃来⽔中的铬⼀、实验⽬的1.学习原⼦吸收分光光度法的基本原理;2.了解原⼦吸收分光光度法的基本构造及其作⽤;3.掌握原⼦吸收光谱标准曲线法测定⾃来⽔中的铬的原理和⽅法。
⼆、实验原理原⼦吸收光谱法是基于待测元素的原⼦蒸汽对待测元素空⼼阴极灯发射的特征波长光的吸收作⽤⽽建⽴起来的分析⽅法。
吸光度与待测元素浓度的关系遵循朗伯-⽐尔定律,即A=lg(I0/I)=KLc。
原⼦吸收光谱仪的光路图:光信号源—试样系统—波长选择—分析信号转换—分析信号处理输出三、实验仪器及试剂原⼦吸收光谱仪,空⼼阴极灯(铬空⼼阴极灯),⽆油空⽓压缩机,⼄炔钢瓶,铬标准溶液、未知样—⾃来⽔中的铬四、实验内容及数据处理打开⽆油空⽓压缩机,再开⼄炔钢瓶阀,然后打开减压阀,最后再将电脑⼯作站和原⼦吸收光谱仪连接起来,准备测定。
(⼀)标准曲线法测定⾃来⽔中的铬1.设置原⼦吸收实验条件吸收波长:理论上为357.9nm,但本次实验实际⽤的波长为422.15nm灯电流:6mA 狭缝宽度:0.2nm 空⽓流量:8 L/min⼄炔流量:2.2 L/min 燃烧器⾼度:7mm2.仪器稳定,⽤蒸馏⽔清洗雾化器吸液管并作空⽩溶液扣除背景,将雾化器吸液管依次插⼊0.05、0.1、0.2、1.0、2.0、4.0、6.0µg/ml浓度标准系列溶液的容量瓶中,测定系列溶液的吸光度。
然后,⽤蒸馏⽔清洗雾化器吸液管,再测定⾃来⽔样品的吸光度。
3Ac /µg由上可知,当y=0.8032时,x=19.7923,即测定⾃来⽔中钙的浓度为19.7923µg/ml。
(⼆)标准加⼊法测定⾃来⽔中的镁1.设置的原⼦吸收实验条件吸收波长:理论上为284.2nm,但本次实验实际⽤的波长为284.57nm灯电流:6mA 狭缝宽度:0.2nm 空⽓流量:8 L/min⼄炔流量:1.8 L/min 燃烧器⾼度:7mm2.仪器稳定,⽤蒸馏⽔清洗雾化器吸液管并作空⽩溶液扣除背景,将雾化器吸液管依次插⼊0.2、0.3、0.4µg/ml浓度标准系列溶液的容量瓶中,测定系列溶液的吸光度。
火焰原子吸收法测定水中钙的方法验证报告

火焰原子吸收法测定水中钙的方法验证报告有限公司火焰原子吸收法测定水中钙的方法验证报告(实验室)摘要:本文通过对火焰原子吸收法测定水中的钙进行了一系列的验证分析,并利用数理统计方法,计算出方法的最低检出限为 0.013mg/L,标准曲线相关系数为0.9999,精密度为0.4,1.5%,回收率在98%,102%之间。
以上各项指标均符合方法的要求。
关键词:火焰原子吸收法;钙;方法验证一、原理将样品或消解处理过的样品直接吸入火焰,火焰中形成的原子对特征电磁辐射产生吸收,将测得的样品吸光度和标准溶液的吸光度进行比较,确定样品中被测元素的含量。
二、试剂1(硝酸(HNO):优级纯。
32(钙标准贮备液:1000mg/L(环境保护部标准样品研究所提供)。
(硝酸镧溶液:0.1g/mL 3三、仪器及其实验参数1(TAS-990原子吸收分光光度计,配有钙空心阴极灯。
2(波长422.7nm;灯电流 6 mA;狭缝 0.4 nm;测量方式峰高。
四、操作步骤1(试样的制备取10ml样品于50ml容量瓶中,加0.5ml硝酸和1ml硝酸镧溶液,用水稀释至标线,摇匀待测。
2(钙标准使用液配制准确移取1.0ml 1000mg/L的钙标准贮备液于100ml容量瓶中,用1%的硝酸溶液定容至刻度,得10.0mg/L的钙标准使用液。
3(钙校准溶液配制准确移取10.0mg/L的钙标准使用液0,0.50,1.00,2.00,3.00ml于100ml容量瓶中,各加2ml硝酸镧溶液,用1%的硝酸溶液定容至刻度,摇匀。
得0,0.05,0.10,0.20,0.30mg/L的工作曲线溶液。
4(加标回收溶液在100ml样品1和样品2中分别加入0.5ml及1ml浓度为10.0mg/L的钙标准使用液,再各加入2ml硝酸镧溶液和1mlHNO。
3五、测定将原子吸收分光光度计调整到最佳状态后,按照设定的仪器参数进行工作曲线系列及空白液、试样液、加标液的测定。
测定次数为3次。
实验7 原子吸收分光光度法测定自来水中的钙的含量
原子吸收分光光度法测定自来水中的钙的含量一、实验目的1、学习原子吸收分光光度法测定自来水中的钙的含量的基本原理;2、了解原子吸收分光光度计的基本结构和操作技术。
二、实验原理(一)火焰原子吸收分光光度法测定的基本原理是:由待测元素空心阴极灯做为光源,发射出待测元素的特征谱线,当它通过含有待测元素基态原子蒸汽的火焰时,部分被待测元素基态原子吸收而减弱,通过单色器(分光系统)和检测器测得吸光度。
在一定条件下待测元素浓度越大,吸光度越大,根据朗伯比尔定律A=KC,利用一定的定量方法,即可求得待测元素的含量。
(二)火焰原子吸收分光光度法测定的基本过程为:1、选择合适的测定条件主要包括:1)分析线;2)狭缝宽度;3)空心阴极灯工作电流(灯电流,负电压);4)原子化条件;火焰类型,燃气压力及流量,燃烧器高度,火焰高度及长度。
方法为:固定其他条件,只改变某一条件,作吸光度-条件曲线,一般选择吸光度最大处所对应的条件为最佳条件(可参考仪器计算机专家咨询系统F10)。
2、将测定参数及选好的最佳条件输入计算机3、标准曲线(工作曲线)的制作配制一系列浓度的待测元素的标准溶液,测定吸光度,制作吸光度-浓度标准曲线(工作曲线)(计算机自动生成)。
4、未知液浓度测定在同样条件下,测定样品吸光度,利用工作曲线求得未知液浓度(计算机自动生成)。
(三)WFX-1F2B2型火焰原子吸收分光光度计的基本结构1、光源:空心阴极灯2、原子化系统:气体控制单元(燃气压力及流量),雾化器,燃烧头及位置调节机构。
3、分光系统(单色器):波长,狭缝宽度;4、检测系统:光电转换、放大、检测;5、计算机控制系统:电子系统参数的自动控制和测量信息处理。
三、实验步骤1、溶液配制1)钙标准系列溶液配制配制8.0、16.0、24.0、32.0、40.0ug/ml钙标准系列溶液各50ml。
2)未知液配制取自来水50 ml2、仪器的准备1)事先调整好参数如:分析线422.7nm;狭缝宽度0.4nm;空心阴极灯工作电流(灯电流3.0mA,负电压300V);原子化条件;火焰类型空气-乙炔氧化焰,燃气压力及流量,燃烧器高度,火焰高度及长度,进样管,废液桶导管水封等,准备好测定溶液。
火焰原子吸收光谱法测定饮用水中的钙.
火焰原子吸收光谱法测定饮用水中的钙一、实验目的1、了解原子吸收光谱仪的结构及其操作。
2、掌握以原子吸收光谱法进行定量测定的方法。
3、学会优选测定条件方法。
二、实验要求1、要求同学利用所学原子吸收光谱知识,设计出用火焰原子化法对钙元素的测定,选择出最佳测试条件。
2、设计出合理的实验方法(两种)测定出饮用水中的钙。
三、实验条件1、仪器:日立180-80型原子吸收光谱仪;电子天平(0.0001g);空心阴极灯(钙);空气压缩机;容量瓶;移液管;烧杯。
2、试剂:盐酸(优级纯)溶液;HCl(1+2)。
钙标准溶液的配制:Ca=1000μg/mL准确称取2.5000g(优级纯)CaCO3(在120℃,烘2小时),加去离子水50mL,滴加HCl溶液(1+2)至CaCO3完全溶解,移入1000 mL容量瓶中,用去离子水稀释至刻度,摇匀。
工作液的配制:Ca=100μg/mL取10.0 mL钙的标准溶液于100 mL容量瓶中,用去离子水稀释至刻度,摇匀。
四、实验方案1、原理:根据原子吸收定量的原理 A=KLC2、定量的方法:标准曲线法采用标准曲线法定量饮用水中微量钙,以钙标准系列溶液浓度为横坐标,以对应的吸光度为纵坐标绘制一通过原点的直线,在相同的条件下测得样品溶液的吸光度值,进而计算出样品中钙的含量。
标准加入法以钙的标准加入法工作溶液测得吸光度,绘制工作曲线,将其外推,求得饮用水中钙的含量。
3、实验方法3.1系列标准溶液的配制取5个100 mL容量瓶,依次加入0.00, 1.00, 3.00,5.00 ,7.00mL100μg/mL钙的工作标准溶液,用去离子水稀释至刻度,摇匀。
此标准系列钙的浓度为0.00, 1.00, 3.00,5.00 ,7.00 μg/mL。
3. 2 未知样溶液的配制取20mL饮用水于100mL容量瓶中,用去离子水稀释至刻度,摇匀。
3.3标准加入法工作液的配制取4个100 mL容量瓶,各加入10 mL 未知试样溶液,然后依次加入0.0, 1.0, 3.0, 5.0 mL100μg/mL的钙工作标准溶液,用去离子水稀释至刻度,摇匀。
火焰原子吸收光谱法测定水中钙含量
⽕焰原⼦吸收光谱法测定⽔中钙含量实验⼀⽕焰原⼦吸收光谱法测定盐⽔中钙含量⼀、实验原理在使⽤锐线光源条件下,基态原⼦蒸汽对共振线的吸收,符合朗伯-⽐尔定律,即:A=lg(I0/I)=KLN0在试样原⼦化时,⽕焰温度低于3000 K时,对⼤多数元素来讲,原⼦蒸汽中基态原⼦的数⽬实际上⼗分接近原⼦总数。
在⼀定实验条件下,待测元素的原⼦总数⽬与该元素在试样中的浓度呈正⽐。
则:A= c⽤A-c标准曲线法或标准加⼊法,可以求算出元素的含量。
⼆、仪器与试剂1.仪器(1)TAS原⼦吸收分光光度计;钙空⼼阴极灯。
(2)10mL移液管⼀⽀(3)100 mL容量瓶六个(4)2mL移液管⼀⽀2.试剂(1)1.0g.L-1钙标准储备液(2)50 mg.L-1钙标准使⽤液(⽼师完成)配制⽤⽔均为⼆次蒸馏⽔。
三、实验步骤1.配制钙系列标准溶液:2.0,4.0,6.0,8.0,10.0 mg.L-1。
(⽼师完成)2.⼯作条件的设置(⽼师完成,具体实验过程中可能有变动,注意在实验过程中记录。
)(1)吸收线波长Ca 422.7 nm(2)空⼼阴极灯电流 4 mA(3)狭缝宽度0.1 mm(4)原⼦化器⾼度 6 mm(5)空⽓流量 4 L.min-1,⼄炔⽓流量1.2 L.min-13.钙的测定(1)样品(2 个/组):移10.00 mL⾃来⽔于50 mL容量瓶中,⽤蒸馏⽔稀释⾄刻度,摇匀。
(学⽣在C209⾷品分析实验室完成)(2)加标样品(2 个/组):移10.00 mL⾃来⽔样和2.50 mL50 mg.L-1钙标准使⽤液于50 mL容量瓶中,⽤蒸馏⽔稀释⾄刻度,摇匀。
(学⽣在C209⾷品分析实验室完成)(3)在最佳⼯作条件下,以蒸馏⽔为空⽩,测定钙系列标准溶液和⾃来⽔样、加标的⾃来⽔样吸光度A。
(⽼师和学⽣在B102共同完成)4.实验结束后,⽤蒸馏⽔喷洗原⼦化系统2 min,按关机程序关机。
最后关闭⼄炔钢瓶阀门,旋松⼄炔稳压阀,关闭空压机和通风机电源。
火焰原子吸收光谱法测定水中的钙、镁
目录
• 引言 • 实验材料与方法 • 结果与讨论 • 结论 • 参考文献
01 引言
目的和背景
目的
火焰原子吸收光谱法是一种常用的测定水中钙、镁的方法,通过该方法可以快 速、准确地测定水中的钙、镁含量,为水质监测和水处理提供依据。
背景
随着工业化和城市化的快速发展,水污染问题日益严重,尤其是重金属离子如 钙、镁等对水体的影响备受关注。因此,准确测定水中的钙、镁含量对于水处 理和水质监测具有重要意义。
对实验数据进行处理和分析,计算钙、镁 的含量和相关指标。
03 结果与讨论
实验结果
钙含量
实验测得水中钙的含量为12.5mg/L。
精密度
实验结果的相对标准偏差小于5%。
镁含量
实验测得水中镁的含量为3.8mg/L。
准确度
与标准参考物质对比,实验结果的准确度较 高。
结果分析
钙、镁含量分析
实验结果与预期相符,钙、镁含量均在正常范围内。
02 实验材料与方法
实验材料
01
02
03
钙标准溶液
用于制备标准曲线,浓度 为1000mg/L。
镁标准溶液
用于制备标准曲线,浓度 为1000mg/L。
实验用水
符合国家标准的去离子水, 用于稀释标准溶液和样品 处理。
实验设备
原子吸收光谱仪
配备钙、镁空心阴极灯, 具有自动进样器。
火焰原子化器
用于将样品中的钙、镁原 子化,以便进行光谱吸收 测量。
精密度分析
实验结果的精密度较高,说明实验操作和仪器性能稳 定。
准确度分析
与标准参考物质对比,实验结果的准确度较高,说明 实验操作和仪器性能可靠。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
火焰原子吸收光谱法测定水中的钙
一、实验目的
1 、加强理解火焰原子吸收光谱法的原理
2、掌握火焰原子吸收光谱仪的操作技术
3、熟悉原子吸收光谱法的应用
二、方法原理
原子吸收光谱法是基于气态基态原子外层的电子对共振线的吸收。
气态的基态原子数与物质的含量成正比。
当式样组成复杂,配制的标准溶液与式样组成之间差别较大时,常采用标准法,本实验就使用标准加入法,基本方法是在五个容量瓶中加等量的待测式样,分别加入不等量(倍增)的标准溶液,用适当溶剂稀释至一定体积后,依次测出它们的吸光度。
以加入标样的质量为横坐标,相应的吸光度为纵坐标,绘制标准工作曲线,图中横坐标与标准曲线正常的交点与原点的距离X即为容量瓶所含待测元素的质量,再通过计算求出式样的含量。
三、仪器与试剂
1、AA——6200双光束原子吸收分光光度计
2、钙空心阴极灯
3、钙标准溶液10.0Ul/Ml
4、50mL容量瓶5个
5、自来水式样
四、实验步骤
1、按下列数据,设置测量条件
(1)钙吸收线波长422.7nm;(2)、灯电流4ma
(3)、狭缝宽度0.1mm;(4)、空气流量7L/h (5)、乙炔流量 1.4L/min;(6)燃烧器高度8mm
2、吸取5份2.00mL式样溶液,分别置于50ml容量瓶中,各加入钙标准溶液0.00ml,1.00ml,2.00ml,3.00ml,4.00ml 于容量瓶中,以去离子水稀释至该度,配置成一组标准溶液。
3、以去离子水为空白,测定上述各溶液的吸光度。
五、结果处理
1、找出钙含量
2、结果换算。
