附录Ⅵ物质的标准摩尔生成焓标准摩尔生成吉
物质的标准摩尔生成焓

81.67
C6H6(l), 苯
49.028
124.597
172.35
135.77
C6H12(g), 环己烷
-123.14
31.92
298.51
106.27
C6H14(g), 正己烷
-167.19
-0.09
388.85
143.09
C6H14(l), 正己烷
-198.82
-4.08
295.89
63.07
296.59
87.82
C4H8(g), 2-甲基两烯
-16.90
58.17
293.70
89.12
C4H10(g), 正丁烷
-126.15
-17.02
310.23
97.45
C4H10(g), 异丁烷
-134.52
-20.79
294.75
96.82
C6H6(g), 苯
82.927
129.723
194.93
C6H5CH3(g),甲苯
49.999
122.388
319.86
103.76
C6H5CH3(l),甲苯
11.995
114.299
219.58
157.11
C6H4(CH2)(g)邻二甲苯
18.995
122.207
352.86
133.26
C6H4(CH3)2(l),邻二甲苯
-24.439
110.495
-88
-59
270.62
51.38
CHCl3(l), 氯仿
-131.8
-71.4
202.9
116.3
标准摩尔生成焓

标准摩尔生成焓在化学领域中,摩尔生成焓是一个非常重要的概念。
它是指在标准状态下,1摩尔物质生成的焓变化。
摩尔生成焓通常用于描述化学反应的热力学性质,对于理解反应的热力学过程和进行热力学计算都具有重要意义。
本文将对标准摩尔生成焓进行详细介绍,包括其定义、计算方法以及在化学反应中的应用。
首先,我们来看一下标准摩尔生成焓的定义。
标准状态是指物质处于1个大气压下,温度为298K(25摄氏度)的状态。
而摩尔生成焓是指在标准状态下,1摩尔物质生成的焓变化。
通常用ΔH表示,单位是千焦/摩尔(kJ/mol)。
当化学反应发生时,如果生成物的摩尔生成焓为正值,说明反应是放热的;如果生成物的摩尔生成焓为负值,说明反应是吸热的。
标准摩尔生成焓的计算方法通常是通过热化学实验得到的。
在实验中,通常会测量反应前后系统的焓变化,然后根据反应物的摩尔数,计算出摩尔生成焓的数值。
对于气态物质,可以利用燃烧实验来测定其摩尔生成焓;对于溶解反应,可以利用溶解热实验来测定其摩尔生成焓。
通过实验测定得到的摩尔生成焓可以用来推断化学反应的热力学性质,为化学工程和工业生产提供重要参考数据。
标准摩尔生成焓在化学反应中具有重要的应用价值。
首先,它可以用来预测反应的热力学性质。
通过计算反应物和生成物的摩尔生成焓之差,可以得到反应的焓变化,从而判断反应是放热的还是吸热的。
这对于工业生产中的热力学控制非常重要,可以帮助工程师设计和优化化学工艺流程。
其次,摩尔生成焓还可以用来计算反应的热平衡常数。
根据热力学原理,反应的热平衡常数与反应物和生成物的摩尔生成焓之间存在一定的关系,可以通过摩尔生成焓的数值来推导反应的热平衡常数,从而帮助理解和预测反应的平衡状态。
除此之外,标准摩尔生成焓还可以用来比较不同物质之间的热力学性质。
通过比较不同物质的摩尔生成焓,可以了解它们在化学反应中释放或吸收的热量大小,从而评估它们的热稳定性和热化学活性。
这对于材料科学和能源领域的研究具有重要意义,可以帮助科学家们设计新型材料和开发新型能源材料。
2.2.5 物质的标准摩尔生成焓

2. 化学反应的热效应、方向及限度2.2.5 物质的标准摩尔生成焓(Standard Enthalpy of Formation)生成反应:由单质生成化合物的反应。
CO(g) + 1/2O2(g) → CO2(g) ×C石(s) + O2(g) → CO2(g) √物质的标准摩尔生成焓:在标准条件下,温度为T K时,由稳定单质生成1mol某物质时的反应热,叫做该物质在T K时的标准摩尔生成焓。
用Δf H m㊀(T)表示,温度为298.15 K时,T可略去。
f: formation。
单位是kJ·mol-1。
稳定单质:指在298.15 K,101.3 kPa的条件下单质的最稳定状态。
如:H2(g)、Br2(l)、I2(s)、Cl2(g)、Hg(l)、C(石,s)、Cu(s) 等为稳定单质,C(金刚石,s)、Br2(g)、I2(g) 等不是稳定单质。
C(石,s)+O2(g) → CO2(g), Δr H m㊀=-393.5 kJ·mol-1 C(金,s)+O2(g) → CO2(g), Δr H m㊀=-395.4 kJ·mol-1 C(金,s) → C(石,s), Δr H m㊀=-1.9 kJ·mol-11H2(g)+ O2(g) H2O(g)2Δf H m㊀(H2O, g)= -241.82kJ·mol-1Δr H m㊀(稳定单质,T)=0稳定单质的标准摩尔生成焓等于0。
化学热力学规定:298.15 K时,水合H+的标准摩尔生成焓为零,即Δf H m㊀(H+, aq) = 0据此可以获得其他水合离子在298.15 K时的标准摩尔生成焓。
思考题以下反应的恒压反应热是否是标准摩尔生成焓(反应物和生成物都是标准态)?(1)2C(石墨,s) + O2(g)→2CO2(g)(2)CO(g) + 1/2O2(g)→CO2(g)。
附录Ⅵ 物质的标准摩尔生成焓、标准摩尔生成吉
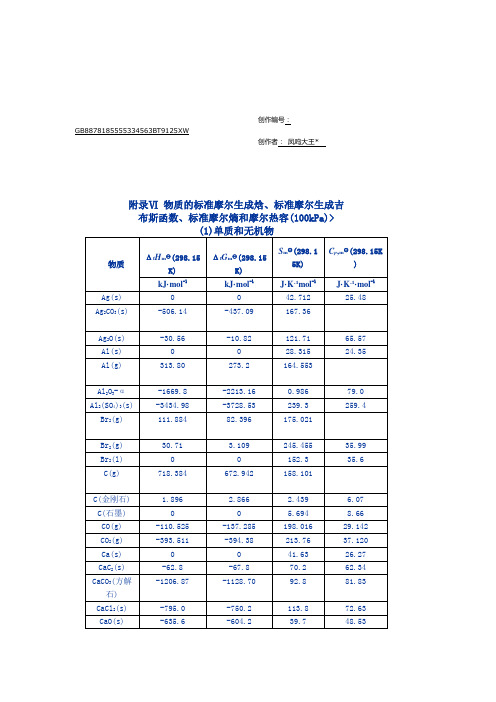
62.783
267.05
63.89
C3H6(g), 丙烷
-103.847
-23.391
270.02
73.51
C4H6(g), 1,3-丁二烯
110.16
150.74
278.85
79.54
C4H8(g), 1-丁烯
-0.13
71.60
305.71
85.65
C4H8(g), 顺-2-丁烯
-6.99
20.80
H2(g)
0
0
130.695
28.83
D2(g)
0
0
144.884
29.20
HBr(g)
-36.24
-53.22
198.60
29.12
HBr(aq)
-120.92
-102.80
80.71
HCl(g)
-92.311
-95.265
186.786
29.12
HCl(aq)
-167.44
-131.17
81.55
103.62
220.10
38.70
N2O4(g)
9.660
98.39
304.42
79.0
N2O5(g)
2ቤተ መጻሕፍቲ ባይዱ51
110.5
342.4
108.0
O(g)
247.521
230.095
161.063
21.93
O2(g)
0
0
205.138
29.37
O3(g)
142.3
163.45
237.7
38.15
-395.18
物质的标准摩尔生成焓

物质的标准摩尔生成焓物质的标准摩尔生成焓是指在标准状态下,1摩尔物质生成的焓变化量。
它是描述化学反应过程中物质生成或消耗热量的重要物理量,也是研究化学反应热力学性质的重要参数之一。
首先,我们来了解一下摩尔生成焓的概念。
摩尔生成焓是指在标准状态下,1摩尔物质生成时所吸收或释放的热量。
在化学反应中,物质的生成焓可以通过化学方程式中反应物和生成物的生成焓之差来计算。
生成焓为负值表示放热反应,反之为吸热反应。
摩尔生成焓的计算通常需要考虑反应物和生成物的物态、温度、压强等因素。
在标准状态下,摩尔生成焓的计算更为简单,因为标准状态下的物质状态已经确定,压强为1大气,温度为25摄氏度。
对于气体的标准摩尔生成焓,通常以气态的生成焓为基准。
例如,氧气的标准生成焓为0,氢气的标准生成焓也为0。
而对于液体和固体的标准摩尔生成焓,通常以元素的稳定形态为基准。
例如,钻石的标准生成焓为0,液态水的标准生成焓也为0。
在化学反应中,摩尔生成焓的大小可以反映出反应的放热或吸热程度。
放热反应的摩尔生成焓为负值,表示反应放出热量;吸热反应的摩尔生成焓为正值,表示反应吸收热量。
这对于工业生产和实验室研究都有重要意义。
在实际应用中,我们可以通过实验测定化学反应的放热或吸热量,从而计算出摩尔生成焓。
这对于确定化学反应的热力学性质、优化工艺条件等都具有重要意义。
总之,物质的标准摩尔生成焓是描述化学反应热力学性质的重要物理量,它可以反映出反应的放热或吸热程度,对于工业生产和实验室研究都具有重要意义。
通过实验测定和计算,我们可以准确地确定化学反应的热力学性质,为工程技术和科学研究提供重要参考。
希望本文对您了解物质的标准摩尔生成焓有所帮助,谢谢阅读!。
标准摩尔生成焓

3
1.化学反应的自发过程和熵变 (1)自发过程
自发过程和非自发过程都是可以进行的,区别在 于自发过程可以自动进行,而非自发过程需要借 助外力才能进行。
在条件变化时,自发过程和非自发过程可以发生 转化。如CaCO3的分解反应,在常温下为非自发 过程,而在910 ℃时,该反应可以自发进行。在 一定条件下,自发过程能一直进行到其变化的最 大程度,即化学平衡状态。
标准摩尔生成焓
4
1.化学反应的自发过程和熵变 (1)自发过程
焓变判据:
很多自发反应,其过程中都伴随有能量 放出,即有使物质体系能量降至最低的 趋势,如H2和O2化合生成水的过程。因此, 早在19世纪,人们就试图用反应的焓变 作为自发过程的判据,m 认为在恒温恒压 下, ∆rHӨ <0 时,过程能自发进行,反 之不能。
表达式中Pi 为该气体分压,当反应中各物质均处于标准 态时,Q=1,则∆rGm = ∆rGmӨ ,可用∆rGmӨ 来判断反应 的方向。但多数反应处于非标准态, ∆rGm ≠ ∆rGmӨ ,此 时,只有当I∆rGmӨI >40kJ·mol−1 时,才可以用∆rGmӨ判定 反应方向。 ∆rGmӨ < −40kJ·mol−1 一般反应能够正向自发进行 ∆rGmӨ > 40kJ·mol−1 一般正向非自发、逆向自发进行过程
标准摩尔生成焓
13
吉布斯(Gibbs)自由能
(1)Gibbs自由能
G =H─TS
上式中,H、T、S均为状态函数, 所以G也为状态函数,上式称吉布斯 函数或吉布斯自由能。
标准摩尔生成焓
14
吉布斯(Gibbs)自由能
(1)Gibbs自由能
G =H─TS
∆G=∆H─T∆S
附录Ⅵ物质地实用标准摩尔生成焓、实用标准摩尔生成吉
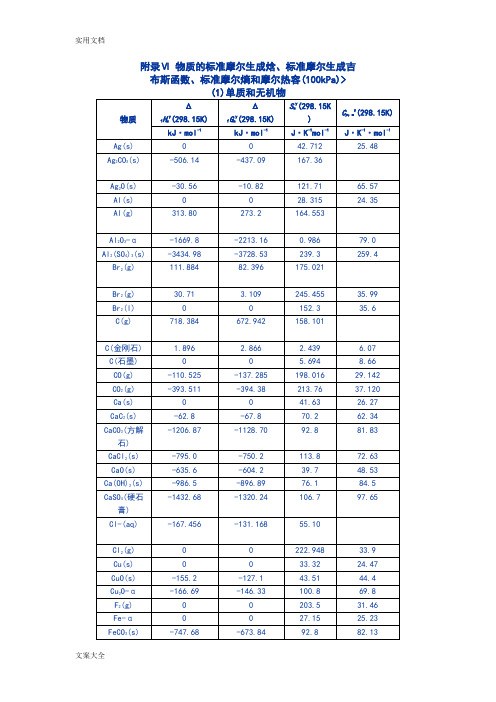
附录Ⅵ物质的标准摩尔生成焓、标准摩尔生成吉布斯函数、标准摩尔熵和摩尔热容(100kPa)>(1)单质和无机物物质Δf H my(298.15K)Δf G my(298.15K)S m y(298.15K)C p,m y(298.15K) kJ·mol-1kJ·mol-1J·K-1mol-1J·K-1·mol-1Ag(s)0042.71225.48 Ag2CO3(s)-506.14-437.09167.36Ag2O(s)-30.56-10.82121.7165.57 Al(s)0028.31524.35 Al(g)313.80273.2164.553Al2O3-α-1669.8-2213.160.98679.0 Al2(SO4)3(s)-3434.98-3728.53239.3259.4 Br2(g)111.88482.396175.021Br2(g)30.71 3.109245.45535.99 Br2(l)00152.335.6 C(g)718.384672.942158.101C(金刚石) 1.896 2.866 2.439 6.07 C(石墨)00 5.6948.66 CO(g)-110.525-137.285198.01629.142 CO2(g)-393.511-394.38213.7637.120 Ca(s)0041.6326.27 CaC2(s)-62.8-67.870.262.34 CaCO3(方解石)-1206.87-1128.7092.881.83CaCl2(s)-795.0-750.2113.872.63 CaO(s)-635.6-604.239.748.53 Ca(OH)2(s)-986.5-896.8976.184.5 CaSO4(硬石膏)-1432.68-1320.24106.797.65Cl-(aq)-167.456-131.16855.10Cl2(g)00222.94833.9 Cu(s)0033.3224.47 CuO(s)-155.2-127.143.5144.4 Cu2O-α-166.69-146.33100.869.8 F2(g)00203.531.46 Fe-α0027.1525.23 FeCO3(s)-747.68-673.8492.882.13FeO(s)-266.52-244.354.051.1 Fe2O3(s)-822.1-741.090.0104.6 Fe3O4(s)-117.1-1014.1146.4143.42 H(g)217.94203.122114.72420.80 H2(g)00130.69528.83 D2(g)00144.88429.20 HBr(g)-36.24-53.22198.6029.12 HBr(aq)-120.92-102.8080.71HCl(g)-92.311-95.265186.78629.12 HCl(aq)-167.44-131.1755.10H2CO3(aq)-698.7-623.37191.2Hl(g)-25.94-1.32206.4229.12 H2O(g)-241.825-228.577188.82333.571 H2O(l)-285.838-237.14269.94075.296 H2O(s)-291.850(-234.03)(39.4)H2O2(l)-187.61-118.04102.2682.29 H2S(g)-20.146-33.040205.7533.97 H2SO4(l)-811.35(-866.4)156.85137.57 H2SO4(aq)-811.32HSO4(aq)-885.75-752.99126.86l2(g)00116.755.97 I2(g)62.24219.34260.6036.87 N2(g)00191.59829.12 NH3(g)-46.19-16.603192.6135.65 NO(g)89.86090.37210.30929.861 NO2(g)33.8551.86240.5737.90 N2O(g)81.55103.62220.1038.70 N2O4(g)9.66098.39304.4279.0 N2O5(g) 2.51110.5342.4108.0 O(g)247.521230.095161.06321.93 O2(g)00205.13829.37 O3(g)142.3163.45237.738.15 OH-(aq)-229.940-157.297-10.539S(单斜)0.290.09632.5523.64 S(斜方)0031.922.60(g)124.9476.08227.7632.55S(g)222.80182.27167.825SO2(g)-296.90-300.37248.6439.79 SO3(g)-395.18-370.40256.3450.70 SO42- (aq)-907.51-741.9017.2(2)有机化合物物质Δf H m y(298.15K)Δf G m y(298.15K)S m y(298.15K)Cp,my(298.15K) kJ·mol-1kJ·mol-1J·K-1mol-1J·K-1·mol-1烃类CH4(g), 甲烷-74.84750.827186.3035.715 C2H2(g), 乙炔226.748209.200200.92843.928 C2H4(g), 乙烯52.28368.157219.5643.56 C2H6(g),乙烷-84.667-32.821229.6052.650 C3H6(g), 丙烯20.41462.783267.0563.89 C3H6(g), 丙烷-103.847-23.391270.0273.51 C4H6(g), 1,3-丁二烯110.16150.74278.8579.54 C4H8(g), 1-丁烯-0.1371.60305.7185.65 C4H8(g), 顺-2-丁烯-6.9965.96300.9478.91 C4H8(g), 反-2-丁烯-11.1763.07296.5987.82 C4H8(g), 2-甲基两烯-16.9058.17293.708912 C4H10(g), 正丁烷-126.15-17.02310.2397.45 C4H10(g), 异丁烷-134.52-20.79294.7596.82 C6H6(g), 苯82.927129.723269.3181.67 C6H6(l), 苯49.028124.597172.35135.77 C6H12(g), 环己烷-123.1431.92298.5116.27 C6H14(g), 正己烷-167.19-0.09388.85143.9 C6H14(l), 正己烷-198.82-4.08295.89194.93 C6H5CH3(g),甲苯49.999122.388319.861.76 C6H5CH3(l),甲苯11.995114.299219.58157.11 C6H4(CH2)(g)18.995122.207352.86133.26 C6H4(CH3)2(l), 邻二甲苯-24.439110.495246.48187.9 C6H4CH3)2(g),17.238118.977357.80127.57 C6H(CH3)2(l), 间二甲苯-25.418107.817252.17183.3 C6H4(CH3)2(g),17.949121.266352.53126.86 C6H4(CH3)2(l), 对二甲苯-24.426110.244247.36183.7含氧化合物HCOH(g), 甲醛-115.90-110.0220.235.36 HCOOH(g), 甲酸-362.63-335.69251.154.4 HCOOH(l), 甲酸-409.20-345.9128.9599.4 CH3OH(g), 甲醇-201.17-161.83237.849.4 CH3OH(l), 甲醇-238.57-166.15126.881.6 CH2COH(g), 乙醛-166.36-133.67265.862.8 CH3COOH(l), 乙酸-487.0-392.4159.8123.4 CH3COOH(g), 乙酸-436.4-381.5293.472.4 C2H5OH(l), 乙醇-277.63-174.36160.7111.46 C2HOH(g), 乙醇-235.31-168.54282.171.1 CH3COCH3(l),丙酮-248.283-155.33200.0124.73 CH3COCH3(g),丙酮-216.69-152.2296.0075.3 C2H5OC2H5(l),乙醚-273.2-116.47253.1CH3COOC2H5(l), 乙酸乙酯-463.2-315.3259C6H5COOH(s), 苯甲酸-384.55-245.5170.7155.2卤代烃CH3Cl(g), 氯甲烷-82.0-58.6234.294.79 CH2Cl2(g), 二氯甲烷-88-59270.6251.38 CHCl3(l), 氯仿-131.8-71.4202.9116.3 CHCl3(g), 氯仿-100-67296.4865.81 CCl4(l), 四氯化碳-139.3-68.5214.43131.75 CCl4(g), 甲氯化碳-106.7-64.0309.4185.51 C6H5Cl(l), 氯苯116.3-198.2197.5145.6含氮化合物NH(CH3)2(g), 二甲胺-27.659.1273.269.37 C5H5N(l), 吡啶78.87159.9179.1C6H5NH2(l), 苯胺35.31153.35191.6199.6 C6H5NO2,(l)硝基苯15.90146.36244.3本附录数据主要取自Handbook of Chemistry and Physics, 70 th Ed., 1990; Editor John A.Dean,Lange's Handbook of Chemistry, 1967。
物质的标准摩尔生成焓

物质的标准摩尔生成焓在化学领域中,摩尔生成焓是一个重要的概念,它用来描述在标准状态下,1摩尔物质在生成过程中吸收或释放的热量。
摩尔生成焓是一个与化学反应相关的热力学量,它可以帮助我们理解化学反应的热力学性质,以及预测反应的热效应。
本文将对物质的标准摩尔生成焓进行详细的介绍和解释。
首先,我们需要了解什么是标准状态。
在化学中,标准状态是指物质的温度为298K(25摄氏度),压强为1个大气压时的状态。
在标准状态下,物质的摩尔生成焓通常用ΔH°表示。
ΔH°的正负值表示了反应是吸热还是放热的,正值表示吸热,负值表示放热。
摩尔生成焓可以通过实验测定得到,也可以通过热力学数据计算得到。
实验测定摩尔生成焓通常需要进行燃烧实验或者溶解实验,通过测定反应前后的温度变化和压强变化,再结合热容和热容量的数据,可以计算出摩尔生成焓的数值。
而通过热力学数据计算摩尔生成焓,则需要使用标准生成焓的数据,结合反应的化学方程式,利用热力学公式进行计算。
摩尔生成焓的数值对于化学反应的研究和应用具有重要意义。
它可以帮助我们预测反应的热效应,判断反应是放热还是吸热的,从而指导工业生产和化学实验的进行。
在工业生产中,了解反应的热效应可以帮助我们设计反应装置,控制反应条件,提高反应的效率和产率。
在化学实验中,摩尔生成焓的数值可以帮助我们理解反应的特性,指导实验的进行,以及解释实验现象。
除了对化学反应有着重要的意义之外,摩尔生成焓还可以帮助我们理解物质的热力学性质。
通过比较不同物质的摩尔生成焓,我们可以了解它们在化学反应中的活性和稳定性,从而为物质的应用提供参考。
同时,摩尔生成焓也可以帮助我们理解物质的结构和键合特性,揭示物质内部的微观过程和规律。
总之,物质的标准摩尔生成焓是一个重要的热力学量,它可以帮助我们理解化学反应的热力学性质,预测反应的热效应,指导工业生产和化学实验的进行,以及揭示物质的热力学性质和微观规律。
通过对摩尔生成焓的研究和应用,我们可以更好地认识和理解化学世界,为化学领域的发展和应用提供重要的支持和指导。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
-25.94
-1.32
206.42
29.12
H2O(g)
-241.825
-228.577
188.823
33.571
H2O(l)
-285.838
-237.142
69.940
75.296
H2O(s)
-291.850
(-234.03)
(39.4)
H2O2(l)
-187.61
-118.04
102.26
40.79
CH2Cl2(g), 二氯甲烷
-88
-59
270.62
51.38
CHCl3(l), 氯仿
-131.8
-71.4
202.9
116.3
CHCl3(g), 氯仿
-100
-67
296.48
65.81
CCl4(l), 四氯化碳
-139.3
-68.5
214.43
131.75
CCl4(g), 甲氯化碳
-106.7
55.10
Cl2(g)
0
0
222.948
33.9
Cu(s)
0
0
33.32
24.47
CuO(s)
-155.2
-127.1
43.51
44.4
Cu2O-α
-166.69
-146.33
100.8
69.8
F2(g)
0
0
203.5
31.46
Fe-α
0
0
27.15
25.23
FeCO3(s)
-747.68
-673.84
98.39
304.42
79.0
N2O5(g)
2.51
110.5
342.4
108.0
O(g)
247.521
230.095
161.063
21.93
O2(g)
0
0
205.138
29.37
O3(g)
142.3
163.45
237.7
38.15
OH-(aq)
-229.940
-157.297
-10.539
S(单斜)
附录Ⅵ 物质的标准摩尔生成焓、标准摩尔生成吉
布斯函数、标准摩尔熵和摩尔热容(100kPa)>
(1)单质和无机物
物质
ΔfHm(298.15K)
ΔfGmy(298.15K)
Smy(298.15K)
Cp,my(298.15K)
kJ·mol-1
kJ·mol-1
J·K-1mol-1
J·K-1·mol-1
Ag(s)
110.495
246.48
187.9
C6H4(CH3)2(g), 间二甲苯
17.238
118.977
357.80
127.57
C6H(CH3)2(l), 间二甲苯
-25.418
107.817
252.17
183.3
C6H4(CH3)2(g), 对二甲苯
17.949
121.266
352.53
126.86
C6H4(CH3)2(l), 对二甲苯
296.00
75.3
C2H5OC2H5(l),乙醚
-273.2
-116.47
253.1
CH3COOC2H5(l), 乙酸乙酯
-463.2
-315.3
259
C6H5COOH(s), 苯甲酸
-384.55
-245.5
170.7
155.2
卤 代 烃
CH3Cl(g), 氯甲烷
-82.0
-58.6
234.29
0.29
0.096
32.55
23.64
S(斜方)
0
0
31.9
22.60
(g)
124.94
76.08
227.76
32.55
S(g)
222.80
182.27
167.825
SO2(g)
-296.90
-300.37
248.64
39.79
SO3(g)
-395.18
-370.40
256.34
50.70
SO42-(aq)
-381.5
293.4
72.4
C2H5OH(l), 乙醇
-277.63
-174.36
160.7
111.46
C2HOH(g), 乙醇
-235.31
-168.54
282.1
71.1
CH3COCH3(l),丙酮
-248.283
-155.33
200.0
124.73
CH3COCH3(g),丙酮
-216.69
-152.2
92.8
82.13
FeO(s)
-266.52
-244.3
54.0
51.1
Fe2O3(s)
-822.1
-741.0
90.0
104.6
Fe3O4(s)
-117.1
-1014.1
146.4
143.42
H(g)
217.94
203.122
114.724
20.80
H2(g)
0
0
130.695
28.83
D2(g)
0
0
5.694
8.66
CO(g)
-110.525
-137.285
198.016
29.142
CO2(g)
-393.511
-394.38
213.76
37.120
Ca(s)
0
0
41.63
26.27
CaC2(s)
-62.8
-67.8
70.2
62.34
CaCO3(方解石)
-1206.87
-1128.70
92.8
-24.426
110.244
247.36
183.7
含 氧 化 合 物
HCOH(g), 甲醛
-115.90
-110.0
220.2
35.36
HCOOH(g), 甲酸
-362.63
-335.69
251.1
54.4
HCOOH(l), 甲酸
-409.20
-345.9
128.95
99.04
CH3OH(g), 甲醇
194.93
C6H5CH3(g),甲苯
49.999
122.388
319.86
103.76
C6H5CH3(l),甲苯
11.995
114.299
219.58
157.11
C6H4(CH2)(g) 邻二甲苯
18.995
122.207
352.86
133.26
C6H4(CH3)2(l), 邻二甲苯
-24.439
-201.17
-161.83
237.8
49.4
CH3OH(l), 甲醇
-238.57
-166.15
126.8
81.6
CH2COH(g), 乙醛
-166.36
-133.67
265.8
62.8
CH3COOH(l), 乙酸
-487.0
ห้องสมุดไป่ตู้-392.4
159.8
123.4
CH3COOH(g), 乙酸
-436.4
-3434.98
-3728.53
239.3
259.4
Br2(g)
111.884
82.396
175.021
Br2(g)
30.71
3.109
245.455
35.99
Br2(l)
0
0
152.3
35.6
C(g)
718.384
672.942
158.101
C(金刚石)
1.896
2.866
2.439
6.07
C(石墨)
0
0
144.884
29.20
HBr(g)
-36.24
-53.22
198.60
29.12
HBr(aq)
-120.92
-102.80
80.71
HCl(g)
-92.311
-95.265
186.786
29.12
HCl(aq)
-167.44
-131.17
55.10
H2CO3(aq)
-698.7
-623.37
191.2
-11.17
63.07
296.59
87.82
C4H8(g), 2-甲基两烯
-16.90
58.17
293.70
89.12
C4H10(g), 正丁烷
-126.15
-17.02
310.23
97.45
C4H10(g), 异丁烷
-134.52
-20.79
294.75
96.82
C6H6(g), 苯
82.927
129.723
81.83
CaCl2(s)
-795.0
-750.2
113.8
72.63
CaO(s)
-635.6
-604.2
39.7
48.53
Ca(OH)2(s)
-986.5
-896.89
76.1
