第二类医疗器械经营备案流程

办理第二类医疗器械经营备案资料
1.第二类医疗器械经营备案表
2.营业执照副本盖章复印件
3.法人、质量负责人身份证、学历证明复印件
4.企业组织机构与部门设置说明
5.专业技术人员一览表
6.专业技术人员身份证、学历证明
7.经营范围、经营方式说明(原件)
8.经营地址库房地址的地理位置平面图,租房合同、房产证复印件
9.经营设施设备目录
10.经营质量管理制度、工作程序等文件目录
11.申请材料真实性的自我保证声明
12.授权委托书
以上资料提交后,相关行政部门会派出工作人员到公司核实。
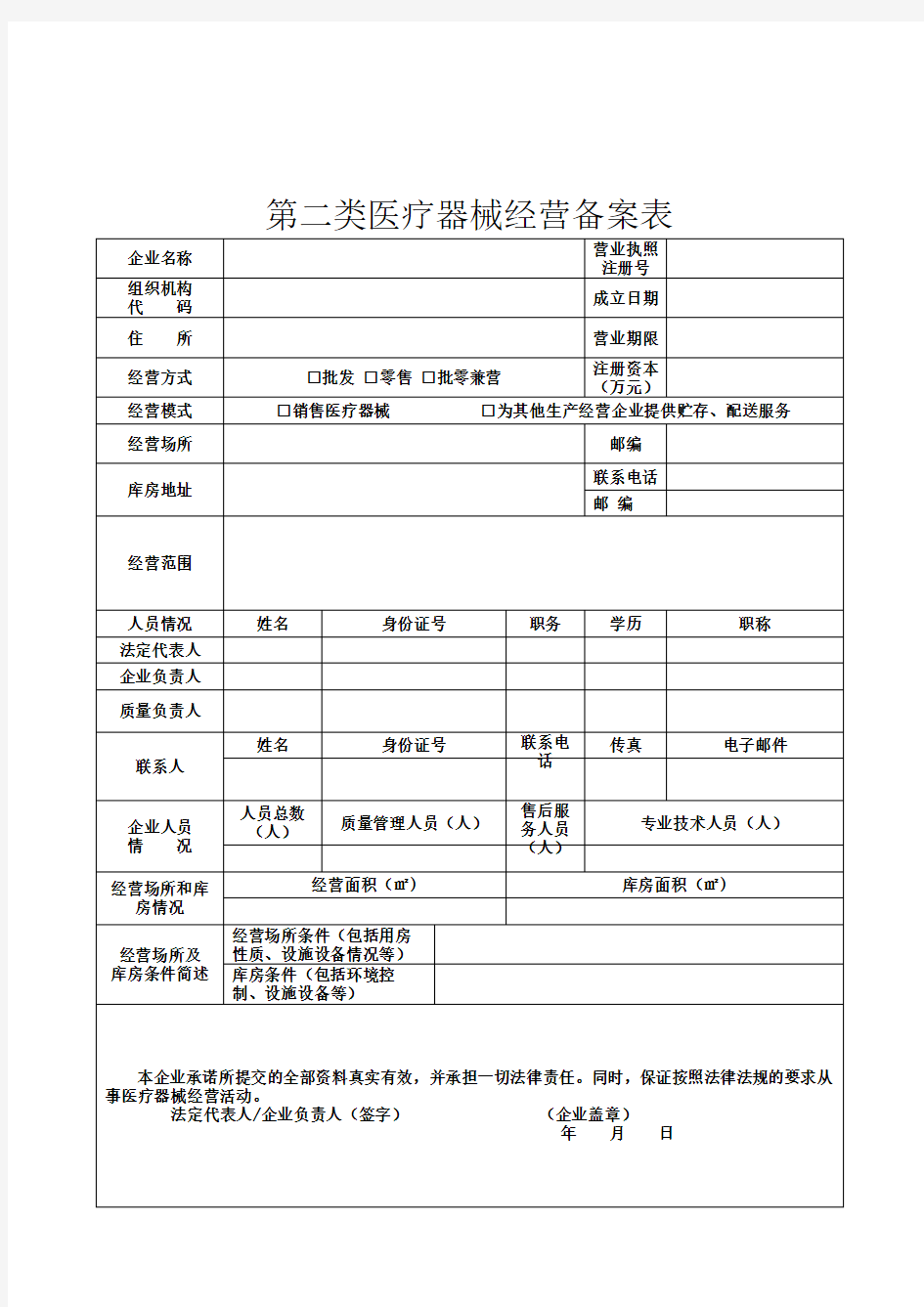
第二类医疗器械经营备案表
填表说明:1.本表按照实际内容填写,不涉及的可缺项。其中,企业名称、营业执照注册号、住所、法定代表人、注册资本、成立日期、营业期限等按照营业执照内容填写。
2.本表经营范围应当按照国家食品药品监督管理部门发布的医疗器械分类目录中规定的管理类别、分
类编码及名称填写。
3.本表经营方式指批发、零售、批零兼营。
组织机构与部门设置说明
组织机构图
部门设置说明:
一、经理职能
领导和动员全体员工认真贯彻执行《医疗器械监督管理条例》等国家有关医疗器械法律、法规和规章等,在“合法经营,质量为本”的思想指导下进行经营管理。对企业所经营医疗器械的质量负全面领导责任。合理设置并领导质量组织机构,保证其独立、客观地行使职权充分发挥其质量把关职能,支持其合理意见和要求,提供并保证其必要的质量活动经费。
二、质量管理员职能
1.负责建立一个质量管理体系。实施质量否决权,指导各部门质量活动编制质量制度,并保证实施审批首营企业首营品种,质量培训。执行国家有关医疗器械监督管理的法律、法规及规章等有关政策的规定,负责企业的全面质量管理工作,确保医疗器械的质量。
2. 经营产品质量追溯、不良事件报告、根据不良事件等级及时上报国家不良反应检测中心。
4. 负责产品召回。
5. 负责执行医疗器械质量验收制度。
三、验收员职能
严格执行医疗器械质量验收制度。
1.验收人员凭到货通知单或随货同行逐批进行验收。
2.对验收不符合验收内容、不符合相关法定标准和质量条款或其他怀疑质量异常的医疗器械,填写拒收报告单,并通知质管部处理。
3.验收时应对医疗器械的包装、标签、说明书以及有关要求的证明文件逐一检查,整件包装中应有产品合格证。
4.验收首营品种,应查看首批到货医疗器械同批号的医疗器械出厂检验合格证明。
5.验收进口医疗器械,应检查包装的标签是否有中文注明的医疗器械名称、主要成份以及进口注册证号,检查中文说明书及合法的相关证明文件。
6.及时填写有关报表和验收记录,并签字负责,按规定保存备查。
四、采购员职能
1. 检查督促本采购部门工作,坚持采购的医疗器械必须是从具有法定资格的供货单位购进的,并收集供货单位的合法证照等资质的证明材料,严禁从私人及证照不全的单位进货,建立供货单位档案。
2. 督促检查本部门签订质量保证协议,配合质量管理部门搞好首营企业、首营品种的审核工作,并检查收集有关的资料,经质管部门审核合格报经理批准后方可进货。
五、销售员主要职能
1.学习执行《医疗器械监督管理条例》等有关条例,规范销售工作行为。
2.销售医疗器械应开具合法票据,做到票、帐、货相符。销售票据应按规定保存,建立医疗器械销售记录,记载医疗器械的销售日期、品名、规格型号、批号、有效期、生产单位、购货单位、单价、数量等项内容。销售记录应保存到有效期满后二年。
六、仓储主要职能
1.仓库管理员应按说明书或者包装标示的贮存要求贮存医疗器械;
2.仓库管理员应按照贮存医疗器械要求采取避光、通风、防潮、防虫、防鼠、防火等措施,应作好仓库安全防范工作,定期对安全的执行情况进行检查确认,并填写“安全卫生检查表”。
3.仓储人员应对搬运和堆垛医疗器械按照包装标示要求规范操作,堆垛高度符合包装图示要求,避免损坏医疗器械包装;
七、维修售后服务员职能
1.产品售出后,应定期进行质量跟踪及售后服务。及时掌握用户对商品使用情况。
2. 对用户在使用产品过程中发生的问题要认真对待及时给予解决并详细做好记录。对产品质量问题要积极与供货单位或生产厂家联系,在规定的时间内给予修复或调换。
3. 因用户使用不当造成商品损坏,应根据企业有关规定进行妥善处理。
4. 销售人员对产品售后服务过程应做好详细记录,并建立售后服务档案,按规定妥善保存。
专业技术人员一览表
填写说明:1.本人签名不得代签,发现代签者按提供虚假材料处理;
2.按相应的经营范围、经营规模和经营方式,请各自参照相关现场检查指导原则及验收标准、实际情况填写。
经营方式说明
(经营/仓储)设施、设备目录
申请材料真实性自我保证声明
我公司办理第二类医疗器械经营备案,提交如下材料:
(请办理企业按顺序填写提交材料目录)
其他材料:
法定代表人(负责人) 保证本企业已认真阅读以下相关法律责任并郑重承诺:此次提交的以上材料内容均经本企业核实,确定属实、有效;保证遵守《医疗器械监督管理条例》、《医疗器械经营监督管理办法》、《医疗器械经营质量管理规范》等法律、法规和规章的规定;如有提供虚假资料、违反法律、法规和规章的情形,愿承担相应法律责任,特此声明。
(申请注销的,还应加上:并承担注销后引起的法律责任的承诺)
公司名称(盖章):
法定代表人(负责人)签名:
年月日
相关法律责任:
1、提供虚假资料或者采取其他欺骗手段取得医疗器械注册证、医疗器械生产许可证、医疗器械经营许可证、广告批准文件等许可证件的,由原发证部门撤销已经取得的许可证件,并处5万元以上10万元以下罚款,5年内不受理相关责任人及企业提出的医疗器械许可申请。
2、伪造、变造、买卖、出租、出借相关医疗器械许可证件的,由原发证部门予以收缴或者吊销,没
所得3倍以上5倍以下罚款;构成违反治安管理行为的,
