对映异构)
第3章对映异构

实例分析
NO2
NO2
HO 1 H H 2 NHCOCHCl2 CH2OH
(-) - 1R,2R –
H OH Cl2CHCOHN H
CH2OH
(+) - 1S,2S –
氯霉素
抗菌活性 (- ) ∶ (+) = 100 ∶ 0.4
合霉素 —— 外消旋体 已淘汰
手性药物
外消旋体的拆分
COOH
HO
CH3
H
Br Cl CH3
H
(1)
COOH
H
OH
CH3
Br CH3 Cl
H
(2)
CH3 Cl Br
H
(3)
(2)=(3)=(4)
Cl
CH3
H
Br
(4)
四、构型标记法
1. D、L 标记法
CHO H OH
CH2OH
D-(+)-甘油醛
HgO
COOH H OH
CH2OH
D-(-)-甘油酸
相对构型
名称
熔点/℃
αm
pKa 溶解度
(+)-乳酸
26
+3.8
3.76
∞
(-)-乳酸
26
-3.8
3.76
∞
(±)-乳酸
18
0
3.76
∞
3. 外消旋体无光学活性,物理性质 与纯的对映体有差异。
三、Fischer投影式
* 3
21
CH3 CH COOH 乳酸
OH
COOH
COOH
CH3
C OH
H
HO C CH3 H
CHO HO H
对映异构学习课件

对映体 旋光 mp 53℃ 基本相同
各自发挥其左右 旋体的生理功能
三、对映体构型的表示方法
1.构型的表示方法
对映体的构型可用立体结构(楔形式和透视式)和费歇尔
(E·Fischer)投影式表示。
式表示:
投影原则:
1° 横、竖两条直线的交叉点代表手性碳原子,位于纸平 面。
2° 横线表示与C*相连的两个键指向纸平面的前面,竖线表示
指向纸平面的后 面。
3° 将含有碳原子的基团写在竖线上,编号最小的碳原 子写
在竖线上 端。
使用费歇尔投影式应注意的问 题:
a 基团的位置关系是“横前竖后 ”。
b 不能离开纸平面翻转180°;也不能在纸平面上旋转90°
或270°与原构型相比。
c 将投影式在纸平面上旋转180°,仍为原构 型。
2. 判断不同投影式是否同一构型的方法 :
(1)将投影式在纸平面上旋转180°,仍为原构 型。
(2)任意固定一个基团不动,依次顺时针或反时针调换另 三个
基团的位置,不会改变原构型。
(3)对调任意两个基团的位置,对调偶数次构型不变,对 调奇
第六章 对映异构
Chap. 6 Enantiomeric of organic Stereochemistry
重点讲授内容:
一、同分异构现象
二、构型异构中的顺反异构
三、构型异构中的对映异构和非对映异构
四、环烷烃的构型异构
五、潜手性中心、潜手性面与手性识别
同分异构现象
构造异构 constitutional
绕轴转动一周,就有n个形象与原形象无法区分,水有两个,氨
有三个,球体有∞个。
对映异构

有机化合物的同分异构构造异构是指分子式相同,而分子中原子相互连接的次序不同的一种异构现象,包括碳胳异构、位置异构和官能团异构。
构造相同,但分子中原子在空间的排列方式不同引起的异构现象称为立体异构(stereoisomerism )。
分子中原子在空间的不同排列方式形成了不同的构型或构象,所以立体异构又分为构型异构与构象异构。
例如顺-2-丁烯与反-2-丁烯这种顺反异构即属于构型异构,丁烷的不同构象和环已烷的不同构象都属于构象异构 构型异构不仅包括顺、反异构,对映异构也属于构型异构,对映异构的分子式相同,构造也相同,只是构型不同。
现在可以把异构现象归纳为:顺反异构由于双键不能自由旋转,所以当两个双键碳原子各连有两个不同的原子或基团时,可能产生两种不同的空间排列方式。
例如2-丁烯:(I) 顺-2-丁烯 (II) 反-2-丁烯(沸点3.7 ℃) (沸点0.88 ℃)两个相同基团(如I 和 II 中的两个甲基或两个氢原子)在双键同一侧的称为顺式,在异侧的称为反式。
这种由于分子中的原子或基团在空间的排布方式不同而产生的同分异构现象,称为顺反异构,也称几何异构。
通常,分子中原子或基团在空间的排布方式称为构型,因此顺反异构也是构型异构,它是立体异构中的一种。
需要指出的是,并不是所有的烯烃都有顺反异构现象。
产生顺反异构的条件是除了σ键的旋转受阻外(双键或环),还要求两个双键碳原子上分别连接有不同的原子或基团。
也就是说,当双键的任何一个碳原子上连接的两个原子或基团相同时,就不存在顺反异构现象了。
例如,下列化合物就没有顺反异构体。
构象异构同分异构构型异构顺反异构对映异构立体异构构造异构碳架异构官能团异构位置异构互变异构C=CCH 3CH 3H HHHCH 3CH 3C=CC=C C=C aa a bbca a当与双键相连的两个碳原子上连有相同的原子或基团时,例如上面的(I)和(II),可采用顺反命名法。
两个相同原子或基团处于双键同一侧的,称为顺式,反之称为反式。
第七章对映异构

2
有机分子的异构现象
通过前面的学习,可知有机化合物具有如下异构现象:
异构体(Isomers) 具有相同分子式的不同化合物
构造异构体 (Constitutional isomers) 化合物中原子的排列顺序不同
立体异构体 (Stereoisomers) 化合物中原子的排列顺序相同, 但是空间排布不同
(a)以 H 原子远离我们的眼睛,按照与碳相连的原子的原子 序数由大到小顺序进行排列,一个是顺时针方向,一个是逆时 针方向。
F H
Br Cl
Cl
H
Br
F
18
(b)交换一个异构体中任何两个原子或原子团,得到 其对映异构体,即得到的化合物原子或原子团在空间的排 列顺序与以前相反。
上面的例子说明,对映异构现象实质:是基团在空间 的不同排列所引起。但是原子或基团的不同排列与旋光 性有什么关系?如何确定每种异构体的空间排列?
H
H
其他的不存在对映异构现
H
A
象。
38
练习:判断下列化合物之间的关系:
1.
与
2.
与
3.
与
解: 1. 一对对映异构体 2. 同一化合物 3. 同一化合物
39
判断对映异构体的方法
最直接的方法是建造一个分子和它的镜像的模型。观察镜像和 分子是否重叠?
是否有对称面、对称轴或对称中心。 寻找手性碳原子(手性中心)。 (但如果有两个或两个以上的手性碳原子有例外,内消旋体)
15
1) 手性中心、 不对称碳原子
(chiral center, asymmetric carbon)
Cl
H
第六章 对映异构

有对称中心的分子非手性,实物与镜可重叠,没 有对映体和旋光性。
③、对称轴 C n ——若通过分子画一轴线,当分子绕此轴 旋转360º /n后,得到与原来分子相同的形象,此轴线就 是该分子的几重对称轴。
H
H H Cl
Cl Cl Cl
Cl
有无对称轴不能 作为判断分子有 无手性的依据。
Cl C2
H
总之,一物质在结构上不存在对称面、对称中心,该 物质的分子有手性,有对映体和旋光性。
四个对映体,其中一对对映体、2 个不同的内消旋体
第五节 构型的标记方法
1、相对构型与绝对构型
D/L表示构型, +/-表示旋光方向, 两者无必然联系。
2、R/S命名规则——1970年IUPAC命名法建议,对映 体的构型用R(拉丁文右)和 S(左)表示
(1)按次序规则将手性碳原子上的四个基团排序。
COOH
二、外消旋体——等量的右旋体和左旋体混合,旋光 方向相反,无旋光性,用(±)或(RS)或(DL)表 示。 外消旋体的物理性质与左旋体或右旋体不同、旋光性 不同、化学性质相似、生理效应为两者的加和。
三、构型表示法——费歇尔投影式 1、透视式
COOH H H OH CH3 乳酸 优点: 形象生动,一目了然 缺点: 书写不方便 COOH C OH CH3 楔形式 H COOH C OH CH3
H Br Br CH3 Br H CH3 Br
CH3 Br H
CH3 H Br CH3 CH3
CH3
H Br
Br H CH3
外 消 旋 体
反-2-丁烯与溴加成
H CH3 C C CH3 H CH3 Br2 C H (2) H Br C CH3 (1) Br
大学化学-第五章-对映异构
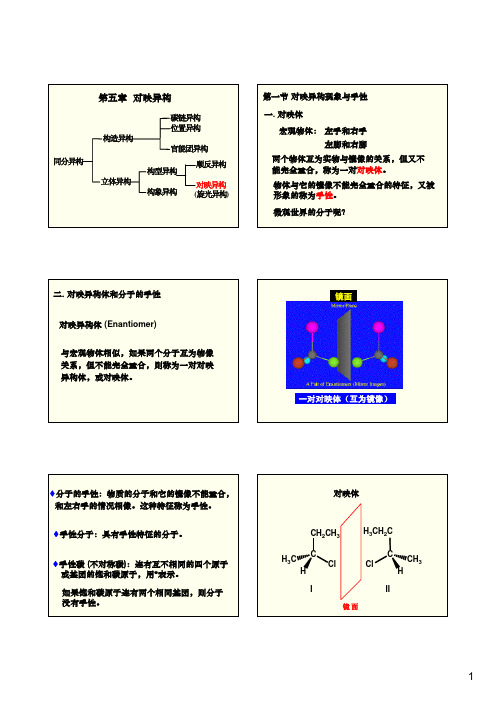
钠光灯
平面偏振光
光平面旋转
3
3. 旋光度和比旋光度
(+)表示右旋 (-)表示左旋
α:旋光度; [α]:比旋光度;
t:温度;
λ:光波长;
C:样品浓度,单位 g/ml;
l: 样品管长度,单位 dm
分子的手性(而不是手性碳)是其具有旋光性 和对映异构现象的充分必要条件。
ቤተ መጻሕፍቲ ባይዱ
除了旋光方向和与手性试剂的反应外,对映体 具有相同的物理和化学性质。
1. 对称面
凡有对称面的分子,不具手性,也没有对映异 构体。
2. 对称中心 有对称中心的分子没有手性。
Cl C
H
H C
Cl
如果一个分子既无对称面也无对称中心, 分子就具有手性。
四. 对映体构型的表示方法-Fischer投影式 分子模型的四面体构型投影在纸面上。 COOH
HO H COOH
CH3 HO
H
CH3
Fischer式
2
Fischer投影式的画法及其含义
• 把横向的基团朝前,竖向的朝后。 • 用光对准分子模型垂直纸面照射,手
性碳用十字交差点表示。 • 因此,Fischer投影式就被赋予了“横
前竖后”的立体含义。
注意: • 不能离开纸面翻转。离开纸面翻转
180o,将变成其对映体。 • 在纸面上转动180o构型不变。
CH2CH3
CH2CH3
H3C
C Cl
H
Cl C CH3 H
CH3
CH3
enantiomers
非对映异构体
含有1个手性碳原子的化合物有2个对映体。 含有2个手性碳原子的化合物最多有4个对映体 和非对映体。 含有n个手性碳原子的化合物最多有2n个对映体 和非对映体。
对映异构名词解释

对映异构名词解释
对映异构是指化学物质中的两种分子,它们的化学式完全相同,但是它们的空间构型却是互为镜像关系。
这种镜像关系是由于分子中的某些原子或基团的排列不同而导致的。
对映异构分子的化学和物理性质可能会有很大的差异,因为它们的空间构型不同,所以它们与其他分子的相互作用方式也会不同。
对映异构物质还会表现出一些特殊的光学性质,比如旋光性和偏振光的旋转方向等。
对映异构分子在药物化学、生物化学、环境化学等领域都有重要的应用。
在药物化学中,对映异构体常常会对药效和副作用产生巨大的影响。
因此,制药公司通常会研究和开发仅含一种对映异构体的药物,以获得更好的疗效和安全性。
在环境化学中,对映异构体也有着重要的意义。
例如,某些农药和工业污染物中含有对映异构体,这些化合物的毒性和生物降解性质都会受到对映异构体的影响。
因此,在环境监测和治理中,对映异构体的分析和鉴定也显得尤为重要。
- 1 -。
对映异构体和非对映异构体名词解释

对映异构体和非对映异构体名词解释下载提示:该文档是本店铺精心编制而成的,希望大家下载后,能够帮助大家解决实际问题。
文档下载后可定制修改,请根据实际需要进行调整和使用,谢谢!本店铺为大家提供各种类型的实用资料,如教育随笔、日记赏析、句子摘抄、古诗大全、经典美文、话题作文、工作总结、词语解析、文案摘录、其他资料等等,想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by this editor. I hope that after you download it, it can help you solve practical problems. The document can be customized and modified after downloading, please adjust and use it according to actual needs, thank you! In addition, this shop provides you with various types of practical materials, such as educational essays, diary appreciation, sentence excerpts, ancient poems, classic articles, topic composition, work summary, word parsing, copy excerpts, other materials and so on, want to know different data formats and writing methods, please pay attention!一、对映异构体的概念。
对映异构体是指一种分子的空间结构与其镜像不重合的异构体。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第八章 对映异构)[目的要求]:1.了解平面偏振光的产生及旋光仪的构造;2.掌握对映异构与分子结构的关系;3.掌握对映体、非对映体、外消旋体、内消旋体、手性、对称因素等立体化学中的基本概念;4.掌握构型的表示及标定;8.1物质的旋光性和比旋光度8.1.1 物质的旋光性在物理学中我们都知道,光波是一种电磁波,其振动的方向和它的前进方向相互垂直。
有无数个平面经过光传播的直线,而普通的光都在所有这些平面上振动。
旋光性物质是指能使偏振光平面旋转的物质。
当在某一平面中振动的偏振光通过旋光性物质时,它出来时就在另一个平面上振动。
能使偏振光振动平面向右旋转称为右旋体,向左旋转则称为左旋体,如乳酸、葡萄糖等都是旋光性物质它们能使偏光振动的平面旋转一定的角度 。
而水、酒精、乙酸等对偏光不发生影响,偏光仍维持原来的振动平面,因此它们都是一些非旋光活性物质。
8.1.2 比旋光度我们知道,物质的旋光性是由有旋光性的化合物的分子所引起,因此旋光度的大小取决于光通过旋光管时碰到的分子的多少。
例如光在20厘米上的旋光管中碰到的分子是在10厘米长的旋光管中的二倍。
因此旋光度也是二倍。
如果旋光性物质在溶液中,光所碰到的分子数将取决于浓度。
在一定长度的旋光管中,光在2克/100ml 的溶液中碰到的溶质分子是1克/100ml 时的二倍,旋光度也将是二倍。
由于物质的旋光度与它的浓度有关,因此为了能比较物质的旋光性能,我们必须修正旋光管长度和溶液的浓度差别,这样旋光度的大小和方向就是每一个别旋光性化合物的特性了。
通常规定1ml 含1克旋光性物质的溶液,放在1Nicol棱棱检偏镜Nicol棱棱起偏镜光源观察偏振光旋转后的偏振光I分米长的旋光管(盛液管)中测得的旋光度称为该物质的比旋光度。
比旋光度是旋光性物质特有的物理常数,用[α]λ20表示。
t为测定时的浓度,λ为采用光的波长,钠光用D表示(λ:5890Å,5869Å)例:肌由乳酸的比旋光度为[α]λ20=+3.8°发酵乳酸则为[α]λ20=-3.8°实际工作中,可用适当浓度C的溶液装在适当长度l的旋光管中进行测定,然后将测得的旋光度α换算为比旋光度[[α],换算公式为:[α]λt=αtλ/ l*cl:旋光管长度(分米)c:溶液浓度(克/ml)αtλ: t℃时,λ波长时浓度为c的溶液旋光仪上测得的旋光度如所用样品为纯液体,浓度c用该液体的密度d代替之。
另外,所测溶液的溶剂不同也会影响物质的旋光度。
因此不用水时需注明溶剂名称。
另外溶液中溶质的溶解缔结与溶剂的作用等都会影响其比旋光度的数字,甚至会改变其方向。
这一节我们学习了物质的旋光性,偏振光的定义,及旋光仪的简单工作原理和旋光度的表示方法。
下一节,我们将讨论物质的旋光性与其分子结构的相互关系,也就是对映异构现象与分子结构的关系。
8.2、分子的手性和对映异构对映异构现象与分子结构的关系在我们所接触到的各种物质中,为什么有些物质具有旋光性,而有些则没有旋光性?为什么旋光性物质又存在着对映异构现象?从唯物辩证法的观点来说,我们知道,现象是本质的表现反映,而则是同类现象中的一般,共同的东西,我们认识的真正任务就是要通过现象认识事物的本质。
有关物质的旋光性和对映异构现象以及它们与分子结构之间关系的理论(也就是旋光现象的本质)更在人们反复实践和比较过程中逐渐认识和不断完善的。
8.2.1 基本概念手性一词首先由Lord Keluin于1893年提出,到60年代才普遍被接受。
手性(来源于希腊暗字"cheir"手目前英文为chirality)定义:实物和镜像不能重合的性质称手性。
分子的对称性:当分子经过某一种对称操作后,其中每一点都恢复在与其原来所占据的相当的位置上,即分子重新复原。
这种特殊操作称为对称操作,这样的分子称为对称分子。
8.2.2 手性和对称因素对称因素 对称操作σ(对称平面) 在一个平面上反映I (对称中心) 通过一个中心倒反Cn (对称轴) 围绕一个轴旋转 弧度Sn (更迭对称轴) 于该轴的平面上反映① 对称面(σ)结论:具有对称面的化合物是非手性分子,它没有对映异构体和旋光性。
例: CH 3CHCl 2 (结合模型分析对称面)如有一个平面可以把分子分割成两部分,而一部分正好是另一部分的镜象,这个平面就是分子的对称面(用σ表示)。
② 对称中心(i )结论:具有对称中心的化合物,是非手性的,它没有对映异构体和旋光性。
若分子中有一点p ,通过p 点画任何直线,如在离p 点等距离的直线两端有相同的原子,则p 点称为分子的对称中心。
(用i 表示)对于绝大多数分子,只要检查它是否有σ与i ,就可确定该分子是否有手性,对于某些特殊分子,检查其有否Sn 轴,没有Sn 州的分子必定有手性,有Sn 轴的分子必定是非手性的,8.3 含一个手性碳原子的对映异构C=C ClH ClH3C COOH HO H 3COOH OHa.R/S构型与物质的旋光性之间没有必然的联系.b.R构型的对映体一定是S构型.c.内消旋体中两个手性C原子,其中一个是R构型,另一个S构型.d.一个手性C原子的构型为R或S所连的原子或基团在空间的相对位置次序有关.8.4 分子构型8.4.1、构型的表示方法投影原则:①横竖的交点为手性C原子。
②“横前竖后”。
③主碳链竖的排列,氧化态最高的C原子放在碳链的顶端。
使用投影式注意问题①投影式在纸面上平移或转动180°,其构型不变。
)②投影式不能在纸面上旋转90°、270°。
③投影式不能离开纸面翻转180°。
(模型)④若将手性C原子上所连任何两个原子或基团相交换,将会使构型变为它的对映体。
即互换位置奇数次,得到的是对映体,互换位置偶数次,是到的是自身。
8.4.2、相对构型和绝对构型8.4.3、构型的命名法R、S构型系统命名法这一方法最初是由R、S、Cahn(伦敦化学会),c.k.Ingold(伦敦大学学院)和V.Prelog(苏黎世,瑞士联邦工学院)于1950年提出,1970年被国际纯粹和应用化学协会(IUPAC)所采用的。
(Prelog是一个在立体化学领域上很有影响的化学家,他出生于南斯拉夫,23岁或博士学位,由于他在环壮化合物的构象和它们的活性之间的关系方面所作出的贡献,于1975年他和J.Conforrth共同获该年的诺贝尔化学奖。
R.S命名法包括二个步骤:步骤1:遵循一套秩序规则(后面讨论),把与手性中心相连接的四个原子或原子团确定一个先后次序。
例:在CHClBrI中,连接在手性中心的四个原子都不同,先后次序只取决于原子序数,由序数越大的原子越优先,即按I①>Br②>Cl③>H④的次序。
步骤2:设想分子的取向是:把次序最后的基团指向离开我们的方向,然后观察其余基团的排列,按各基团优先性从大到小的次序来看,如果我们的眼睛按顺时针方向转动,这个构型标定为R(拉丁:rectus,右);如果是逆时针方向,这个构型定为S(拉丁:sinister,左)。
于是,下面的构型I和II是这样看的:原子序优先性顺序规则的具体内容是什么呢?如何依据这些规则确定不同基因的原子序优先行性呢?这里介绍几条主要的规则,并举例说明如下:(1)首先比较和手型碳原子相连接的原子的原子序,原子序数大者优先。
对于同位素,质量大者优先。
(2)当直接和手型碳原子相连的原子相同时,可再比较第二个原子;如果第二个原子有几个,只要其中一个原子序数最大则优先。
当第二个原子又都相同时,则可再比较第三个原子,余此类推。
(3)双链和三链可分别看作两次和三次余有关之因素的结合。
括中元素表示他不再连有其它原子,因此,与连有其它原子的该元素比较,根据第二规则,则后者优先。
在有机化学中立体结构的表达经常采用的是Fiseher 式,式中横线指向纸平面后方。
因此,当原子序优先性最低的基团处于竖线时,就可直接从式中另三个基团的排列方向读出构型,以C*①②③④为例,设四个基团的原子序优先性顺序为①>②>③>④,但是当原子序优先性最低的基团处于横线时,这个基团④指向纸面前方,那么若要求从手型碳原子向它(C*-4)看去,就要翻转整个分子,才能得到正确的结果。
否则的话,仍然对原来式子由前向后看去,所看到的①--②--③的空间排列方向,就必然和R/S 命名法规定的观察结果相反。
因此,我们也可简便地对优先性顺序最低基团处于横线的Fischer 式进行直接观察,并将观察结果加以反转,就可得到正确的构型名称。
采用这个规则,可迅速确定有关手性化合物的构型,规则可描述为下面口诀“大小标记,一二三四。
横向相加,左小减上,右小减下”符合规则,构型是R ,其余为S 。
例:(+)-2-氯丁烷例:小结e.R/S 构型与物质的旋光性之间没有必然的联系.f.R 构型的对映体一定是S 构型.g.内消旋体中两个手性C 原子,其中一个是R 构型,另一个S 构型.h.一个手性C 原子的构型为R 或S 所连的原子或基团在空间的相对位置次序有关. R/S 命名最大的优点是一个能够普遍应用的方法。
8.5、具有两个手性碳原子化合物的对映异构Cl >C 2H 5>CH 3>H S构型C 2:OH >COOH >CHOHCOOH R 构型C 3:OH >COOH >CHOHCOOH R 构型(2R,3R)-(+)-酒石酸1.含有两个不同手性C 原子的化合物① 2,3,4—三羟基丁酸 HOOCC *HOHC *HOHCOOH 2,3,4-三羟基丁酸(P80.)其中: Ⅰ和Ⅱ,Ⅲ和Ⅳ是对映体;Ⅰ和Ⅲ,Ⅱ和Ⅳ为非对映异构体。
② 非对映异构体:不呈镜象对映关系的立体异构称为非对映异构体。
其性质: a. 物理性质不同。
b. 比旋光度也不同,旋光方向可能一样,也可能不一样.c. 化学性质相似.③ 随手性C 原子数目增多,其对映异构体的数目也增多。
分子中有几个不相同的手性C 原子时,可有2n 个对映异构。
可组成2n-1个外消旋体。
2.含有两个相同手性C 原子的化合物① 酒石酸 HOOC-CHOH-CHOH-COOH (幻灯片124号) (P81.)② 内消旋体:由于分子中含有两个相同的手性C 原子,分子的两半部分互为物体与镜 象关系,从而使分子内部旋光性相互抵消的光学活性化合物为内消旋体.凡是含有两个相同的不对称C 原子的化合物,都有三种立体异构体:一个是左旋 的, 一个是右旋的,一个是内消旋的。
③ 内消旋体和外消旋体a.都不具有光学活性。
b.内消旋体是一种纯物质,不能分离成具有旋光性的化合物。
外消旋体是混合物,可分离出具有旋光性的两种物质。
8.6、异构体的分类COOH C C CH 2OH 134COOH C C CH 2OH 14(Ⅰ)(Ⅱ)(2S,3S)(2R,3R)COOH C C CH 2OH H 14COOH C H C CH 2OH 14(Ⅳ)(Ⅲ)(2S,3R)(2R,3S)COOH C C COOH H 14COOH C H C COOH 124(Ⅰ)(Ⅱ)(2S,3S)(2R,3R)COOHC COOH COOH H C COOH H (Ⅳ)(Ⅲ)(2S,3R)(2R,3S)构造异构(凡分子中原子互相连接次序不同而产生的异构现象)位置异构碳干异构官能团异构CH3CH=CHCH2CH3CH2=CHCH2CH2CH3CH3CH2CH2CH3CH3CHCH3CH3CH3CH2OCH3CH3CHCH3OH互变异构CH3CCH2COOEt CH3C=CHCOOEtO OH。
