有机化学--第三章不饱和烃烯烃和炔烃
有机化学第3章 不饱和烃

Cl
Br
CC
H
Cl
(Z)-1,2-二氯-1-溴乙烯 (反-1,2-二氯-1-溴乙烯)
Cl C
H
Cl C
Br
(E)-1,2-二氯-1-溴乙烯 (顺-1,2-二氯-1-溴乙烯)
28
6. 烯炔的命名
第三章 烯烃和炔烃 (三、烯烃和炔烃的命名)
• 编号时尽可能使重键的位次之和最低。 • 当双键和三键处于两头相同的位次时,
反式:两个取代基在环异侧 顺式:两个取代基在环同侧
15
第三章 烯烃和炔烃 (二、烯烃和炔烃的同分异构)
问题:下列化合物是否存在顺反异构?
CH3
C2H5 D
C=C
H
Cl H
H C=C
CH3
CH2-CH-CH3 CH-CH3
16
第三章 烯烃和炔烃 (三、烯烃和炔烃的命名)
三、烯烃和炔烃的命名
1. 简单的烯烃常用普通命名法
98
7
CH3
CH2CH3
10,10-二甲基-3-乙基-9-异丙基-4-十一碳烯
例3
4 CH3 3 CH2CH3
4 –甲基–3–乙基环庚烯
12
例4 CH3CC CCH2CH3 2 –甲基–3–己炔
CH3
19
4. 烯基与炔基
第三章 烯烃和炔烃 (三、烯烃和炔烃的命名)
CH2 CH
乙烯基 (vinyl)
3. 烯烃的比重都小于1,都是无色物质,溶于有机溶剂,不溶于水。
CH3 C C CH3
H
H
沸点(bp): 3.7℃ 熔点(mp): -138.9℃
CH3
H
CC
H
CH3
0.88℃
有机化学 第三章 不饱和烃

(2) 炔烃的结构
以乙炔为例。 仪器测得:C2H2中,四个原子共直线:
0.106nm 0.120nm
H CC H
量子化学的计算结果表明,在乙炔分子中的碳原 子是sp杂化:
激发 杂化
杂化
2个sp p轨道
二个sp杂化轨道取最大键角为180°,直线构型:
C
乙炔分子的σ骨架:
HC
CH
每个碳上还有两个剩余的p轨道,相互肩并肩形成2个π键:
第三章 不饱和烃
(一) 烯烃和炔烃的结构 (二) 烯烃和炔烃的同分异构 (三) 烯烃和炔烃的命名 (四) 烯烃的物理性质 (五) 烯烃和炔烃的化学性质 (六) 烯烃和炔烃的工业来源和制法
第三章 不饱和烃
含有碳碳重键(C=C或C≡C)的开链烃称为不饱和烃。 例如:
(一) 烯烃和炔烃的结构
(1) 烯烃的结构 (2) 炔烃的结构
CH=CH2
5-乙烯基-2-辛烯-6-炔
(3) 烯烃的顺反异构体的命名
(甲) 顺反命名法
两个双键碳上相同的原子或原子团在双键的同一侧者, 称为顺式,反之称为反式。例:
2-丁烯: H3C
CH3
C=C
H
H
( I):m.p
。
-132 C
顺-2-丁烯
H3C
H
C=C
H
CH3
(II):m.p -105。C
反-2-丁烯
H C
H
CH3 C
H
丙烯的结构
H C
H
C2H5 C
H
丁烯的结构
小结
π键的特性:
①π键不能自由旋转。 ②π键键能小,不如σ键牢固。
碳 碳 双 键 键 能 为 611KJ/mol, 碳 碳 单 键 键 能 为 347JK/mol,
《有机化学》(第四版)第三章-不饱和烃(习题答案)

《有机化学》(第四版)第三章-不饱和烃(习题答案)第三章不饱和烃思考题习题3.1 写出含有六个碳原子的烯烃和炔烃的构造异构体的构造式。
其中含有六个碳原子的烯烃,哪些有顺反异构?写出其顺反异构体的构型式(结构式)。
(P69) 解:C6H12有13个构造异构体,其中4个有顺反异构体:CH2=CHCH2CH2CH2CH3CH3CH=CHCH2CH2CH3CH3CH2CH=CHCH2CH3(Z,E)(Z,E)CH2=CCH2CH2CH3CH3CH2=CHCHCH2CH3CH3CH2=CHCH2CHCH3CH3CH3C=CHCH2CH33CH3CH=CCH2CH3CH3CH3CH=CH2CHCH33(Z,E) (Z,E)CH2=CHCCH3CH3CH3CH2=CCHCH3CH3CH3CH3C=CCH3CH3CH3CH22CH3CH2CH3C6H10有7个构造异构体:CH CCH2CH2CH2CH3CH3C CCH2CH2CH3CH3CH2C CCH2CH3CH CCHCH2CH33CH CCH2CHCH33CH CC(CH3)3CH3C CCHCH33习题3.2 用衍生物命名法或系统命名法命名下列各化合物:(P74)(1) (CH3)2CHCH=CHCH(CH3)2对称二异丙基乙烯or 2,5-二甲基-3-己烯 (2) (CH 3)2CHCH 2CH=CHCHCH 2CH 3CH 3123456782,6-二甲基-4-辛烯(3) CH 3CH 2CCCH 2CH 3123456二乙基乙炔 or 3-己炔(4) CH 3CH 2C(CH 3)2C CH123453,3-二甲基-1-戊炔(5) CH 2=CHCH 2C CH123451-戊烯-4-炔(6)HCC C=CCH=CH 2CH 2CH 2CH 3CH 2CH 2CH 31234563,4-二丙基-1,3-己二烯-5-炔(7) CH 3CH 32,3-二甲基环己烯 (8)CH 3CH 35,6-二甲基-1,3-环己二烯习题3.3 用Z,E-命名法命名下列各化合物:(P74)(1) ↑C=CCH 2CH 3H ClBr↑ (Z)-1-氯-1-溴-1-丁烯 (2) ↓C=CFCH 3ClCH 3CH2↑ (E)-2-氟-3-氯-2-戊烯(3) ↑C=CCH 2CH 3CH 2CH 2CH 3H CH 3↓ (E)-3-乙基-2-己烯 (4) ↓C=CCH(CH 3)2CH 2CH 2CH 3CH 3H↑ (E)-3-异丙基-2-己烯习题3.4 完成下列反应式:(P83)(1) C 3H 7C CC 3H 7C=C H C 3H H C 3H 7(2) 3C 3H 7C CC 3H 7C=C H C 3H C 3H 7H(3) + Br 2HC 2H 5C 2H 5HH C 2H 5BrC 2H(4)C C HOOCCOOH C=C HOOCBrBrCOOH+ Br 2习题3.5 下列各组化合物分别与溴进行加成反应,指出每组中哪一个反应较快。
有机化学b教学课件-第3章不饱和烃:烯烃、炔烃和二烯烃--课后更新

第3章不饱和烃:烯烃、炔烃和二烯烃出列反应的主要产物并给出合的反应机z 写出下列反应的主要产物,并给出合理的反应机理。
Br 2h ν反应机理:Br 2h νBr ⋅链引发:Br ⋅HBr ++链转移:Br 2+Br ⋅+链终止Br ⋅+链终止:z写出下列反应的主要产物,并给出合理的反应机理。
出列反应的主要产物并给出合的反应机HBr反应机理:H+Br−不饱和烃烯烃炔烃二烯烃3.1 烯烃烯烃:是一类含有碳碳双键的不饱和烃。
式通式:C Hn2n与环烷烃互为构造异构体烯烃的结构 乙烯的结构轨道侧面重叠成的键重叠程z 由两个p 轨道侧面重叠而成的π键,重叠程度比σ键小的多。
所以π键不如σ键稳定,易断裂。
双键键长比碳碳单键的键长短。
键能为:610.9-347.3键能为:347.3 KJ/mol=263.6KJ/molπ键电子云比较分散,有较大的流动性,容z键电子云比较分散有较大的流动性容易极化变形,化学反应性较强。
乙烯的结构构造异构:因碳链的不同和双键在碳链上的 构造异构因碳链的不同和键在碳链上的位置不同产生的各种异构体。
位置异构位异构碳链异构顺反异构:π键不具轴对称性,双键旋转受阻。
33立体异构:构型立体异构构型双键碳原子上各连有两个不相同的原子或基团时烯烃的命名(系统命名法)z 母体命名为“烯”,编号时优先照顾官能团双键。
①选择主链②编号:不饱和碳近端开始135246③写出名称:注明双键位置4-甲基-2-己烯154甲基环321,5-二甲基环戊烯链长大于十个碳时,烯前加“碳”字,如:十一碳烯z 链长大于十个碳时,烯前加碳字,如:十碳烯烯烃顺反异构体的命名z 在顺反异构体的系统命名前加“顺”或“反”表示构型。
相同基团在双键同侧称为顺,异侧称为反。
顺-2-丁烯1234反-2-氯-2-丁烯反-2-丁烯烯烃的顺反异构现象a ab b(i)(ii)(iii)(iv)z 顺反异构的必要条件:双键所连的碳原子分别连有两个不同的原子或基团。
第六讲 第三章 不饱和烃:烯烃和炔烃(2)
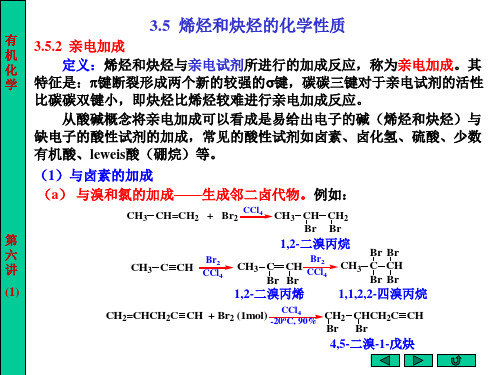
C C
+
H-X
-X -
C=C H
+
+X快
C=C X H
乙烯基碳正离子
由于卤素的吸电子作用, 阶段。 几 1 由于卤素的吸电子作用,反应能控制在加一分子 HX 阶段。 加成, 加成 常用汞盐和铜盐做催化剂。 点 2 与HCl加成,常用汞盐和铜盐做催化剂。 讨 3 与卤化氢的加成,在相应卤离子(如:(CH3 )4N+Cl-)存在下, 与卤化氢的加成,在相应卤离子( 存在下, 论 通常进行反式加成。例如: 通常进行反式加成。例如:
*1. Markovnikov规则 不对称烯烃与氯化氢等极性试剂进行加成反应时, 规则 不对称烯烃与氯化氢等极性试剂进行加成反应时, 氢原子总是加到含氢较多的双键碳原子上, 氢原子总是加到含氢较多的双键碳原子上,氯原子或其它原子或基团则加 到含氢较少的或不含氢的双键碳原子上。这条经验规则简称马氏规则。 到含氢较少的或不含氢的双键碳原子上。这条经验规则简称马氏规则。 例如
CH3CH2CH=CH2 + HBr HAc 80% (CH3)2C=CH2 + HCl CH3CH2CH2CH2Br
~100%
(CH3)2C CH3 Cl
第 六 讲 (6)
*2. 不对称炔烃与卤化氢等极性试剂进行加成反应时,也符合马氏规则。 不对称炔烃与卤化氢等极性试剂进行加成反应时,也符合马氏规则。 Br 例如 (CH3)2CHC CH HBr (CH3)2CHC=CH2 HBr (CH3)2CH C CH3
NaCl CH2=CH2 + Br2 水溶液
Br H2C CH2 Br 1,2-二溴乙烷 二溴乙烷
Cl H2C CH2 Br 1-氯-2-溴乙烷 氯 溴乙烷
有机化学-第三章不饱和烃:烯烃和炔烃

a
18
分子的结构包括分子的构造、构型和构象。
同分异构
构造异构
碳架异构 官能团位次异构 官能团异构
互变异构
立体异构
构型异构
顺反异构 对映异构
构象异构
a
19
当两个双键碳原子均连接不同的原子或基团时,即产 生顺反异构现象。如下列三种形式的烯烃都有顺反异构 体,而其它形式的烯烃则没有顺反异构体。
a
20
3.3 烯烃和炔烃的命名
构 型 异 构 体 : ( I) 和 ( Ⅱ ) 是 由 于 构 型 不 同 而 产 生 的 异 构 体 , 称 为 构 型 异 构 体 (configurational isomers)。构型异构体具有不同的物理性质。
a
17
顺反异构体:像(I)和(Ⅱ)这种构型异构体通常用顺、反 来区别,称为顺反异构体(cis and trans ismers),也称几 何异构体(geometric ismers)。
对于碳原子数相同的烯烃顺反异构体,顺式异构 体的沸点比反式异构体略高,而熔点则是反式异构体 比顺式异构体略高。
a
44
与烷烃相似,折射率也可用于液态烯烃和炔烃的鉴 定和纯度的检验。在分子体系中,由于电子越容易极化, 折射率越高,因此,烯烃和炔烃的折射率一般比烷烃大。
a
45
3.5 烯烃和炔烃的化学性质
不饱和链烃分子中同时含有碳碳双键和三键的化合物 称为烯炔。在系统命名法中,选择含有双键和三键在内的 最长碳链作为主链,一般称为“某烯炔”(“烯”在前、 “炔”在后),碳链的编号遵循“最低系列”原则,使双 键、三键具有尽可能低的位次号,其它与烯烃和炔烃命名 法相似。
a
37
但主链编号若双键、三键处于相同的位次供选择时,优 先给双键以最低编号。例如:
有机化学第03章 烯炔烃
~
。
具有下列构型的烯烃均有顺反异构: 具有下列构型的烯烃均有顺反异构:
a b
C
a C b
a b
C
C
a d
a b
C
C
d e
注意:任何一个双键C上有相同基团,则无顺反异构。 注意:任何一个双键C上有相同基团,则无顺反异构。
⑵ 命名 顺反命名: ①顺反命名:
若取代基的第一个原子相同,则要外推比较。 ③若取代基的第一个原子相同,则要外推比较。 例: 比较大小: —CH2OH , —CH2CH3 原子序数: ﹥ 原子序数:O﹥C ∴前者为较优基团 比较大小: 比较大小: —C(CH3)3 ; C(C,C,C) ) —CH(CH3)2 ; C(C,C,H) —CH2CH3 ; C(C,H,H)化轨道 sp杂化的C原子, 杂化的 杂化轨道的电负性。 的电负性大于sp2杂化轨道的电负性。 从而使叁键比双键键短;叁键中π 从而使叁键比双键键短;叁键中π键P 轨道之间重叠程度及核对π 轨道之间重叠程度及核对π电子的束缚 力均大于烯烃。 力均大于烯烃。 炔烃π键的断裂和极化较烯烃困难。 ∴炔烃π键的断裂和极化较烯烃困难。
a
b
例题1 例题1
C
C
CH3 H
d
e
C
若 a >b , 若 a >b ,
C CH3 H
d>e d> d< d <e
C
则:(Z)(Z)(E)则:(E)C H CH3
CH3 H
(Z)-2-丁烯 ) 丁烯
(E)-2-丁烯 ) 丁烯
例题2 例题2
CH3 C2H5
C
CH3 C H
CH3 C2H5
有机化学3--- 烯烃和炔烃
3.4 烯烃和炔烃的化学性质
◇ 反应机理和烯烃与卤素的加成相似: 第一步:
第二步:
H X 慢 C C H X
C C
H
X
快
C C
H X
不同的是: 第一步进攻的是H+, 且不生成鎓离子; 第二步X- 的进攻也不一定是反式加成。 ◇ 烯、炔与HX等的加成反应以用于工业生产:
CH2 CH2 HCl AlCl3 130~250℃ CH3CH2Cl
C
Br
速度控制步骤
溴鎓离子
C Br
C
Br
快 Br
Br C C
反式加成产物
3.4 烯烃和炔烃的化学性质
◇ 反应经历溴鎓离子、反式加成。
Br
H C CH 3 C CH3 H Br 2 H3 C H C
+ -
Br H CH 3 H Br
-
H 3C C C
H
C Br
CH 3 CH 3 H C Br C
Br
H2
H
H
C2 H4
H
H
CH2=CH2
H-CH2-CH2-H
3.4 烯烃和炔烃的化学性质
R-C C-R' H2 Pd
R C C
R'
H2 Pd
H
H
RCH2CH2R'
常用催化剂:Pt , Pd , Ni,一般难控制在烯烃阶段。 林德拉(Lindlar)催化剂,一种部分毒化的Pd催化剂,能降 低活性,选择性氢化炔键而不影响烯键,且得顺式烯烃。
同碳数烯烃顺反异构体,因几何形状(结构)不同,物理 性质不同。
CH3 C
H
CH3
H C C
H
《有机化学》第三章 不饱和烃
吸电子基团: +NR3>NO2>CN>COOH>F>Cl>Br>I>COOR>OR>
COR>SH>OH> C CR>C6H5>CH=CH2>H
诱导效应的特点:
(1)诱导效应的强弱取决于原了或基团的电负性的大小
的两原子可相对的自由旋转。 能相对自由旋转。Βιβλιοθήκη c.键的可极化度:较小。 较大
1.2 单烯烃的异构现象
1.2.1 结构异构
CH3 CH2 CH CH2 CH3 CH CH CH3
1-丁 烯
2-丁 烯
官能团碳碳双键 位置异构
CH3 C CH2 2-甲 基 丁 烯 CH3
碳链异构
结构异构是由于分子中各原子的结合顺序不同而引起的, 位置异构和碳链异构均属于结构异构。
(2) 与卤化氢的加成
CH3CH CHCH3 + HCl CH3CH2CHCH3
2–丁烯
HBr CH3CH2CH CH2
Markovnikov规则
Cl
2–氯丁烷
Br
CH3CHCH CH3
80 %
CH3CHCH2 CH2Br 20 %
当不对称的烯烃与卤化氢等极性试剂加成时,氢原总
是加到含氢较多的双键碳原子上,卤原子(或其子或
上相互重叠。
从侧面重叠。
电子云的分布情况 a. 电子云集中于两原子 电子云分布在 键所
核的连线上,呈圆柱形分布。 在平面的上下两方,呈块
状分布。
第3章 烯烃 炔烃 二烯烃
pm 109 H 134 pm C C H 121°
H 117. 5° H
2. 炔烃的结构
炔烃分子中C≡C叁键碳原子是 sp杂化。 sp 杂化轨道中 s 成分比 sp2 杂化和 sp3 杂 化的高,键长 C=C(134pm)比 C—C (154pm)短。以乙炔为例:
H
C
120 pm
108 pm C H
H3C H
C=C
CH2CH3 CH3
顺 -3-甲 基 -2-戊 烯
反 -3-甲 基 -2-戊 烯
CH3 C=C CH3CH2
CH3 CH(CH3)2
CH2Cl C=C CH3
CH3 CH2CH3
顺 -2,3,4-三甲基 -3-己烯
反 -2,3-二甲基 -1-氯 -2-戊烯
CH3 C=C CH3CH2 Br
CH3
a≠b 且 c≠d
2、顺/反(cis/trans)命名法:
(1) a=c或b=d时的顺/反异构标记 相同的原子或原子团在双键的同侧为顺 式,异侧为反式。
a b C C
c d
a=c或b=c 或 a=d或
CH3 H C C
H CH3
H CH3 C C
H CH3
H3C H
C=C
CH3 CH2CH3
180°
C=C(134pm),C—C(154pm)
比较σ键和π键的异同点:
σ键的特点 (1)形成: (3)重叠程度: 键能: 沿键轴 大 大 轴对称 (5)旋转性: (6)存在形式: 可以独立 (2)重叠方式: “头碰头” π键的特点 垂直于键轴 “肩并肩” 小 小 呈块柱状 平面对称小 不能 不能
(二)诱导效应(inductive effect)
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2020/7/11
8
2.π键与σ键不同,π键不能单独存在,只能与σ键共存于双 键和三键中;π键不是沿成键两原子核联线为对称轴交盖 的,而是由p轨道侧面平行交盖,因此只有当p轨道的对称 轴平行时交盖程度最大。若碳碳之间相对旋转则平行破坏, 这时π键必将减弱或断裂,所以碳碳双键与单键不同,是 不能自由旋转的 。
2020/7/11
20
3.3 烯烃和炔烃的命名
3.3.1 烯基和炔基
烯烃和炔烃分子从形式上去掉一个氢原子后剩下的基 团,分别称为烯基和炔基,必要时加以定位,定位数放在 基名之前,定位时碳原子的编号以连接基的碳原子编号为1。
2020/7/11
21
与烷基相似,一个不饱和烃从形式-亚乙烯基。
2020/7/11
7
3.1.3 π键的特性
1. π键是由两个p轨道从侧面平行交盖而成的,轨道交盖程度一般比σ
键要小,另外,π键的电子云不像σ键的电子云那样集中于两个成键 原子核之间的联线上,而是在成键原子周围分散成上下两层,这样 原子核对π电子的束缚力较小,所以π电子云具有较大的流动性,易 受外界电场影响而发生极化,因此,与σ键比较, π键不如σ键牢固, 不稳定而容易断裂,表现较大的化学活泼性。
2020/7/11
22
3.3.2 烯烃和炔烃的命名
1. 衍生命名法
烯烃的衍生命名法是以乙烯为母体,将其它烯烃看作 乙烯的烷基衍生物来命名;炔烃的命名是以乙炔为母体, 将其它炔烃看作乙炔的烷基衍生物来命名。例如:
2020/7/11
23
54
3
2
1
2.系统命名法
3,3-二甲基-1-戊炔
(1)选择含有重键在内的最长碳链作为主链,支链作为
2020/7/11
9
3.1.4 碳原子轨道的sp杂化 HCCH
1/2s +1/2p
2020/7/11
sp杂化碳原子的p轨道分布图
10
3.1.5 碳碳三键的组成
在乙炔分子中,一个碳原子以sp杂化轨道与另一 个成键碳原子的sp杂化轨道相互交盖而形成碳碳σ键。 同时两个三键碳原子各以另一个sp杂化轨道与氢原子 的1s轨道交盖形成碳氢σ键。乙炔分子中的三个σ键, 其对称轴同在一条直线上。
碳架异构 官能团位次异构 构造异构 官能团异构 互变异构
2020/7/11
14
2020/7/11
15
碳碳双键不能绕键轴自由旋转。因此,当两个双键碳 原子各连有两个不同的原子或基团时,可能产生两种不同 的空间排列方式。
2020/7/11
16
一些烯烃的物理性质
构型:(I)和(Ⅱ)的分子式相同,构造亦相同,但分子中的原子在空间 排列不同。分子中原子在空间的排列形式称为构型。
2020/7/11
5
由于每个碳原子上余下的p轨道的对称轴垂直于同一 平面,且彼此平行,这样两个p轨道就从侧面相互平行交 盖成键,组成新的轨道,称为π轨道。处于π轨道的电子称 为π电子,这样构成的共价键称为π键。
2020/7/11
6
π键的形成,若根据分子轨道理论的近似处理也一样, 两个碳原子的p轨道通过原子轨道的线性组合而形成两个分 子轨道,一个是比原来原子轨道能量低的成键轨道π,一个 是比原来原子轨道能量还要高的反键轨道π*。
2020/7/11
11
在两个三键碳原子上各余下的两个相互垂直的p轨 道,其对称轴两两平行,从侧面相互交盖而形成两个 互相垂直的π键。两个π键的电子云围绕在两个碳原子 核联线的上、下、左、右,对称分布在碳碳σ键周围。
2020/7/11
12
由以上讨论可知,碳碳双键是由一个σ键和一个π键 组成,碳碳三键是由一个σ键和两个π键组成,但通常分 别用两条或三条单线表示,其模型如下。
2020/7/11
18
分子的结构包括分子的构造、构型和构象。
同分异构
构造异构
碳架异构 官能团位次异构 官能团异构
互变异构
立体异构
构型异构
顺反异构 对映异构
构象异构
2020/7/11
19
当两个双键碳原子均连接不同的原子或基团时,即产 生顺反异构现象。如下列三种形式的烯烃都有顺反异构 体,而其它形式的烯烃则没有顺反异构体。
2020/7/11
3
3.1.1 碳原子轨道的sp2杂化
H
H
CC
H
H
1/3s +2/3p
2020/7/11
4
3.1.2 碳碳双键的组成
在乙烯中,成键的两碳原子各以一个sp2杂化轨道彼 此交盖形成一个C—C σ键,并各以两个sp2杂化轨道分 别与两个氢原子的1s轨道形成两个C—H σ键,这样形成 的五个σ键其对称轴都在同一平面内。
第三章 不饱和烃:烯烃和炔烃
在开链碳氢化合物分子中,含有碳碳重键(碳碳双键 或/和碳碳三键)时统称开链不饱和烃或不饱和脂肪烃, 简称不饱和烃(unsaturated hydrocarbon)。
含有一个碳碳双键者称为烯烃(alkenes),亦称单烯 烃,通式为CnH2n,碳碳双键( C=C)是烯烃的官能团。
2020/7/11
13
3.2 烯烃和炔烃的同分异构
与烷烃相似,烯烃和炔烃也有同系列,相邻两个同系 物之间也相差一个CH2,CH2也是它们的系差。
烯烃和炔烃不仅存在碳架异构,还存在官能团位次 (重键位次)异构。无论是碳架异构还是官能团位次异构, 都是由于原子在分子中的排列和结合的顺序不同,即成键 顺序不同引起的,都属于构造异构。
构型异构体:(I)和(Ⅱ)是由于构型不同而产生的异构体,称为构型异 构体(configurational isomers)。构型异构体具有不同的物理性质。
2020/7/11
17
顺反异构体:像(I)和(Ⅱ)这种构型异构体通常用顺、反 来区别,称为顺反异构体(cis and trans ismers),也称几 何异构体(geometric ismers)。
2020/7/11
1
含一个碳碳三键者称为炔烃(alkynes),通式为CnH2n-2, 碳碳三键(一C≡C一)是炔烃的官能团。分子中既含有碳碳 双键,又含有碳碳三键者称为烯炔。
2020/7/11
2
3.1 烯烃和炔烃的结构
碳碳双键是由两对共用电子构成,通常用两条短线表 示:C=C。碳碳三键由三对共用电子构成,通常用三条 短线表示:C≡C。但实验事实表明,它们都不是由两个 或三个σ键加合而成:
