初三化学上册单元练习题及答案之令狐文艳创作
预防与控制医院感染习题及答案之令狐文艳创作

第七章预防与控制医院感染试题令狐文艳一、解释名词(20分)[1]医院感染[2]清洁[3]消毒[4]灭菌二、填空题(6分)[1]构成感染链的三个基本条件是感染源、()和()。
[2]根据病原体的来源分类,可将医院感染分为()感染和()感染。
[3]紫外线灯管消毒空气时,有效距离不超过()米,照射时间为()分钟。
三、判断题(5分)[1]只要在出院后发生的感染即不属于医院感染。
()[2]医院感染的对象主要包括住院患者和医院工作人员。
( )[3]只要在住院期间发生的感染均属于医院感染。
( )[4]已感染的患者和病原携带者是最重要的感染源。
( )[5]压力蒸汽灭菌法是热力消毒灭菌法中效果最为可靠的一种方法。
( )四、选择题(10分)[1]医院感染的主要对象是( )A、门诊患者B、急诊患者C、住院患者D、探视者E、陪护着[2]破伤风病人用过的换药器械的处理:( )A、用水冲洗后消毒B、消毒后清洁C、水泡后消毒D、清洁后消毒E、以上都不对[3]以下不属于医院感染的是( )A、新生儿肺炎B、新生儿脐炎C、新生儿腹泻D、新生儿败血症E、新生儿硬肿症[4]关于高压蒸汽灭菌,不正确的是:( )A、无菌包不宜过大B、放置无菌包不宜太紧C、布类物品放在金属物品之下D、高压锅内物品不能装得太多E、放置时各包之间要有空隙[5]流感病人出院后病室空气消毒,常用消毒剂为:( )A、食醋B、苯扎溴铵C、酒精D、氯胺E、漂白粉五、简答题(9分)[1]简述医院感染发生的原因。
(5分)[2]简述医院感染的危害。
(4分)答案部分一、名词解释[1]医院感染:是指住院患者在医院内获得的感染,包括在住院期间发生的感染和在医院内获得而出院后发生的感染;但不包括入院前已开始或入院时已处于潜伏期的感染。
[2]清洁:是指用物理方法清除物体表面的污垢、尘埃和有机物,其目的是去除和减少微生物而非杀灭微生物。
[3]消毒:是指用物理或化学方法清除或杀灭传播媒介上除芽孢以外的所有病原微生物。
初三化学拔高题之令狐文艳创作

点燃 MnO 2 高温 化学拔高题令狐文艳第一部分 选择题(共40分)一、(本题包括15小题,每小题2分,共30分。
每小题只有一个选项符合题意。
)1.古诗词给我们留下了宝贵的精神财富,下列诗句中一定发生化学变化的是A.白玉做床金做马(引自《红楼梦》)B.大河上下,顿失滔滔(引自毛泽东诗词)C.古今将相在何方?荒冢一堆草没了. (引自《红楼梦》)D.粉身碎骨浑不怕,要留清白在人间.(引自明朝于谦诗)2.双氧水和二氧化锰制氧气反应中,反应前后质量和化学性质都没改变的是A.H 2O 2B.MnO 2C.H 2OD.O 23.在CO + CuO ==== Cu + CO 2反应中,Cu 元素由+2价变为0价,H 元素由0价变为+1价。
这类有化合价变化的反应属于氧化还原反应。
据此判断,下列反应不属于氧化还原反应的是A. S + O 2 ==== SO 2B. Na 2CO 3 +Ca(OH)2 = CaCO 3↓+ 2NaOHC. 2KClO ===== 2KCl + 3O 2↑D.3CO + Fe 2O 3=== 2Fe +3CO 24.在下列试验物质导电性的实验中,接通电源后不亮的灯泡是A .①②B .③④⑤C .③④D .②⑤5.“神舟六号”载人飞船于去年下半年成功发射,搭载2名航天员在太空飞行了5天。
目前,中国航天的目标将瞄准建立空间站和空间实验室。
若在太空飞船中点燃一根火柴,火柴会A .能够燃烧,和地球上现象相同B .不能持续燃烧,很快就熄灭C .能够燃烧,且燃烧更剧烈D .以上答案都不对6.与 中的“l ”关系密切的是A .质子数、电子总数B .元素化学性质、化合价C .物质状态、电子层数D .原子结构、中子数7.用酸A 跟足量的碳酸钠固体反应,并将生成的气体通入澄清石灰水中,在较长一段时间内未发现石灰水变浑浊,则酸A 是A .浓硫酸B .稀硫酸C .磷酸①盐酸 ②无水酒精 ③NaOH 溶液 ④NaCl 溶液 ⑤H 2O ② ① ③ ④ ⑤D.浓盐酸8.下列变化中存在化学能转化为光能的是A.灯泡通电发光 B.镁条在空气中燃烧 C.锌与稀盐酸反应 D.电解水9.某溶质溶解在水中,形成的溶液与水相比较,一定不会改变的是A.沸点 B.导电性 C.颜色 D.水分子的构10.在实验室中常将白磷浸没在水中保存,其主要目的是A.降低白磷的着火点B.防止白磷与空气接触C.使白磷与水结合成稳定的物质D.将白磷溶解不易着火11.要检验某物质中是否含有淀粉,下列使用的试剂正确的是A.用稀盐酸B.用紫色的石蕊试液C.用碘水或碘酒D.用浓硝酸、重金属盐或甲醛12.关于用水制二级能源氢气,以下研究方向不正确的是A.设法将太阳能聚焦,产生高温,使水分解产生H2B.寻找高效催化剂,使水分解产生氢气,同时吸收能量C.构成水的氢和氧都是可以燃烧的物质,因此可研究在水不分解情况下,使氢成为二级能源D.寻找特殊化学物质,用于开发廉价能源,以分解水制取H 213.将一套如图所示的密闭装置放在天平上,使天平平衡,经过一段时间后,出现的情况是 A .指针偏左,食盐溶液一定变浓,烧碱变质B .指针偏左,食盐溶液一定变浓,烧碱潮解C .指针偏右,食盐溶液一定变浓,烧碱潮解D .指针偏右,食盐溶液一定饱和,烧碱潮解14.下列实验操作,能达到预期目的的是①用托盘天平称取5.6g CuO 粉末②用10mL 水和10mL 酒精配制成20mL 酒精溶液③将50g 溶质质量分数为10%的稀盐酸加热蒸发掉25g 水,得到溶质质量分数为20%的盐酸④用10mL 量筒量取8.2mL 水A .①④ B.①②④ C.①③④ D.②③15.小莹同学向过量的稀硫酸中加入一定质量的镁条后,绘制了如下表示其变化过程的坐标曲线图,其中不正确的是二、(本题包括4小题,每小题2分,共8分。
常用化学仪器及使用方法之令狐文艳创作
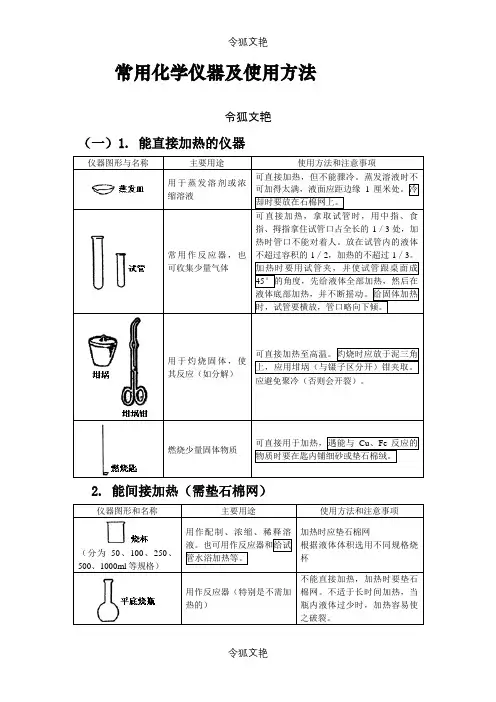
常用化学仪器及使用方法令狐文艳(一)1. 能直接加热的仪器仪器图形与名称主要用途使用方法和注意事项用于蒸发溶剂或浓缩溶液可直接加热,但不能骤冷。
蒸发溶液时不可加得太满,液面应距边缘1厘米处。
冷却时要放在石棉网上。
常用作反应器,也可收集少量气体可直接加热,拿取试管时,用中指、食指、拇指拿住试管口占全长的1/3处,加热时管口不能对着人。
放在试管内的液体不超过容积的1/2,加热的不超过1/3。
加热时要用试管夹,并使试管跟桌面成45°的角度,先给液体全部加热,然后在液体底部加热,并不断摇动。
给固体加热时,试管要横放,管口略向下倾。
用于灼烧固体,使其反应(如分解)可直接加热至高温。
灼烧时应放于泥三角上,应用坩埚(与镊子区分开)钳夹取。
应避免聚冷(否则会开裂)。
燃烧少量固体物质可直接用于加热,遇能与Cu、Fe反应的物质时要在匙内铺细砂或垫石棉绒。
2. 能间接加热(需垫石棉网)仪器图形和名称主要用途使用方法和注意事项(分为50、100、250、500、1000ml等规格)用作配制、浓缩、稀释溶液。
也可用作反应器和给试管水浴加热等。
加热时应垫石棉网根据液体体积选用不同规格烧杯用作反应器(特别是不需加热的)不能直接加热,加热时要垫石棉网。
不适于长时间加热,当瓶内液体过少时,加热容易使之破裂。
用作在加热条件下进行的反应器不能直接加热,应垫石棉网加热。
所装液体的量不应超过其容积1/2。
用于蒸馏与分馏,也可用作气体发生器加热时要垫石棉网。
也可用其他热浴。
用作接受器用作反应器,常用于滴定操作一般放在石棉网上加热。
在滴定操作中液体不易溅出。
3. 不能加热的仪器仪器图形与名称主要用途使用方法及注意事项用于收集和贮存少量气体上口为平面磨砂,内侧不磨砂,玻璃片要涂凡士林油,以免漏气,如果在其中进行燃烧反应且有固体生成时,应在底部加少量水或细砂。
分装各种试剂,需要避光保存时用棕色瓶。
广口瓶盛放固体,细口瓶盛放液体。
瓶口内侧磨砂,且与瓶塞一一对应,切不可盖错。
反应热、中和热、燃烧热的联系与区别之令狐文艳创作
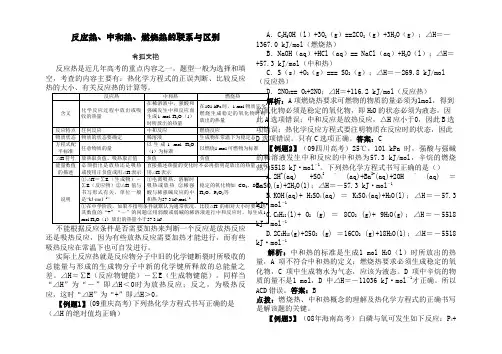
反应热、中和热、燃烧热的联系与区别令狐文艳反应热是近几年高考的重点内容之一,题型一般为选择和填空,考查的内容主要有:热化学方程式的正误判断、比较反应反应热中和热燃烧热含义化学反应过程中放出或吸收的热量在稀溶液中,强酸和强碱发生中和反应而生成1 mol H2O(l)时所放出的热量在101 kPa时,1 mol物质完全燃烧生成稳定的氧化物时所放出的热量反应特点任何反应中和反应燃烧反应物质状态物质的状态要确定稀溶液生成物在常温下为稳定态方程式配平标准任意物质的量以生成1 mol H2O(l)为标准以燃烧1 mol 可燃物为标准△H符号放热取负值、吸热取正值负值负值能量数值的描述必须指出是放热还是吸热或使用正负值或用△H表示直接描述热量的变化时不必再指明是放出的热量,可用△H表示说明①△H=∑E(生成物)-∑E(反应物)②△H值与书写形式有关,单位一般是“kJ·mol-1”①电离吸热、溶解时吸热或放热②稀强酸与稀强碱反应的中和热为57.3 kJ·mol-1稳定的氧化物如CO2、SO2、H2O、P2O5等①在中学阶段,如果不指明条件就默认为通常状况,比较△H的相对大小时要考虑其数值的“+”“-”的问题②用弱酸或弱碱的稀溶液进行中和反应时,每生成1 mol H2O(l)放出的热量小于57.3 kJ还是吸热反应,因为有些放热反应需要加热才能进行,而有些吸热反应在常温下也可自发进行。
实际上反应热就是反应物分子中旧的化学键断裂时所吸收的总能量与形成的生成物分子中新的化学键所释放的总能量之差。
△H=∑E(反应物键能)-∑E(生成物键能)。
同样当“△H”为“-”即△H<0时为放热反应;反之,为吸热反应,这时“△H”为“+”即△H>0。
【例题1】(09重庆高考)下列热化学方程式书写正确的是(△H的绝对值均正确)A.C2H5OH(l)+3O2(g)==2CO2(g)+3H2O(g);△H=-1367.0 kJ/mol(燃烧热)B.NaOH(aq)+HCl(aq)== NaCl(aq)+H2O(l);△H=+57.3 kJ/mol(中和热)C.S(s)+O2(g)=== SO2(g);△H=-269.8 kJ/mol (反应热)D.2NO2== O2+2NO;△H=+116.2 kJ/mol(反应热)解析:A项燃烧热要求可燃物的物质的量必须为1mol,得到的氧化物必须是稳定的氧化物,即H2O的状态必须为液态,因此A选项错误;中和反应是放热反应,△H应小于0,因此B选项错误;热化学反应方程式要注明物质在反应时的状态,因此D选项错误。
0.1M氢氧化钠标准溶液的配置之令狐文艳创作

0.1mol/L氢氧化钠标准溶液
令狐文艳
(一)配制
称取4.2g分析纯氢氧化钠溶于蒸馏水中,稀释至1升(约1千克) 。
(二)标定
1. 苯二甲酸钾(分子量204.23)标定:称取经120℃干燥过的分析纯苯二甲酸氢钾(KHC8H4O4)4.0000g(四位有效数字)于250ml烧杯中,加蒸馏水100ml,温热使其溶解,加入酚酞指示剂2~3滴,用配置好的氢氧化钠溶液滴定至淡红色,并在2分钟内不变色为终点。
KHC8H4O4+NOH→KNaC8H4O4+H2O
N = G /(V×0.2042)
式中:N------标准氢氧化钠的当量浓度
G------苯二甲酸氢钾的重量(g)
V------耗用标准氢氧化钠溶液的体积
2. 盐酸标定:用移液管吸取已标定的0.1N盐酸溶液25ml于250ml的锥形瓶中,加蒸馏水80ml,加入甲基橙指示剂3~4滴,用配置好的氢氧化钠溶液滴定至黄色,并在2分钟内不变色为终点。
N = ( N1×25)/ V
式中:N------标准氢氧化钠的当量浓度
V------耗用标准氢氧化钠溶液的体积
N1------标准盐酸的当量浓度。
碱式碳酸铜的制备之令狐文艳创作

实验项目:碱式碳酸铜的制备令狐文艳实验目的:通过碱式碳酸铜制备条件的探求和生成物颜色,状态的分析,研究反应物的合理配料比并确定制备反应合适的温度条件,以培养独立设计实验的能力。
实验药品及仪器:仪器:台秤、烧杯,玻璃棒、吸滤瓶、布氏漏斗,试管,滴管、吸量管药品:CuSO4·5H2O、Na2CO3实验原理:根据CuSO4与Na2CO3反应的化学方程式:2 CuSO4+ 2Na2CO3+H2O=Cu2(OH)2CO3↓+2 Na2SO4+ CO2↑可制得Cu2(OH)2CO3实验内容:1、反应物溶液配制分别称取12.5g CuSO4·5H2O, 5.3 g Na2CO3,各配成100ml0.5mol/L的溶液。
2、制备反应条件的探求(1)CuSO4和Na2CO3溶液的合适配比置于四支试管内均加入2.0ml 0.5mol/L CuSO4溶液,再分别取0.5mol/LNa2CO3溶液1.6ml,2.0ml,2.4ml,2.8ml依次加入另外四支编号的试管中。
将八支试管放在75℃的恒温水浴中。
几分钟后,依次将CuSO4溶液倒入Na2CO3溶液中,振荡,水浴加热。
通过比较反应的速度、沉淀的多少、沉淀的颜色得出最佳物料比。
(2)反应温度的探求分别在三支试管中加入2.0ml CuSO4溶液,另取三支试管,各加入由上述实验得到的合适用量的Na2CO3溶液,从两列试管中各取一支,分别置于室温,50℃、100℃的恒温水浴中,数分钟后将CuSO4倒入Na2CO3溶液中,振荡,由实验结果确定制备反应的合适温度。
3、碱式碳酸铜制备取60ml 0.5mol/L CuSO4溶液根据上面实验确定的反应物的合适比例及适宜温度制取Cu2(OH)2CO3。
沉淀完全后,用蒸馏水洗涤沉淀数次,直到沉淀中不含SO42-为止,吸干。
将所得产品用水浴烘干,待冷至室温后称量,计算产率。
数据记录及处理2 CuSO4 ~ Cu2(OH)2CO3得2×160 2220.6×160÷250×12.5 x 320÷4.8=222÷x , x=3.33g∴理论产量=3.33g实验十九碱式碳酸铜的制备一、实验目的1. 通过查阅资料了解碱式碳酸铜的制备原理和方法。
九年级化学上册实验题之令狐文艳创作
实验题练习令狐文艳1.过氧化钠(Na2O2)是一种浅黄色的固体,常温下能与二氧化碳反应生成氧气:2Na2O2+2CO2=2Na2CO3+O2某学生以石灰石、稀盐酸和过氧化钠为原料制取氧气,设计出如下图所示实验装置,请你按下列要求回答:(1)编号为a、b、c的仪器名称:a______ b_______ c_______(2)A装置中反应的化学方程式是:______________________________;(3)检验D装置中是否收集满氧气的方法是:_______________________;(4)表明过氧化钠样品已完全反应的现象是:_________________________2.冬日里的一天,某班教室的暖气片和暖气管的接口处突然爆裂,里面喷出大量的黄色液体,并伴有一些红褐色的固体。
水暖师傅、老师及同学们进行了紧急抢修。
事后,同学们出于好奇收集了红褐色固体进行探究。
[初步分析]红褐色固体的主要成分是铁锈,铁锈的成分复杂,主要是________。
由此联想到铁在空气中锈蚀,实际上是铁跟_______________、_______________等物质相互作用,发生一系列复杂的化学反应,使铁转化为铁的化合物的过程。
[搜集资料]①不溶性碱 加热金属氧化物+水(反应前后元素化合价不变);②暖气片是由生铁铸成的;③暖气用水为硬度较大的自来水; ④铁与铜都是属于金属,有部分相似的化学性质。
如:铜在潮湿的空气中可以形成铜绿[化学式为223()Cu OH CO ]。
[提出猜想]请根据上述任意一条资料分析,红褐色物质中还可能含有的物质是____________(写一种物质即可),你猜想的依据是____________________________________________________________________________________________________________________________。
人教版九年级化学课本习题答案之令狐文艳创作
人教版九年级化学课本(上册)习题答案令狐文艳第10页:1. 物理变化和化学变化的主要区别是什么?举例说明。
答:物理变化和化学变化的主要区别是有无新物质生成。
例如:汽油挥发、铁水铸成锅是物理变化;木柴燃烧、铁的生锈是化学变化。
2.下列现象哪些是物理变化,哪些是化学变化?为什么?(1)潮湿的衣服经太阳晒,变干了。
答:是物理变化,因为水的本质没有改变,无新物质生成。
(2)铜在潮湿的空气里生成铜绿。
答:是化学变化,因为有新物质铜绿生成。
(3)纸张燃烧。
答:是化学变化,因为有新物质水和二氧化碳生成。
(4)瓷碗破碎。
答:是物理变化,因为瓷碗的本质没有改变,无新物质生成。
(5)铁生锈。
答:是化学变化,因为有新物质铁锈生成。
(6)石蜡熔化。
答:是物理变化,因为石蜡的本质没有改变,无新物质生成。
(7)寒冷的冬天在玻璃窗前呼吸,玻璃上出现一层水雾。
答:是物理变化,因为水的本质没有改变,无新物质生成。
(8)下雪天把一团雪放在温暖的房间里,雪融化。
答:是物理变化,因为水的本质没有改变,无新物质生成。
3.为什么说点燃蜡烛时既有物理变化又有化学变化?答:因为蜡烛受热熔化无新物质生成,是物理变化;蜡烛燃烧有新物质水和二氧化碳生成,是化学变化。
所以说点燃蜡烛时既有物理变化又有化学变化。
4.下列哪些是物质的物理性质,哪些是物质的化学性质?为什么?(1)空气是没有颜色、没有气味的气体。
答:是物理性质,因为这是描述空气的颜色、气味、状态。
(2)水沸腾时能变成水蒸气。
答:是物理性质,因为这是不需要发生化学变化就表现出来的性质。
(3)食物在人体中消化,最后能变成水、二氧化碳等。
答:是化学性质,因为这是在化学变化中表现出来的性质。
(4)以粮食为原料能酿酒。
答:是化学性质,因为这是在化学变化中表现出来的性质。
(5)铜的密度是8.9g/cm3,熔点是1083℃。
答:是物理性质,因为这是描述铜的密度、熔点。
(6)二氧化碳能使澄清的石灰水变浑浊。
氢氧化钠标准溶液的标定之令狐文艳创作
氢氧化钠标准溶液的标定
令狐文艳
1.仪器
电子分析天平(200g,0.1mg);1台;
碱式滴定管(50mL),1只;
锥形瓶(250mL),3只;
2.试剂
邻苯二甲酸氢钾,基准试剂;
酚酞指示剂,10g/L;
氢氧化钠标准溶液,约0.2mol/L;
3.操作步骤
用差减称量法准确称取基准试剂邻苯二甲酸氢钾 1.0g (准确至0.0002g)于250mL锥形瓶中,加入80~100mL蒸馏水,溶解后,加入2滴酚酞指示剂,用待标定的氢氧化钠溶液滴定至溶液呈微红色,并保持30s不褪色即为终点,平行标定三次。
4.结果计算
c(NaOH)——氢氧化钠的浓度,mol/L;
m(KHP)——邻苯二甲酸氢钾的质量,g;
V(NaOH)——NaOH溶液的消耗体积,mL;
M(KHP)——邻苯二甲酸氢钾的摩尔质量,204.2g/moL。
5.数据记录与处理
1. 记录递减法称取基准物邻苯二甲酸氢钾的质量。
2. 记录消耗NaOH滴定液的体积。
3. 计算的NaOH浓度及所标定浓度的相对平均偏差。
生物药剂学与药物动力学习题及答案1-15章之令狐文艳创作
第一章生物药剂学概述令狐文艳【习题】一、单项选择题1.以下关于生物药剂学的描述,正确的是A.剂型因素是指片剂、胶囊剂、丸剂和溶液剂等药物的不同剂型B.药物产品所产生的疗效主要与药物本身的化学结构有关C.药物效应包括药物的疗效、副作用和毒性D.改善难溶性药物的溶出速率主要是药剂学的研究内容2.以下关于生物药剂学的描述,错误的是A.生物药剂学与药理学和生物化学有密切关系,但研究重点不同B.药物动力学为生物药剂学提供了理论基础和研究手段C.由于生物体液中药物浓度通常为微量或痕量,需要选择灵敏度高,专属重现性好的分析手段和方法D.从药物生物利用度的高低就可判断药物制剂在体内是否有效二、多项选择题1.药物及剂型的体内过程是指A.吸收B.渗透C.分布 D.代谢 E.排泄2.药物转运是指A.吸收B.渗透C.分布 D.代谢E.排泄3.药物处置是指A.吸收 B.渗透 C.分布 D.代谢 E.排泄4.药物消除是指A.吸收 B.渗透 C.分布 D.代谢 E.排泄三、名词解释1.生物药剂学;2.剂型因素;3.生物因素;4.药物及剂型的体内过程四、问答题1.生物药剂学的研究工作主要涉及哪些内容?2.简述生物药剂学研究对于新药开发的作用。
【习题答案】一、单项选择题1.C 2.D二、多项选择题1.ACDE 2.ACE 3.CDE 4.DE三、名词解释1.生物药剂学:是研究药物及其剂型在体内的吸收、分布、代谢与排泄过程,阐明药物的剂型因素、机体的生物因素与药理效应三者之间相互关系的科学。
2.剂型因素主要包括:(1)药物的某些化学性质:如同一药物的不同盐、酯、络合物或衍生物,即药物的化学形式,药物的化学稳定性等。
(2)药物的某些物理性质:如粒子大小、晶型、晶癖、溶解度、溶出速率等。
(3)药物的剂型及用药方法。
(4)制剂处方中所用辅料的种类、性质和用量。
(5)处方中药物的配伍及相互作用。
(6)制剂的工艺过程、操作条件和贮存条件等。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
《第一单元走进化学世界》令狐文艳1.如下图,下列化学实验操作正确的是_________________,错误的是___________________。
2.实验是科学研究的重要手段,正确操作是获得成功的重要保证。
请填空:①熄灭酒精灯火焰时应____________________________________。
②读取量筒内液体体积时视线应_____________________________。
③用漏斗过滤时漏斗中液面不应_____________________________。
④给试管内液体加热时,试管口不应_________________________。
3.用容积为 15 mL的试管盛液体加热时,最多可盛液体________mL4.下列仪器不宜用来加热的是------------------------------------()A.量筒B.烧杯C.试管D.蒸发皿5.实验时,不宜用作化学反应容器的仪器是-----------------------------()A.烧杯B.烧瓶C.试管D.量筒6.下列实验操作正确的是----------------------------------------------()A.没有说明药品用量时,固体、液体都可以取任意量B.使用试管夹时,将试管夹从试管口往下套,夹在试管中部C.实验用剩的药品要放回原瓶,以免浪费药品D.实验室取用固体药品一般用药匙,有些块状固体可用镊子7.某学生用托盘天平称取 3.3g食盐,称量时指针若左偏,此时应该----------------------()A.增加药品 B.减少药品 C.增加砝码 D.减少砝码8.某同学用托盘天平称量 5.3 g( 1 g 以下用游码)药品,称量时砝码和药品的位置放反了,则所称药品的质量是---------------------------------------()A.5.3 g B.5.1 g C.4.7 g D.5.4 g9.用量筒量取20 mL水,读数时视线仰视,则所取水的实际体积是-----------------------()A.20 mL B.大于20 mL C.小于20 mLD.无法估计10.向量筒中注入水,俯视读数为20毫升,倒出一部分水后,仰视读数为12毫升,则实际倒出来的水的体积------------------------------------()A.小于8毫升 B.大于8毫升 C.等于8毫升 D.无法确定《第二单元我们周围的空气》1.二百多年前,法国化学家_______________通过实验,得出了空气由________和________组成,其中_________约占空气总体积的1/5的结论。
2.空气的成分按________计算,大约是:氮气占__________、氧气占__________、_____________占0.94%、________________占0.03%、其他气体和杂质占0.03%。
3.化学反应的基本特征是_____________________________________。
4.在实验室里,常采用分解_______________溶液、加热_____________或加热_____________的方法制取氧气。
反应的化学方程式分别为____________________________________________、_______________________________________、_________________________________________上述反应均属于________________(判断反应类型)。
5.下列不属于氧化物的是---------------------------------------()A.二氧化锰 B.五氧化二磷C.高锰酸钾D.过氧化氢6.下列几种物质中,可用来测定空气组成的为-----------------------------()A.铁B.碳C.硫D.红磷7.在盛满空气的密闭容器中燃烧会使瓶内压强明显降低的是--------------()A.铁B.碳C.磷D.硫8.硫在氧气中燃烧是化学变化的主要依据是---------------------()A.发出明亮的蓝紫色火焰 B.生成有刺激性气味的气体C.放出大量的热 D.硫粉逐渐减少9.实验室用高锰酸钾反应制取少量氧气请回答下列问题:⑴指出图中的五处错误:1_______________________________________________②_______________________________________________③_______________________________________________④_______________________________________________⑤_______________________________________________⑵改正装置后,该实验有如下操作步骤:a.把集气瓶装满水倒置水槽里;b.开始收集气体;c.放好酒精灯;d.检验气密性;e.装药品;f.固定盛有药品的试管;g.撤去燃着的酒精灯;h.给药品加热;i从水槽中拿出导管。
其操作的正确顺序为________________________________。
⑶若检验集气瓶中是否装有氧气:________________________________________________;⑷若检验集气瓶中是否已集满氧气(排空气法):___________________________________________________ ___________________________⑸由于氧气的密度比空气_________________,收集氧气时可用_______________法,又因为氧气_________溶于水,收集它时可用_______________法。
欲得到较纯净的氧气(尽可能不含空气)最好选用________________法收集。
收集到气体的集气瓶要______________放在桌上。
《第三单元自然界的水》1.下列有关分子和原子的说法中,错误的是-------------------()A.原子是由原子核和核外电子构成的B.保持水的化学性质的粒子是水分子C.分子的质量总比原子的质量大 D.在化学反应中分子可分而原子不可分2.下图中的事例能说明分子间的间隙变小的是-------()3.水蒸发过程中,水分子________(填“变”或“不变”),只是____________在改变,因而属于________变化,变化前后水的化学性质________(填“变”或“不变”);电解水的实验中,正极得到______气,负极得到______气,正负两极气体的体积比是_________,质量比是_________,由该实验得出的结论是___________________________________________。
电解水的化学方程式为:______________________________,属于__________反应,反应前后,________改变,________________没有变。
4.说水资源丰富是因为____________________________________,说水资源缺乏是因为__________________________________。
5.爱护水资源,一方面要___________________;另一方面要__________________________。
6.水体污染的来源主要有__________________、_________________、_________________。
7.如何区分硬水和软水?___________________________________________________ ___________________________________________________________ ______________________________。
8.列举两个使用硬水的危害:___________________________________________________ _______________________________________________________ ______________________________。
9.⑴请指出图中存在的明显错误:①__________________________________________②__________________________________________⑵实验中如果发现滤液浑浊,试分析可能的原因:①_________________________________;②________________________________。
应采取什么措施。
10.化学课上,张老师展示出《你们都来污染我》的图片,引起全班同学的深思。
课后,同学们围绕“水的污染与防治”的主题进行研究性学习。
⑴生活污水的再利用,既能减少水污染,又能节约水。
①若生活污水中含有碎菜叶、鱼鳞片、泥沙等固体杂质,要除去这些固体杂质,可采用沉淀、等方法。
②生活污水经处理后,可用于浇花、等。
③若生活污水中含有Na2CO3,请你设计一个实验来验证污水中含有CO32-实验步骤实验现象实验结论⑵方玲从《福建日报》上获悉:养猪业是龙岩的四大产业之一,但大量的排泄污水对九龙江流域造成严重污染。
在五年艰苦的治污过程中,实行:“猪—沼—草—猪”生态养殖循环模式,实现“零排放”。
其中“猪—沼”就是将猪的粪便转化成沼气作为燃料,沼气的主要成分是,其完全燃烧的化学方程式为。
⑶调研后,同学们提出下列预防和治理水污染的建议,其中合理的是(填字母)。
A.科学使用高效低毒的农药、化肥 B.禁止在所有水域内养殖C.禁止在饮用水的水源保护区设置排污口⑷如果你是学习小组的成员,你还想调研的一个问题是。
《第四单元物质构成的奥秘》1.物质由____________、____________和_____________等微小粒子构成。
2.核电荷数=____________=______________。
相对原子质量=___________+___________。
3.地壳中含量最多的金属元素和非金属元素形成的化合物名称是__________,符号是______。
4.碳的相对原子质量为------------------------------------------()A.12g B.1/12g C.12D.1.66×10-27kg5.据报道,俄罗斯科学家最近合成了核电荷数为114的元素的原子,经测定该原子的相对原子质量为289,则中子数为------------------------------()A.175 B.114 C.61 D.2896.某全麦饼干部分营养成分的含量如下表所示,表中的“铁、镁、锌、钙”是指-----()营养成分铁镁锌钙含量(mg/100g)4.5~590~1003~4280~300A.分子B.原子C.元素D.非金属7.下列试剂瓶标签上的化学式书写错误的是--------------()8.目前市场上的补钙药剂很多,右图是某品牌补钙药品的部分说明书。
