高三常见气体制备 吸收装置
2015届高考化学总复习 第八章 第四节常见气体的制备精讲课件

现象 说明
烧杯中有气泡产生,停 止微热,冷却后导气管 末端形成一段水柱,且 保持一段时间不下降
液面的高度差不变
针对训练
1.某研究性学习小组为合成 1丁醇,查阅资料得知一条 合成路线: 一定条件 CH CH===CH +CO+H ――――→
3 2 2
H2 CH3CH2CH2CHO――――→ Ni,△ CH3CH2CH2CH2OH。 浓H2SO4 CO↑+H O, CO 的制备原理: HCOOH――――→ 并设计 2 △ 出原料气的制备装置。
CuSO4
⑤品红溶液
解析:本题主要通过有机反应考查化学实验的基本方法
和技能。 (2) 考虑到CO 逸出时带有 HCOOH 和 H2O等杂质,因 此需先除去 HCOOH 等蒸气 ——c 中装 NaOH 溶液,再除去水 蒸气 ——d 中装浓 H2SO4 ; a 的作用是利于分液漏斗中液体的 顺利滴下——使压强恒定,b应起到安全瓶的作用——防倒吸。 (3)设计实验检验混合气体的各种成分时,要注意其他气体的 存在对此的干扰,先检验能干扰其他气体检验的气体并除去, 检验气体过程中不能产生未检验的气体。分析问题(3)中提供 的试剂的作用,可先检验水 —— 用④,再用⑤检验 SO2 并用 ①除去 SO2( 因 SO2 干扰丙烯的检验 ) ,然后,用③检验 CO2 , 最后用②检验丙烯,因KMnO4氧化丙烯时要生成CO2。
请填写下列空白: (1) 实验室现有锌粒、稀硝酸、稀盐酸、浓硫酸、 2丙醇,从 中选择合适的试剂制备氢气、丙烯,写出化学反应方程式:
______________________ , _____________________________
______________________________________________。 (2)若用以上装置制备干燥纯净的CO,装置中a和b的作用分别 是 __________________ 、 ________________ ; c 和 d 中盛装的 试剂分别是 ______________ , ________________ 。若用以上
常见气体制备装置归纳

C.CH4 D.NH3
5、设计了四种制备气体的方案:(1) 加热稀硫酸和乙
醇制备乙烯;(2) 加热稀盐酸和二氧化锰制备氯气;
(3)用稀硫酸和大理石制备二氧化碳;(4)用稀硝酸和
硫化亚铁制备硫化氢。不宜采用的方案有哪些?D
A.只有(1)和(2)
B.只有(1)和(3)
C.只有(3)和(4)
图2
图3
图4
图5
图6
gfr
5
(4)启普发生器及简易装置
图7
图8
图9 图10
图11 图12
gfr
6
3、固体+液体或液体+液体加热制气体
①反应容器:试管、烧瓶 ②加液容器:分液漏斗 ③注意事项:见图16、17
图13
图14
图1gf5r
图16
图17
7
二、气体净化装置: 根据净化剂的状态和条件选择
gfr
编 A中物 B中物 C中
号质
质 气体
有关化学方程式
(1) Na2SO3
浓硫酸 SO2
Na2SO3 +H2SO4(浓) ═ Na2SO4 +SO2↑+H2O
(2) Cu
浓硝酸 NO2
Cu + 4HNO3(浓) ═ Cu(NO3)2+ 2NO2↑+2H2O
(3) KMnO4 浓盐酸 Cl2
2KMnO4 + 16HCl ═ 2KCl g+fr 2MnCl2+5Cl2↑+ 8H2O
在瓶E和F之间连接装有干燥剂的装置
gfr
21
7根据下面实验图填空和回答问题:(1)烧瓶中所发生的主
要反应的化学方程式是 2H2SO4(浓)+2Na,Br+MnO2═MnSO4+Br2↑+
高三化学一轮复习——常见气体的制备

心志要坚,意趣要乐。
追胸踪有着 凌鹿云的志4猎,.人无是高氨看不不可气见攀山。通 的。入氯化铝溶液中,现象是先有白色沉淀后溶解。( × )
自信是成功的第一秘诀 天才是由于对事业的热爱感而发展起来的,简直可以说天才。
人壮若志有 与志毅,力提万是事事示可业为的:。双翼氢。 氧化铝是两性氢氧化物,只溶于强酸和强碱,不溶于氨水。
大丈夫处世,不能立功建业,几与草木同腐乎? 男儿不展同云志,空负天生八尺躯。 有志者自有千方百计,无志者只感千难万难。
5.用如图所示实验装置制备 BaSO3 沉淀:
( ×)
提示:硝酸根在酸性条件下具有强氧化性,可使二氧化硫氧化为硫酸,得到硫酸 钡沉淀。
微练一 常见气体的制备
1.用 NH4Cl 和 Ca(OH)2 制备 NH3,在如图所示装置中,反应发生装置、气体收
实验室合成氨装置如图1所示,试回答:
一、气体制备实验的基本思路 防倒吸
找杂质? 实验原理:反应方程式
如何测量气 体体积?
常见气体的制备
酸性气体:CO2、SO2、NO2、HCl、Cl2、H2S、HBr、HI 碱性气体:NH3 中性气体:H2、O2、N2、NO、CH4、CO、CH2=CH2、C2H2 强还原性气体:H2S、HBr、HI、SO2
气体的收集
a
b
气体体积测定
气体体积测定
①调平;②读数;③实验;④恢复室温; ⑤调平;⑥读数
母鸡的理想不过是一把糠。 雄心志四海,万里望风尘。 无钱之人脚杆硬,有钱之人骨头酥。 志当存高远。 少年心事当拿云。 胸有凌云志,无高不可攀。 治天下者必先立其志。 卒子过河,意在吃帅。 立志难也,不在胜人,在自胜。 谁不向前看,谁就会面临许多困难。 石看纹理山看脉,人看志气树看材。 卒子过河,意在吃帅。 穷人的孩子早当家。 贫困能造就男子气概。 少年心事当拿云。 壮志与毅力是事业的双翼。 人生不得行胸怀,虽寿百岁犹为无也。 谁不向前看,谁就会面临许多困难。 顶天立地奇男子,要把乾坤扭转来。 有志者能使石头长出青草来。 沧海可填山可移,男儿志气当如斯。 强行者有志。 不为穷变节,不为贱易志。 有志者自有千方百计,无志者只感千难万难。
2023届高三化学二轮复习+考点突破--常见气体的制备与收集
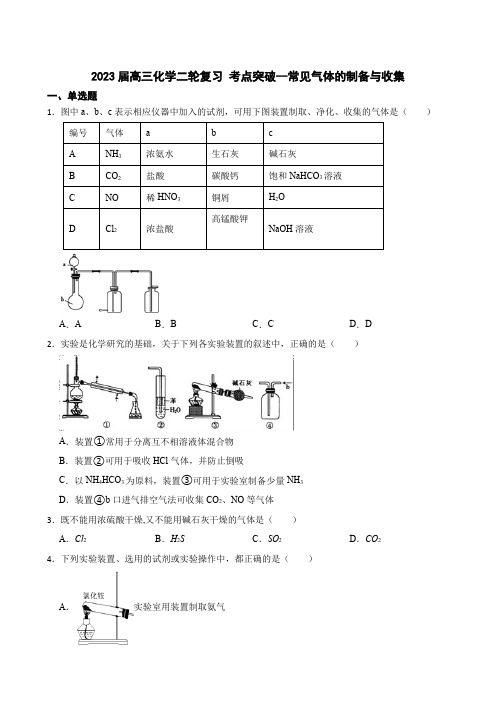
2023届高三化学二轮复习考点突破--常见气体的制备与收集一、单选题1.图中a、b、c表示相应仪器中加入的试剂,可用下图装置制取、净化、收集的气体是()编号气体a b cA NH3浓氨水生石灰碱石灰B CO2盐酸碳酸钙饱和NaHCO3溶液C NO稀HNO3铜屑H2OD Cl2浓盐酸高锰酸钾NaOH溶液A.A B.B C.C D.D 2.实验是化学研究的基础,关于下列各实验装置的叙述中,正确的是()A.装置①常用于分离互不相溶液体混合物B.装置②可用于吸收HCl气体,并防止倒吸C.以NH4HCO3为原料,装置③可用于实验室制备少量NH3D.装置④b口进气排空气法可收集CO2、NO等气体3.既不能用浓硫酸干燥,又不能用碱石灰干燥的气体是()A.Cl2B.H2S C.SO2D.CO2 4.下列实验装置、选用的试剂或实验操作中,都正确的是()A.实验室用装置制取氨气B.用装置吸收氨气,并防止倒吸C.用装置稀释浓硫酸D.用装置除去CO2中的HCl5.实验室用环戊醇(沸点160.8℃,密度0.96g/mL)与溴化氢反应制备溴代环戊烷(沸点138℃,密度1.37g/mL),其反应原理如下:OH+NaBr+H2SO4Br+NaHSO4+H2O,则制备溴代环戊烷的装置可以选择()A.B.C.D.6.要设计一套实验室利用液体和液体加热反应制备气体的装置,现设计了五步操作,正确的程序是()①将蒸馏烧瓶固定在铁架台上②将酒精灯放在铁架台上,根据酒精灯确定铁圈高度,固定铁圈,放好石棉网③用漏斗向蒸馏烧瓶中加入一种液体反应物,再向分液漏斗中加入另一种液体反应物,并将导气管放入气体收集器中④检查装置的气密性(利用对固定装置微热的方法检查气密性)⑤在蒸馏烧瓶上装好分液漏斗,连接好导气管A.②①⑤④③B.④①②⑤③C.①②⑤④③D.①⑤④②③7.下面关于图所示实验装置的使用方法中叙述正确的是()①用于排水集气:充满水,B进气,A排放水②用于收集密度比空气大的气体:A进气,B排放空气③用于收集密度比空气小的气体:B进气,A排放空气④用于洗气:装入洗液,A进气,B出气⑤用于测量气体的体积:充满水,B进气,A出水,计算溢出水的体积.A.全正确B.②③④⑤C.①③④⑤D.①②③④8.实验室用铁屑、液溴与苯制取溴苯,提纯粗溴苯需要过滤、水洗、碱洗、干燥、蒸馏等操作(上述操作可能多次,且不代表实验顺序),完成提纯实验不需要的实验装置有()A.B.C.D.9.下列有关实验的操作正确的是()实验操作A 除去NaHCO3固体中混有的NH4Cl直接将固体加热B 实验室收集Cu与稀硝酸反应成的NO向上排空气法收集C检验非金属性Cl>C在Na2SiO3溶液中加入足量HClD检验某溶液中是否有NH4+取该溶液于干净的试管中,加NaOH浓溶液加热,并用湿润的红色石蕊试纸检验A.A B.B C.C D.D10.以CO2和Na2O2为原料,制取纯净干燥的O2,实验装置如下,下列说法正确的是()A.装置②的作用是干燥O2B.装置③中试剂可以是NaOH溶液C.制备反应的化学方程式为:Na2O3+CO2=Na2CO3+O2D.收集氧气应选择装置b11.下列装置正确且能达到对应实验目的的是()A.用图1装置进行银镜反应B.用图2装置检验溴乙烷消去后的产物是否含乙烯C.用图3装置制备乙酸乙酯D.用图4装置比较乙酸、碳酸、苯酚的酸性强弱12.下列气体制备实验设计中,药品和装置都合理的是()A.图1:碳酸钠与盐酸反应制备CO2B.图2:铜片与稀硝酸反应制备NOC.图3:消石灰与氯化铵固体反应制备NH3D.图4:二氧化锰与浓盐酸反应制备Cl2二、填空题13.如图1装置常用于实验室制备气体(1)写出实验室用该装置制备O2化学方程式(2)若利用该装置制备干燥NH3,试管中放置药品是(填化学式);仪器a中放置药品名称是(3)图2装置实验室可用于制备常见的有机气体是.仪器b名称是有学生利用图B装置用浓氨水和生石灰制备NH3,请说明该方法制取NH3的原因(4)学生甲按图3所示探究氨催化氧化,用一只锥形瓶倒扣在浓氨水试剂瓶口收集氨气,然后将红热的螺旋状铜丝插入锥形瓶中;片刻,锥形瓶中气体变为红棕色.下列叙述正确的是A.如图收集氨气是利用氨水的密度较小B.锥形瓶必须干燥C.收集氨气时间越长,红棕色现象越明显D.铜丝能保持红热(5)学生乙对学生甲的实验提出了异议,认为实验中产生的红棕色气体可能是空气中的氮气氧化后造成的,你认为学生乙的说法合理吗?请你设计一个简单实验证明学生乙的说法是否正确.14.如图所示装置是化学实验室中的常用装置,它有多种用途,以下各项用途和操作都正确的是(填序号).a.洗气或干燥装置:瓶内放一定体积溶液,由a管口进气b.用于收集不溶于水的气体:瓶内充满水,由b管口进气c.提供少量CO:瓶内充满CO,b管口接自来水龙头d.H2S和SO2反应的装置:由a管口通入H2S,b管口通入SO2e.病人输氧时用于观察输氧速度:瓶内装适量水,b接病人鼻腔.15.如图为实验室制取自来水的装置示意图,根据图示回答下列问题.(1)图中有(填数值)处明显的错误.(2)A仪器的名称是,B仪器的名称是.(3)实验时A中除加入适量自来水外,还需加入少量,其作用是.(4)要检测锥形瓶中的蒸馏水是否含有Cl﹣,需要的两种化学试剂是(填化学式).16.如图为实验室制取蒸馏水的装置示意图,请根据图示回答下列问题.(1)图中有两处明显的错误分别是①②(2)图中A仪器的名称是(3)实验时A中除加入自来水外,还需加入少量,其作用是.(4)区别自来水和蒸馏水可用的试剂是.三、综合题17.氨基锂(LiNH2)是一种白色有光泽的结晶或粉末,熔点是390℃,沸点是430℃,溶于冷水,退热水则强烈水解。
氯气的制备及高中常见气体制备知识拓展
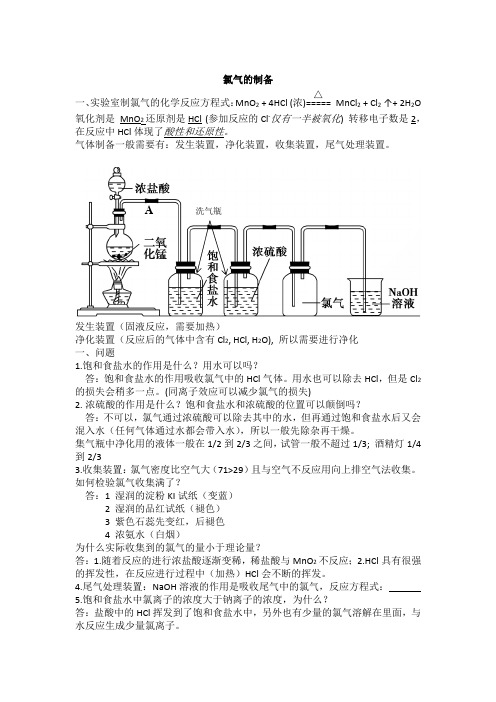
氯气的制备一、实验室制氯气的化学反应方程式:MnO 2 + 4HCl (浓)=====△ MnCl 2 + Cl 2 ↑+ 2H 2O氧化剂是 MnO 2还原剂是HCl (参加反应的Cl -仅有一半被氧化) 转移电子数是2,在反应中HCl 体现了酸性和还原性。
气体制备一般需要有:发生装置,净化装置,收集装置,尾气处理装置。
发生装置(固液反应,需要加热)净化装置(反应后的气体中含有Cl 2, HCl, H 2O), 所以需要进行净化一、问题1.饱和食盐水的作用是什么?用水可以吗?答:饱和食盐水的作用吸收氯气中的HCl 气体。
用水也可以除去HCl ,但是Cl 2的损失会稍多一点。
(同离子效应可以减少氯气的损失)2. 浓硫酸的作用是什么?饱和食盐水和浓硫酸的位置可以颠倒吗?答:不可以,氯气通过浓硫酸可以除去其中的水,但再通过饱和食盐水后又会混入水(任何气体通过水都会带入水),所以一般先除杂再干燥。
集气瓶中净化用的液体一般在1/2到2/3之间,试管一般不超过1/3; 酒精灯1/4到2/33.收集装置:氯气密度比空气大(71>29)且与空气不反应用向上排空气法收集。
如何检验氯气收集满了?答:1 湿润的淀粉KI 试纸(变蓝)2 湿润的品红试纸(褪色)3 紫色石蕊先变红,后褪色4 浓氨水(白烟)为什么实际收集到的氯气的量小于理论量?答:1.随着反应的进行浓盐酸逐渐变稀,稀盐酸与MnO 2不反应;2.HCl 具有很强的挥发性,在反应进行过程中(加热)HCl 会不断的挥发。
4.尾气处理装置:NaOH 溶液的作用是吸收尾气中的氯气,反应方程式:5.饱和食盐水中氯离子的浓度大于钠离子的浓度,为什么?答:盐酸中的HCl 挥发到了饱和食盐水中,另外也有少量的氯气溶解在里面,与水反应生成少量氯离子。
A 洗气瓶6. 将干燥的红纸条放在A 处导管口,红纸条会褪色吗?为什么?答:会褪色,氯气中含有水蒸气,会有HClO 生成,具有漂白作用。
常见气体的制取

常见气体的实验室制取【考纲要求】1.掌握常见气体的实验室制法(包括所用试剂、仪器、反应原理和收集方法)2.与其它各部分知识、技能的综合应用。
【知识要点】一、课本中的气体制备二、气体的制取实验室气体制备的一般步骤有:制取→净化→收集→尾气吸收(一)气体的发生装置常见的气体制取装置有:或填写下表:32H2+4HCl MnClCaCl2)选择发生装置的根据是。
(二)气体的净化装置或欲除去下列气体中的杂质,写出选用的试剂和装置气体选择净化装置的根据是。
(三)气体的收集装置 或或或选择收集装置的根据是 。
(四)气体的尾气吸收选择尾气吸收装置的根据是 。
【典型例题】例1、(课本《必修1》P99页)下图是实验室制取氨气的常用装置,某同学欲用该装置制取、收集干燥纯净的氨气,试分析其是否严谨?若不严谨,应如何改进?试画出改进后的实验装置图。
例2、(课本《必修1》P50页)铁能与水蒸气反应,反应化学方程式为 。
常用反应装置如下图。
如果提供给你3支试管、水槽、蒸发皿、胶塞、导管、酒精喷灯及其他必要的仪器和物品,设计一套简单的实验装置,使还原铁粉与水蒸气反应(这套装置应包括水蒸气发生、水蒸气与铁粉反应、检验产生的气体等部分)。
画出你设计的装置简图。
例4、(课本《选修6》P22)回忆初中化学课程中制取二氧化碳的实验,思考下列问题:(1)能够通过化学反应产生二氧化碳气体的物质有哪些?(2)制取二氧化碳的实验中,以什么物质为反应物(原料)?为什么?(3)反应的装置是如何选择和安装的?(4)如果要制备干燥的气体产物,应如何设计装置?例3、(课本《必修1》P92页)现给你一试管二氧化氮,其他药品和仪器自选。
请你设计实验,要求尽可能多地使二氧化氮被水吸收。
画出你设计的装置简图,简述实验步骤、现象并进行解释。
例5、某化学兴趣小组的甲、乙两位同学对测定化学反应速率非常感兴趣,为此进行了有关的实验探究,实验记录如下。
[实验目的] 测量锌和稀硫酸反应的速率[实验用品] 锥形瓶、双孔塞、分液漏斗、直角导管、50mL注射器、铁架台、、量筒;锌粒、1mol·L-1的H2SO4、4mol·L-1的H2SO4。
2014年高考化学黄金易错点专题汇编:专题27 常见气体制备的发生装置与收集

1.下图装置可用于制取、提纯并收集表格中的四种气体(a、b、c表示相应仪器中加入的试剂),其中可行的是2. 根据下图所示的实验装置回答问题:(1)实验室用高锰酸钾制取比较干燥的氧气应选用的发生装置是________(填序号,下同),收集装置为________。
(2)实验室用双氧水制取并收集较纯的氧气时应选用的发生装置是________,收集装置为________。
(3)实验室用氯化铵与熟石灰两种固体加热制取氨气,氨气的密度比空气的小,极易溶于水。
推断:实验室制取氨气应选用的发生装置为________,收集装置为________。
(4)利用废弃的可乐瓶和底部有小孔的试管(试管小孔处事先放有一缝隙很小的铜网)组成制取氧气的装置(如图所示)。
该装置中A中应盛放________,B中应放进________,若使正在发生的反应停止,可以通过________来实现。
3.下列选用的实验仪器或实验装置符合实验要求且安全的是()4.下列制备和收集气体的实验装置合理的是()A.用氯化铵和氢氧化钙固体制NH3B.用铜片和稀硝酸制NOC.用锌粒和稀硫酸制H2D.用双氧水和二氧化锰制O25. 某学生想利用图中所示装置(烧瓶位置不能移动)收集下列气体:①H2、②Cl2、③CH4、④HCl、⑤NH3、⑥NO、⑦NO2、⑧SO2,下列操作正确的是()A.烧瓶是干燥的,由A进气收集①③⑤B.烧瓶是干燥的,由B进气收集②④⑥⑦⑧C.在烧瓶中充满水,由A进气收集①③⑤⑦D.在烧瓶中充满水,由B进气收集⑥6.检查装置气密性是化学实验中的重要操作之一。
按要求回答下列问题:(1)下列关于不进行气密性检查可能导致后果的叙述中,正确的是________。
A.收集不到气体B.造成环境污染C.观察到的实验现象有误D.引发爆炸事故(2)为检查如图所示简易气体发生装置的气密性,甲、乙两位同学进行了以下操作和方案设计:①甲同学认为,只要往漏斗中加水,便可检验其气密性是否良好。
第四章第21讲常见气体的制备、净化和收集2025年高考化学一轮复习

第21讲 常见气体的制备、净化和收集[复习目标] 1.掌握常见气体的制备、净化、收集及尾气处理的方法。
2.能对整套气体制备及性质实验装置进行分析,并能处理相关问题。
考点一 常见气体的制备、净化、收集及尾气处理必备知识夯实1.常见气体的发生装置 (1)固体+固体――→△气体发生装置如图:制备气体:□1O 2、□2NH 3等 (2)固体(液体)+液体――→△气体发生装置如图:制备气体:□3Cl 2、CH 2===CH 2(需加温度计)等 (3)固体+液体(不加热)→气体发生装置如图:制备气体:选择合适的试剂和装置能制取中学化学中常见的气体,如NH 3(□4生石灰、□5浓氨水)、O 2(MnO 2、□6H 2O 2溶液)、Cl 2(KMnO 4、□7浓盐酸)、SO 2(□8Na 2SO 3、较浓硫酸)等2.常见气体的除杂装置4.(1)实验室制取Cl2时,尾气的处理可采用□1b装置。
(2)制取CO时,尾气的处理可采用□2a、c装置。
(3)实验室制取NH3时,尾气的处理可采用□3d装置。
名师课堂点拨实验室中制取气体时实验装置的设计关键能力提升一、常见气体的制备和收集1.(2023·北京石景山区模拟)实验室制备下列气体所选试剂、制备装置及收集方法均正确的是()【解析】制取NO2可选用Cu和浓硝酸反应,不能选用稀硝酸,A错误;NH4Cl受热分解生成NH3和HCl,遇冷时NH3和HCl重新化合生成NH4Cl,不能用于制取NH3,B错误;H2O2在MnO2催化下分解生成H2O和O2,可用排水法收集O2,C正确;KMnO4和浓盐酸在常温下反应生成Cl2,Cl2的密度大于空气的密度,采用向上排空气法收集,选择装置c,D错误。
【答案】C2.实验室制取下列气体,所选反应试剂、制备装置与收集方法均合理的是()【解析】铜与稀硝酸生成NO且反应不需加热,NO与空气中的氧气反应生成NO2,不能用排空气法收集NO,A错误;乙醇在浓硫酸作用下迅速升高温度到170 ℃,乙醇生成乙烯气体,乙烯难溶于水,可以用排水法收集,B正确;氨的密度小于空气,应该使用向下排空气法收集,C错误;Na2SO3和硫酸反应不需要加热,且SO2能与水反应,不能用排水法收集,D错误。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
;
向试管中到入过量的稀硝酸,并迅速盖上带铜丝
③ 和导管的橡皮塞
;
④ 待反应完全后,将右边导管插入试管内接近液面 ;
⑤ 将铜丝插入到溶液中
;
⑥用注射器向试管内推入氧气(或空气)
(2)若烧瓶充满水,可收集的气体有________,这时气体 由________口进入。
(3)若在烧瓶内装入浓硫酸进行干燥气体,则 可用此装置的气体有____________,这时气体 由________口进入。
(4)若烧杯是干燥的,不能用此装置来收集的 气体是___。
【答】(1) ②④⑦⑧ (2)①③⑥,A (3)①②③④⑥⑧,B (4)⑥
4、尾气处理装置
▪总原则 ▪(1)有毒、污染环境的气体不能直接排放。 ▪(2)尾气吸收要选择合适的吸收剂和吸收装置。
•直接吸收:Cl2、H2S、NO2 防倒吸:HCl、NH3、SO2 •常用吸收剂:水,NaOH溶液,硫酸铜溶液 ▪(3)可燃性气体且难用吸收剂吸收:燃烧处理或袋装。
4、尾气处理装置
(1)水溶解法 如:HCl、NH3等。 (2)碱液吸收法
▪ (3)冷却反应装置
▪ 5.2 判断原则
Hale Waihona Puke 6、排水量气装置标准 装置
注意事项: 左端水位与右 端水位相平
变化 装置
注意事项: 量筒内的水位与 水槽中水位相平 .
[例1]:
(1)在没有现成的CO2气体发生器的情况下,请你选用 下图中的部分仪器,装配成一个简易的、能随开随用、随
关随停的CO2气体发生装置。应选用的仪器是(填入仪器
的编号)
。
(2)若用上述装置制取CO2气体,而实验室只有稀硫酸、 浓硝酸、水、块状纯碱、块状大理石,比较合理的方案应
选用的药品是
。
[例2]:
为制取纯净的气体A可用下图所示的装置,生成A的速度 可通过滴液的速度控制,图中B、C、D均为液体,且为下列 试剂中某一种:
浓硫酸、稀硫酸、浓硝酸、稀硝酸、浓盐酸、稀盐酸、浓 氨水、稀氨水、蒸馏水、饱和氢硫酸溶液、饱和石灰水
如:Cl2、H2S、CO2、 SO2、NO2、NO等。
(3)燃烧或袋装处理法
如 : CH4 、 C2H4 、 C2H2 、 H2、CO等。
4、尾气处理装置
(4)防倒吸吸收
标准装置
安全瓶装置
②防倒吸吸收 图 5-27-1
5、气体性质实验装置
▪ 5.1 装置分类
▪ (1)常温反应装置
▪ (2)加热反应装置
[例5]铜与浓硝酸反应和铜与稀硝酸反应,产物
不同,实验现象也不同。
⑴某课外活动小组为了证明并观察到铜与稀 硝酸反应的产物为NO,设计了如左图所示
的实验装置。请你根据他们的思路,选择下
列药品,完成该实验,并叙述实验步骤。
药品:稀硝酸、稀盐酸、锌粒、碳酸钙固体
步骤:①检查装置的气密性;
② 向试管中加入一定量碳酸钙固体
[例4]:
某集气瓶中充满了HI气体,试设计一个装置表 示:将这种气体排出烧瓶,并粗略证明它确实是HI 气体,写出有关反应的离子方程式。
【答】:往装有气体的瓶中注入浓磷酸,使气体排出, 用盛有适量水的烧杯吸收排出的气体(玻璃管下端接一个 倒置漏斗),一段时间以后,取少量烧杯中的溶液,测得 PH值小于7;加入用硝酸酸化的硝酸银溶液,如发现有黄 色沉淀生成,则可说明原气体是HI气体。
请回答:A、B、C、D、E各是什么物质?
【答】:A是氯化氢气体,B是浓盐酸,C、D、E均是浓硫酸
[例3]:
利用下图所示装收集以下8种气体(图中烧瓶位置不得移 动):①H2 ②Cl2 ③CH4 ④HCl ⑤NH3 ⑥NO ⑦H2S ⑧SO2
(1)若烧瓶是干燥的,则由A口进气,在B口可收集的气体 有(用数字表示,下同)________________.
