ch-4(1)
CH_(4)气体对非分散红外吸收法测定废气中SO_(2)的影响

CH4气体的废气中SO2时一定要确保所用仪器不会 被CH4干扰,尤其是购置时间较长的仪器,防止因为 甲烷气体的干扰造成监测结果失真。
收稿日期:2020-09-30 第一作者简介:张飞龙(1990—),男,山西运城人,本科,忻州
师范学院,环境保护中级工程师,现从事环境监测工作。
每一个固有振动对应一个光谱吸收带 ,它们的波长
分别为 3.43,6.53,3.31,7.66 |xm[3]。 本文选取了不同制造厂家的非分散红外法二氧
化硫便携式监测仪对不同浓度的的二氧化硫气体、 甲烷气体、二氧化硫和甲烷混合气体进行了测定,研
究甲烷对非分散红外吸收法测S02的干扰程度,同 时得出相应的结论。
1设备和标气 本次实验选用的设备为红外烟气分析仪 MGA5
型(MRU GmbH 公司 74172NSU-Obereisesheim 生产
制造)、便携式红外烟气综合分析仪ZR-3220型(青 岛众瑞智能仪器有限公司)、便携式红外气体分析仪
(上接第11页)
4)烧结生产中需要考虑成本,增加配炭,提高T 燃料比,增加了烧结成本,不利于烧结,但利于炼铁, 生产过程应权衡考虑。
5虑瞬护姑和冶金性能,建议 烧结矿适宜的w(FeO)应控制在9.0%左右较为适宜。
6)本次实验的范围小,且未进行平行实验验证, 数据结果可能存在偏差。
参考文献
[1]高新洲.烧结矿冶金性能影响因素与控制[G].2013年全国烧结 球团技术交流年会论文集.
《医用有机化学》课后习题答案(总)
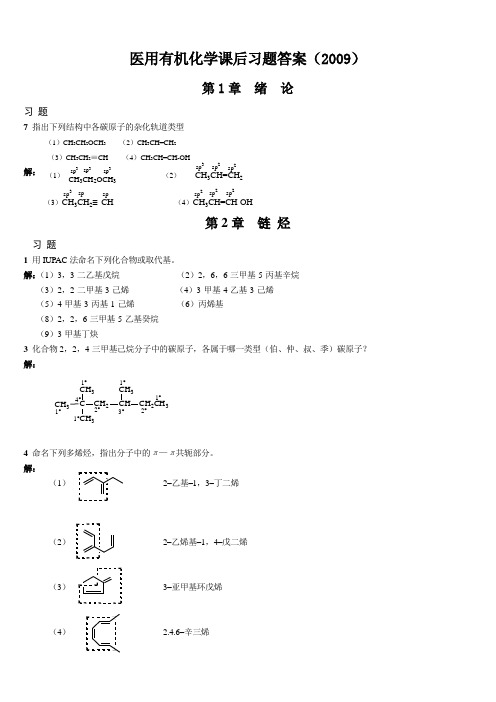
医用有机化学课后习题答案(2009)第1章 绪 论习 题7 指出下列结构中各碳原子的杂化轨道类型(1)CH 3CH 2OCH 3 (2)CH 3CH=CH 2 (3)CH 3CH 2≡CH (4)CH 3CH=CH-OH解:第2章 链 烃习 题1 用IUPAC 法命名下列化合物或取代基。
解:(1)3,3-二乙基戊烷 (2)2,6,6-三甲基-5-丙基辛烷 (3)2,2-二甲基-3-己烯 (4)3-甲基-4-乙基-3-己烯 (5)4-甲基-3-丙基-1-己烯 (6)丙烯基 (8)2,2,6-三甲基-5-乙基癸烷 (9)3-甲基丁炔3 化合物2,2,4-三甲基己烷分子中的碳原子,各属于哪一类型(伯、仲、叔、季)碳原子? 解:CH 3CCH 3CH 3CH 2CHCH 3CH 2CH 31°4°1°2°1°3°2°1°1°4 命名下列多烯烃,指出分子中的π—π共轭部分。
解:(1) 2–乙基–1,3–丁二烯(2) 2–乙烯基–1,4–戊二烯(3) 3–亚甲基环戊烯(4) 2.4.6–辛三烯spsp2sp 3sp 2sp 2spsp 2CH 3CH=CH 2sp 2(1) (2)(3)CH 3CH 2≡CH (4)CH 3CH=CH-OH CH 3CH 2OCH 3sp 3sp3sp 3sp 3(5)5–甲基–1.3–环己二烯(6)4–甲基–2.4–辛二烯9 将下列自由基按稳定性从大到小的次序排列: 解:(3)>(2)>(1)>(4)10 按稳定性增加的顺序排列下列物质,指出最稳定者分子中所含的共轭体系。
解:(1)d >b >c >a (2)d >c >b >a12下列化合物有无顺反异构现象?若有,写出它们的顺反异构体。
解:(1)无 (2)有C=CCH 3HH 2H 5C =CCH 3HHC 2H 5(3)有C =CHC =CH BrCl C 4H 9Br ClC 4H 9(4)有3C =CBrCl HCH 3C =CBr ClH(6)有C =CC 2H 5CH 3C 2H 5CHCH 3CH 3C =CC 2H 5CH 32H 5CHCH 3CH 314 经高锰酸钾氧化后得到下列产物,试写出原烯烃的结构式。
2024-2025学年福建省福州市高三上学期第一次质量检测化学试题

2024~2025学年高三年级第一次质量检测化学试题(完卷时间75分钟;满分100分)可能用到的相对原子质量:H 1− C 12− O 16− Zn 65−一、选择题:本题共10小题,每小题4分,共40分。
在每小题给出的四个选项中,只有一项是符合题目要求的。
1.福建舰拥有世界上最先进的雷达系统,其雷达射频微波器件所用的碳化硅材料能实现电信号的可控改变。
下列关于碳化硅的说法错误的是( )。
A .C 原子的杂化类型为3sp B .属于高分子化合物 C .熔点高、硬度大D .属于半导体材料2.“扑热息痛”是重要的解热镇痛药,其结构如下。
下列有关该物质的说法正确的是( )。
A .分子式为872C H NOB .含有2种官能团C .所有原子可能处于同一平面D .能与溴水发生加成反应3.寿山石的主要成分为()44108Z W Y YX ,X 、Y 、Z 、W 为四种原子序数递增的短周期不同族元素,X 是周期表中半径最小的原子,基态Y 原子有2个未成对电子,W 的L 层电子数是M 层的2倍。
下列说法正确的是( )。
A .原子半径Z <W B .简单氢化物的稳定性Y <W C .电负性Z >XD .Z 最高价氧化物的水化物呈两性4.乙烯在Ag 的催化作用下可发生反应:Ag2222CH CH O 2=+ →,下列说法错误的是( )。
A .2211.2L CH CH =所含的原子数目为A 3NB .221.4g CH CH =中所含的电子数目为A 0.8NC .1mol 环氧乙烷中含有σ键的数目为A 7ND .常温常压下,216g O 发生反应时,转移电子的数目为A 2N5.利用绿矾()42FeSO 7H O ⋅制备电极材料4LiFePO 的前驱体4FePO 的流程如下:下列说法正确的是( )。
A .溶解过程中34H PO 可抑制2Fe +的水解 B .可以用KSCN 溶液判断反应是否完全C .过滤需要的玻璃仪器有烧杯、玻璃棒、分液漏斗D .反应中氧化剂与还原剂的物质的量之比为2:16.我国科研团队研究发现GaZrO x 双金属氧化物可形成氧空位,具有催化性能,实现2CO 加氢制甲醇,其反应机理如图所示。
MOFs材料的CH_(4)存储研究进展

山 东 化 工 收稿日期:2020-12-02作者简介:林 叶,女,本科生;通信作者:刘秀萍,讲师,博士。
MOFs材料的CH4存储研究进展林 叶,祝钰灵,李伟华,胥 莹,刘秀萍(临沂大学材料科学与工程学院,山东临沂 276000)摘要:天然气的主要成分是甲烷,是一种非常有潜力的清洁能源。
但是由于甲烷在标准条件下体积能量密度低、安全性差等问题,使其在实际存储传输中的应用受到很大限制。
为了常规化使用甲烷燃料,开发出一种安全、低成本的高效甲烷存储策略是当前迫切解决的问题。
MOF材料作为一类新型高效吸附分离材料,由于其高比表面积、可设计性、尺寸可调节性强等优点,受到气体存储领域的极大关注。
本文综述了MOF材料作为甲烷储存材料的研究进展,MOF材料储存甲烷的主要影响因素为静电相互作用、范德华相互作用和框架的灵活性等。
关键词:MOF材料;甲烷存储;研究进展;影响因素中图分类号:TQ424 文献标识码:A 文章编号:1008-021X(2021)04-0082-03ResearchprogressofCH4storageinMOFmaterialsLinYe,ZhuYuling,LiWeihua,XuYing,Liuxiuping(CollegeofMaterialsScienceandEngineering,LinyiUniversity,Linyi 276000,China)Abstract:Naturalgas(NG),whosemaincomponentismethane,isacleanenergysourcewithgreatpotential.However,thestoragefortransportationapplicationsofmethaneisgreatlylimitedduetoitslowvolumetricenergydensityunderstandardconditionsandpoorsafety.Toroutinelyusemethanefuel,itisquiteurgenttodevelopalow-costandsafesolutionformethanestorage.Asanewtypeofadsorptionandseparationmaterialwithhighefficiency,MOFmaterialhasattractedgreatattentioninthefieldofgasstoragebecauseofitscharacteristicssuchashighsurfaceareas,outstandingdesignabilityandmodifiableporestructure.Thispaperreviewsthecurrentresearchstatusandtheinfluencingfactorsmainlyincludingelectrostaticinteraction,vanderWaalsinteractionandflexibilityofframeworkformethanestorageinMOFmaterials.Keywords:MOFmaterials;methanestorage;researchprogress;influencefactor 随着社会生产力和科学技术的迅速发展,全球能源使用量呈指数级增长,因此,目前急需清洁能源代替传统石油基燃料,从而降低碳排放量[1-2]。
1,3―丁二烯的1,2―加成和1,4―加成

摘要:从分子的极化讨论了1,3-丁二烯的加成反应,解释了为什么在高温和强极性溶剂中主要为1,4-加成产物,而在低温和弱极性溶剂中为1,2-加成产物。
关键词:丁二烯加成极化共轭效应有机化学中讲到1,3-丁二烯有共轭体系,产生共轭效应,在性质上除了有1,2-加成外,还有特殊的1,4-加成,而在低温和弱极性溶剂中主要是1,2-加成,而在高温和强极性溶剂中主要是1,4-加成产物。
由于书上没有解释为什么,学生感到困惑,是不是就是一个实验结论,只需记住就可以了,实际上我们可以试着从分子的极化加以解释。
如1,3-丁二烯与溴化氢加成,其产物是1-溴-2-丁烯和3-溴-1-丁烯,但基本没有4-溴-1-丁烯:对1,3-丁二烯的1,4-加成和1,2-加成的解释,大多是根据正碳离子的分布情况和电荷的转移情况来解释的,形成的正碳离子所带电荷越分散,正碳离子越稳定,这可以理解马氏规则的主要产物,如1,2-加成主要生成3-溴-1-丁烯而不是4-溴-1-丁烯,但不能很好的解释1,4-加成以及弱极性、低温下主要为1,2-加成产物,而强极性、高温下为1,4-加成产物。
1,3-丁二烯的结构是ch2=ch-ch=ch2,有∏-∏共轭体系,其中任何一个c的p轨道的电子都不是局限于两个c原子之间,而是可以在任意一个c原子周围运动,形成离域。
结果使c1-c2,c2-c3,c3-c4之间的键长相差无几,形成键长平均化。
丁二烯是非极性分子,但它们之间同样存在着分子间作用力---色散力,由于分子热运动以及碰撞,电子云可以产生“瞬间”变形。
由于丁二烯的特殊结构,电子云在四个c原子之间发生相对位移,原来正负电荷重心重合的分子变为正负电荷重心不重合了,从而产生“瞬时偶极”:一端电子云的密度大,带部分负电荷,另一端则带部分正电荷。
1,3-丁二烯与hbr加成反应的历程是亲电加成反应,所以,丁二烯与溴化氢加成时是溴化氢离解出的带正电荷的氢离子h+先加在丁二烯瞬时带负电的一端(如c1端),形成:这一步是慢反应,紧接着带负电的溴离子br-加在丁二烯带正电荷的一端(c4端),这一步的反应是快反应:这样形成的产物是1,4-加成产物,即1-溴-2-丁烯。
烷烃
4—甲基—3—乙基
⑦写名称
取代基在前,“某烷”在后,将两者名写在一起
6 7 8 CH3 CH2 —CH2 —CH3 | | 例: CH3—CH—CH2—CH2—CH—CH2—CH3 |2 1 3 4 5| CH3 CH3
2,2,5—三甲基—5—乙基辛烷
练习:用系统命名法命名下列有机物
CH3—CH2—CH2 | CH2 戊烷 | CH3 CH3 |2 1 5 4 3 CH3—CH2—CH—CH—CH3 | CH3
同分异构现象和同分异构体
[讨论]下面是正丁烷和异丁烷的组成和某些物质性质,试分析有 何异同并探讨其原因。 名 称 分子式 C4H10 相对分子质量 熔 58 点 沸 点 相对密度 0.5788 正丁烷 -138.4 -0.5
CH 3—CH—CH— CH2 —CH 3 2 CH 3 CH 3CHCH2CH 2CH 3
CH 3 或者: CH 3CH(CH3 )CH2CH 2CH 3
它们对应的结构简式:
乙烷: H H | | H-C-C-H | | H H 丙烷: H H H | | | H-C-C-C-H | | | H H H
CH3CHCH3 CH3
3烷烃的名称:
碳原子数 分子式 名称
1 CH4
2 C 2H 6
3 4 5 C3H8 C4H10 C5H12
甲烷 乙烷
丙 烷 丁烷
戊烷
6 7 8 9 10 碳原子数 分子式 C6H14 C7H16 C8H18 C9H20 C10H22 名称
己 烷 庚 烷 辛烷 壬烷 癸 烷
碳原子数大于十时,以汉字数字代表称某烷,
①找起点 主链中离支链最近端作为起点 先简单取代基 再繁取代基 ②编序号 用阿拉伯数字给主链碳原子编号 以确定支链的位置
大学有机化学答案第五版
大学有机化学答案第五版【篇一:有机化学-第五版-华北师范大学等-李景宁-全册-课后习题答案(完整版)】3、指出下列各化合物所含官能团的名称。
(1) ch3ch=chch3答:碳碳双键 (2) ch3ch2cl 答:卤素(氯) (3) ch3chch3答:羟基(4) ch3ch2 c=o 答:羰基 (醛基)ch3cch3(5)答:羰基 (酮基)(6) ch3ch2cooh 答:羧基 (7)2答:氨基(8) ch3-c≡c-ch3 答:碳碳叁键4、根据电负性数据,用和标明下列键或分子中带部分正电荷和负电荷的原子。
答:6、下列各化合物哪个有偶极矩?画出其方向(1)br2 (2) ch2cl2 (3)hi(4) chcl3(5)ch3oh (6)ch3och3 答:以上化合物中(2)、(3)、(4)、(5)、(6)均有偶极矩(2) h2c(6)h3ccl (3)i(4)cl3 (5)h3cohch37、一种化合物,在燃烧分析中发现含有84%的碳[ar(c)=12.0]和16的氢[ar(h)=1.0],这个化合物的分子式可能是(1)ch4o(2)c6h14o2 (3)c7h16(4)c6h10 (5)c14h22 答:根据分析结果,化合物中没有氧元素,因而不可能是化合物(1)和(2);在化合物(3)、(4)、(5)中根据碳、氢的比例计算(计算略)可判断这个化合物的分子式可能是(3)。
第二章习题解答1、用系统命名法命名下列化合物(1)2,5-二甲基-3-乙基己烷(3)3,4,4,6-四甲基辛烷(5)3,3,6,7-四甲基癸烷(6)4-甲基-3,3-二乙基-5-异丙基辛烷2、写出下列化合物的构造式和键线式,并用系统命名法命名之。
(3)仅含有伯氢和仲氢的c5h12答:符合条件的构造式为ch3ch2ch2ch2ch3;键线式为;命名:戊烷。
3、写出下令化合物的构造简式(2)由一个丁基和一个异丙基组成的烷烃(4) 相对分子质量为100,同时含有伯、叔、季碳原子的烷烃答:该烷烃的分子式为c7h16。
有机化学第二、三章习题答案
《有机化学》第二章、第三章习题答案P39习题1.用系统命名法命名下列化合物:(1) (2)(3) (4)(5) (6) (7) (8)解:(1)2,3,3,4-四甲基戊烷; (2) 3-甲基-4-异丙基庚烷; (3) 3,3-二甲基戊烷; (4) 2,6-二甲基-3,6-二乙基辛烷;(5) 2,5-二甲基庚烷; (6) 2-甲基-3-乙基己烷; (7) 2,2,4 –三甲基戊烷; (8) 2-甲基-3-乙基庚烷。
2.试写出下列各化合物的构造式:(1)2,2,3,3-四甲基戊烷; (2) 2,3-二甲基庚烷; (3) 2,2,4-三甲基戊烷; (4) 2,4-二甲基-4-乙基庚烷;(5) 2-甲基-3-乙基己烷; (6) 三乙基甲烷; (7) 甲基乙基异丙基甲烷; (8) 乙基异丁基叔丁基甲烷;解:(1)(CH 3)3CC(CH 3)2CH 2CH 3; (2) (CH 3)2CHCH(CH 3)CH 2CH 2CH 2CH 3;(3) (CH 3)3CCH 2CH(CH 3)2;(4) (CH 3)2CHCH 2C(CH 3)(C 2H 5)CH 2CH 2CH 3; (5) (CH 3)2CHCH(C 2H 5)CH 2CH 2CH 3; (6) (C 2H 5)3CH; (7) CH 3CH 2CH(CH 3)CH(CH 3)2; (8) (CH 3)2CHCH 2CH(C 2H 5)C(CH 3)3。
3.用不同符号标出下列化合物中伯(1)、仲(2)、叔(3)、季(4)碳原子:(1) (2)4.下列化合物的系统命名对吗?如有错,指出错在哪里?试正确命名之。
(1)2-乙基丁烷; (2)2,4-2甲基己烷;(3) 3-甲基十二烷;(4) 4-丙基庚烷; (5)4-二甲基辛烷;(6)1,1,1-三甲基-3-甲㸨C H 3㜩RC hC ĨcH 3Ĩ2C Ĩ(C H3Ĩ䄲chSchRchchchRchRchSchSchHchSIRC H 3C H ĨC 猨穃HĨĨĨC H 2C 瑈3C Ĩ3C 䑈RĨ䝈 C Ĩ2@chR@cchRchSchHC Ĩ3)2C H 2C H 3C Ĩ3ĨC H 3C 聈C H 2CCC H 2C H 3ĨH 2C H3C H 3畃H 錳C H 3C H 31111122234411CH 3CH(CH 3)CH 2C ĨC H S)Ĩ䑃H (C Ĩ3)罃H 2CH 31Ĩ1Ĩ4Ĩ3Ĩ21基戊烷。
2024年重庆高考化学试卷(原卷+解析)
机密★启用前【考试时间:6月9日8:30-9:45】重庆市2024年普通高等学校招生统一考试化学试卷注意事项:1.作答前,考生务必将自己的姓名、考场号、座位号填写在试卷的规定位置上。
2.作答时,务必将答案写在答题卡上,写在试卷及草稿纸上无效。
3.考试结束后,须将答题卡、试卷、草稿纸一并交回。
可能用到的相对原子质量:N 14 O 16 Ru 101一、选择题:本题共14小题,每小题3分,共42分。
在每小题给出的四个选项中,只有一项是符合题目要求的。
1.“五味调和百味香”,下列调味品的有效成分表达错误..的是6126C H O NaCl 醋酸谷氨酸钠A.AB.BC.CD.D2.常温下,下列各组离子在指定溶液中能大量共存的是A.氨水中:++2--43K Na SO NO 、、、 B.稀硫酸中:+2+--33Na Ba NO HCO 、、、C .4KMnO 溶液中:2++--Fe H Cl Br 、、、 D.2NaAlO 溶液中:+3+-2-44NH Fe Cl SO 、、、3.下列各分子既含有2sp 杂化的原子又能与2H O 形成氢键的是A.33CH CHB.2CH =CHBrC.3CH COOHD.322CH CH NH 4.下列实验原理或方法正确的是A.向溴的4CCl 溶液中通入石油裂解气,溶液褪色,证明气体为乙烯B.向盛有银氨溶液的试管中滴入乙醛,振荡,水浴温热,可生成银镜C.向饱和NaCl 溶液中先通入2CO 至饱和,再通入3NH ,可析出3NaHCO 固体D.向PbS 黑色悬浊液中加入22H O ,生成白色4PbSO 沉淀,证明()sp sp 4K (PbS)>K PbSO 5.某合金含Mg Al Si Mn 、、、和Cu 等元素。
下列说法正确的是A.Si 的电负性大于AlB.Mn 和Cu 均为d 区元素C.Mg 的第一电离能小于AlD.基态时,Mg 原子和Mn 原子的单电子数相等6.某小组用下图中甲作为气体发生装置,其他装置根据实验需求选用(加热及夹持装置略)。
1,3―丁二烯的1,2―加成和1,4―加成
摘要:从分子的极化讨论了1,3-丁二烯的加成反应,解释了为什么在高温和强极性溶剂中主要为1,4-加成产物,而在低温和弱极性溶剂中为1,2-加成产物。
关键词:丁二烯加成极化共轭效应有机化学中讲到1,3-丁二烯有共轭体系,产生共轭效应,在性质上除了有1,2-加成外,还有特殊的1,4-加成,而在低温和弱极性溶剂中主要是1,2-加成,而在高温和强极性溶剂中主要是1,4-加成产物。
由于书上没有解释为什么,学生感到困惑,是不是就是一个实验结论,只需记住就可以了,实际上我们可以试着从分子的极化加以解释。
如1,3-丁二烯与溴化氢加成,其产物是1-溴-2-丁烯和3-溴-1-丁烯,但基本没有4-溴-1-丁烯:对1,3-丁二烯的1,4-加成和1,2-加成的解释,大多是根据正碳离子的分布情况和电荷的转移情况来解释的,形成的正碳离子所带电荷越分散,正碳离子越稳定,这可以理解马氏规则的主要产物,如1,2-加成主要生成3-溴-1-丁烯而不是4-溴-1-丁烯,但不能很好的解释1,4-加成以及弱极性、低温下主要为1,2-加成产物,而强极性、高温下为1,4-加成产物。
1,3-丁二烯的结构是ch2=ch-ch=ch2,有∏-∏共轭体系,其中任何一个c的p轨道的电子都不是局限于两个c原子之间,而是可以在任意一个c原子周围运动,形成离域。
结果使c1-c2,c2-c3,c3-c4之间的键长相差无几,形成键长平均化。
丁二烯是非极性分子,但它们之间同样存在着分子间作用力---色散力,由于分子热运动以及碰撞,电子云可以产生“瞬间”变形。
由于丁二烯的特殊结构,电子云在四个c原子之间发生相对位移,原来正负电荷重心重合的分子变为正负电荷重心不重合了,从而产生“瞬时偶极”:一端电子云的密度大,带部分负电荷,另一端则带部分正电荷。
1,3-丁二烯与hbr加成反应的历程是亲电加成反应,所以,丁二烯与溴化氢加成时是溴化氢离解出的带正电荷的氢离子h+先加在丁二烯瞬时带负电的一端(如c1端),形成:这一步是慢反应,紧接着带负电的溴离子br-加在丁二烯带正电荷的一端(c4端),这一步的反应是快反应:这样形成的产物是1,4-加成产物,即1-溴-2-丁烯。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
me m p 6.7 1011 9.1 1031 1.7 1027 Fg G 2 r (5.3 1011 ) 2
3.7 10 47 N
F电 F万
三、电场强度 1. 电场 超距作用 场的概念 电场的特点: (1) 对位于其中的带电体有力的作用 (2) 电场力的传递是需要时间的 电荷 电荷 电场 电荷
dx dE 2 0
b 2
方向沿 x 轴正向。
所以,平板在 P 点产生场强
dx b E b 2 2 0 2 0
方向沿 x 轴正向。
dx h hdx dE y dEcos 20 r r 20 x 2 h 2 b xdx 2 E x dE x b 0 2 2 2 20 x h x P1
b 2 b 2
dx
x
o
r b
h
dE x
dE
P2 θ dE y y
dE y
dx a csc d
2
a
O
2
2
x
2 2
r a x a csc
2 2
dE x cos d 4 0 a
dE y sin d 4 0 a
2
1
y dE y
dE
P
dEx
1
r
dq
a
O
2
x
讨论
Ex dEx (sin 2 sin 1 ) cos d 4 0 a 4 0 a sin d (cos 1 cos 2 ) E y dE y 4 0 a 4 0 a
质点
F2 F1 在给定电场中的确定点来说: q1 = q2 = E
定义: 电场中某点的电场强度的大小等于单 位电荷在该点受力的大小,其方向为
正电荷在该点受力的方向。
F E q0
3. 电场强度叠加原理
点电荷产生的场 F
点电荷系:
E
FK
K
1 q1q2 er 2 4 0 r
F 1 q E e 2 r q0 40 r
q0
1 qK EK e 2 r K K 4 0 rK
点电荷系在某点P产生的电场强度等于各点电荷单独在该 点产生的电场强度的矢量和。这称为电场强度叠加原理。 连续分布带电体:
dE
dq
dE
1 dq e 2 r 4 0 r
x [1 2 2 1/ 2 ] 2 0 (R x )
r
x E [1 2 2 1/ 2 ]i 2 0 (R x )
R
O
例 如图一宽为 b 的无限长均匀带电平面薄板,其电荷密度为σ 。 求 (1)平板所在平面内,距薄板边缘为 a 处的电场强度; (2)通过薄板的几何中心的垂直线上与薄板的距离为 h 处的 电场强度。 z 解 dx 如图, dx (1)距薄板边缘为a 处的电场强度 a x P1 x
0 8.85418782 1012 (C2 N 1 m 2 )或(F m 1 )
F
讨论
1 q1q2 er 2 4 0 r
(1) 库仑定律适用于真空中的点电荷;
(2) 库仑力满足牛顿第三定律;
(3) 电荷之间距离小于 1010 m 时, 库仑定律仍保持有效.至于 大距离方面,虽然未作过实验验证,但也并没有特殊的理由 预料在大距离情况下库仑定律将失效.
例 氢原子中电子和质子的距离为 5.3 1011 m
求 此两粒子间的静电力和万有引力。 解 两粒子间的静电力大小为
1 e 9.0 10 (1.6 10 ) 8 Fe 8 . 1 10 N 2 11 2 4 0 r (5.3 10 )
2 9 19 2
两粒子间的万有引力为
a
O
P
1 dq dE 40 r 2
x
dq
x
1 dq 1 (q L)dx dE 2 2 L L 4 0 (a 2 - x ) 4 0 (a 2 - x )
方向沿 x 轴正向。
L q dx 1 q E 2 L 4 0 L 0 (a 2 x ) 0 4a 2 L2
方向沿 x 轴正向。
又另解:如图建立坐标系,由:
dq
a
O
P
1 dq dE 4 0 r 2
-x
x
1 dq 1 (q L)dx dE 2 2 L L 4 0 (a 2 - x ) 4 0 (a 2 - x )
方向沿 x 轴正向。
0 q dx 1 q E 2 L 4 0 L L (a 2 x ) 0 4a 2 L2
例 长为 L 的均匀带电直杆,电荷线密度为
求 它在空间一点P 产生的电场强度。(P点到杆的垂直距离为 a )
解
dq dx
1 dx dE 2 4 0 r
dEx dE cos
由图上的几何关系
dE y dE sin
1
y dE y P
dE
dEx
r
dq
x acot
2 1
无限长直均匀带电线
1 0 2
Ey 2 0 a
cos1 Ey 2 0 a
Ex 0
P点位于中垂线时
2 1
Ex 0
例 长为 L 的均匀带电直杆,电荷线密度为, 求 它在其延长上 P 点的电场强度。
(P 点到杆的中心距离为 a )
方向沿 x 轴正向。
已知带电系统的电荷分布时,根据电场强度的定义 求电场中任一点P的电场强度,其方法和步骤是: 根据给定的电荷分布,恰当的选择电荷元和坐标系;
应用点电荷电场强度的计算公式,在选定的坐标系中 写出某一电荷元dq在P点电场强度 dE ;
再应用电场强度叠加原理将每个电荷元产生的电场强度 相加,即可得到该点的电场强度;
dq
dS (面分布)
dV (体分布)
对不同电荷分布的带电体可分别表示如下 E
线带电体:
1 dq L 4 0 r 2 er
dq
dL ( 为电荷线密度) E
1 dL L 4 0 r 2 er 1 dS S 4 0 r 2 er
面带电体:
r
P
dE dE
V
dq E e 2 r 4 0r
dE
dq
r
P
1 cos Ex dq 2 4 0 r 1 cos Ey dq 2 4 0 r 1 cos Ez dq 2 4 0 r
dl (线分布)
: 电荷线密度 :电荷面密度 :电荷体密度
库仑:(1736—
1806)法国物理学 家,使用自己创 制的扭秤得出了 库仑定律。在力 学方面,还确定 了摩擦定律。
q1q2 0 F21 k 2 e21 r
q1
e
0 21
r
q1
q2
F21
1 k 4 0
q1q2 0 F12 k 2 e12 r
F12
0
q2
真空中的介电常数
r
0 e12
第4章 电场和磁场
麦克斯韦:19世纪伟大的英国物理学家、数学家。麦克斯韦建 立的电磁场理论,将电学、磁学、光学统一起来,是19世纪 物理学发展的最光辉的成果,是科学史上最伟大的综合之一.
§4.1
一、电荷
1. 正负性: 2. 量子性
静电场的描述
同种电荷相斥;异种电荷相吸
Q ne
3. 守恒性
e 1.602 176 462(63) 10 19 C
解:
dq dx
O
L 2
1 dx dE 4 0(a x) 2
a
dq
P
x
dx E dE 2 4 ( a x ) L 0 L
2 2
L 2
L q 2 2 2 2 0 4a L ( 0 4a L )另解:如图建立坐标Fra bibliotek,由:o
b
dx E b 2 0 a x 2 ab ln 2 0 a
b 2 b 2
P2
y
ab E ln i 2 0 a
dx (2)距薄板的几何中心的垂直距离为 h 处的电场强度 dE 2 0 r dx x xdx dE x dEsin z 20 r r 20 x 2 h 2
电荷
(3) 电场是客观存在的一种物质
(4) 带电体在电场中运动, 电场力要作功
2. 电场强度E 带电量为Q 的带电体: 在其周围空间产生电场 带电体周围不同点,电场的强弱和方向一 般是不相同 电场力的大小和方向不仅与检验电荷所在处 的电场有关,而且与检验电荷本身电量的大小、 正负有关
检验电荷
带电量足够小
x cos r
r ( R 2 x 2 )1/ 2
讨论
1 qx E 4 0 ( R 2 x 2 )3 / 2
x
dE x
dE
dE
E0 (1) 当 x = 0(即P点在圆环中心处)时,
P
(2) 当 x>>R 时
1 q E 4 0 x 2
r
R O
可以把带电圆环视为一个点电荷 (3) 当 x 2 R 时
dq dS(为电荷面密度) E dq dV (为电荷体密度) E
体带电体:
1 4 0
dV
r
2
V
er
注意:场强叠加是矢量叠加,dE 方向不同时应先分解,然 后在同方向上积分求和,最后,用矢量和计算合场强。
