铜绿假单胞菌检验原始记录Microsoft Word 文档
微生物检验记录表
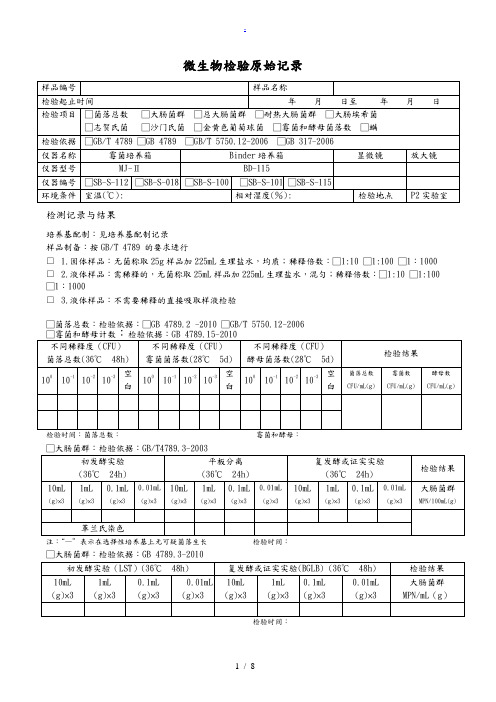
微生物检验原始记录
检测记录与结果
培养基配制:见培养基配制记录
样品制备:按GB/T 4789 的要求进行
□ 1.固体样品:无菌称取25g样品加225mL生理盐水,均质;稀释倍数:□1:10 □1:100 □1:1000 □ 2.液体样品:需稀释的,无菌称取25mL样品加225mL生理盐水,混匀;稀释倍数:□1:10 □1:100 □1:1000
□ 3.液体样品:不需要稀释的直接吸取样液检验
□菌落总数:检验依据:□GB 4789.2 -2010 □GB/T 5750.12-2006
检验时间:菌落总数:霉菌和酵母:
□大肠菌群:检验依据:GB/T4789.3-2003
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
检验时间:
□总大肠菌群:检验依据:GB/T 5750.12-2006
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
□耐热大肠菌群:检验依据:GB/T 5750.12-2006
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
□大肠埃希氏菌:检验依据:GB/T 5750.12-2006
检验时间:
□致病菌□沙门氏菌□志贺氏菌□金黄色葡萄球菌
检验依据 GB 317.4-.10-2006
检测人:复核人:
微生物限度检验记录(复合膜)
检验人:复核人:
微生物限度检验记录(辅料)
检验人:复核人:
微生物限度检验记录(铝箔、PVC硬片)
微生物限度检验记录(半成品、成品)
检验人:复核人:
微生物限度检验记录(辅料)
检验人:复核人:。
铜绿假单胞菌检验

3. 结果报告
根据蓝色或绿色菌落的计数和确证性试验的
结果,计算每250mL水样中的铜绿假单胞菌数 量,结果以CFU/250mL计。 生融合而可能影响计数的精确度。
受到严重污染或培养时间过长时,菌落会产
铜绿假单胞菌(Pseudomonas aeruginosa) ATCC 27853——阳性对照菌株 大肠埃希氏菌(Escherichia coli) ATCC 25922——阴性对照菌株
平铺时应避免在滤膜和培养基之间夹留着气泡。
2.2.3 检验程序
结果观察:
所有显蓝色或绿色(绿脓色素)的菌落,初步判定 为铜绿假单胞菌。 所有发荧光不产绿脓色素疑似铜绿假单胞菌菌落, 进行乙酰胺肉汤确证性试验。
将其它所有红褐色不发荧光的菌落进行氧化酶测试、 乙酰胺肉汤、金氏B培养基确证性试验。
1.1 生物学特性
无特殊营养要求,该菌在普通营养琼脂上生长良 好,琼脂通常会被染成蓝绿色或黄绿色。 该菌在血琼脂平板上生长为灰绿色或蓝绿色菌落, 并形成透明溶血环。 在营养肉汤中呈混浊生长,液面可长出菌膜,菌液 上层为蓝绿色。
1.1 生物学特性
生化反应: 1)氧化酶阳性; 2)液化明胶; 3)硝酸盐还原试验阳性; 4)吲哚阴性; 5)绿脓菌素试验阳性; 6)其它生化试验(糖利用试验、脱羧酶试验等等)。
-P:呈蓝/绿色的菌落数(所有证实为铜绿假单胞 菌的菌落)。 -F: 显荧光的菌落数。 -R: 呈红褐色的菌落数。 -nF:进行产氨测试的显荧光菌落数。 -CF:产氨阳性的显荧光菌落数。 -nR:进行产氨、氧化酶、金氏B培养基上显荧光测 试的红褐色菌落数。 -CR:产氨、氧化酶、金氏B培养基上显荧光测试均 呈阳性的红褐色菌落数。
胃镜中铜绿假单胞菌的微生物学鉴定

果 为 革 兰 氏 阴性 杆菌 。对 培养 液 真接 进 行 镜检 , 发现 有 鱼梭 样运 动的杆菌 。
4 1 氧化 酶试验 .
取 -4 块 洁净 的 白色 滤纸 片 放 在 灭菌 平 皿 内 , 无 菌玻 棒挑 , 用 取可 疑 菌 落 涂在 滤 纸 片上 , 然后 在 其上 滴 加 一 滴新 配 制 的 l 二 % 甲基 对 苯二 胺试 液 , 0 3 s内出现 紫 红色 , 阳性 。 为
药 物 研 究
44 绿 脓 菌素试 验 . 在 普通 琼 脂斜 面培 养基 内 , 入 三氯 甲烷 5 加N O GM J C
6 32 戊 二醛消 毒剂危 险因素 的防 护 戊 二醛消毒 剂危险 因素 .. 主要包 括 : )2 ( 2作场所通风 不 良; ) 11 ( N毒过 程不密 闭; ) 2 ( 未及时处理 配 3 制 与丢 弃溢 出的 戊二 醛 ; ) 人防 护不 到位 等 。 (个 4 戊 二 醛 消 毒 室应 有足 够 空 间保证 戊 二醛 蒸 气 充 分稀 释 , 气 空 交换 次 数 至少 1 / 0次 h。局 部 排风 罩 应安 装 在 戊二 醛蒸 气 排 出点 的水 平位 置 , 度 8 ~10 尺 / n 管道 排 气罩应 与室 外大 气 面速 0 0英 mi ; 非循 环 排 气 系统相 连 , 离人 与空 气 吸入 管 ; 管道 排气 系统 的 蒸 远 非 气应 释 放至 戊 二醛 过 滤 系统 , 滤 后清 洁 空 气 回至房 内 , 过 并定 期监 测其 过 滤效 率 , 定期 更 换 。工 作人 员应 能察 觉 到任 何来 源 的气 流 ,
能利 用 枸 檬 酸盐 。见 表 l 。 4 3 4 ℃生 长试 验 . 2
药品微生物限度检验记录(铜绿甲单胞菌)

氧化酶试验
培养基
名称
营养琼脂培养基
绿
脓
菌
试
验
培养基
名称
PDP琼脂培养基
批号
批号
培养
温度
℃
培养
温度
℃
时间
日时至日时,计小时
时间
日时至日时,计小时
现象:
现象:
结果判定:
结果判定:
检验项目标准规定检验结果
铜绿假单胞菌每1不得过检出□未检出 □检出结论:检验人:复核人:
药品微生物限度检验记录
(铜绿假单胞菌)
检验号REC-QC-057-00
品名
跌打活血散(混合生药粉)
规格
批号
数量
来源
紫外消毒时间
时分至时分
取样日期
报告日期
检验依据
铜绿假单胞菌
增菌培养:取供试液10ml,直接接种至适量(不少于100ml)的胆盐乳糖培养基中,培养。
培养基
名称
胆盐乳糖培养基
培养
温度
℃
批号
时间
日时至日时,计小时
分离培养:取上述培养物,划线接种于溴化十六烷基三甲铵琼脂培养基的平板上,培养。
培养基
名称
溴化十六烷基三甲铵琼脂培养基
培养
温度
℃
批号
时间
日时至日时,计小时
现象:
确证试验:从上述分离平板上挑选2〜3个疑似菌落,分别接种于营养琼脂培养基斜面上,培养18〜24小时。取斜面培养物进行革兰染色、镜检及氧化酶试验。
铜绿假单胞菌的菌种鉴定

铜绿假单胞菌的菌种鉴定全文共四篇示例,供读者参考第一篇示例:铜绿假单胞菌(Pseudomonas aeruginosa)是一种常见的革兰氏阴性细菌,属于假单胞菌属(Pseudomonas),广泛存在于自然界中,是一种耐受力很强的细菌。
铜绿假单胞菌在人类和动植物体内都有可能成为病原菌,引起多种感染疾病,如呼吸道感染、尿路感染、皮肤感染等。
对铜绿假单胞菌的菌种鉴定十分重要。
铜绿假单胞菌的菌种鉴定主要包括形态学观察、生理生化特性检测、分子生物学方法等。
形态学观察是最为简单直观的方法,通过观察细菌在琼脂培养基上的形态特征来初步鉴定。
铜绿假单胞菌在琼脂培养基上形成典型的青绿色凝块状菌落,通常呈金黄色至淡黄色,具有辛辣气味。
除了形态学观察外,生理生化特性检测也是菌种鉴定的重要方法之一。
铜绿假单胞菌具有一系列特殊的生理生化特性,如利用氧化物作为唯一氧化剂和膜脂组成特殊等。
铜绿假单胞菌产生溶血素、胞外聚合物酶、脂肪酶等多种外源酶,可以降解寡糖、脂质等物质。
分子生物学方法也成为现代菌种鉴定的重要手段。
通过PCR扩增和测序技术,可以对靶基因进行测序分析,比如16S rRNA基因序列分析。
铜绿假单胞菌16S rRNA序列具有较高的保守性,同时又有足够的变异性,能够帮助界定种和属的分类关系。
在进行铜绿假单胞菌菌种鉴定的过程中,需特别注意以下几点:1. 选择合适的菌落:铜绿假单胞菌菌落为青绿色,有金黄色至淡黄色的边缘。
需避免选择其他青绿假单胞菌属菌种带来的干扰。
2. 确认生理生化特性:对于一些特殊的生理生化特性,如氧化物利用情况、酶产生等,可以通过专门的生化试验进行验证。
3. 结合分子生物学方法:如果需要进一步确定菌种的归属,可结合分子生物学方法进行16S rRNA序列分析,加深对菌种的认识。
铜绿假单胞菌的菌种鉴定是一项重要且复杂的工作,需要结合形态学观察、生理生化特性检测和分子生物学方法等多种手段进行综合分析。
只有准确鉴定出铜绿假单胞菌的菌种,才能更好地开展相关的医学、环境等研究工作,为防治相关感染病害提供科学依据。
食品中铜绿假单胞菌检测

自动生化鉴定仪器 生化试剂条(以国标法为参照,二者符 合率99.6%- 参考文献)
操作步骤-水样过滤
在100级的洁净工作台进行过滤操作。 首先用无菌镊子夹取灭菌滤膜边缘部分, 将粗糙面向上,贴放在已灭菌的滤床上, 固定好滤器,将250mL水样或稀释液通 过孔径0.45μm的滤膜过滤,然后将过滤 后的滤膜贴在已制备好的CN琼脂平板上, 平铺并避免在滤膜和培养基之间夹留着 气泡。
测试的红褐色菌落数。
– cR是产氨、氧化酶、金氏B培养基上显荧光测试 均呈阳性的红褐色菌落数。
• 举例
N=17+16×(2/5)+10×(3/5) – 17:呈蓝/绿色的菌落数; – 16:没有绿脓色素但显荧光的菌落数; – 2:产氨阳性的显荧光菌落数; – 5:进行产氨测试的显荧光菌落数; – 10:呈红褐色的菌落数; – 3:产氨、氧化酶、金氏B培养基上显荧光测试均
呈阳性的红褐色菌落数;
– 5:进行产氨、氧化酶、金氏B培养基上显荧光测 试的红褐色菌落数。
• 样品稀释 若样品污染严重,建议对样品进行稀
释,如10倍递增稀释:取30ml样液加入 至270ml无菌生理盐水中,混匀,以此类 推,进行系列稀释。
• 报告 结果以 CFU/250ml计。
• 其他确证试验方法
产荧光素实验(金氏B培养基)
化妆品菌落总数检测原始记录

生理盐水、卵磷脂吐温80营养琼脂培养基、0.5%TTC(氯化三苯四氮唑)溶液
样品制备
取g(mL)样品以mL无菌生理盐水稀释为1:10样品稀释液。
实验步骤
1、用灭菌吸管吸取1:10稀释的检液2mL,分别注入到两个灭菌平皿内,每皿1mL。另取1mL注入到9mL灭菌生理盐水试管中(注意勿使吸管接触液面),更换一支吸管,并充分混匀,制成1:100检液。吸取2mL,分别注入到两个灭菌平皿内,每皿1mL。如样品含菌量高,还可再稀释成1:1000,1:10000,……等,每个稀释度应换1支吸管。
备注:
项目编号
样品名称
检测项目
铜绿假单胞菌
样品性质
收样时间
检测时间
环境条件
温度: ℃ 湿度: %
检测依据及方法
《化妆品安全技术规范》2015版 第五章 微生物检验方法 2 菌落总数检验方法
设备及编号
电热恒温培养箱DHP-9082B(KLM-YQSB-006)、生物安全柜BHC-1300ⅡA2(KLM-YQSB-002)、立式蒸汽灭菌器LDZM-60KCS-Ⅱ(KLM-YQSB-022)、恒温恒湿培养箱HSP-150BE(KLM-YQSB-007)、水浴锅HH-4双列四孔(KLM-YQSB-017)
3、为便于区别化妆品中的颗粒与菌落,可在每100mL卵磷脂吐温80营养琼脂中加入1mL0.5%的TTC溶液,如有细菌存在,培养后菌落呈红色,而化妆品的颗粒颜色无变化。
4、菌落计数方法:先用肉眼观察,点数菌落数,然后再用5倍~10倍的放大镜检查,以防遗漏。记下各平皿的菌落数后,求出同一稀释度各平皿生长的平均菌落数。
2、将融化并冷至45℃~50℃的卵磷脂吐温80营养琼脂培养基倾注到平皿内,每皿约15mL,随即转动平皿,使样品与培养基充分混合均匀,待琼脂凝固后,翻转平皿, 置36℃±1℃培养箱内培养48h±2h。另取一个不加样品的灭菌空平皿,加入约15mL卵磷脂吐温80营养琼脂培养基,待琼脂凝固后,翻转平皿,置36℃±1℃培养箱内培养48h±2h,为空白对照。
微生物限度检验记录

微生物限度检验记录一、检验目的:确认产品是否满足微生物限度要求,保证产品的安全性和质量。
二、检验项目:1.总大肠菌群:用于评估产品是否受到粪便污染。
2.霉菌和酵母菌:用于评估产品是否受到霉菌和酵母菌的污染。
3.沙门氏菌:用于评估产品是否受到沙门氏菌的污染,沙门氏菌是一种常见的食源性病原菌。
4.铜绿假单胞菌:用于评估产品是否受到铜绿假单胞菌的污染,铜绿假单胞菌是一种常见的致病菌。
5.谷氨酰胺酶阳性菌:用于评估产品是否受到谷氨酰胺酶阳性菌的污染,谷氨酰胺酶阳性菌是一种常见的致病菌。
三、检验步骤:1.样品准备:从产品中取得一定量的样品,确保样品的代表性。
2.样品处理:根据产品的不同特性,选择适当的方法进行样品处理,如水解、稀释等。
3.培养基制备:根据所需的检验项目,制备相应的培养基。
4.培养基接种:将处理后的样品接种到相应的培养基中,利用无菌技术确保操作的无菌。
5.培养:将接种过的培养基培养在适宜的温度和湿度条件下,培养一定的时间,一般为24-72小时。
6.检查结果:观察培养基上是否有菌落形成,记录菌落的数量和形态特征。
7.鉴定:对培养出的菌落进行进一步的鉴定,如形态学观察、生理生化特性测试等。
8.统计和分析:根据检查结果,统计并分析微生物的数量,计算出产品的微生物限度。
四、检验结果:1.总大肠菌群:每克不超过100个。
2.霉菌和酵母菌:每克不超过10个。
3.沙门氏菌:每克不得检出。
4.铜绿假单胞菌:每克不得检出。
5.谷氨酰胺酶阳性菌:每克不得检出。
五、检验记录样例:日期:2024年4月1日样品名称:XXX产品检验员:XXX检验项目:1.总大肠菌群结果:每克10个,符合微生物限度要求。
2.霉菌和酵母菌结果:每克2个,符合微生物限度要求。
3.沙门氏菌结果:未检出,符合微生物限度要求。
4.铜绿假单胞菌结果:未检出,符合微生物限度要求。
5.谷氨酰胺酶阳性菌结果:未检出,符合微生物限度要求。
六、结论:根据检验结果,XXX产品符合微生物限度要求,产品安全可靠。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
检验项目
现象
结果
分离
培养
十六烷三甲基溴化铵琼脂平板
要求
36±1℃;18h~24h。
培养
___日___时至___日___时
革兰氏染色、镜检
鉴定生化试验
氧化酶试验
绿浓素试验
要求
36±1℃;18h~24h。
培养
___日___时至___日___时
硝酸盐还原
要求
36±1℃;18h~24h。
培养
___日___时至___日___时
CDC-GS-140-2014
**疾病预防控制中心
铜绿假单胞菌检验原始记录共页第页
样品编号
样品名称
检验依据
仪器设备名称、规格型号、
生物显微镜:CX31
电热恒温培养箱: PYX-DHX×50
检验环境
温度:℃湿度:%Biblioteka H检验日期样品复苏
样品制备
1.以无菌操作取检样g(mL)加入mL SCDLP液体培养基,振荡混匀,于36±1℃培养18-24h.
明胶液化
要求
36±1℃;18h~24h。
培养
___日___时至___日___时
42℃生长
要求
41℃-42℃;18h~24h。
培养
___日___时至___日___时
实验结果
备注
检验者:审核者:年月日
