茶多酚提取实验上课讲义
茶多酚提取综合试验(1)

茶叶提取茶多酚综合实验一、实验目的1)熟悉酒石酸亚铁法测定茶多酚含量;2)掌握天然植物中提取活性物质的实验方案设计及操作方法;3)熟练掌握各种实验操作的正确方法;4)熟悉数据处理及科技论文的写作方法。
二、实验原理茶多酚是一类以儿茶素类为主体的多酚类化合物,由于其酚性羟基易氧化而提供质子H +,而具有抗氧化和消除自由基作用,是一种理想的天然抗氧化剂。
含醇羟基的有机溶剂对植物多酚具有良好的溶解性,而含水的有机溶剂对多酚的溶解能力比纯有机溶剂大,这是因为含水有机溶剂可破坏多酚分子间的氢键从而减弱了多酚间的缔合,有利于多酚的溶出。
二、试验仪器及药品BS210S 电子分析天平 722分光光度仪 KQ-5200超声波振荡器RE-52D 旋转蒸发器 粉碎机试验原料:苏州碧螺春绿茶(2008年春制取,冰箱保存).... ....三、试剂与溶液配制1.标准溶液的配制:精确称取没食子酸乙酯(100℃烘干燥1h )25mg ,水溶解,定容至25mL 容量瓶中,作为标准溶液。
2.酒石酸铁溶液称取硫酸亚铁(GB 664)1.0g ,酒石酸钾钠(GB 1288)5.0g ,加水溶解并定容至1L ,可稳定10天。
3.pH7.5的磷酸缓冲液a 液: 1/15mol/L 的磷酸氢二钠溶液:称取磷酸氢二钠(GB 1263)23.877g ,加水溶解并稀释至1L 。
b 液: 1/15mol/L 的磷酸二氢钾溶液:称取经110℃烘干2h 的磷酸二氢钾(GB 1274)2.2695g ,加水溶解至250mL 。
c 液:.取a 液85mL 和b 液15mL 混匀,即得pH7.5的缓冲液。
四、试验方法(一)分析方法多酚类物质能与亚铁离子生成紫蓝色络合物。
用分光光度法测定其含量。
虽然各种儿茶素的呈色度不同,但茶多酚中的儿茶素组成范围大致相同,在此范围内,对吸光度的影响不大,故用一条标准曲线即可。
此标准曲线与没食子儿茶素没食子酸酯的标准曲线一致,但因没食子儿茶素没食子酸酯不易得到,故用没食子酸乙酯。
茶多酚的提取

实验名称:普洱茶多酚的提取研究及抗氧化作用的研究姓名:学号:桌号:一.实验目的1. 掌握从茶叶或茶叶的下脚料屮提取茶多酚的方法;2. 学:握用分光光度计测定茶多酚总量的方法;3. 棠握酒石酸铁比色法测定茶多酚的含帚:二.实验原理产物:茶多酚物理性质:茶多酚在常温下呈浅黄或浅绿色粉末.易溶于温水(40°C — 80°C) 和含水乙醇中;稳定性极强,在pH值4一8、250°C左右的环境中,1.5个小时内均能保持稳定,在三价铁离子下易分解。
1989年被中国食品添加剂协会列入GB2760-89食品添加剂使用标准,1997年列为中成药原料。
茶多酚是茶叶屮多酚类物质的总称,为白色无定形粉末,易溶于水。
茶多酚具有很好的抗氧化活性, 且抗氧化性优于丁基羟基茴香瞇(BHA)、二丁基羟基甲苯(BHT)、叔丁基对苯二酚(TBHQ)等。
国内外学者对茶多酚进行了急性毒性、亚急性毒性和各种药理试验研究,结果表明茶多酚安全无毒。
茶多酚不仅是一种新型的天然抗氧化剂,还具有明显的抗衰老、消除人体过剩的白由基、去脂诚肥、降低血糖、降低血脂利胆固醇、预防心血管疾病、抑制肿瘤细胞等药理功能,在食品加工、医药、口用化工等领域具有重要的应用化学性质:茶多酚是从茶叶中提取的全天然抗氧化食品, 具有抗氧化能力强,无毒副作用,无异味等特点。
离子沉淀法提取普洱茶多酚1.原理普洱茶是以云南省一定区域内的云南大叶种晒青毛茶为原料,经过后发酵加工成的散茶和紧压茶,其外形色泽褐红内质汤色红浓明亮,香气独特陈香,滋味醇厚回甘,叶底褐红⑴.普洱茶具有降血糖、降血脂、杀死癌细胞、抗突变、防癌等功能[2]・其中具有药理作用的主要成分是茶多酚、茶多糖等.茶多酚有降血糖、延缓衰老、抑制动脉粥样硬化、防癌抗癌等作用[3];主题为黄烷醇(儿茶素)类,儿茶素占60-80%o类物质茶多酚乂称茶糅或茶单宁,是形成茶叶色香味的主要成份之一,也是茶叶中有保健功能的主要成份之一。
从茶叶或茶叶下脚料中提取茶多酚

实验4 从茶叶或茶叶下脚料中提取茶多酚一、实验目的(1) 掌握从茶叶或茶叶下脚料中提取茶多酚的方法。
(2) 掌握用分光光度法测定茶多酚总量的方法。
二、实验原理目前,茶叶消费日趋高档化,而中、低档茶受国际市场影响常滞销、积压严重,这种现象制约的茶叶产业的发展。
与此同时,在茶叶生产及加工过程中还有大量修剪枝叶及加工副产品,这些产品多作为废物而为加以充分利用。
因此,寻求经济新增长点及开辟茶叶新用途成了各国各地区茶学界的重要议题。
茶叶综合利用已成为茶叶发展中的新亮点。
茶的综合利用是以茶(含茶树的根、茎、花、果、种子等)为原料,对茶的内含物进行综合开发,达到物尽其用,以增加收益。
众所周知,茶叶有诸多保健作用,这与茶叶中富含茶多酚、咖啡因、茶多糖和茶氨酸等有效成分有密切关系。
茶多酚不仅是一种天然的食品抗氧化剂,而且还是多种保健品及药品的生产原料;咖啡因是多种饮料的添加剂,在医药上也有广泛的应用;茶多糖有降血糖、血脂和增强机体免疫力等功效;美国科学家发现茶氨酸能使人体抵御SARS 病毒感染的能力增强5倍,是极有潜力的新型抗病毒、细菌和真菌的新型药品和保健品的成分。
由此可见,对这些有效成分进行制备并加以利用,不仅是解决中、低档茶及茶副产品出路的有效途径之一,而且可产生重大的经济效益和社会效益。
从清洁生产的思想出发,对有效成分进行有效提取,提出清洁生产工艺,考虑到实验整体安排这里主要以提取茶多酚为主开展讨论。
热水 乙酸乙酯 HCl 氯化锌 升华 浓缩有机相 上清液 浓缩→萃取(氯仿)→水相→沉析(乙醇)→茶多糖 脱盐结晶 沉淀剂 滤液 咖啡因 茶氨酸 茶渣茶叶中富含多烃基的酚性物质——茶多酚。
茶多酚的主要组分是儿茶素,占茶多酚含量的80%左右。
茶多酚中几种主要儿茶素所占的比例分别为:L-表没食子儿茶素没食子酸酯(L-EGCG )50%~60%,L-表儿茶素没食子酸酯(L-ECG )15%~20%,L-表没食子儿茶素(L-EGC )10%~15%,L-表儿茶素(L-EC )4%~6%。
茶叶有效成分的提取
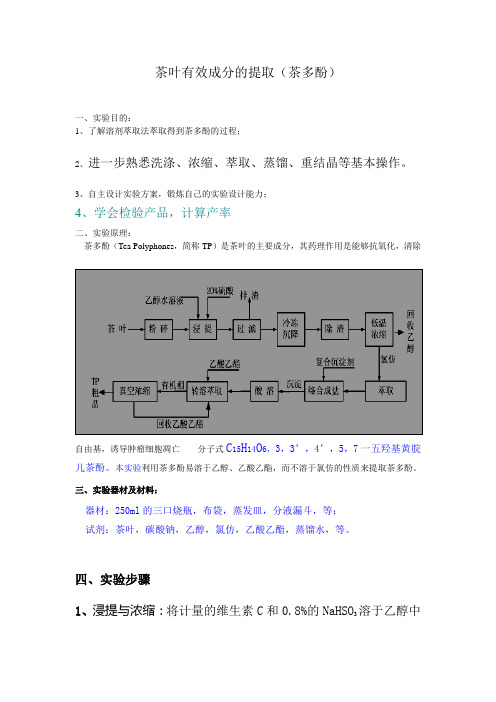
茶叶有效成分的提取(茶多酚)一、实验目的:1、了解溶剂萃取法萃取得到茶多酚的过程;2、进一步熟悉洗涤、浓缩、萃取、蒸馏、重结晶等基本操作。
3、自主设计实验方案,锻炼自己的实验设计能力;4、学会检验产品,计算产率二、实验原理:茶多酚(Tea Polyphones,简称TP)是茶叶的主要成分,其药理作用是能够抗氧化,清除自由基,诱导肿瘤细胞凋亡分子式C15H14O6,3,3’,4’,5,7一五羟基黄脘儿茶酚。
本实验利用茶多酚易溶于乙醇、乙酸乙酯,而不溶于氯仿的性质来提取茶多酚。
三、实验器材及材料:器材:250ml的三口烧瓶,布袋,蒸发皿,分液漏斗,等;试剂:茶叶,碳酸钠,乙醇,氯仿,乙酸乙酯,蒸馏水,等。
四、实验步骤1、浸提与浓缩:将计量的维生素C和0.8%的NaHSO3溶于乙醇中配制成2500ml 80%的溶液;将粉碎细化后的绿茶加入到三口烧瓶中,并将配制的乙醇溶液分别以1200ml,800ml,500ml分三批加入到三口烧瓶中,搅拌升温回流浸提;浸提时间分别为60min,40 min,30 min,每次的浸提液分别倾出到烧杯中放入冷冻箱内,并将茶渣挤滤干,整个浸提过程中保持PH<5,浸提液置于冷冻箱中冷冻2个小时或者过夜后进行提液抽滤,将上层清液抽出,计量后放入1000ml的单口烧瓶中进行常压浓缩,回收其中的乙醇,得到浸提浓缩液,并记录其体积;并计算浸提物料的收率。
1.2 络合:将浓缩液加入100ml的80%乙醇溶液,用CHCL3进行萃取,每次用CHCL3150ml,共萃取4次,取萃取余相加入到四嘴瓶中;向体系加入络合剂三氯化铝和三氯化铁,搅拌,用5%的氨水调节PH值介于5~5.5之间,维持温度在30~35℃之间,并缓慢搅拌使络合沉淀完全;将得到的固液悬浮液进行抽滤,并用蒸馏水100ml分两次洗涤滤饼,进行抽干,称量滤饼质量。
1.3 酸化转溶:将所得的滤饼用10%HCL 600ml溶解,过滤除去不溶物;用乙酸乙酯萃取4~5次,每次用400~500ml;得到的萃取液,用含1.5%的柠檬酸,20%的NaHSO3的溶液进行水洗1次;乙酸乙酯相用无水Na2SO4 200g 进行干燥,并过滤;用100ml烧瓶将上述滤液进行真空旋转干燥,应用减压干燥,并控制外边的水浴温度为35℃左右,并保证旋蒸时间充分;得TP重量,计算全程百分收率;并回收络合剂。
茶多酚的提取

须经反复除杂精制,需要用的有机溶剂量较大。生产中应用的有机溶剂,部分存 在回收困难、能耗较大、生产成本较高、有毒性等问题,如工艺处理不当,产品 可能存在有机溶剂的残留。 b. 金属离子沉淀法茶多酚在一定条件下可与某些金属离子络合生成结晶 性沉淀,使其从浸提液中分离出来,与茶叶中的咖啡碱、单糖、氨基酸等组分分 离,从而制备茶多酚。该法制备茶多酚的主要步骤为:茶叶经热水浸提后,调节 pH 值,加入沉淀剂形成茶多酚与金属离子的沉淀物,沉淀经酸转溶和乙酸乙酯 萃取,干燥后可得茶多酚产品。常用的沉淀剂有 Al3 +、Ca2 +、Fe2 +、Mg2 +、 Zn2 +、Ba2 +等多种离子,其中 Zn2 +、Al3 +是茶多酚得率较高的弱酸性沉淀剂, 但存在于产品中的 Al3+易引发老年性痴呆症,故多选用 Zn2+为沉淀剂。余兆祥 等采用 Zn2+和 Al3+的复合沉淀剂提取低档绿茶中的茶多酚, 获得了纯度大于 96% 的淡黄色茶多酚晶体,提取率为 10.4%,较单一沉淀剂高约 1%。金属离子沉淀 法制取茶多酚, 在茶叶浸提液中加入沉淀剂即可得到茶多酚与金属的结晶性沉淀 物,因而不必浓缩浸提液,可在一定程度上降低能耗;同时,该方法选择性强, 产品纯度较高,无须使用大量的有机溶剂和氯仿等有毒物质,成本低。但是,该 方法需在碱性条件下进行, 再以酸转溶, 大量酸碱溶液的利用, 导致废液、 废渣、 废水处理量大, 对环境污染大; 此外, 茶多酚容易被氧化而损失较大。 综合来看, 虽然该方法生产的茶多酚产品中,咖啡碱含量低,但因使用重金属盐作沉淀剂, 产品中重金属离子残留高,而金属离子有一定的毒性,达不到食品工业标准,限 制了产品的应用。 c. 柱层析法柱层析法的原理是利用样品中组分在两相之间的分配系数不同, 而达到分离的目的。常采用硅胶、氧化铝、活性炭、聚酰胺、凝胶、离子交换树 脂和大孔吸附树脂等固态物质作为载体。根据所采用的树脂类型的不同,可分为 吸附柱分离法、离子交换柱分离法和凝胶分离法。该方法的一般工艺流程为:茶 叶浸提→过滤→滤液超滤→用树脂吸附→乙醇洗脱→回收乙醇→干燥→茶多酚 产品。该方法用于提取茶多酚,工艺简单、能耗较低、安全,有利于实现大规模 生产, 以乙醇作为有机溶剂, 也有无毒、 易回收、 残留低、 对环境无污染等优点; 选择出适用于分离的树脂材料, 具有机械强度好、 解吸和再生容易、 使用寿命长、 成本低的优点。
茶多酚提取实验

蚌埠学院生物与食品工程系综合实验实验名称:茶多酚的提取工艺试验一、实验目的及要求:1.了解茶多酚的性质和用途。
2.了解植物天然产物的常规提取及精制方法。
3.通过本实验的具体操作,掌握并熟悉茶多酚的提取与精制的方法及其操作原理和步骤。
4.掌握提取精制过程中茶多酚的分析检测方法。
二、实验原理:茶多酚是茶叶中多酚类物质的总称,含量约占茶叶干重量的20%-30%。
茶多酚可以消除超氧阴离子和过氧化氢自由基,同时具有抑菌、杀菌,有效降低大肠对胆固醇的吸收,增强机体免疫能力等功能。
目前,茶多酚被广泛的用作食品、饮料、药品和化妆品的天然添加成分。
(离子沉淀法)茶多酚易溶于热水,与一些金属离子形成络合物,并在一定pH值下溶解度很低。
形成的金属离子络合物溶于酸溶液后,茶多酚再次转变成游离状态,再用对茶多酚有更好选择性的溶剂进行萃取、浓缩和干燥,即可得到茶多酚的纯品。
三、实验仪器:电动搅拌器、离心机、pH试纸、真空干燥箱、抽虑瓶、旋转蒸发仪、真空泵、天平、紫外分光光度计、容量瓶、烧杯、量筒等。
四、实验试剂及材料:氯化钠、碳酸氢钠、柠檬酸、硫酸铝、盐酸、亚硫酸氢钠、乙酸乙酯、维生素C(抗坏血酸)、磷酸氢二钠、磷酸二氢钾、硫酸亚铁、酒石酸钾钠、硫酸、绿茶等五、实验内容及步骤:1.浸提1.1 预处理:粉碎干茶叶;粉碎的目的是与液体的接触面增大,使提取率增高;1.2 提取:准确称取经过预处理的干茶叶末10. 00g,按照单因素实验的料液比、浸提温度、浸提时间分别搅拌浸提。
过滤(用抽滤的方法)得到茶多酚提取液。
用附一的方法测提取液中的茶多酚含量。
单因素实验步骤:(1)将称取得10.00g茶叶末置于500ml烧杯中,加入200mL蒸馏水,在85℃下,分别提取0.5h、0.75h、1.0h、1.25h、1.5h,测提取液的吸光度,绘制曲线图,找出最佳提取时间。
(2)称取得10.00g茶叶末置于500ml烧杯中,加入200mL蒸馏水,在所测得的最佳提取时间下,分别在75℃、80℃、85℃、90℃、95℃下浸提,测提取液的吸光度,绘制曲线,找出最佳提取温度。
茶多酚的提取纯化工艺研究

茶多酚的提取纯化工艺研究一、实验目的:研究茶多酚在茶叶中的大致含量,并分析比较现有的醇提和水提工艺,结合不同的纯化方法,通过具体的实验数据,比较得出其优缺点,为工业化生产提供指导。
二、实验原理:1.,(粗提部分)茶多酚易溶于热水,含水乙醇和乙酸乙酯等溶液中,而不溶于氯仿,苯等试剂,利用茶多酚在上述溶剂中具有具有不同分配系数等特性,经过多次萃取进进行提取分离纯化。
2.,(纯化部分)未氧化的茶多酚及其初级氧化产物易溶于乙酸乙酯3,(纯化部分)茶多酚能与无机盐中的金属离子(如Ca2+、Mg2+ 、Zn2+ 等)配位生成沉淀而对茶多酚进行分离4,在一定PH值条件下,酒石酸能与多酚类物质反应形成蓝紫色络合物,该络合物在540nm波长下具有最大吸光度。
在适当范围内,茶多酚的含量与络合物的吸光度成正比,符合朗柏-比尔定律,因此可用分光光度法对茶多酚定量分析。
三、实验仪器:干茶,真空干燥箱,分液漏斗,旋转蒸发仪,乙醇,氯仿,乙酸乙酯,纱布,烧杯,玻棒,漏斗,电子天平,水浴锅,95%乙醇,氯化钙(无水),氯化镁,硫酸,氨水均为分析纯。
索氏抽提器;PHS一3C数字酸度计;800型离心沉淀器;GSP一805型圆盘搅拌器;79—1磁力加热搅拌器;UV-9100紫外可见分光光度计;微波炉;LD4—800大容量低速离心机。
四、实验步骤:(一):茶多酚乙醇提取和有机溶剂纯化实验(3次平行实验)1、乙醇提取:称茶叶磨碎样3g于烧杯中,加入5倍量(15ml)85%乙醇,将烧杯置于30-40℃水浴锅中,浸提20min,浸提过程不断搅拌,然后滤出滤液,剩下的茶渣再加2-3倍量(约6~9 ml)85%乙醇,再浸提20min,过滤。
合并两次滤液。
(取3ml留样分析)2、减压浓缩:将滤液装入旋转蒸发仪中,在40-50度水浴温度下减压浓缩至基本除去乙醇为止。
3、氯仿除去杂质:将浓缩液装入分液漏斗中,将同等体积的氯仿加入,摇匀后混合液分为两层。
茶多酚物理实验报告

茶多酚物理实验报告茶多酚物理实验报告茶多酚是一种在茶叶中广泛存在的物质,具有多种生物活性和药用价值。
本实验旨在通过物理实验方法,探究茶多酚的一些基本性质和特点。
实验一:茶多酚的提取首先,我们需要从茶叶中提取茶多酚。
取适量的绿茶叶,将其研磨成细末,然后将茶末与乙醇混合,搅拌均匀。
接着,用滤纸过滤混合物,得到茶多酚溶液。
实验二:茶多酚的紫外吸收光谱将茶多酚溶液置于紫外可见分光光度计中,进行紫外吸收光谱测定。
茶多酚在紫外光区域(200-400nm)具有较强的吸收峰,主要在270-280nm附近。
根据吸收峰的强度和位置,可以初步判断茶多酚的含量和结构。
实验三:茶多酚的溶解度为了研究茶多酚的溶解性质,我们在实验中使用了不同溶剂,如水、乙醇和丙酮。
将茶多酚溶解于不同溶剂中,并观察其溶解情况。
实验结果显示,茶多酚在水中溶解度较高,而在乙醇和丙酮中溶解度较低。
这是因为茶多酚是一种多酚类化合物,其溶解度受到溶剂极性的影响。
实验四:茶多酚的氧化性茶多酚具有较强的氧化性,可以与氧气发生反应产生氧化产物。
在实验中,我们将茶多酚溶液与空气接触一段时间,观察溶液的颜色变化。
实验结果显示,茶多酚溶液由无色逐渐变为深棕色,这是由于茶多酚发生氧化反应产生了氧化产物。
实验五:茶多酚的抗氧化性茶多酚具有良好的抗氧化性,可以抑制自由基的产生和氧化反应的发生。
为了研究茶多酚的抗氧化性,我们使用了DPPH自由基清除实验。
将DPPH溶液与茶多酚溶液混合,观察溶液颜色的变化。
实验结果显示,茶多酚能够与DPPH自由基发生反应,使其从紫色变为淡黄色,表明茶多酚具有较强的抗氧化性。
综上所述,茶多酚是一种具有多种生物活性和药用价值的物质。
通过物理实验,我们可以了解茶多酚的提取方法、紫外吸收光谱特性、溶解度、氧化性和抗氧化性等基本性质。
这些实验结果对于深入研究茶多酚的药理学和生物学活性具有重要意义,也为茶叶的加工和利用提供了科学依据。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
茶多酚提取实验
蚌埠学院
生物与食品工程系
综合实验
实验名称:茶多酚的提取工艺试验
一、实验目的及要求:
1.了解茶多酚的性质和用途。
2.了解植物天然产物的常规提取及精制方法。
3.通过本实验的具体操作,掌握并熟悉茶多酚的提取与精制的方法及其操作原理和步骤。
4.掌握提取精制过程中茶多酚的分析检测方法。
二、实验原理:
茶多酚是茶叶中多酚类物质的总称,含量约占茶叶干重量的20%-30%。
茶多酚可以消除超氧阴离子和过氧化氢自由基,同时具有抑菌、杀菌,有效降低大肠对胆固醇的吸收,增强机体免疫能力等功能。
目前,茶多酚被广泛的用作食品、饮料、药品和化妆品的天然添加成分。
(离子沉淀法)茶多酚易溶于热水,与一些金属离子形成络合物,并在一定pH值下溶解度很低。
形成的金属离子络合物溶于酸溶液后,茶多酚再次转变成游离状态,再用对茶多酚有更好选择性的溶剂进行萃取、浓缩和干燥,即可得到茶多酚的纯品。
三、实验仪器:
电动搅拌器、离心机、pH试纸、真空干燥箱、抽虑瓶、旋转蒸发仪、真空泵、天平、紫外分光光度计、容量瓶、烧杯、量筒等。
四、实验试剂及材料:
氯化钠、碳酸氢钠、柠檬酸、硫酸铝、盐酸、亚硫酸氢钠、乙酸乙酯、维生素C(抗坏血酸)、磷酸氢二钠、磷酸二氢钾、硫酸亚铁、酒石酸钾钠、硫酸、绿茶等
五、实验内容及步骤:
1.浸提
1.1 预处理:粉碎干茶叶;粉碎的目的是与液体的接触面增大,使提取率增高;
1.2 提取:准确称取经过预处理的干茶叶末10. 00g,按照单因素实验的料液比、浸提温度、浸提时间分别搅拌浸提。
过滤(用抽滤的方法)得到茶多酚提取液。
用附一的方法测提取液中的茶多酚含量。
单因素实验步骤:
(1)将称取得10.00g茶叶末置于500ml烧杯中,加入200mL蒸馏水,
在85℃下,分别提取0.5h、0.75h、1.0h、1.25h、1.5h,测提取液的吸光度,绘制曲线图,找出最佳提取时间。
(2)称取得10.00g茶叶末置于500ml烧杯中,加入200mL蒸馏水,在所测得的最佳提取时间下,分别在75℃、80℃、85℃、90℃、95℃下浸提,测提取液的吸光度,绘制曲线,找出最佳提取温度。
(3)在上述的最佳提取温度,最佳提取时间下,分别用1:10、1:15、1:20、1:25、1:30的料液比浸提,绘制提取液的吸光度曲线,找出最佳料液比。
单因素:
①料液比(g/L):1:10 1:15 1:20 1:25 1:30
②浸提温度(℃):75 80 85 90 95
③浸提时间(h):0.5 0.75 1.0 1.25 1.5
取单因素实验的每个因素的最佳范围内的值,做三因素三水平的正交实验。
实验结果记录在附五的实验记录表格中。
通过对正交实验进行极差分析后选出最优组合,进行下一步实验。
2.盐析
加氯化钠于茶叶浸提液中,质量分数为2-6%,静置0.5-1.5h 后过滤(可用抽滤或者离心的方式)。
3.沉淀
在上述滤液中加入茶叶重量2%~5%的NaHSO3,然后加入茶叶重量20%的硫酸铝饱和水溶液,加热至70℃~80℃,用15%NaHCO3溶液在快速搅拌下调节pH至5~6,此时有大量沉淀析出,沉淀自然沉降一段时间后过滤,最后用等体积70℃热水洗涤沉淀三次。
4.酸溶
将沉淀在快速搅拌下放入到一定料酸比体积下的pH=2.5~4.5的硫酸水溶液中溶解沉淀,控制酸转溶液的pH、酸溶时间,少量胶状沉淀经抽提去除。
用附一的方法测酸转溶液中茶多酚的含量
单因素实验步骤:
(1)将上一步骤所得的沉淀放入有40mL、pH=3.0的硫酸水溶的烧杯中,溶解,分别溶解40min、45min、50min、55min、60min,离心除去沉淀,测酸转溶液的吸光度,绘制曲线,找出最佳酸转时间。
(2)取上一步骤所得的沉淀放入有40mL硫酸水溶液的烧杯中,控制硫酸的pH为2.5、3.0、3.、4.0、4.5,在(1)的最佳酸转时间下,溶解,离心去除沉淀,测酸转溶液的吸光度,绘制曲线,找出最佳酸转浓度。
(3)取沉淀置于有20mL、30mL、40mL、50mL、60mL硫酸水溶液的烧杯中,在上述的最佳酸转浓度、最佳酸转时间下,溶解,离心去除沉淀,测酸转溶液的吸光度,绘制曲线,找出最佳酸浓度。
单因素:
①酸浓度(pH):2.5 3.0 3.5 4.0 4.5
②料酸比(g/mL):1:2 1:3 1:4 1:5 1:6
③酸转时间(min):40 45 50 55 60
三因素(酸浓度;料酸比;酸转时间)
取单因素实验的每个因素的最佳范围内的值,做三因素三水平的正交实验。
实验结果记录在附六的实验记录表格中。
通过对正交实验进行极差分析后选出最优组合,进行下一步实验。
5.萃取
加入茶叶重量2%-5%的NaHSO3至酸转溶液中,然后用体积0.3-1.5倍的乙酸乙酯萃取1-5次,每次萃取时间2-10min,合并萃取液。
测萃余相体积,并取样分析计算萃余相中茶多酚的总量,计算茶多酚的萃取率。
6.洗涤
加入茶叶重量1-3%的维生素C至萃取液体积0.4倍的水中,用柠檬酸调节水溶液的pH=2.5-3.0,等分成2份对乙酸乙酯萃取液洗涤两次。
7.蒸发浓缩
将洗涤后的乙酸乙酯相在50~70℃下真空蒸发回收乙酸乙酯,待浓缩成膏状物时,加入膏状物2倍体积的无水乙醇洗涤挂在壁上的物料,继续浓缩成稠的膏状物。
计算其中茶多酚的含量。
六、实验注意事项:
1.茶多酚易氧化,分离过程中注意避免高温,过酸或过碱并尽量缩短提取时间。
2.沉淀完全后应尽快抽提滤出沉淀,酸溶过程一定要充分,控制好溶液pH。
七、思考题:
通过对本工艺的实验结果进行分析,讨论分析哪些因素影响茶多
酚产品的产率?怎样影响的?应如何控制?
附一:提取过程中茶多酚的分析测定方法(定量)
准确吸取待测溶液1ml,将其稀释1~25倍(稀释成15倍),再从稀释液中准确吸取1ml,注入25ml的容量瓶中,加水4ml和酒石酸亚铁溶液5ml,充分混合,再加pH=7.5的磷酸盐缓冲溶液至刻度,用1cm比色杯,在波长540nm处,以试剂空白液作参比,测定吸光度。
计算公式:茶多酚(g/ml)=1.957AX/500
A:吸光度 X:稀释倍数。
1)酒石酸亚铁溶液
1g硫酸亚铁和5g酒石酸钾钠用水溶解并定容至至1L,放置过夜后使用。
2)pH=7.5的磷酸二氢钾缓冲液
A液:称取磷酸氢二纳23.877g,溶解并定容至至1L;
B液:称取经110度烘干2h的磷酸二氢钾9.078g,加水溶解并定容至至1L
A液85ml和B液15ml混匀即可。
附二:计算项目:
1)浸提液中茶多酚的总量及茶多酚的浸提率计算
浸提液中茶多酚的总量(g)=浸提液中茶多酚的含量(g/ml)×浸提液体积(ml)
茶多酚的浸提率=[浸提液中茶多酚的总量(g)/原料茶叶末中茶多酚的总量(g)]×100%
2)经过盐析、沉淀及酸溶后茶多酚的总量和回收率计算
酸转溶液中茶多酚的总量(g)=酸转溶液中茶多酚的含量
(g/ml)×酸转溶液的体积(ml)
酸转溶液中茶多酚的回收率=[酸转溶液中茶多酚的总量(g)/浸提液中茶多酚的总量(g)]×100%
3)萃余相中茶多酚的总量和茶多酚的萃取率计算
萃余相中茶多酚的总量(g)=萃余相中茶多酚的含量(g/ml)×萃余相溶液的体积(ml)
茶多酚的萃取率=100%×[酸转溶液中茶多酚的总量(g)-萃余相中茶多酚的总量(g)] /酸转溶液中茶多酚的总量(g)
4)茶多酚的最终得率计算
100%×[酸转溶液中茶多酚的总量(g)-萃余相中茶多酚的总量(g)]/原料茶叶的重量
附四:
附五:
附六:
料液比g/ml 1:10 1:15 1:20 1:25 1:30 吸光度0.189 0.172 0.162 0.103 0.106 茶多酚含量(g) 0.222 0.303 0.38 0.302 0.373
浸提温度℃50 60 70 80 90 吸光度0.084 0.092 0.124 0.251 0.185
浸提时间min 20 30 40 50 60
吸光度0.098 0.118 0.181 0.185 0.184
酸浓度mol/L 2 3 4 5 6 吸光度0.13 0.141 0.147 0.137 0.122
料酸比g/mL 1:10 1:15 1:20 1:25 1:30 吸光度0.186 0.206 0.107 0.121 0.116 茶多酚含量(g) 0.0546 0.0819 0.063 0.089 0.102
酸转时间min 5 10 15 20 25
吸光度0.098 0.138 0.154 0.11 0.123
实验号 A B C D 茶多酚含量酸浓度料酸比酸转时间空列(g)
实验1 1 1 1 0.00657552 实验2 1 2 2 0.00146775 实验3 1 3 3 0.0070452 实验4 2 1 2 0.00504906 实验5 2 2 3 0.0017613 实验6 2 3 1 0.0105678 实验7 3 1 3 0.0017613 实验8 3 2 1 0.007485525 实验9 3 3 2 0.00598842 K10.005 0.004 0.008
K20.006 0.004 0.004
K30.005 0.008 0.004
R 0.001 0.004 0.004。
