大学化学期末试卷
太原理工大学《有机化学》2020-2021学年第一学期期末试卷
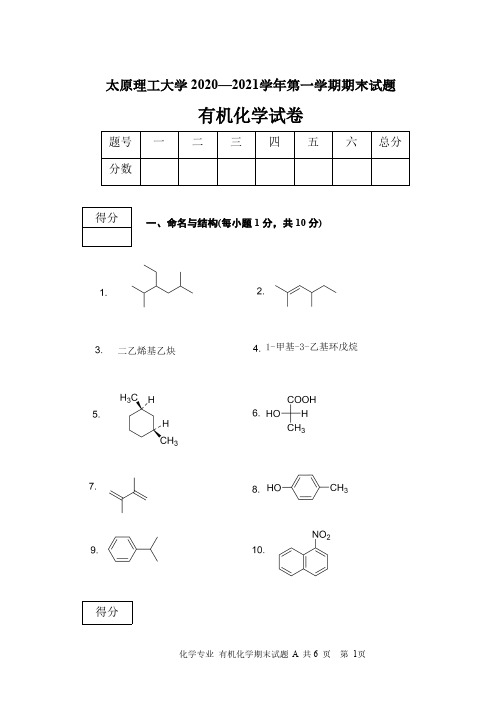
题太原理工大学2020—2021学年第一学期期末试题有机化学试卷号一二三四五六总分分数一、命名与结构(每小题1分,共10分)得分得分二、选择题(每小题2分,共20分)123456789101.烷烃在卤代反应中,不同氢的活性次序是()。
A.3。
H>2。
H>1。
HB.1。
H>2。
H>3。
HC.活性次序相同D.不能卤代2.下列烯烃相对最稳定的是()。
3.下列碳正离子稳定性最大的是()。
4.傅克酰基化反应中,常用的酰基化剂是()。
A卤代烃B烯烃和醇C酰卤D酸酐5.下列化合物中,具有手性碳的是()。
A.CH3CH2CHBrCH3B.(CH3)2CHCHBrCH(CH3)2C.CH3CH2CHBrCH2CH3D.CH3CH2CBr2CH36.下列两个化合物属于()。
A对映体B非对映体C同一化合物D顺反异构体7.含有n个不相同的手性碳,有多少个旋光异构体()。
A2n个B2n-1个C2个D比2n个少8.顺-1-甲基-4-异丙基环己烷的优势构象是()9.进行SN1反应速率最快的是()。
A.2-环戊基-2-溴丁烷B1-环戊基-1-溴丙烷C.2-环戊基-1-溴丁烷D.溴甲基环戊烷10.下列四种自由基,稳定性最强的是()。
得分三、完成下列反应(每空2分,共30分)四、区别下列各组化合物(每小题5分,共15分)1.2-甲基丁烷3-甲基-1-丁烯3-甲基-1-丁炔2.3-溴环己烯氯代环己烷碘代环己烷3.1-丁醇2-丁醇2-甲基-2-丙醇五、简答及合成题(每小题5分,共15分)1.不对称烯烃和卤化氢加成时符合马氏规则,什么是马氏规则?举例说明。
得分得分2.由3.以1-溴丁烷为原料合成戊酸。
六、推测结构(共10分)分子式为C 9H 12,,的芳香烃A,用酸性高锰酸钾氧化后,得到二元酸。
将A 进行硝化,只得到两种一硝基产物。
试推测A 的结构式。
并写出各步反应式。
得分。
赣南师范大学无机化学期末考试试卷

赣南师范大学无机化学期末考试试卷一、单选(共40小题,每题2分,共80分。
)(题下选项可能多个正确,只能选择其中最佳的一项。
)1.下列溶液中与血浆等渗的是:() [单选题] *A.90g/L的NaCl溶液B.9g/L的NaCl溶液(正确答案)C.100g/L的葡萄糖溶液D.50g/L的NaHCO3溶液E.20g/L的乳酸钠溶液2.下列溶液能使红细胞发生皱缩的是:() [单选题] *A.1.5g/L的NaHCO3溶液B.1.0 g/L的NaCl溶液C.9g/L的NaCl溶液D.100g/L的葡萄糖溶液(正确答案)E.20g/L的乳酸钠溶液3.欲使半透膜两侧的溶液不发生渗透现象的条件是:() [单选题] *A.两溶液酸度相等B.两溶液体积相等C.两溶液的物质的量浓度相等D.两溶液的渗透浓度相等(正确答案)E.两溶液温度一致4.配制300ml、0.10mol/L的NaOH溶液,需要称取固体NaOH(M=40)的质量为:() [单选题] *A.1.2g(正确答案)B.1.2mgC.4.0gD.4.0mgE.40g5.在下列单位中,哪一个是物质的量浓度的单位:() [单选题] *A.g·LB.g·molC.g·mLD.mol·L(正确答案)E.16.对于物质的体积分数,下列表示正确的是:() [单选题] *A.φ=VB/V(正确答案)B.ρ=mB/VC.wB=mB/mD.CB= nB/VE.E.xB=mB/M7.在生活中,常用75℅酒精消毒,这个浓度是指:() [单选题] *A.物质的量浓度B.质量浓度C.体积分数(正确答案)D.质量分数E.摩尔质量浓度8.溶液、胶体和悬浊液这三种分散系的根本区别是() [单选题] *A.是否是大分子或离子的聚集体B.能否透过滤纸或半透膜C.是否均匀、稳定、透明D.分散质微粒直径的大小(正确答案)E.没有区别9.胶粒稳定的主要原因是:() [单选题] *A.布朗运动B.胶粒带电(正确答案)C.溶剂化膜D.丁达尔现象E.渗透现象10.某可逆反应的正反应为吸热反应,欲使平衡向逆反应方向移动,可采取的措施是:() [单选题] *A.升高温度B.降低温度(正确答案)C.加催化剂D.加压E.减压11.有关催化剂的叙述不正确的是() [单选题] *A.能改变化学反应的历程B.能降低反应的活化能C.能使不反应的物质相互发生反应(正确答案)D.反应前后质量没有发生变化E.催化作用是化学作用12.增加气体反应物的压强能加快化学反应速率的原因是() [单选题] *A.增加了反应体系内分子总数B.增加了反应体系内活化分子数C.降低了化学反应的活化能D.增加了单位体积的活化分子数(正确答案)E.减少了单位体积的活化分子数13.一些药物需要保存在冰箱中,以防其变质,其主要作用是() [单选题] *A.避免与空气接触B.保持药物干燥C.避免药物受光照D.降低温度,减缓药物变质的反应速率(正确答案)E.以上都不对14.若用NH3和HCl来配置缓冲溶液,缓冲溶液的抗碱成分是:() [单选题] *B.HClC.NH4Cl(正确答案)D.NH3E.OH-15.人体血液中最重要的缓冲对的抗酸成分是:() [单选题] *A.H3PO4B.H2PO4-C.HCO3-(正确答案)D.H2CO3E.H2O16.正常人血浆的pH范围是:() [单选题] *A.7~8B.7~7.5C.7.5~8D.7.45~7.55E.7.35~7.45(正确答案)17.下列化合物中,属于两性物质的是:() [单选题] *A.HClB.NaOHC.H2O(正确答案)D.NH4Cl18.根据酸碱质子理论,下列叙述不正确的是:() [单选题] *A.H2CO3和CO32-不是共轭酸碱对B.酸越强,其共轭碱也越强(正确答案)C.酸失去质子转变成共轭碱D.酸碱反应的实质是质子的转移E.碱得到质子生成其共轭酸19.当pH=4的时候,则 [H+]的浓度为:() [单选题] *A.5B.104C.10-4(正确答案)D.4E.1020.下列酸中,属于一元弱酸的是:() [单选题] *A.HAc(正确答案)B.H2CO3C.H3PO4D.H3BO3E.H2SO321.同离子效应将使弱电解质的电离平衡:() [单选题] *A.左移(正确答案)C.不移动D.无法确定E.以上都对22.室温下,1.0mol/L氨水中,水的离子积常数为() [单选题] *A.1.0×10-10B.1.0×10-4C.1.0×10-14(正确答案)D.1.0×10-7E.2.0×10-723.下列溶液中酸性最强的是() [单选题] *A.pH=5B.pH=2C.[H+]=0.1mol/L(正确答案)D.[OH-]=10-2mol/LE.[OH-]=10-7mol/L24.在含有CrO42-和Cl-的混合溶液中加入AgNO3溶液,先有白色沉淀生产,后有砖红色沉淀生成,这种现象称为:() [单选题] *A.分步沉淀(正确答案)B.沉淀的生成C.沉淀是转化D.沉淀的溶解E.以上都不对25.在AgCl饱和溶液中加入NaCl,使其溶解度减小的现象称为() [单选题] *A.盐效应B.同离子效应(正确答案)C.缓冲效应D.配位效应E.沉淀效应26.沉淀生成的必要条件是() [单选题] *A.Ip>Ksp(正确答案)B.加入强电解质C.加入与难溶强电解质具有相同离子的盐D.Ip<KspE.加入氧化剂或还原剂27.下列化合物中,S的氧化数为+4的是:() [单选题] *A.H2SB.Na2S2O3C.Na2SO3(正确答案)D.Na2SO4E.S28.在原电池中, 发生氧化反应的是:() [单选题] *A.正极B.负极(正确答案)C.正极和负极D.正极或负极E.以上都对29.13号元素在元素周期表的位置是:() [单选题] *A.4周期ⅠA族B.4周期ⅡA族C.3周期ⅢA族(正确答案)D.4周期ⅥA族E.4周期ⅢA族30.某元素处在元素周期表的第三周期,该元素原子的电子层数为:() [单选题] *A.1B.2C.3(正确答案)D.4E.531.水的沸点“反常”,这是由于分子间存在着:() [单选题] *A.范德华力B.共价键C.氢键(正确答案)D.离子键E.E.配位键32.配合物中特征化学键是:() [单选题] *A.离子键B.共价键C.配位键(正确答案)D.氢键E.化学键33.下列盐中,难溶于水的是:() [单选题] *A.Ca(HCO3)2B.CaCO3(正确答案)C.Na2CO3D.(NH4)2CO3E.NH4Cl34.下列物质中,不能用做消毒剂的是:() [单选题] *A.氯水B.臭氧C.双氧水D.蒸馏水(正确答案)E.都不能做消毒剂35.H2O2不具备的性质是:() [单选题] *A.氧化性B.还原性C.不稳定性D.酸性E.既没有氧化性也没有还原性(正确答案)36.下列物质中与Cl2 作用能生成漂白粉的是:() [单选题] *A.CaCO3B.CaSO4C.Mg(OH) 2D.Ca(OH) 2(正确答案)E.MgSO437.下列化学药品在实验室常作氧化剂的是:() [单选题] *A.硫酸铜B.活泼金属C.高锰酸钾(正确答案)D.氯化钠E.水38.用自来水养金鱼时,通常先将自来水日晒段时间后,再注入鱼缸,其目的是()[单选题] *A.利用紫外线杀死水中的细菌B.提高水温,有利于金鱼生长C.增加水中氧气的含量D.促进水中的次氯酸分解(正确答案)E.以上说法均不正确39.下列关于Al(OH) 3性质的叙述错误的是() [单选题] *A.Al(OH) 3是两性的,其酸性与碱性相当B.可溶于酸C.Al(OH) 3是两性的,其酸性弱于碱性(正确答案)D.可溶于过量的强碱E.Al(OH) 3是碱性的40.参与构成人体和维持机体正常生理功能的元素称为:() [单选题] *A.人体微量元素B.人体常量元素C.人体必需元素(正确答案)D.人体有益元素E.人体有害元素二、是非(共10小题,每题1分,共10分。
(完整版)大学无机化学期末试卷及答案

《无机化学》试题学号:姓名:座号:系别:年级:专业:总分合计人:复核人:一、单项选择题(在每小题列出的四个选项中只有一个选项是符合题目要求的,请选出正确选项并在“答题卡”的相应位置上涂黑。
多涂、少涂、错误均无分。
每小题1分,共40分)1、对于Zn2+/Zn电对,增大Zn2+的浓度,则其标准电极电势将()A 增大B 减小C 不变D 无法判断2、Cu2+离子的外层电子构型为()A 8eB 18e型C 18+2eD 9~17e型3、设氨水的解离平衡常数为K。
浓度为m mol·L-1的氨水溶液,b若将其用水稀释一倍,则溶液中OH-的浓度(mol·L-1)为()Am 21 B θb K m ⋅21 C 2/m K b ⋅θD 2m4、已知θsp K (Ag 3PO 4) = 1.4×10-16,其溶解度为 ( )A 1.1×10-4mol·L -1;B 4.8×10-5mol·L -1;C 1.2×10-8mol·L -1;D 8.3×10-5mol·L -15、下列各组物质,能自发发生反应的是 ( )A Cu 、Cu 2+;B Cr 2O 72-、Cr 3+;C MnO 2、Mn 2+;D SnCl 4、Sn 6、3d轨道的磁量子数可能是( )A 1,2,3B 0,1,2C 0,±1D 0, ±1, ±27、下列各分子中,以sp 3不等性杂化轨道成键的是 ( )A BeCl 2B PCl 3C BF 3D SiH 48、熔化下列晶体时,只需克服色散力的是 ( )A HFB AgC KFD CO 29.已知V E A /θ:Cr 2O 72- +1.36 Cr 3+ -0.41 Cr 2+ -0.86 Cr ,则判断发生歧化反应的是 ( )A 都不能B Cr 2O 72-C Cr 3+D Cr 2+ 10.下列各物质中,熔点最高的是()A K2OB MgOC CaOD Na2O11稀溶液依数性的本质是()A. 渗透压B. 沸点升高C. 蒸汽压下降D. 凝固点降低12要降低反应的活化能,可以采取的手段是( )A. 升高温度B. 降低温度C. 移去产物D. 使用催化剂13如果一个反应的吉布斯自由能变为零,则反应( )A. 能自发进行B. 是吸热反应C. 是放热反应D. 处于平衡状态14.反应A + B C,焓变小于零,若温度升高10℃,其结果是( )A.对反应没有影响B. 使平衡常数增大一倍C.不改变反应速率D.使平衡常数减小15.在HAc-NaAc缓冲溶液中,若[HAc]>[NaAc],则该缓冲溶液()A.抗酸能力强于抗碱能力B.抗酸能力弱于抗碱能力C.抗酸能力等于抗碱能力D.无法判断16.在室温下,0.0001mol.L-1NH3水溶液中的pKw是()A. 14B. 10C.4D.817.按酸碱质子理论考虑,在水溶液中既可作酸亦可作碱的物质是( )A.Cl-B. NH4+C. HCO3-D. H3O+18.AgCl在纯水中溶解度比0.10 mol·L-1 NaCl溶液中(AgCl: K sp = 1.77×10-10 ) ( )A.大B.小C.一样大D.无法判断19.CaSO4在0.1mol.L-1NaNO3溶液中的溶解度比在纯水中( )A.略有减小B.略有增加C.相等D.无法判断20.已知:Ksp,AgCl=1.8×10-10,Ksp,Ag2CrO4=1.1×10-12在等浓度的CrO42-和Cl-的混合溶液中,逐滴加入AgNO3时:()A.先产生AgCl↓B.先产生Ag2CrO4↓C.两种同时沉淀D.两者都不沉淀21.在酸性溶液中,当适量的KMnO4与Na2SO3反应时出现的现象是()A. 棕色沉淀B. 紫色褪去C.绿色溶液D.都不对22.下列电对中值最大的是( )A. (Ag+/Ag) B. (Ag(NH3)2+/Ag) C. (AgCl /Ag) D. (AgI/Ag)23.当pH = 10 时,氢电极的电极电势是- ( )A.-0.59 VB. -0.30 VC. 0.30 VD. 0.59 V24.4s电子的径向分布图有: ( )A.3个峰B.2个峰C.4个峰D.1个峰25.属于主量子数n= 3 的一个电子的四个量子数n,l,m,m s 取值正确的是( )A. 3,2,1,0B.3,2, -1,C. 3,3,1,D. 3,1, 2,26.量子力学中所说的原子轨道是指( )A.波函数ψn,l,m,ms B.电子云C.波函数ψn,l,m D.概率密度27.ψ(4,2,1)代表简并轨道中的一个轨道是( )A.4p轨道B.4d轨道C.4s轨道D.4f轨道28.下列轨道上的电子,在xy平面上的电子云密度为零的是()A.3S B.3P x C.3Pz D.3Py29.某元素原子基态的电子构型为[Ar] 3d 8 4s2 ,它在元素周期表中的位置是()A.s区B.p区C.d区D.f区30. Ag的价电子层结构是()A.3d 10 4s1 B.3d 9 4s2C.4d 10 5s1D.4d 10 4s2 31下列分子和离子中中心原子成键轨道不是sp2 杂化的是( )A.BF3 B.HCHO C.C2H4 D.NH332按分子轨道理论,O2的键级是-( )A.1 B.1C.2D.233.下列各分子中,偶极矩为零的分子为( )A.H2 O B.NH3 C.BF3 D.HCl34.下列化合物中没有氢键的是( )A.C2H4B.NH3C.HFD.H2O35.NH3中N原子采取的杂化方式是:()A. SP2B. SP3等性C. SP2dD. SP3不等性36.[Ni(en)3]2+离子中镍的价态和配位数是( )A .+2,3B . +3,6C . +2,6D . +3,3 37. Fe(Ⅲ)形成的配位数为 6 的外轨配合物中,Fe 3+离子接受孤对电子的空轨道是 ( )A .d 2sp 3B . sp 3d 2C .p 3d 3D . sd 5 38.能够用于鉴定Fe 3+的特效试剂有( )A.KSCNB. HClC. 邻二氮菲D. 赤血盐39.在热碱性溶液中,次氯酸根离子不稳定,它的分解产物是 ( )A .Cl -和Cl 2 B .Cl -和ClO 3-C .Cl -和ClO 2-D .Cl -和ClO 4- 40.在温度T 和压力p 时理想气体反应:(ⅰ)2H 2O(g)=2H 2(g)+O 2(g)θ1K ;(ⅱ)CO 2(g)=CO(g)+1/2O 2(g)θ2K 则反应:(ⅲ)CO(g)+H 2O(g)=CO 2(g)+H 2(g)的θ3K 应为( ) A θθθ213/K K K = , B θθθ213K K K ⋅= ,C θθθ213/K K K =,D θ3K =θ1K +θ2K二、判断题(判断正确答案,选项并在“答题卡”的相应位置填涂,认为正确的涂“A”错误的涂“B ”。
《大学化学》期末考试试卷附答案

《大学化学》期末考试试卷附答案一、选择题(共15小题,每小题3分,共45分)1、某反应的ΔrHmΘ<0 ,当温度升高时,其平衡常数的数值将()。
A、增大B、不变C、减小D、先增大后减小2、当主量子数n=3时,则角量子数l的取值为()。
A、1、2、B、 0、1、2C、0、1D、0、±1、3、某温度下,反应2NO(g)+O2(g)=2NO2(g)达到平衡,是因为()。
A、反应已停止B、反应物中的一种已消耗完C、正逆反应的速率相等D、反应物均已消耗完毕4、下列化合物晶体中,既存在离子键又存在共价键的是()。
A、H2OB、 NaBrC、 CH3OHD、Na2O25、蔗糖的凝固点为()。
A、0℃B、高于0℃C、低于0℃D、无法判断6、已知某元素核外电子排布式为1s22s22p2,该元素在周期表中所属的分区为()。
A、 s区B、d区C、 f区D、 p区7、质量作用定律只适用于()。
A、实际上能进行的反应B、一步完成的简单反应C、化学反应方程式中反应物和产物的化学式系数均为1的反应D、已进行完的反应8、对于反应 Cr2O72- + 6Fe2+ + 14H+ = 2Cr3+ + 6Fe3+ + 7H2O,其ΔrGm= –nFE,式中n等于()。
A、1B、6C、3D、129、下列物质中熔点最高的是()。
A、SiB、CO2C、ZnSD、Fe3C10、下列叙述中错误的是( )。
A、原电池的反应是氧化还原反应B、原电池的能量变化是由化学能变为电能C、原电池的能量变化是由电能变为化学能D、原电池的负极发生氧化反应11、某元素原子的外层电子构型为3s23p3原子中未成对电子数为()。
A、1B、2C、3D、012、等温等压下且不做非体积功条件下,反应自发进行的判据是()。
A、ΔHΘ<0B、ΔSΘ<0C、ΔG<0D、ΔfHmΘ<013、水具有反常的沸点,是因为分子间存在()。
A、色散力B、诱导力C、取向力D、氢键14、欲配制pH=5.0的缓冲溶液,则下列哪一种化合物及其盐的混合溶液合适?()。
大学化学期末考试卷(含答案)

大学化学期末考试卷学院:专业:行政班:姓名:学号:座位号:-------------------------------密封线-------------------------------一、选择题(每小题 分,共 分)、某反应的Δ❒☟❍Θ ,当温度升高时,其平衡常数的数值将( )。
✌、 增大 、不变 、减小 、先增大后减小、当主量子数⏹ 时,则角量子数●的取值为( )。
✌、 、 、 、 、 、 、 、 、 、± 、、某温度下,反应 ☠☎♑✆ ☎♑✆☠ ☎♑✆达到平衡,是因为( )。
✌、反应已停止 、反应物中的一种已消耗完、正逆反应的速率相等 、反应物均已消耗完毕 、下列化合物晶体中,既存在离子键又存在共价键的是( )。
✌、☟ 、 ☠♋❒ 、 ☟ ☟ 、☠♋ 、蔗糖的凝固点为( )。
✌、 ℃ 、高于 ℃ 、低于 ℃ 、无法判断 、已知某元素核外电子排布式为 ♦ ♦ ☐ ,该元素在周期表中所属的分区为( )。
✌、 ♦区 、♎区 、 ♐区 、 ☐区、质量作用定律只适用于( )。
✌、实际上能进行的反应 、一步完成的简单反应 、化学反应方程式中反应物和产物的化学式系数均为 的反应、已进行完的反应、对于反应❒ ☞♏ ☟ ❒ ☞♏ ☟ ,其Δ❒☝❍ ⏹☞☜,式中⏹等于( )。
✌、 、 、 、、下列物质中熔点最高的是( )。
✌、 ♓ 、 、☪⏹ 、☞♏、下列叙述中错误的是☎ ✆。
✌、 原电池的反应是氧化还原反应、 原电池的能量变化是由化学能变为电能、 原电池的能量变化是由电能变为化学能、 原电池的负极发生氧化反应、某元素原子的外层电子构型为 ♦ ☐ 原子中未成对电子数为( )。
✌、 、 、 、、等温等压下且不做非体积功条件下,反应自发进行的判据是( )。
✌、Δ☟Θ 、Δ Θ 、Δ☝ 、Δ♐☟❍Θ 、水具有反常的沸点,是因为分子间存在( )。
大学无机化学期末试卷及答案.doc

《无机化学》试题学号:姓名:座号:系别:年级:专业:总分合计人:复核人:一、单项选择题(在每小题列出的四个选项中只有一个选项是符合题目要求的,请选出正确选项并在“答题卡”的相应位置上涂黑。
多涂、少涂、错误均无分。
每小题1分,共40分)1、对于Zn2+/Zn电对,增大Zn2+的浓度,则其标准电极电势将()A 增大B 减小C 不变D 无法判断2、Cu2+离子的外层电子构型为()A 8eB 18e型C 18+2eD 9~17e型3、设氨水的解离平衡常数为K。
浓度为m mol·L-1的氨水溶液,b若将其用水稀释一倍,则溶液中OH-的浓度(mol·L-1)为()Am 21 B θb K m ⋅21 C 2/m K b ⋅θD 2m4、已知θsp K (Ag 3PO 4) = 1.4×10-16,其溶解度为 ( )A 1.1×10-4mol·L -1;B 4.8×10-5mol·L -1;C 1.2×10-8mol·L -1;D 8.3×10-5mol·L -15、下列各组物质,能自发发生反应的是 ( )A Cu 、Cu 2+;B Cr 2O 72-、Cr 3+;C MnO 2、Mn 2+;D SnCl 4、Sn 6、3d轨道的磁量子数可能是( )A 1,2,3B 0,1,2C 0,±1D 0, ±1, ±27、下列各分子中,以sp 3不等性杂化轨道成键的是 ( )A BeCl 2B PCl 3C BF 3D SiH 48、熔化下列晶体时,只需克服色散力的是 ( )A HFB AgC KFD CO 29.已知V E A /θ:Cr 2O 72- +1.36 Cr 3+ -0.41 Cr 2+ -0.86 Cr ,则判断发生歧化反应的是 ( )A 都不能B Cr 2O 72-C Cr 3+D Cr 2+ 10.下列各物质中,熔点最高的是()A K2OB MgOC CaOD Na2O11稀溶液依数性的本质是()A. 渗透压B. 沸点升高C. 蒸汽压下降D. 凝固点降低12要降低反应的活化能,可以采取的手段是( )A. 升高温度B. 降低温度C. 移去产物D. 使用催化剂13如果一个反应的吉布斯自由能变为零,则反应( )A. 能自发进行B. 是吸热反应C. 是放热反应D. 处于平衡状态14.反应A + B C,焓变小于零,若温度升高10℃,其结果是( )A.对反应没有影响B. 使平衡常数增大一倍C.不改变反应速率D.使平衡常数减小15.在HAc-NaAc缓冲溶液中,若[HAc]>[NaAc],则该缓冲溶液()A.抗酸能力强于抗碱能力B.抗酸能力弱于抗碱能力C.抗酸能力等于抗碱能力D.无法判断16.在室温下,0.0001mol.L-1NH3水溶液中的pKw是()A. 14B. 10C.4D.817.按酸碱质子理论考虑,在水溶液中既可作酸亦可作碱的物质是( )A.Cl-B. NH4+C. HCO3-D. H3O+18.AgCl在纯水中溶解度比0.10 mol·L-1 NaCl溶液中(AgCl: K sp = 1.77×10-10 ) ( )A.大B.小C.一样大D.无法判断19.CaSO4在0.1mol.L-1NaNO3溶液中的溶解度比在纯水中( )A.略有减小B.略有增加C.相等D.无法判断20.已知:Ksp,AgCl=1.8×10-10,Ksp,Ag2CrO4=1.1×10-12在等浓度的CrO42-和Cl-的混合溶液中,逐滴加入AgNO3时:()A.先产生AgCl↓B.先产生Ag2CrO4↓C.两种同时沉淀D.两者都不沉淀21.在酸性溶液中,当适量的KMnO4与Na2SO3反应时出现的现象是()A. 棕色沉淀B. 紫色褪去C.绿色溶液D.都不对22.下列电对中值最大的是( )A. (Ag+/Ag) B. (Ag(NH3)2+/Ag) C. (AgCl /Ag) D. (AgI/Ag)23.当pH = 10 时,氢电极的电极电势是- ( )A.-0.59 VB. -0.30 VC. 0.30 VD. 0.59 V24.4s电子的径向分布图有: ( )A.3个峰B.2个峰C.4个峰D.1个峰25.属于主量子数n= 3 的一个电子的四个量子数n,l,m,m s 取值正确的是( )A. 3,2,1,0B.3,2, -1,C. 3,3,1,D. 3,1, 2,26.量子力学中所说的原子轨道是指( )A.波函数ψn,l,m,ms B.电子云C.波函数ψn,l,m D.概率密度27.ψ(4,2,1)代表简并轨道中的一个轨道是( )A.4p轨道B.4d轨道C.4s轨道D.4f轨道28.下列轨道上的电子,在xy平面上的电子云密度为零的是()A.3S B.3P x C.3Pz D.3Py29.某元素原子基态的电子构型为[Ar] 3d 8 4s2 ,它在元素周期表中的位置是()A.s区B.p区C.d区D.f区30. Ag的价电子层结构是()A.3d 10 4s1 B.3d 9 4s2C.4d 10 5s1D.4d 10 4s2 31下列分子和离子中中心原子成键轨道不是sp2 杂化的是( )A.BF3 B.HCHO C.C2H4 D.NH332按分子轨道理论,O2的键级是-( )A.1 B.1C.2D.233.下列各分子中,偶极矩为零的分子为( )A.H2 O B.NH3 C.BF3 D.HCl34.下列化合物中没有氢键的是( )A.C2H4B.NH3C.HFD.H2O35.NH3中N原子采取的杂化方式是:()A. SP2B. SP3等性C. SP2dD. SP3不等性36.[Ni(en)3]2+离子中镍的价态和配位数是( )A .+2,3B . +3,6C . +2,6D . +3,3 37. Fe(Ⅲ)形成的配位数为 6 的外轨配合物中,Fe 3+离子接受孤对电子的空轨道是 ( )A .d 2sp 3B . sp 3d 2C .p 3d 3D . sd 5 38.能够用于鉴定Fe 3+的特效试剂有( )A.KSCNB. HClC. 邻二氮菲D. 赤血盐39.在热碱性溶液中,次氯酸根离子不稳定,它的分解产物是 ( )A .Cl -和Cl 2 B .Cl -和ClO 3-C .Cl -和ClO 2-D .Cl -和ClO 4- 40.在温度T 和压力p 时理想气体反应:(ⅰ)2H 2O(g)=2H 2(g)+O 2(g)θ1K ;(ⅱ)CO 2(g)=CO(g)+1/2O 2(g)θ2K 则反应:(ⅲ)CO(g)+H 2O(g)=CO 2(g)+H 2(g)的θ3K 应为( ) A θθθ213/K K K = , B θθθ213K K K ⋅= ,C θθθ213/K K K =,D θ3K =θ1K +θ2K二、判断题(判断正确答案,选项并在“答题卡”的相应位置填涂,认为正确的涂“A”错误的涂“B ”。
大学有机化学期末考试原题试卷(A)

、、
、下列卤代烃与AgNO
、2-甲基氯丁烷
、3-甲基-1-丁烯
、下列物质能发生碘仿反应的是(
、乙酸B、乙醇
7、下列化合物中沸点最高的是(
、CH3CH CH3
、CH3CH OCH2CH3
8、下列各组物质中互为同分异构体的是(
七、推断结构式。
(15分)
1、化合物A分子式为C6H12O,不与托伦试剂或饱和亚硫酸氢钠反应,但能与羟胺反应,A经催化氢化得分子式C6H14O的B。
B与浓硫酸共热得分子式C6H12的C。
C经臭氧氧化再还原水解,生成分子式均为C3H6O的D和E。
D能发生碘仿反应,但不能发生银镜反应;E能发生银镜反应,但不能发生碘仿反应。
试写出A、B、C、D、E的构造式。
(不必写反应式)(9分)
2、某化合物A的分子式为C8H14O,A可迅速使溴水褪色,也能与苯肼反应生成黄色沉淀,但不能发生银镜反应。
A经酸性高锰酸钾氧化生成丙酮及另一化合物B。
B具有酸性,与NaOI反应生成碘仿和丁二酸。
试写出A、B可能的构造式。
(不必写反应式)(6分)试卷︵B ︶
第4页︵共4页︶
河南科技大学教务处。
大学有机化学期末考试原题试卷(B)
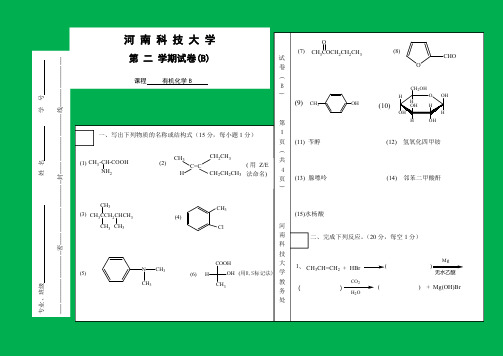
CH3
2、 CH3CH2CHCHCH3
KOH- 醇
(
)
Br
KMnO4 H+
(
)+(
C(CH3)3
3、
+ CH3Cl
无水AlCl3 (
) KMnO4 /H2SO4 (
) )
试
三、单项选择题(请把答案填入下列方格中,共 30 分,每小
卷 题 2 分)
︵1
2
3
4
5
6
7
8
9
10
B
︶ 11 12 13 14 15
14、甲苯和氯气在光照条件下的反应属于 反应历程,在 FeCl3 催化 科
下的反应属于 反应历程
技
五、简答题(每小题 5 分,共 10 分)
A、自由基取代,亲电取代 B、亲电取代,自由基取代
C、自由基取代,亲核取代 D、亲电取代,亲核取代 15、下列醇与 Lucas 试剂反应,反应速率最快的是
大 1、用简单化学方法区别下列化合物
------------------------------密-------------------------------封-----------------------------线------------------------
学号
河南科技大学
第 二 学期试卷(B)
课程 有机化学 B
O
试
(7) CH3COCH2CH2CH3
Mg
)
无水乙醚
CH3
CH3
教 务(
CO2
)
(
H2O
) + Mg(OH)Br
处
专业、班级
------------------------------密-------------------------封------------------------线---------------------------------
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
大学化学期末试卷大学化学期末试卷加答案学院________ 姓名_________ 学号_________闭卷考试时间:120分钟一、选择题(每小题分,共24分)1、某反应的ΔrHmΘ<0 ,当温度升高时,其平衡常数的数值将()。
A、增大B、不变C、减小2、当主量子数n=3时,则角量子数l的取值为()。
A、1、2、B、0、1、2C、0、1D、0、±1、3、某温度下,反应2NO(g)+O2(g)=2NO2(g)达到平衡,是因为()。
A、反应已停止B、反应物中的一种已消耗完C、正逆反应的速率相等4、下列化合物晶体中,既存在离子键又存在共价键的是()。
A、H2OB、NaBrC、CH3OHD、Na2O25、蔗糖的凝固点为()。
A、0℃B、高于0℃C、低于0℃D、无法判断6、已知某元素核外电子排布式为1s22s22p2,该元素在周期表中所属的分区为()。
A、s区B、d区C、f区D、p区7、质量作用定律只适用于()A、实际上能进行的反应B、一步完成的简单反应C、化学反应方程式中反应物和产物的化学式系数均为1的反应8、对于反应Cr2O72- + 6Fe2+ + 14H+ = 2Cr3+ + 6Fe3+ + 7H2O,其ΔrGm= –nFE,式中n等于()。
A、1B、6C、3D、129、下列物质中熔点最高的是()A、SiB、CO2C、ZnSD、Fe3C10、下列叙述中错误的是( )。
A、原电池的反应是氧化还原反应B、原电池的能量变化是由化学能变为电能C、原电池的能量变化是由电能变为化学能D、原电池的负极发生氧化反应11、某元素原子的外层电子构型为3s23p3原子中未成对电子数为()。
A、1C、3D、012、等温等压下且不做非体积功条件下,反应自发进行的判据是A、ΔHΘ<0B、ΔSΘ<0C、ΔG<0D、ΔfHmΘ<013、水具有反常的沸点,是因为分子间存在()。
A、色散力B、诱导力C、取向力D、氢键14、欲配制pH=的缓冲溶液,则下列哪一种化合物及其盐的混合溶液合适?()A、HF (pKa=B、CH3COOH (pKa=C、NH3·H2O (pKb=D、HCN(pKa=15、对于下列基元反应:A + 2B = C,其速率常数为k,若某个时刻(时间以s计),A的浓度为2mol/L,B的浓度为3mol/L,则反应速率v=()。
A、6k mol·L-1 ·s-1B、12k mol·L-1 ·s-1C、18k mol·L-1 ·s-1D、36k mol·L-1 ·s-116、在温度T的标准状态下,若已知反应A→2B的标准摩尔反应焓△r HΘm,1,与反应2A→C的标准摩尔反应焓△r H Θ,则反应C→4B的标准摩尔反应焓△r HΘm,3与△r HΘm,1及△r HΘm,2的关系为△rHΘm,3=()。
A、2△r HΘm,1+△r HΘm,2B、△r HΘm,1-2△r HΘm,2C、△r HΘm,1+△r HΘm,2D、2△r HΘm,1-△r HΘm,2二、填空题(21分)1、原电池(-)Pt |Fe2+(C1),Fe3+(C2)|| Fe2+(C3),Fe3+(C4)| Pt(+)负极上发生的电极反应式:____________________;正极上发生的电极:________________________。
该电池属于____________电池。
1、根据热力学第一定律,封闭体系的热力学能变化值反应的ΔU=____________。
2、决定电子运动状态的四个量子数中,__________反映了原子轨道的形状;_______反映了原子轨道的空间取向;对于自旋量子数ms,可以取的数值只能为__________________。
3、在等温等压条件下,某反应的KΘ=1,则其ΔrG mΘ的值等于_______________。
4、同离子效应能使弱电解质的解离度______________。
如HAc溶液中加入_________________或_________________(两类物质)均能起到同离子效应的作用。
5、在等温下,若化学平衡发生移动,其平衡常数___________(填减小、增大、不变)。
6、原子轨道沿两核连线以“头碰头”方式重叠形成的共价键叫_______键,以“肩并肩”方式重叠形成的共价键叫_______键。
7、根据杂化轨道理论,BF3分子中B采取_______杂化,BF3的空间构型为____________;NH3分子中N采取_________杂化, NH3的空间构型为____________。
8、已知PbI2的溶度积Ks=×10-9,则PbI2在mol/dm3Pb(NO3)2溶液中的溶解度为_________ mol/dm3。
9、已知MnO4-+8H++5e-=Mn2++4H2O,φ(MnO4-/Mn2+)=。
试根据能斯特公式确定φ(MnO4-/Mn2+)与pH的关系式是_________________________________。
10、CCl4分子与H2O分子间的相互作用力有___________________________。
三、问答题(每题6分,共计18分)1、写出7N原子、25Mn原子、20Ca2+的核外电子排布式?N:7Mn:25Ca2+202、影响化学反应速率的主要因素有哪些?质量作用定律的意义是什么?对一般的化学反应,速率方程式的反应级数能否直接根据化学反应方程式来写?为什么?3、当铜锌原电池(-)Zn |Zn2+(1mol/L) || Cu2+(1mol/L)| Cu(+)工作一段时间后,原电池的电动势是否发生变化?为什么?四、是非题(每题1分,共计7分)1、1、反应的ΔH就是反应的热效应。
()2、2、催化剂能改变反应历程,降低反应的活化能,但不能改变反应的ΔrG mΘ。
()3、3、两种分子酸HX溶液和HY溶液有同样的pH,则这两种酸的浓度相同。
()4、4、多电子原子轨道的能级只与主量子数n有关。
()5、5、电极电势的数值与电极反应的写法无关,而平衡常数的数值随反应式的写法而变。
()6、对于某一化学反应,若升高温度,其正反应速率v增加,逆反应速率v减小。
()7、在微观粒子中,只有电子具有波粒二象性。
()五、计算题(共30分)1(6分)计算下列反应的(1)ΔrHmΘ;(2) 进行1mol反应时的体积功w` 和(3)ΔrUmΘ。
R=?mol-1?K-1CH4(g) + 4 Cl2(g) = CCl4(l) + 4 HCl(g)ΔfHmΘ/kJ?mol-1 02、(6分)某温度时,和在密闭容器中进行反应生成SO3气体,测得起始时和平衡时(温度不变)系统的总压力分别为300kPa和220kPa。
试利用上述实验数据求该温度时2SO2(g) + O2(g) = 2SO3(g)的标准平衡常数和SO3的转化率。
3、(9分)已知,0.799Ag e Ag V+Θ+==,如果在溶液中加入NaCl,使产生AgCl沉淀后,溶液中的[Cl–]=1mol/L,试计算其电极电位。
4、(9分)向含有KCl、KI各·l-1的混合溶液中,逐滴加入沉淀剂AgNO3溶液,那种离子先沉淀?氯离子沉淀时溶液中碘离子的浓度是多少?已知:Ks(AgI)=×10-17 ,Ks(AgCl)=×10-10《大学化学基础》试卷2(答案)1 2 3 4 5 6 7 8C B CD C D B B9 10 11 12 13 14 15 16A C C C DBC D二、填空题(21分)1. Fe2+–e = Fe 3+、Fe 3++e = Fe2+、浓差电池2.ΔU = q+w_3. 角量子数,磁量子数,±1/24. 0 kJ/mol5. 降低,醋酸盐,强酸6. 不变7. σ键,π键8. sp2,平面三角形;不等性sp3,三角锥形9.×10-4mol/L。
10. φ(MnO4-/Mn2+)=φ(MnO4-/Mn2+)–(/5)lg[C Mn2+/(C 8H+? C MnO4-)]11.色散力、诱导力三、问答题(每题6分,共计18分)1、7N:1s22s22p3Mn:1s22s22p63s23p63d54s225Ca2+:1s22s22p63s23p6202、影响化学反应速率的主要因素有:浓度、温度、压力和催化剂。
质量作用定律的意义:对于元反应,化学反应速率与反应物的浓度(以反应方程式中反应物的化学计量系数为指数)的乘积成正比。
反应级数指反应速率方程中各反应物浓度的指数之和。
对于元反应,反应速率方程等于反应物浓度(以方程式中其系数为指数)的乘积,因此其反应级数为方程式中反应物的系数之和。
对于复杂反应,反应速率方程并不一定等于反应物浓度(以方程式中其系数为指数)的乘积,,所以反应级数不能直接根据反应方程式来写。
3、原电池的电动势会发生变化。
铜锌原电池工作一段时间后,电解质溶液中的铜离子浓度降低,锌离子浓度增大,根据能斯特公式可知,随着铜离子浓度降低,锌离子浓度增大,原电池电动势变小。
四、是非题(每题1分,共计7分)1.(×)2.(√)3.(×)4.(×)5.(√)6.(×)7.(×)五、计算题(共30分)1、(6分)ΔrH mΘ= 4×+-= kJ/molw体=– p·△V= –△nRT = –(-1)××= molΔrU mΘ=ΔrH mΘ+ w体=mol +mol= kJ/mol2、(6分)2SO2(g) + O2(g) = 2SO3(g)=300kPa起始量(mol) P总压P SO 2=300kPa×8/(8+4) =200 kPa P O 2=300kPa×4/(8+4) =100 kPa 平衡分压(Pa) 200–2x 100–x 2x P 总压=220kPa 200–2x +100–x+2x = 220 x=80kPaSO 2(g)的转化率=2×80/200=80%101.6101sp spK K Ag Cl +--??===3、(9分) 解:根据电极电位的能斯特公式100.0591lg1.6100.7990.5780.2211V ??Θ-=+=-=上面计算得到的电极电位实际上是下电对的标准电极电位。
()()AgCl s e Ag s Cl --+=+4、(9分) (1)开始沉淀时,需要的Ag +的浓度分别为:108()1.7710: 1.77100.01sp Ag Cl K AgCl AgCl C C +-Θ--?===?mol/L1715()8.5110:8.51100.01sp Ag I K AgI AgI C C +-Θ--?===?mol/L故先生成AgI 沉淀。
