大学化学试卷
大学有机化学试题1..
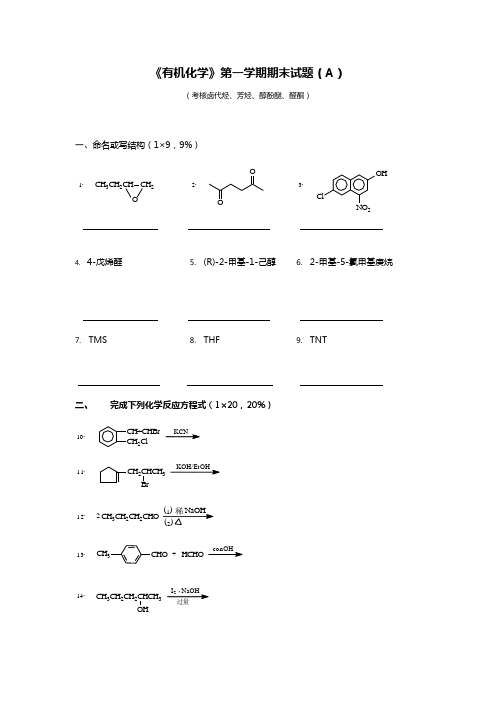
《有机化学》第一学期期末试题(A )(考核卤代烃、芳烃、醇酚醚、醛酮)一、命名或写结构(1×9,9%)CH 3CH 2CH CH 2O1.OO2.ClNO 2OH3.4. 4-戊烯醛5. (R)-2-甲基-1-己醇6. 2-甲基-5-氯甲基庚烷7. TMS8. THF9. TNT二、完成下列化学反应方程式(1×20,20%)CH=CHBr CH 2ClKCN10.CH 2CHCH 3BrKOH/EtOH11.CH 3CH 2CH 2CHO212.CHOCH 3HCHOconOH-+13.CH 3CH 2CH 2CHCH 3OHI 2 NaOH 过量14.(CH 3)2CHOHPBr 315.CH 3(CH 2)3Cl+16.AlCl 3OH OHH+17.CH 3MgBr18.HCHO 乙醚,H 3O+OPh 3P=CH 2+20.CH 3CH 2CH 2CHO21.+NaHSO 3(饱和O CO22.(CH 3)2CHMgBr23.O(1)醚(2)2+OCH 2CH=CHREt Me200C。
24.OHH 2SO 4HNO 325.HCHOHCl26.++ZnCl 2无水CH 3CH=CHCH 2CH 2CHOAg(NH 3)2+OH-27.C CH 3H 3C OHCHON H++H+28.2C 2H 5OH Odry HCl29.+三、有机理论部分(5×5,25%)30按沸点从大到小排列成序,并简要说明理由。
CH 2CH CH 2OH OH OHCH 3CH 2CH 2OH CH 3CH 2CH 2OCH 3CH 2CH CH 2OH OH OCH 3(a)(b)(c)(d)31.按羰基的活性从大到小排列成序,并简要说明理由。
CH 3CH O CH 3CCHOO CH 3CCH 2CH 3O (CH 3)3CCC(CH 3)3O(a)(b)(c)(d)32.解释:为什么化合物无论是进行S N 1还是进行S N 2反应都十分困难?33.写出反应机理CH 2CH 2ClClCH CH 3+(过量)AlCl 3无水34.写出反应机理OO四、有机结构分析部分(4×4,16%)35.用化学方法鉴别化合物C2H5Br CH3O CH2Br C2H5OHA B C36.用化学方法鉴别化合物O OH OHOHA B C D37.根据所给化学式、IR、NMR主要数据,推测化合物的结构C4H8O IR/cm-1: 2970, 2878, 2825, 2718, 1724; NMR: δH: 9.5(三重峰,1H)38.化合物A的分子式为C8H14O。
大学有机化学期末考试题含三套试卷和参考答案大全

有机化学测试卷(A )一.命名下列各化合物或写出结构式(每题1分,共10分) 1.2.3-乙基-6-溴-2-己烯-1-醇 3. 4. 5.邻羟基苯甲醛 6.苯乙酰胺 7. 8.对氨基苯磺酸9. 10.甲基叔丁基醚二. 试填入主要原料,试剂或产物(必要时,指出立体结构),完成下列各反应式。
(每空2分,共48分)1. 2.3. 4. 5. 6. 7. 8.3+H 2OOH -SN 1历程+9.10. 11. 12. 三. 选择题。
(每题2分,共14分)1. 与NaOH 水溶液的反应活性最强的是( )2. 对CH 3Br 进行亲核取代时,以下离子亲核性最强的是:( )3. 下列化合物中酸性最强的是( )(A) CH 3CCH (B) H 2O (C) CH 3CH 2OH (D) p-O 2NC 6H 4OH(E) C 6H 5OH (F) p-CH 3C 6H 4OH 4. 下列化合物具有旋光活性得是:( ) C, (2R, 3S, 4S)-2,4-二氯-3-戊醇CH = C H 2HBr Mg5. 下列化合物不发生碘仿反应的是( )A、C6H5COCH3B、C2H5OHC、 CH3CH2COCH2CH3D、CH3COCH2CH36. 与HNO2作用没有N2生成的是( )A、H2NCONH2B、CH3CH(NH2)COOHC、C6H5NHCH3D、C6H5NH27. 能与托伦试剂反应产生银镜的是( )A、CCl3COOH B、CH3COOHC、 CH2ClCOOH D、HCOOH四. 鉴别下列化合物(共6分)苯胺、苄胺、苄醇和苄溴五. 从指定的原料合成下列化合物。
(任选2题,每题7分,共14分)1. 由溴代环己烷及不超过四个碳原子的化合物和必要试剂合成:2.由指定原料及不超过四个碳原子的化合物和必要的试剂合成:3.由指定原料及不超过四个碳原子的化合物和必要的试剂合成:4. 由苯、丙酮和不超过4个碳原子的化合物及必要的试剂合成:5. 由指定的原料及必要的有机试剂合成:六. 推断结构。
完整版)大学分析化学试题和答案

完整版)大学分析化学试题和答案分析化学试卷一一。
填空(每空1分,共35分)1.写出下列各体系的质子条件式:1) NH4H2PO4: [H+]+[H3PO4]=[OH-]+[NH3]+[HPO42-]+2[PO43-]2) NaAc-H3BO3: [H+]+[HAc]=[H2BO3-]+[OH-]2.符合朗伯-比尔定律的有色溶液,当有色物质的浓度增大时,其最大吸收波长不变,透射比减小。
3.检验两组结果是否存在显著性差异采用t检验法,检验两组数据的精密度是否存在显著性差异采用F检验法。
4.二元弱酸H2B,已知pH=1.92时,[H2B]=[HB-];pH=6.22时[HB-]=[B2-],则H2B的pKa1=1.92,pKa2=6.22.5.已知Φ(Fe3+/Fe2+)=0.68V,Φ(Ce4+/Ce3+)=1.44V,则在1mol/L H2SO4溶液中用0.1000 XXX滴定0.1000 mol/L Fe2+,当滴定分数为0.5时的电位为0.68V,化学计量点电位为1.06V,电位突跃范围是0.86-1.26V。
6.以二甲酚橙(XO)为指示剂在六亚甲基四胺缓冲溶液中用Zn2+滴定EDTA,终点时溶液颜色由黄色变为红色。
7.某溶液含Fe3+10mg,用等体积的有机溶剂萃取一次后,该溶液中剩余0.1mg,则Fe3+在两相中的分配比为99:1.8.容量分析法中滴定方式有直接滴定,反滴定,置换滴定和间接滴定。
9.I2与Na2S2O3的反应式为I2+2S2O32-=2I-+S4O62-。
10.以波长为横坐标,吸光度为纵坐标,测量某物质对不同波长光的吸收程度,所获得的曲线称为吸收光谱曲线;光吸收最大处的波长叫做最大吸收波长,可用符号λmax表示。
11.紫外可见分光光度计主要由光源、单色器、吸收池、检测部分四部分组成。
12.XXX灵敏度以符号S表示,等于M/ε;XXX灵敏度与溶液浓度有关,与波长无关。
13.在纸色谱分离中,水是固定相。
大学有机化学题库 选择题

0774
在DNA分子中,正确的碱基配对是:
(A) A-T(B) U-A(C) C-A(D) G-A
69. 2分(0775)
0775
必需氨基酸:
(A)可在人体内由糖转变而来
(B)能在人体内由其他氨基酸转化而来
(C)不能在人体内合成,必需从食物获得
(D)可在人体内由有机酸转化而来
(A)脱氨酸(B)丙氨酸(C)甘氨酸(D)组氨酸
44. 2分(0749)
0749
某氨基酸溶液在电场作用下不发生迁移,这时溶液的pH叫做:
(A)低共熔点(B)中和点(C)流动点(D)等电点
45. 2分(0750)
0750
用茚三酮试验时,下列氨基酸的哪一个不产生紫色反应?
(A)脯氨酸(B)色氨酸(C)丙氨酸(D)甘氨酸
0718
下列杂环化合物中偶极矩方向错误的是:
16. 2分(0719)
0719
下列化合物中沸点最高的是:
(A)吡咯(B)咪唑(C)噻唑(D)吡唑
17. 2分(0720)
0720
苯胺(a)、吡啶(b)、六氢吡啶(c)、吡咯(d)碱性强弱次序是:
(A) a>b>c>d(B) b>a>c>d(C) c>b>a>d(D) d>c>a>b
23. 2分(0726)
0726
血红蛋白中含有血红素,它的主要生物功能是:
(A)输送O2(B)储存O2(C)输送Fe(D)储存Fe
24. 2分(0727)
0727
苯(a)、吡咯(b)、呋喃(c)、噻吩(d)的芳香性强弱次序是:
(A) a>b>c>d(B) d>c>b>a(C) a>d>b>c(D) c>d>b>a
大学有机化学试题和答案

试卷一一、命名下列各化合物或写出结构式(每题1分,共10分) 1.C C H C(CH 3)3(H 3C)2HCH(Z )-或顺-2,2,5-三甲基-3-己烯2.3-乙基-6-溴-2-己烯-1-醇 3.OCH 3(S)-环氧丙烷4.CHO3,3-二甲基环己基甲醛5.邻羟基苯甲醛OHCHO6.苯乙酰胺 7.OHα-萘酚8.对氨基苯磺酸9.COOH4-环丙基苯甲酸10.甲基叔丁基醚二. 试填入主要原料,试剂或产物(必要时,指出立体结构),完成下列各反应式。
(每空2分,共48分) 1.CH CH 2ClCHBrKCN/EtOH答BrCN2.OHCCHCH 2CH 2CH 2CHOC1C1;答 3. 答 4.+CO 2CH 3答CO 2CH35.1, B 2H 62, H 2O 2, OH -1, Hg(OAc)2,H 2O-THF 2, NaBH 4答OH OH(上面)(下面)6.OOOOO答 NH 2NH 2, NaOH,(HOCH 2CH 2)2O7. CH 2ClClNaOH H 2OCH 2OHCl8.ClCH 3+H 2OOH -SN 1历程答CH 3OH+CH 3OH9.答OO CH 3CH 2CH 2C CH 3OOCH 3O10.BrBrZnEtOH答11.CH = C H 2CH 3COCH 3H 2O ①②HBrMg 醚H+C O CH 3+Cl 2H +答CO CH 2Cl12.三. 选择题。
(每题2分,共14分)1、与NaOH 水溶液的反应活性最强的是( A )2. 对CH 3Br 进行亲核取代时,以下离子亲核性最强的是:( B )3. 下列化合物中酸性最强的是( D )(A) CH 3CCH (B) H 2O (C) CH 3CH 2OH (D) p-O 2NC 6H 4OH(E) C 6H 5OH (F) p-CH 3C 6H 4OH 4. 下列化合物具有旋光活性得是:( A ) C, (2R, 3S, 4S)-2,4-二氯-3-戊醇5. 下列化合物不发生碘仿反应的是( C ) C 6H 5COCH 3 B 、C 2H 5OHC 、 CH 3CH 2COCH 2CH 3D 、CH 3COCH 2CH 3 6. 与HNO 2作用没有N 2生成的是( C )A 、H 2NCONH 2B 、CH 3CH (NH 2)COOHC 、C 6H 5NHCH 3D 、C 6H 5NH 2 7. 能与托伦试剂反应产生银镜的是( D ) CCl 3COOH B 、CH 3COOH C 、 CH 2ClCOOH D 、HCOOH 四、鉴别下列化合物(共6分) 苯胺、苄胺、苄醇和苄溴五、从指定的原料合成下列化合物。
吉林大学普通化学期末试题

吉林大学09—10学年第一学期普通化学A 试卷一、每小题只有一个选项符合题意,请将答案的代码填入题末的括号内。
(每小题1分, 共10分)1、干冰升华吸收能量以克服…………………………………..………… ( ) A 、 键能 B 、 取向力 C 、 色散力 D 、 诱导力2、金属表面因氧气分布不均匀而被腐蚀,称为差异充气腐蚀,此时金属溶解处是( )A 、在氧气浓度较大的部位;B 、在氧气浓度较小的部位;C 、在凡有氧气的部位;D 、以上均不正确。
3、下列各组量子数中不合理的是…………………………………………………. ( )A 、2,1,0,+21B 、2,2,0,+21C 、2,0,0, -21D 、1,0,0,+21 4、酸雨是指雨水的pH 小于……………………………………………………………( ) A 、6.5; B 、6.0; C 、5.6; D 、7.05、通常线性非晶态高聚物中,适宜作塑料且加工性能较好的是…………………...( ) A 、T g 值和T f 值均高; B 、T g 值和T f 值均低; C 、T g 值低,T f 值高; D 、T g 值高,T f 值低。
6、AgCl 在下列物质中溶解度最大的是……………………………………………….( )A 、纯水;B 、6 mol·kg –1 NH 3·H 2O ;C 、0.1 mol·kg –1NaCl 溶液;D 、0.1 mol·kg –1BaCl 2溶液。
7、下列物质中 不等于零的是:..………………………………………….( )A 、I 2(g );B 、C (石墨); C 、Fe (s );D 、Cl 2(g )8、稀土金属通常保存在………………………………………………………………( )A 、汽油中;B 、柴油中;C 、煤油中;D 、酒精中。
9、下列离子属于9 ~17电子构型的是……………………………………………….( )A 、Br - ;B 、Sc 3+; C 、Zn 2+; D 、Fe 2+10、下列分子中,偶极矩不为零的是…………………………………………………( )A 、NCl 3;B 、BF 3 ;C 、CCl 4 ;D 、CS 2二、每小题有一个或两个选项符合题意,请将答案的代码填入题末的括号内。
吉林大学化学期中考试
三、简答题 (共12分)
1、请用动力学理论解释,在其他条件一定时,为什 么升高温度化学平衡会向吸热反应方向移动?
T2 T1 当 一定时,k2/k1与Ea成正比。 T1T2 k2 (吸) 对可逆反应,Ea(吸)>Ea(放),所以
k2 Ea T2 T1 ln k1 R T1T2
8. 下列方程式中,能正确表示AgCl (s)的ΔfHmӨ的是 ( B ) A Ag (s)+1/2Cl2( l )→ AgCl (s) B Ag (s)+1/2Cl2 (g)→AgCl (s) C 2Ag (s)+Cl2 (g)→ 2AgCl (s) D Ag+(aq)+Cl-(aq)→ AgCl (s) 9. 在300℃时反应CH3CHO → CH4+CO的活化能为190 kJ· -1。 mol 当加入催化剂后,反应的活化能降低为136.0 kJ· -1。问加 mol 入催化剂后的反应速率是原来的几倍 ( C ) A 2.53×109倍 B 2.53×108倍 C 8.35×104倍 D 8.35×106倍 10. 增加反应物浓度,化学反应速率加快的原因是( B ) A 反应物的活化分子百分数增加 B 反应物活化分子的数目增加 C 活化能降低 D 化学反应的速率常数增加
5. 已知298.15K时,Zn + 2H+( a mol· -1)→ Zn2+ (1.0 L mol· -1) +H2 ( 1.00×105Pa ),组成原电池,测得其电 L 动势E为 0.46 V,已知 E Ө (Zn2+/Zn)=-0.76V,则氢电 极溶液中pH为 ( D ) A 10.2 B 2.5 C 3.0 D 5.1 6. 电极电势与pH无关的电对是 ( D ) A H2O2/H2O B IO3-/I C MnO2/Mn2+ D MnO4-/MnO427. 下列过程中,ΔG = 0的是 ( B ) A 理想气体向真空膨胀 B 氨在水中解离达平衡 C 炸药爆炸 D乙醇溶于水
《大学化学基础》课程试卷(6)全解
11.在标准条件下,下列反应均向正方向进行
Cr2O72-+ 6Fe2++ 14H+= 2Cr3++ 6Fe3++ 7H2O
2Fe3++ Sn2+= 2Fe2++ Sn4+
它们中间最强的氧化剂和最强的还原剂是()
A.Sn2+和6Fe3+B.Cr2O72-和Sn2+C.Cr2+和Sn4+D.Cr2O72-和Fe3+
4.在公式lnKθ=nFEθ/RT中,下列有关描述正确的是( )
A.Kθ是标准状态的标准平衡常数B.Eθ是标准状态的电动势
C.Eθ是任意状态的电动势D.Kθ是298K时的标准平衡常数
5.下列电对中,当H+浓度增大时,电极电势不变的是()
A.Cl2/Cl-B.Cr2O72-/Cr3+C.MnO4-/Mn2+D. AsO43-/AsO33-
得
分
五、计算题(共25分)
1. (本小题7分)
计算反应2Fe2O3(s)+3C(s)→4Fe(s)+3CO2(g)自发进行的温度条件。[已知:Fe2O3(s)、CO2(g)在298K的标准摩尔生成热(焓)△fHmθ分别为–824.2、–393.50 kJ·mol-1;Fe2O3(s)、C(s)、Fe(s)、CO2(g)在298K的标准熵Smθ分别为87.4、5.74、27.28、213.64J·mol-1·K-1,可忽略温度对标准摩尔生成焓及标准熵的影响]。
3.(本小题5分)
用杂化轨道理论说明BF3分子共价键的形成,并指出其空间构型、键角及每一杂化轨道所含的s成份和p成份多少。
南昌大学有机化学-期末试卷
4、画出1,3,5-己三烯在基态时的HOMO 和LUMO 轨道图。
5、指出下列反应协同反应的类型A.HHB.OO OOO OC.OH O OOHD.Me MeMeMe6、比较下列化合物的酸性顺序( )A. B.C. D.SHSHOH SO 3H7、指出下列化合物的类别,并写出名称。
A.B. C. D.SS SH S CH 3OCH 3CH 3H 2NSO 2NH C NH 2NHDsfa8、在有机合成中保护羰基的常用试剂是( ) 实打实的、大苏打、9、在合成多肽时,保护氨基的试剂是( )A. B. C. PCl 5D. HCl OC Cl CH 3OPhCH 2O C Cl10、有机合成中常利用官能团的性质差异合成目标分子。
写出下列反应的目标产物。
A.B.ClClNaCN OEtO O Ph 3P +-CH 3CHCH 3C.OEtO O RoNaICH 2CH 2CH 2Cl11、在有机合成中常利用分子的对称性,使合成问题简化。
下列化合物应怎样拆分并合成。
A.CH 3OC C 2H 5H C C 2H 5H O CH 3B.PhC CPhOH CH 3OHCH 3二、完成反应1.N1) KMmO 42) H +―H 2O2.NH NO 3H 2SO 4NaNH 2NH 2甘油, 浓H 2SO 4硝基苯LiAlH 43.4.CH 3CH BrCH 3Ph 3Pn ―BuLi5.NaOHSHC 2H 5Br6.C C H 2SH H 2SH OC CH 2CH 3CH 3H 2兰尼镍7.S S H C 2H 51) n ―BuLi 2) Br(CH 2)4BrH 3O +Hg ++8.1) KMnO 42) H +CH 3SO 2ClNH 39.hvCH 3CH310.LiAlH 4CH 2CH COOEt11.HO CH 2C CHO 干燥 HCl1) Na2) CH 3CH 2CH 2Cl12.1) O 32) Zn/H 2OPh OHH 3PO 413.1) NaOH, H 2O 2) H + ,HCNCH 3C CH 2COOHCH3OC CH 314.2OO15. HCOOC 2H 51) CH 3CH 2CH 2CH 2MgBr 2) H 3O +CrO 3吡啶三、合成1、从n —BuOH 及必要试剂合成CH 3C CH 3OH( CH 2)5CH 3― 2、从C 2H 5Br 及必要试剂合成C 2H 5C OH C 2H 5C 2H 53、从丙醛合成CH 3CH 2CHCH CHO CH 34、从O及必要试剂合成HOOC(CH 2)4C CH 3O5、用切断法合成COOHCHO6、从乙炔及必要试剂合成(meso)—3,4—己二琼7、用切断法合成O 8、用必要试剂合成N N NCH3N NCH3NCH3CH3CH3 CH39、OHOOC OH10、HOCHOO O11、CH3OC CH3OC CH2CH2CH C CH3OCH3南昌大学2004-2005学年第二学期期末考试试卷(B)课程名称:有机化学题号一二三四五总分标准分20 30 6 20 24 100实得分阅卷人一、命名或写出结构式1.β-D-甲基吡喃葡萄糖苷稳定构象式2.2,3,4,6-四-O-甲基-D-吡喃葡萄糖3.谷氨酸4.甘氨酰丙氨酸5.三软脂酸甘油脂6.(+)-纤维二糖7.(+)-蔗糖 8.-果糖9.(Z 、Z )-9,12-十八碳二烯酸(亚油酸) 10.(Z 、E 、E )-9。
大学-无机化学试卷绝密
r r r (aq) r b 无机化学考试试题一、选择题(每题只有一个正确答案,在 a 、b 、c 、d 下打√,每题 1 分, 共 30 分)1、当一个反响以 ln k ~1/T 作图时,直接影响直线斜率的因素是 a 、反响的焓 b 、反响的吉布斯函数变c 、热力学能d 、反响的活化能2、催化剂可以增大化学反响速率,主要是由于反响的a 、△ G θm 降低b 、△ H θm 上升c 、△ S θm 上升d 、E a 降低3、以下哪一物种的△f G θm 等于零 a 、Br 2(g) b 、Br – c 、Br 2(l) d 、Br 2(aq)4、在等温等压条件下,某反响的△ G θ m.298= 10 kJ ⋅mol -1,说明该反响 a 、在标准态下,298K 时能自发进展b 、在标准态下,298K 时不能自发进展c 、在非标准态下,肯定能自发进展d 、在非标准态下,肯定不能自发进展5、298K ,H 2O (l) = H 2O (g)到达平衡时,体系的水蒸气压为 3.13kPa ,则 K θ 为以下数值中的哪一个a 、100b 、0.0313c 、3.13d 、16、依据酸碱电子理论,通常的中和反响是生成a 、一种协作物的反响b 、另一种较稳定协作物的反响c 、两种协作物的反响d 、中性分子酸和碱的反响7、HAc 的标准解离常数 K θa ,NaAc 的标准水解离数是a 、(K θa K θw )1/2b 、K θa / K θwc 、K θw / K θad 、(K θw / K θa )1/28、将 10g0.1mol ⋅L -1MgCl 2 和 10g0.01mol ⋅L -1 氨水相混合后,将消灭以下哪 一种状况[K θsp [Mg(OH)2]=1.2×10-11,K θ (NH 3)=1.8×10-5]a 、Q < K θspb 、Q = K θspc 、Q > K θspd 、Q ≤ K θsp9、假定 Sb 2S 3 的溶解度为 x ,则 Sb 2S 3 的溶度积应为a 、K θsp =x 5 b 、 K θsp =6xc 、K θsp =x 2d 、K θsp =108x 5班 级姓 名 考试成绩 课 程 无机化学 考试时间 年 月 日r 10、△ G θm 是一个氧化复原反响的标准吉布斯函数变,K θ是标准平衡常数, E θ是标准电动势,以下哪组所表示的△ G θ r m 、K θ、E θ关系是全都的 a 、△ G θ >0 E θ<0 K θ<1 b 、△ G θ >0 E θ>0 K θ>1 r m r m c 、△ G θ >0 E θ<0 K θ>1 d 、△ G θ <0 E θ<0 K θ>1 r m r m11、以下电对中,E θ值最大者是a 、E θ(AgI/Ag)b 、E θ(AgCl/Ag)c 、E θ[Ag(NH 3)2+/Ag]d 、E θ(Ag +/Ag)12、以下氧化剂中,随氢离子浓度增加而氧化性增加的是a 、Cl 2b 、FeCl 2c 、AgCld 、K 2Cr 2O 7 13、AgBr 沉淀易溶于哪一种水溶液中a 、H 2SO 4b 、AgNO 3c 、NaOHd 、Na 2S 2O 314、己知[Cu(edta)2-]和[Cu(en)2]2+的标准稳定常数分别为 6.3×1018 和 4.0 ×1019,试推断两者稳定性大小应符合以下哪种状况a 、前者大于后者b 、前者与后者差不多c 、前者小于后者d 、不肯定15、以下哪项用量子数描述的电子亚层可以容纳最多的电子数a 、n=3,l =2b 、n=4,l =3c 、n=5,l =0d 、n=5,l =3,m= +116、IB 族元素的原子半径比相应的 VIII 族元素的原子半径大,缘由是a 、d 电子越多,半径越大b 、IB 族的金属性比 VIII 族的强c 、最外层电子受屏蔽效应大d 、测定的试验方法不同17、在 PCl 3 分子中含有a 、1 个 sp 3-p σ键b 、2 个 sp 3-p σ键c 、3 个 sp 3-p σ键d 、5 个 sp 3-p σ键18、用杂化轨道理论推想以下分子的空间构型为直线形的是a 、SbH 3b 、CeH 4c 、CS 2d 、H 2Te19、依据分子轨道理论,O 2+中的键级是a 、0.5b 、1c 、1.5d 、2.520、以下化合物中,有分子内氢键的是a 、H 3BO 3b 、C 2H 6c 、N 2H 4d 、HNO 321、在协作物[Pt(NH 3)6] [PtCl 4]中,两个中心离子铂的氧化态是a 、都是+8b 、都是+6c 、都是+4d 、都是+222、依据晶体场理论,高自旋协作物的理论判据是a 、分裂能>成对能b 、电离能>成对能c 、分裂能>成键能d 、分裂能<成对能23、在八面体场中,既能形成低自旋又能形成高自旋协作物的过渡元素的d 电子数应为a、1~3 个b、2~5 个c、4~6 个d、6~9 个24、电子构型一样的离子,其极化力最强的是a、高电荷和半径大的离子b、高电荷和半径小的离子c、低电荷和半径大的离子d、低电荷和半径小的离子25、金属锂应保存在以下哪种物质之中a、汽油b、煤油c、枯燥空气d、液体石蜡26、以下有关硼烷的说法不正确的选项是a、BH 是最简洁的硼烷3b、乙硼烷中,2 个硼原子间靠氢桥键结合c、乙硼烷是最简洁的硼烷d、乙硼烷遇水发生水解,产物有氢气27、以下排列挨次中,符合氢卤酸的酸性递增挨次的是a、HI、HBr、HCl、HFb、HF、HCl、HBr、HIc、HBr、HCl、HF、HId、HCl、HF、HI、HBr28、以下离子中,哪一个由于d 亚层的电子到达半布满而特别稳定a、Fe3+b、Cu2+c、Co2+d、Cr3+29、以下元素中,其化合物较多呈现颜色的是a、碱金属b、碱土金属c、过渡元素d、卤素30、通常用什么试剂鉴定镍离子a、N-亚硝基( )苯胲胺b、丁二酮肟c、硝基苯偶氮间苯二酚d、二苯基联苯胺二、简答题(简要答复以下各问题,每题8分,共32分)1、通过计算比较,以下两组元素的原子作用在最外层电子上的有效核电荷大小,并依据计算结果说明,主、副族元素变化规律有何差异?(1)V Cr Mn (2)Na Si Cl2、己知[Fe(CN)6]4-和[Fe(NH3)6]2+的磁矩分别为0 和5.2B.M.。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
大学化学(Ⅱ)试卷(A)
试卷号:B070003
学院___________ 专业___________
姓名___________ 学号___________
(请考生注意:本试卷共 5 页)
一、对的在题末括号内填“+”、错的填“-”。
(本大题分10小题, 每小题1分, 共10分)
1、室温时,在总压力为200 Pa 的两种气体的混合物中,氯气的分压力为100 Pa,这意味着Cl2的物质的量是混合气体总的物质的量的一半。
答:()
2、反应Fe + SnCl2 = FeCl2 + Sn 是氧化还原反应,而反应2FeCl3 + SnCl2 = SnCl4 +2FeCl2不是氧化还原反应。
答:()
3、由反应Cu + 2Ag+=Cu2+ + 2Ag 组成原电池,当c(Cu2+ ) = c(Ag+ ) = 1.0 mol⋅dm-3时,E= E-E= E(Cu2+/Cu) -2E(Ag+/Ag)。
答:()
4、盐类水溶液电解产物的一般规律是:若阳极是惰性电极(如石墨),则首先是OH-放电生成O2,其次才是简单离子S2-或I-、Br-、Cl-等放电。
答()
5、升高反应温度,能使反应速率常数k和标准平衡常数K都增大。
答:()
6、由于Cu+离子与Na+离子的半径相近,离子所带电荷相同,故NaOH 和CuOH 碱性相近。
答()
7、将50℃的一定量的水,置于密闭容器中,会自动冷却到室温(如20℃)。
此时密闭容器内水的熵值变小,即∆S < 0。
这说明在密闭容器中的自发过程,系统本身不一定要熵增加。
答()
8、铁原子失去2 个电子成为Fe2+,失去3 个电子才成为Fe3+,故在水溶液中Fe2+比Fe3+更稳定。
答:()
9、外层电子构型为18 电子的离子都是位于p 区或ds 区元素的离子。
答()
10、弱电解质溶液的解离度和解离常数,可采用pH 法或电导率法测定。
答()
二、将一个或两个正确答案的代码填入题末的括号内。
若正确答案只有一个,多选时,该题为0分;若正确答案有两个,只选一个且正确,给1分,选两个且都正确给2分,但只要选错一个,该小题就为0分。
(本大题分10小题, 每小题2分, 共20分)
1、下列各外层电子构型中,不属于Cu、Fe、Mn 原子的是答()
(1)3d64s2
(2)3d104s1
(3) 3d54s2
(4)6s2
2、下列对高分子材料改性的措施中,属于化学改性的是答()(1) 橡胶中加炭黑(2) 聚乙烯氯化
(3) 由环氧树脂制玻璃钢(4) 聚氯乙烯中加增塑剂
3、25℃时,在容积为100 cm3的真空容器中装有1 mol H2O,其平衡压力为3.2 kPa。
若改用200 cm3的真空容器代替,平衡压力为答:()
(1) 32 kPa (2) 6.4 kPa (3) 3.2 kPa (4) 101 kPa
4、对于反应:4Al+3O2+6H2O=4Al(OH)3,运用公式∆r G= -nFE时,其中n为
答:()
(1) 1 (2) 12
(3) 3 (4) 4
5、在由气体A 与B 组成的混合气体中,组分A 的分压力与总压力之比等于答:()(1) A 组分的摩尔分数(2) A 组分的分体积与总体积之比(3) B 组分的分压力与总压力之比 (4) A 组分与 B 组分的分体积之比
6、NH3比PH3的沸点高,其主要原因是答:()
(1) 氨分子体积较小
(2) 氨的电偶极矩大于零
(3) 氨具有较大的键角
(4) 氨分子间存在氢键
7、下列各系统中,具有最大摩尔熵值的是答:()(1) 20 K 时的冰(2) 273.15 K 时的冰
(3) 373.15 K 时的水蒸气(4) 400 K 时的水蒸气
8、确定多电子原子中,轨道的能量的是答()(1) n (2) n和l
(3) n,l和m (4) n,l,m和m s
9、在相同的温度和压力下,气体A 充满烧瓶时,测得A 的质量为0.34 g;若改为充满O3时,测得O3气体的质量为0.48 g。
则A 气体可能是(相对原子质量:H 为1,O 为16,S 为32。
)答:()(1) O2(2) SO2(3) H2S (4) PH3
10、下列氧化剂中,其氧化性随c (H+ )的增大而增强的是答:()
(1)Ag+
(2)Cr2O72-
(3)O2
(4)Cl2
(5)Fe3+
三、填空题。
(本大题共15小题,总计30分)
2、(本小题1分)
在M电子层中,原子轨道最多可有_______________条。
4、(本小题2分)
阿仑尼乌斯公式的指数式为_____________________,它反映了反应速率受__________ 影响的规律。
5、(本小题2分)
在共价键C-C,C=C 和C C 中,键能最大的是_____________,键长最长的是__________。
6、(本小题2分)
某元素的原子序数为31,其基态原子中共有___________ 个能级分布有电子。
其+3 价离子的外层电子分布式为_____________________,7、(本小题2分)
预测第七周期的稀有气体元素的原子序数为______,外层电子构型为______________。
8、(本小题1分)
化学氧化法处理工业废水和城市供水,最常采用的氧化剂是________________。
9、(本小题2分)
乙二胺与乙二酸两种单体发生缩聚反应后,所得的高聚物称聚酰胺-22,其结构简式为________________________________。
10、(本小题2分)
画出下列原子轨道角度分布的示意图:
2s
_____________________________________
2p x
_____________________________________
11、(本小题2分)
填写出氢在下列物质中形成的化学键类型:
在HCl中_______________________,在NaOH 中__________________________,
在NaH中_______________________,在H2中____________________________。
12、(本小题3分)
将反应FeCl2 (aq) + (1/2) Cl2 (g) = FeCl3 (aq) 组成原电池,可用电池符号表示为:_______________________________________________________。
14、(本小题3分)
第26 号元素,其原子外层电子构型为_____________,属___________ 族的元素。
作用在该原子的最外层某一个电子上的有效核电荷数为___________。
15、(本小题4分)
已知某温度时反应Zn(s) + Cu2+(aq) = Cu(s) + Zn2+(aq) 的K= 2⨯1037。
若系统中起始浓度c(Cu2+) = c(Zn2+) = 0.1 mol⋅dm-3,且同时有下列条件时,分别会出现什么现象。
(1) Zn(s),Cu(s) 均存在:_____________________________________;
(2) 有Zn(s),无Cu(s):________________________________________;
(3) 有Cu(s),无Zn(s):________________________________________;
(4) Zn(s),Cu(s) 均不存在:______________________________________。
四、根据题目要求,通过计算解答下列各题。
(本大题共5小题,总计40分)
1、(本小题7分)
已知由H2CO3-HCO3-组成的缓冲溶液,其中c(H2CO3)=1.25⨯10-3mol⋅dm-3,c(HCO3-)=2.5⨯10-2 mol⋅dm-3,求此缓冲溶液的pH 值。
[ 已知H2CO3:K=4.3⨯10-7 , K=5.61⨯10-11 ]
2、(本小题7分)
已知:E(Fe3+/Fe2+)=0.77 V,E(I2/I-)=0.54 V,判断反应2Fe3++2I- 2Fe2++I2进行的方向,并计算25℃时该反应的标准平衡常数。
3、(本小题9分)
试计算25℃时PbSO4在纯水中和在0.040 mol⋅dm-3的Na2SO4溶液中的溶解度(mol⋅dm-3)分别为多少?( 已知25℃时K(PbSO4)=1.82⨯10-8 )
4、(本小题8分)
已知25℃时,Cl2(g)+H2O(l)=HCl(aq)+HClO(aq) 的平衡常数:K=3.0⨯10-5,HClO(aq)= H+(aq)+ClO-(aq) 的K=3.0⨯10-8,计算下列反应在25℃、标准态下装配成原电池的电动势。
Cl2(g)+2OH-(aq)=ClO-(aq)+Cl-(aq)+H2O(l)
5、(本小题9分)
用于制备半导体硅的反应:SiO2(s) + 2C(s) = Si(s) + 2CO(g),有关热力学数据如下表。
试通过计算:
(1) 判断此反应在298.15 K 和标准条件下能否自发进行;
(2) 估计在标准条件下自发进行的最低温度。
S。
