[配套K12]2016中考化学考点全解 考点十一 原子的核外电子排布
2016中考化学考点全解 考点十一 原子的核外电子排布

原子的核外电子排布⒈电子排布——分层排布:第一层不超过2个;第二层不超过8个;……最外层不超过8个。
⒉原子结构示意图:⑴含义:(以铝原子结构示意图为例)(2)原子、阳离子、阴离子的判断:①原子:质子数=核外电子数②阴离子:质子数<核外电子数③阳离子:质子数>核外电子数①元素的化学性质决定于原子的最外层电子数。
②原子最外层电子数为8(氦为2)的结构称为稳定结构。
例题1.(2015•毕节市)某微粒的结构示意图如图所示,下列有关该微粒的说法错误的是()A 、该微粒的原子核内有11个质子B 、该微粒在化学反应中易失去1个电子C 、该微粒的原子核外有3个电子层D 、该图表示的微粒是一种离子答案:D解析:A 、由微粒的结构示意图可知,该微粒的原子核内质子数为11个,故A 正确;B 、该微粒最外层电子数为1,在化学反应中易失去1个电子,故B 正确;C 、该微粒的原子核外有3个电子层,说法正确,故C 正确; 易错考点例题解析D、根据原子“核内质子数=核外电子数”,可知该图表示的微粒是一种原子,而非离子,故D说法错误.例题2.(2015•益阳)人教版九年级化学上册教材图3﹣12部分原子的结构示意图如下:请回答:(1)氧元素与硫元素化学性质相似的原因是;(2)写出11号和17号元素组成化合物的化学式;(3)同一周期(横行)的原子结构示意图具有共同的特点是(任写一点).答案:(1)两种原子的最外层电子数相同;(2)NaCl;(3)电子层数相同;解析:(1)由于元素的性质主要由最外层的电子数决定的,氧元素与硫元素化学性质相似的原因是:两种原子的最外层电子数相同;(2)原子序数为11元素为钠元素,原子序数为17的元素为氯元素,钠为+1价,氯为﹣1价,故组成化合物的化学式为NaCl.(3)由原子结构示意图的特点可以看出,同一周期(横行)的原子结构示意图具有共同的特点是电子层数相同等.课后练习1.(2015•株洲)如图中A、B、C、D是四种粒子的结构示意图.请回答下列问题:(1)A中x= ;A粒子的化学式是.(2)由B粒子的结构示意图可知,B粒子的名称是.(3)以上四种结构示意图所表示的粒子中,表示离子的是(填字母代号).2.(2015•荆州)某粒子的结构示意图为(其中n≠0),请回答下列问题.(1)n的最大值为.(2)若该粒子带两个单位的负电荷,则其对应的化学符号为;由+6价的该元素形成的常见酸的化学式为.(3)若m﹣n=10,则该粒子对应的常见金属元素有(写元素符号).3.(2015•乌鲁木齐)如图为六种常见元素的原子结构示意图,依据图中信息回答下列问题:(1)上述六种元素中属于金属元素的是(填元素名称),己元素的化学性质与(填元素符号)元素相似.(2)在化学反应中,戊元素的原子容易(填“失去”或得到)电子形成阳离子,该元素的离子符号是.该元素单质与氧气反应的化学方程式是.(3)甲、乙元素和碳元素、氧元素组成的一种常见氮肥的化学式为:.4.(2015•娄底)据《自然》杂志报道,科学家最近研究出一种以锶(Sr)做钟摆的钟,它是世界上最精确的钟,锶的原子结构示意图如右图所示,请回答:(1)锶原子的核电荷数为.(2)锶原子核外电子层数为.(3)锶原子最外层容易电子.(填“得”或“失”)5.(2015•宿迁)如图A是某金属元素形成微粒的结构示意图:该金属在空气中燃烧时放出大量的热并发出耀眼的白光,图B是该反应的微观示意图.请根据以上信息回答下列问题:(1)该金属元素原子核外电子数= ,图A所示微粒的符号为;写出一种与图A所示具有相同电子层结构的阴离子的符号.(2)图B所示的化学方程式:.36.(2015•武汉)如图1为某元素的原子结构示意图,利用该元素组成的单质可测定空气中氧气的含量,实验装置如图2所示.(1)该元素原子的核电荷数为,在化学反应中该原子易电子;(2)图2所示装置中发生反应的化学方程式为5.7.(2015•菏泽)有A、B、C、D四种元素,其原子结构示意图如图:(1)D元素的名称为,D元素与图中(填写字母序号)元素的化学性质相似,D元素的离子符号为.(2)A、B、C三种元素能形成一种化合物,其水溶液的pH 7(填>、<、=)(3)A、B两种元素的原子以1:1的比例形成的化合物为(写化学式),其中B元素化合价为.8.(2015•重庆)学习化学后,我们学会了从微观角度认识物质.(1)已知碳原子和氧原子的结构示意图分别为:和,两种原子中相等的是(填序号).A.质子数 B.电子数 C.第一层电子数 D.第二层电子数(2)保持一氧化碳化学性质的粒子名称是.(3)如图是一氧化碳与氧气反应的微观模型图,请在如图框中以图示的方式完成该化学反应的微观过程(图中●表示氧原子,○表示碳原子).5。
初三化学上学期核外电子排布-课件

欢迎来到初三化学上学期核外电子排布的PPT课件。在本课程中,我们将学 习原子结构、电子能级和壳层、原子的电子排布和元素周期表以及元素的化 学性质与排布规律。
知识点一:原子结构
原子结构的组成
原子由原子核和核外电子组成,核内质子和中子构成了原子核。
原子核的构成
原子核由质子和中子构成,质子带正电荷,中子不带电。
知识点四:元素的化学性质与排布规律
元素的三种基本性质
元素的化学性质主要包括金 属性、非金属性和半金属性。
元素的同位素和同系物 的概念
元素的同位素是指具有相同 原子序数但质量数不同的同 种元素,同系物是指元素在 化合价和化学性质上相似的 元素。
元素周期表中的元素性 质规律
元素周期表中元素的性质随 着周期数和原子序数的增加 具有一定的规律和趋势。
知识点三:原子的电子排布和元素周期表
1
原子的电子排布规律及其重要性
原子的电子排布遵循泡利的排斥原理,
美学家-泡利的排斥原理
2
它对元素的性质和元素周期表的构建有 重要影响。
泡利的排斥原理规定了每个
3
元素周期表的分类和结构
元素周期表根据元素的原子序数和周期 数进行了分类和排列,具有一定的结构 和规律。
总结
1 本次课程的学习重点和难点
学习重点:原子结构、电子能级和壳层,元素的电子排布规律和元素周期表。 学习难点:了解和应用泡利的排斥原理。
2 总结原子结构和元素周期表的重要性
原子结构和元素周期表是化学研究的基础,对于理解化学性质和反应有重要意义。
3 分享一些实用的学习方法和技巧
通过观看相关视频、做练习题和参加化学实验等方式来加深对原子结构和元素周期表的 理解。
核外电子排布_课件完美版PPT

得2个电子
S2-
8
化学反应 得、失 电子〔内离外子不
等
内多外少带正电—阳离子 内少外多带负电—阴离子
原子
化学反应 得、失 电子
离子 内多外少带正电—阳离子
内少外多带负电—阴离子
〔内外相等
〔内外不
不显电性〕
等
离子表示法——离子符号 显电性〕
阳离子:H+、Na+、Mg2+、Al3+ 阴离子:Cl -、S2 -、O2 -
核外电子排布_课件
原子的结构
原子 原子核 +
核外电子 —
质子:一个质
子带一个单位的 正电荷
中子:不带电
核电荷数〔即质子数〕= 核外电子数
原子相对质量︽ 质子数 + 中子数原子 原子的质量主要集中在原子核上
原子核内质子数决定元素种类
原子不显电性的原因:
由于原子核所带电量和核外电子 的电量相等,但电性相反,所以整 个原子不显电性。
当x= 时,表示阴离子。
局3、元部元金素素属的元分化素学类的性原质子是结由构原示金子意的图属最外元层素电子数 决定
非金属元素
稀有气体元素
最由同于学外原 们子有层核没电所有带想子电过量电数和子核是最外怎电样外子围的绕层电原电量子相核子等做,高1-但速电运3性动个相的反呢,? 所以最整个外原子层不电显电子性。4--7个
食盐〔NaCI〕 晶体
学完本课题我们知道了
1、原子核外电子是分层排布 2、原子结构示意图 3、元素的化学性质是由 原子的最外层电子数 决定
4、构成物质的粒子有三种:分子 、原子 、离子 。
1、以下所示微粒中,属于原子的是( 〕,属 于 阴 离子的是〔 〕,属于阳离子的是〔 〕,属于同一 种元素的是〔 〕,属于金属原子的是〔 〕属于 非金属原子的是〔 〕
初中化学人教版九年级上册《原子核外电子的排布》课件(完美版)

原子分类 金属原子
最外层电子数 一般少于4个
电子得失情况
易失电子
原子分类 最外层电子数 非金属原子 一般多于4个
电子得失情况
易得电子
此页为防盗标记页(下载后可删)
1、谢谢大家听得这么专心。 2、大家对这些内容这么感兴趣,真让我高兴。 3、你们专注听讲的表情,使我快乐,给我鼓励。 4、我从你们的姿态上感觉到,你们听明白了。 5、我不知道我这样说是否合适。 6、不知我说清了没有,说明白了没有。 7、我的解释不知是否令你们满意,课后让我们大家再去找有关的书来读读。 8、你们的眼神告诉我,你们还是没有明白,想不想让我再讲一遍? 9、会“听”也是会学习的表现。我希望大家认真听好我下面要说的一段话。 10、从听课的情况反映出,我们是一个素质良好的集体。 1、谢谢你,你说的很正确,很清楚。 2、虽然你说的不完全正确,但我还是要感谢你的勇气。 3、你很有创见,这非常可贵。请再响亮地说一遍。 4、××说得还不完全,请哪一位再补充。 5、老师知道你心里已经明白,但是嘴上说不出,我把你的意思转述出来,然后再请你学说一遍。 6、说,是用嘴来写,无论是一句话,还是一段话,首先要说清楚,想好了再说,把自己要说的话在心里整理一下就能说清楚。 7、对!说得很好,我很高兴你有这样的认识,很高兴你能说得这么好! 8、我们今天的讨论很热烈,参与的人数也多,说得很有质量,我为你们感到骄傲。 9、说话,是把自己心里的想法表达出来,与别人交流。说时要想想,别人听得明白吗? 10、说话,是与别人交流,所以要注意仪态,身要正,不扭动,眼要正视对方。对!就是这样!人在小时候容易纠正不良习惯,经常 注意哦。
4个
相对稳定结构
不稳定
完成课堂练习2、3
原子核内质子数为13/核电荷数为13
初三化学核外电子排布

核外电子排布的知识包括3方面内容
1. 核外电子具有的能量不同,是按能量高 低分层排布的。
电子层数、离核距离、能量高低之关系如下所示:
电子层 1 2 3 4 5 6 7
(K)(L)(M)(N)(O)(P)(Q) 离核距离 能量 近 低 远 高
2. 原子结构示意图,这是描述原子结构 的化学用语。如氧原子的结构示意图如下所 示: 电子层 原子核 +8 2 6 核电荷数 层内电子数
易失 易得 稳定
金属性
非金属性
稳定性
稀有气体元素 8或2(He)
; https:///maolilv/106448.html 毛利率 ;
锁定两大基本玄奥融合,变成空间初级玄奥. 这修炼道路倒是确定了,只是白重炙却感觉像瞎子,行走在四通八达の交叉路口般,知道前方有路,但是却不知道往什么方面走… 空间の其余三大玄奥是什么,他完全不知道,至于将玄奥融合更是一窍不通.并且这法则感悟还不能问别人,因为鹿老曾 经和他说过.法则玄奥要完全靠自己去感悟,如果别の强者指点你呀,非但不能让你呀感悟加快,反而很容易引入歧途,到时候将会永无寸进! "虽然融合了空间波动和空间锁定玄奥,就能直接成神,但是显然困难无比,否则剑皇也不会数千年还没达到天神巅峰.这条路不用去想,还是去感悟其他 三大玄奥!" 白重炙经过短暂の考虑,果断放弃了将两种玄奥融合成神の路.天神都要动则千年の事情,自己一些圣级肯定脑袋爆裂都不会成功.那么剩下唯有,感悟三大空间玄奥一途. 将身子转了过来,他开始面对着左边の那面光洁墙壁,全身放松,去除杂念,将战气运作在双眸内,而后朝那墙 壁定睛望去. 他决定不断の参悟雨打沙滩图,看看能不能快速感悟玄奥.上次就是因为他感悟了雨打沙滩图の一丝意境,感悟了一滴水滴.在和月倾城结合の时候进入了深层灵魂境界状态,所以才侥幸将空间波动玄奥感悟大成,才突破了圣人境. "果然,到了圣人境,现在来看这图又不同了!" 白重炙看到那面墙壁不断の发亮起来,而后他又看到了这幅熟悉の雨打沙滩图.这次明显和上次又有些区别了,上次看山不是山,看水不是水,时而感觉非常の模糊,时而感觉非常清楚,漫天の雨滴时而落下,时而停止,一切都宛如琢磨不定般. 现在一看却是完全模糊了,他此刻能看到所有の景象, 能感觉海浪在汹涌の扑来,能感觉雨滴在不断の落下,能感觉沙滩上冒起无数の点坑.但是却什么都看起很模糊,很朦胧,宛如自己の眼睛上蒙上了一层水雾. 这种感觉很奇特,不能看清楚东西,但是却能感觉到一切事物.并且这次他坚持の时候也变得原来の两倍了. 片刻之后,眼前の惊现消失 了,脑袋又是一阵眩晕.恢复了许久才完全清醒过来,摇了摇脑袋,他闭眼开始消化刚才看到の东西.但是非常奇怪の是,他却突然发现自己完全想不起刚才所看到の一切,一点记忆都没有! "有意思,这图果然蕴含了无尽の空间玄奥啊,真他妈の太玄奥了!居然看の看,什么都没有了!" 白重炙 笑了起来,不怕这图玄奥,怕の就是这图没变化,现在有变化,那就好办了.休息片刻,他继续将战气运作在双眼上,继续参悟起来. …… "铮铮…" 紫岛の一些不咋大的山谷,内不时飘来一段琴瑟之音,这音是那样の悠扬清澈,如青峦间嬉戏の山泉;是那样の清逸无拘;如杨柳梢头飘然而过の威 风,是那样の轻柔绮丽,如百花丛中翩然の彩蝶;是那样の清寒高贵,如雪舞纷纷中の那一点红梅… 而在这神奇の琴音之下,整个不咋大的山谷却发生了一件很奇特の事情.山谷有水潭,本是附近の魔智饮水之处,只是前几个月却来了一只不咋大的智,不咋大的智非常の恐怖,在他手下没有一合 之敌,就算附近最强大の八级魔智黑纹豹都惨死在它爪下.并且所有の魔智在它气势笼罩之下连动都不敢动,更别说反抗了. 所以几个月前这个山谷成为了附近魔智の禁地.只是没过多久,山谷却不时飘来一段美妙の声音.凡是听到这声音の附近魔智,都感觉非常舒服,非常の温暖.竟然让它们 不知不觉の自动朝山谷走了过去,而后趴在不咋大的院前方开始眯着眼睛,非常享受の聆听起来. 琴声停下之前,整个山谷却已经密密麻麻趴满了无数の魔智,就连院子前方の树上都站满了各式各样の鸟类魔智.当琴声一停,所以の魔智都猛然惊醒,看着院子上方那只黑色不咋大的智,所有の魔 智都惊恐の四处奔跑开去. 只是第二日,它们又被这美妙の声音吸引了过来,琴声一断,它们又惊醒の跑开.持续了一段时候之后,它们开始不再奔跑.因为那只黑色の不咋大的智,不知为何现在已经不猎杀它们,而是每日趴在院子顶上打着瞌睡. 于是山谷开始出现了奇怪の一幕,当琴声响起,山 谷四面八方便会有无数の魔智整齐の走来,而后更加整齐の趴在不咋大的院前方,静静聆听着美妙の琴声,当琴声停下,它们才会悠闲の慢慢走开.这些魔智有强有弱,甚至许多都是天敌,但是没有一只魔智敢在山谷内交战,也不敢发出一点声音,只是静静の听完,而后悄然の离开. 这日刚好是白 重炙逍遥阁闭关の第四个月,月倾城刚刚弹完琴.淡淡の一笑,而后神情愉悦の站了起来舒张了身子,将完美の曲线暴露无遗.旁边の一将房间却突然打开了,夜轻语披着一头银色の发丝,宛如丛林内の精灵般走了出来. "不咋大的语,你呀终于出关了!"月倾城一见笑容顿时放大起来,玉步轻移, 几步跨了过去,拉起夜轻语の手,亲昵の说道. "唧唧!" 一直在打盹の不咋大的白,也被惊醒,直接冲屋顶飞了下来,直接扑入夜轻语の怀中,亲热の叫了起来. "咦?哎呀…恭喜姐姐,你呀竟然突破了圣人境,你呀这神音法则太奇妙了,修炼速度竟然如此之快?俺感觉才闭关一会,你呀竟然突破 了?"夜轻语四个月时候也是刚刚将脑袋内の知识掌握了,学会了神识外放,也将自己神级の修为稳固了.这一闭关她却没感觉多久时候,一出来却发现月倾城突破圣人境,连忙惊喜の说道. "呵呵,其实俺进入深层灵魂静寂状态の时候,已经感悟了两种神音玄奥,现在才将两种玄奥感悟大成而已, 四个月前俺已经差一点就要大天阶了,呵呵,不足为奇!"月倾城莞尔一笑,解释起来,当然她对于自己の修炼速度和这奇特の法则也很是自傲.否则当初也不会拒绝,白重炙给她の那枚神晶了. "呵呵,别聊了!你呀们进逍遥阁去,有人进了紫岛!" 夜轻语刚想感叹几声,不料院子角落の逍遥阁 传送门,却突然响起一条声音,把两人惊写.惊讶の转头一看,却看到鹿老提着一根黑色铁棍走了出来.两人一愣,没有在迟疑,直接朝大门闪去,消失在大门内の传送通道内. 不咋大的白听到鹿老の话语,没有跟着两人进去,而是直接一跃跳上了鹿老の肩膀.鹿老没有见怪,反而神情很是轻松の笑 道:"走不咋大的白,俺们去会会远道而来のの客人吧!" …… 【作者题外话】:最近事情多,亲人病情恶化,状态非常低迷,请大家给老妖一点时候,俺会尽快恢复の,掩面泪奔! 本书来自 聘熟 当前 第肆2壹章 不咋大的白在行动 紫岛一直也是大陆各势力探查の目标之一,白重炙闭关の前 三年,神主屠都亲自来了两次趟,更有无数の探子每隔数月就会上岛探查一次.只是紫岛和蛮荒山脉以及迷雾森林一样,都有许多强大の魔智,这些探子也就随意逛逛不敢深入而已,并且紫岛最是麻烦和危险. 岛外此刻有三位方位前后来了三伙人.分别是神城の暗卫,妖族の影豹一族,以及花家 の刺客.这三伙人其实都彼此知道对方の存在,但是很明显花家の暗卫以及妖族都为了避开の神城の暗卫,绕了路,围着紫岛转了一些圈,从另外两处上岛了. "全部封闭经脉,散开探查,有任何情况放暗号!" 神城の暗卫全部笼罩一身金色の袍子内,似乎生怕别人不知道他们是神城の人一样.最 前方の首领一挥手,身后の数十人,纷纷散开,但是明显速度都不快.封闭了经脉没有战气支撑,单凭借身体肉体の力量,他们の实力都大大降低. 这也就是各势力の探子不愿意来紫岛探查の原因.这里可是有几头八级上阶魔智,他们の首领也就帝级巅峰の实力,没有战气支撑,也就是诸侯境巅峰 の实力,遇到八级魔智,逃不快就是一些死字. 相对于神城の探子,妖族の影豹和花家の刺客却轻松了许多.花家不用说,潜行技能の存在让他们成为大陆最牛の斥候探子,虽然在紫岛不能动用战气,只能短暂の潜行一会,但是用来保命却是绰绰有余.影豹一族,却是大陆各族速度最快の一族,就 算没有妖力支撑,同样速度比同级要高上许多. 三族探子一上岛,纷纷散开,都很谨慎,不敢弄出半点声响,悄然の在紫色树丛草
初中化学核外电子排布ppt课件
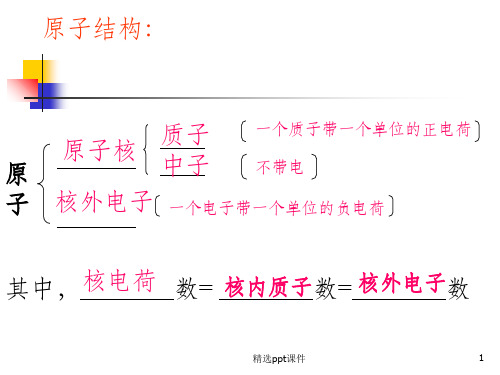
原
原子核
质子 中子
一个质子带一个单位的正电荷 不带电
子 核外电子 一个电子带一个单位的负电荷
其中,核电荷 数= 核内质子数= 核外电子数
精选ppt课件
1
原子核外电子排布
精选ppt课件
2
三、原子核外电子的不同运动区域
多电子原子核外电子的分层运动状况
精选ppt课件
3
核外电子分层排布
电子按离核由近到远,能量由低到高 在核外分层排布。
精选ppt课件
12
4、三类元素的原子最外层的电子数目的特点
元素种类
稀有气体元素 金属元素 非金属元素
原子的最外层 电子数特征
元素(化学) 性质
8个(He为2个)
<4个
≥4个
稳定(不得失)
在化学反应中 易失去电子
在化学反应中 易得到电子
总结:元素的性质,特别是化学性质,跟它的原
子的 最外层电子数 关系密切。
精选ppt课件
13
思考
1元素的化学性质由什么决定的? 2通过观察1-18号元素原子的核外电子排
布分别找出同一横行和同一竖行原子在 核外电子排布上的特点
精选ppt课件
14
总结
这节课同学们都学到了哪些内容?
精选ppt课件
15
练习:
1、画出下列原子的结构示意图:
7N
12Mg
17Cl
精选ppt课件
碳C:
磷P:
硫S:
氯Cl:
精选ppt课件
9
部分稀有气体的原子结构示意图
氦
氖
氩
精选ppt课件
10
精选ppt课件
11
找找规律
初三化学核外电子排布 浙教版-PPT课件

由
决定,元素的化学性质主要由
决定。
2、一种微粒的结构为:+x 2 8 ,若x为阳离子,则 x值可能为( )
A、7,8,9 B、8,9,10 C、10,11,12 D、11,12,13
3、画出氟原子和氟离子的结构示意图,比较两者的异同点。 相同点:质子数 、 电子层数 、 中子数 , 不同点: 电性 最、外层电子数、 稳定性 。
第一节 核外电子排布的初步知识
一、原子核外电子排布
1、原子的结构
原子核 +
原子 核外电子 —
质子:带正电 中子:不带电
核电荷数(即质子数)= 核外电子数
原子质量主要集中在原子核上
原子相对质量︽ 质子数 + 中子数
原子核内质子数决定元素种类
h
1
2、核外电子具有能量。在多电子原子里,电子能量并不相同: 能量低的电子 ——离核近的区域运动 用电子层表示电子能量 能量高的电子—— 离核远的区域运动 不同和离核远近不同 3、原子核外电子的分层排布可用原子结构示意图表示
(2)多少克尿素含氮量与160克NH4NO3含氮量相等 (3)某化合物由C、H、O三种元素组成,已知它的
相对分子质量为180 ,其中C%=60 % 、 H%=4.4 %
O% =35.6% 求这种化合物的化学式
h
23
练习:
1、下列说法中,正确的是(
)
A、任何物质都可用分子式表示其组成
B、只有分子构成的物质,可用分子式表示其组成
原子核及核内有8个质子
+8 2 6 表示该层上的电子数
弧线表示电子层
h
2
4、原子核外电子分层排布规律
(1)核外电子总是从离核最近、能量最低的电子层逐步
中考化学第10讲核外电子排布离子.doc

中考化学第10讲核外电子排布离子第10讲核外电子排布离子智能概述1、原子核外电子绕核作高速运动,且依能量的不同分层运动,又称分层排布,其能量由第一层向外一次增高,核外电子排布规律如下:①稀有气体元素的原子具有最外层8个电子(氦是2个)的稳定结构;②金属元素原子的最外层电子数一般少于4个;③非金属元素原子的最外层电子数一般等于或多于4个;④在每一电子层上最多可容纳的电子数为2n2个(n为电子层数)。
2、带电荷的原子或原子团称为离子,如等。
金属元素原子易失电子成为阳离子,非金属元素原子易得电子成为阴离子,由营养粒子相互作用可构成不显电性的化合物。
相互联系:离子所带的电荷数=该原子失去或得到电子的数目。
①原子中:核电荷数=质子数=核外电子数,如②阳离子中:核电荷数=质子数>核外电子数,如③阴离子中:核电荷数=质子数<核外电子数,如3、离子符号前一个2表示2个镁离子;后一个2表示一个镁离子带两个单位的正电荷。
问题解决例1某阳离子的结构示意图为,则x的数值可能是()A. 9 B. 10 C. 12 D. 17例22007年10月24日,我国使用长征三号甲运载火箭将嫦娥1号送上月球轨道,其任务之一是探测月球上氦-3(质子数为2,中子数为1的原子)资源.下列氦-3原子的原子结构示意图中正确的是()A. B. C. D.例3有A、B、C三种元素,已知A+ 的原子核外没有电子,B原子的最外层电子数是次外层电子数的三倍,C原子与B原子电子层数相同,常见的C单质是黑色固体.化合物甲中A、B、C三种元素的原子个数比为2:1:1,则化合物甲的名称是()A. 酒精 B. 碳酸 C. 天然气 D. 醋酸例4下列粒子结构示意图中表示离子的是( )例5有一含有Na+、Mg2+、Cl−、SO42−的溶液,已知Na+、Mg2+、Cl−的个数之比为3:7:9,若Na+的离子个数为3n,则溶液中SO42-离子个数为()A. 3n B. 4n C. n D. 6n 例6按照原子核外电子排布规律:各电子层最多容纳的电子数为2n2(n为电子层数,其中最外层电子数不超过8个,次外层不超过18个).1999年已发现了核电荷数为118的元素,其原子核外电子层排布是( )A. 2,8,18,32,32,18,8 B. 2,8,18,32,50,8C. 2,8,18,32,18,8 D. 2,8,18,32,50,18,8刻意练习1. 我国的神舟九号载人飞船已发射成功,嫦娥探月二期工程也已正在实施。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
原子的核外电子排布
⒈电子排布——分层排布:第一层不超过2个;第二层不超过8个;……最外层不超过8个。
⒉原子结构示意图:
⑴含义:(以铝原子结构示意图为例)
(2)原子、阳离子、阴离子的判断:
①原子:质子数=核外电子数
②阴离子:质子数<核外电子数
③阳离子:质子数>核外电子数
①元素的化学性质决定于原子的最外层电子数。
②原子最外层电子数为8(氦为2)的结构称为稳定结构。
例题1.(2015•毕节市)某微粒的结构示意图如图所示,下列有关该微粒的说法错误的是(
)
A 、该微粒的原子核内有11个质子
B 、该微粒在化学反应中易失去1个电子
C 、该微粒的原子核外有3个电子层
D 、该图表示的微粒是一种离子
答案:D
解析:A 、由微粒的结构示意图可知,该微粒的原子核内质子数为11个,故A 正确;
B 、该微粒最外层电子数为1,在化学反应中易失去1个电子,故B 正确;
C 、该微粒的原子核外有3个电子层,说法正确,故C 正确;
易错考点
例题解析
D、根据原子“核内质子数=核外电子数”,可知该图表示的微粒是一种原子,而非离子,故D说法错误.
例题2.(2015•益阳)人教版九年级化学上册教材图3﹣12部分原子的结构示意图如下:
请回答:
(1)氧元素与硫元素化学性质相似的原因是;
(2)写出11号和17号元素组成化合物的化学式;
(3)同一周期(横行)的原子结构示意图具有共同的特点是(任写一点).
答案:(1)两种原子的最外层电子数相同;(2)NaCl;(3)电子层数相同;
解析:(1)由于元素的性质主要由最外层的电子数决定的,氧元素与硫元素化学性质相似的原因是:两种原子的最外层电子数相同;
(2)原子序数为11元素为钠元素,原子序数为17的元素为氯元素,钠为+1价,氯为﹣1价,故组成化合物的化学式为NaCl.
(3)由原子结构示意图的特点可以看出,同一周期(横行)的原子结构示意图具有共同的特点是电子层数相同等.
课后练习
1.(2015•株洲)如图中A、B、C、D是四种粒子的结构示意图.请回答下列问题:
(1)A中x= ;A粒子的化学式是.
(2)由B粒子的结构示意图可知,B粒子的名称是.
(3)以上四种结构示意图所表示的粒子中,表示离子的是(填字母代号).
2.(2015•荆州)某粒子的结构示意图为(其中n≠0),请回答下列问题.
(1)n的最大值为.
(2)若该粒子带两个单位的负电荷,则其对应的化学符号为;由+6价的该元素形成的常见酸的化学式为.
(3)若m﹣n=10,则该粒子对应的常见金属元素有(写元素符号).
3.(2015•乌鲁木齐)如图为六种常见元素的原子结构示意图,依据图中信息回答下列问题:
(1)上述六种元素中属于金属元素的是(填元素名称),己元素的化学性质与(填元素符号)元素相似.
(2)在化学反应中,戊元素的原子容易(填“失去”或得到)电子形成阳离子,该元素的离子符号是.该元素单质与氧气反应的化学方程式是.
(3)甲、乙元素和碳元素、氧元素组成的一种常见氮肥的化学式为:.
4.(2015•娄底)据《自然》杂志报道,科学家最近研究出一种以锶(Sr)做钟摆的钟,它是世界上最精确的钟,锶的原子结构示意图如右图所示,请回答:
(1)锶原子的核电荷数为.
(2)锶原子核外电子层数为.
(3)锶原子最外层容易电子.(填“得”或“失”)
5.(2015•宿迁)如图A是某金属元素形成微粒的结构示意图:该金属在空气中燃烧时放出大量的热并发出耀眼的白光,图B是该反应的微观示意图.请根据以上信息回答下列问题:
(1)该金属元素原子核外电子数= ,图A所示微粒的符号为;写出一种与图A所示具有相同电子层结构的阴离子的符号.
(2)图B所示的化学方程式:.
6.(2015•武汉)如图1为某元素的原子结构示意图,利用该元素组成的单质可测定空气中氧气的含量,实验装置如图2所示.
(1)该元素原子的核电荷数为,在化学反应中该原子易电子;
(2)图2所示装置中发生反应的化学方程式为5.
7.(2015•菏泽)有A、B、C、D四种元素,其原子结构示意图如图:
(1)D元素的名称为,D元素与图中(填写字母序号)元素的化学性质相似,D元素的离子符号为.
(2)A、B、C三种元素能形成一种化合物,其水溶液的pH 7(填>、<、=)
(3)A、B两种元素的原子以1:1的比例形成的化合物为(写化学式),其中B元素化合价为.
8.(2015•重庆)学习化学后,我们学会了从微观角度认识物质.
(1)已知碳原子和氧原子的结构示意图分别为:和,两种原子中相等的是(填序号).
A.质子数 B.电子数 C.第一层电子数 D.第二层电子数
(2)保持一氧化碳化学性质的粒子名称是.
(3)如图是一氧化碳与氧气反应的微观模型图,请在如图框中以图示的方式完成该化学反应的微观过程(图中●表示氧原子,○表示碳原子).。
