有机化学第十一章 酮和醛
有机化学第五版第十一章醛和酮课后习题答案

第十一章醛和酮习题答案最新版1. 用系统命名法命名下列醛、酮;解:1 2-甲基-3-戊酮24-甲基-2-乙基己醛3反-4己烯醛4Z-3-甲基-2庚烯-5-炔-4-酮53-甲氧基-4-羟基苯甲醛 6对甲氧基苯乙酮7反-2-甲基环己基甲醛83R-3-溴-2-丁酮93-甲酰基戊二醛10螺癸-8-酮2. 比较下列羰基化合物与HCN加成时的平衡常数K值大小;1Ph2CO 2PhCOCH3 3Cl3CHO 4ClCH2CHO5PhCHO6CH3CHO解:1<2<5<6<4<3原因: HCN对羰基加成是亲核加成,能降低羰基碳原子上电子云密度的结构因素将会使K值增大,故K值顺序是:6<4<3,而羰基碳原子的空间位阻愈小,则K值增大,故K 值的顺序是:1<2<5<6 ,综合考虑:则K值顺序是:1<2<5<6<4<3;6. 完成下列反应式对于有2种产物的请标明主次产物;解:7. 鉴别下列化合物:解:或12. 如何实现下列转变解:13. 以甲苯及必要的试剂合成下列化合物;解:1214. 以苯及不超过2个碳的有机物合成下列化合物;解:2解:18. 化合物F,分子式为C10H16O,能发生银镜反应,F对220 nm紫外线有强烈吸收,核磁共振数据表明F分子中有三个甲基,双键上的氢原子的核磁共振信号互相间无偶合作用,F经臭氧化还原水解后得等物质的量的乙二醛、丙酮和化合物G,G分子式为C5H8O2,G能发生银镜反应和碘仿反应;试推出化合物F和G的合理结构;解:19. 化合物A,分子式为C6H12O3其IR谱在1710 cm-1有强吸收峰,当用I2-NaOH处理时能生成黄色沉淀,但不能与托伦试剂生成银镜,然而,在先经稀硝酸处理后,再与托伦试剂作用下,有银镜生成;A的I HNMR 谱如下: δ s,3H,δ d, 2H , δs,6H , δt,1H;试推测其结构;解:20. 某化合物A,分子式为C5H12O,具有光学活性,当用K2Cr2O7氧化时得到没有旋光的B,分子式为 C5H10O,B与CH3CH2CH2MgBr作用后水解生成化合物C,C能被拆分为对映体;试推测A、B、C结构;解:2013-4-9。
有机化学 第十一章 醛酮(1)

E1
E2
19
四. 化学性质(C.P.)
结构分析 讨论1: 比较苯酚C-O与醛酮C=O的结构? C杂化形式 苯酚 醛酮 sp2 sp2 O杂化形式 sp2 sp2(国外)
H H
C O
H
C O
H
20
结构分析 讨论1: 比较苯酚C-O与醛酮C=O的结构?
H
H
C O
H
+
-
C O
H
C
H
O
H
O O CH3 C CH2 C CH3
14
2. 命名
普通命名法
醛:αβγδ… 标记取代基位置
CH3CHCH2CHO CH3 CH3OCH2CH2CH2CHO CH=CHCHO
-甲基丁醛
γ-甲氧基丁醛
-苯基丙烯醛
酮:某某基酮(与醚相似)
O CH 3 C HC CH 3
O CH2 CH C CH3
O C CH3
CH3
甲基异丙基酮
甲基乙烯基酮
苯基甲基酮 15
2. 命名
系统命名法
脂肪醛酮:选含羰基(位次小)的最长C链为母体,称某醛(酮);
O CH3CH2CHCH2C CH2CH3 CH3
5-甲基-3-庚酮
当主链中有 C=C 时,称烯醛或烯酮;
O CH2 CH C CH3
O (CH3)2CHCHCH=CHCCH3 Cl 6-甲基-5-氯-3-庚烯-2-酮
加酸反应速率减小,加入大量酸,放许多天也不反应。
● 反应条件:碱催化
● 增碳的反应:制备增1个C的羧酸
● 范围: 醛、大多数甲基酮
28
(一) 羰基的亲核加成 1. 与氢氰酸加成
大学有机化学重点知识总结第十一章 醛、酮
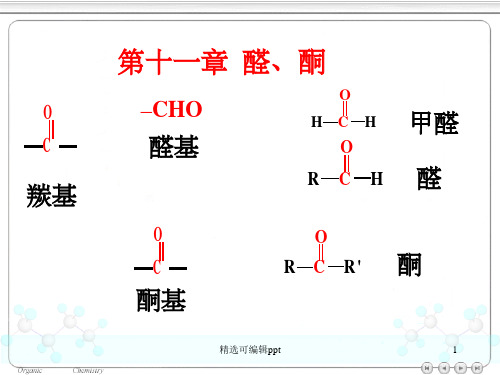
—制备增加2个C原子的伯醇:
+
H2C CH2
-+
RM gBr
O -
(C2H5)2O
R C H 2 C H 2 O M g B r
H 3O + H O C H 2C H 2R
精选可编辑ppt
42
33.
CH3 ( NBS )
CH2Br
Mg
(
干醚
CH2MgBr )
① O / 干醚
(
② H3O+
CH2CH2CH2OH )
R C O R '+H 2 O H +
R CO +2 R 'O H
(R '')HO R '
(R '')H
精选可编辑ppt
33
H +
O O C H 3
( )+ ( )
O
CH2CH2CH2CH CH3OH
HO
O
O
O
C OCH3 H
O O
C OCH3
H OC H2CH 2OH
精选可编辑ppt
34
(3)活性:醛>酮 酮一般用原甲酸三乙酯形成缩酮
O C
羰基
第十一章 醛、酮
–CHO
醛基
O HCH
O
RCH
甲醛 醛
O
C
酮基
O
R C R' 酮
精选可编辑ppt
1
烃基
脂肪族醛和酮 芳香族醛和酮
醛和酮
饱和醛和酮
的分类 烃基是否饱和 不饱和醛和酮
一元醛和酮
羰基个数 二元醛和酮
多元醛和酮
有机化学第十一章 醛酮

NaCl + SO2↑ + H2O
Na2CO3 NaHCO3 + Na2SO3
(C)转化成α-羟基腈 α-羟基磺酸钠与NaCN作用,其磺酸基则被氰基取代生成α-
羟基腈。如:
CHO NaHSO3
OH C
Na C N
SO3Na
OH C
CN
HCl H2O
OH C
COOH
优点:可以避免使用易挥发、有毒的HCN,且产率较高。
O
O
CH3-C-CH2-C-CH3
2,4 戊二酮
H3C O
3 甲基环戊酮
练习
命名下列化合物。
O CH3 CH3CCH2C=CH2
4-甲基-4-戊烯-2-酮
CH3CHCH2CHO OH
3-羟基丁醛
O CH3CHCH2CCH3
Cl
4-氯-2-戊酮
O CCH3
CHO
CHO
苯乙酮
CH2CHO
苯甲醛
CH3
3-甲基苯甲醛
= = R
++ δ
δ
R δ+ δ
CO >
CO
H
R
羰基碳原子连有基团的体积↑,空间位阻↑,不利于亲核试剂
进攻,达到过渡状态所需活化能↑,故反应活性相对↓。
综上所述,下列醛、酮进行亲核加成的相对活性为:
Cl3C C=O
H
> C=O
> CH3 C=O
R
> C=O
Ar
> C=O
>
H
H
H
H
H
= CH3 C O >
α -二醛或酮:两个羰基直接相连。 β -二醛或酮:两个羰基间隔一个碳原子。
第十一章 醛和酮
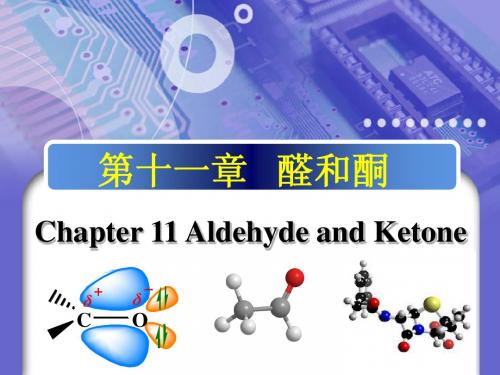
SO 3Na CH 3CH 2CH 2CHO +NaHSO 3 CH 3CH 2CH 2CH OH
SO 3Na Na 2CO 3 CH 3CH 2CH 2CH CH 3 CH 2CH 2CHO +Na 2SO 3 +NaHCO 3 H 2O OH
第十一章 醛和酮
Chapter 11 Aldehyde and Ketone
δ
+
δ
C
O
Company Logo
Contents
1
醛和酮的分类和命名★
醛和酮的物理性质◎
2
3 4
2
醛和酮的化学性质★
醛和酮的制备◎
Company Logo
第一节 醛和酮的分类和命名
醛和酮均含有羰基的化合物
O C
羰基碳原子上同时连有两个烃基的叫酮 羰基碳原子上至少连有一个氢原子的叫醛。
27
6、CH 3CC 6H 5 O
7、C 6H 5CHO
O
3>2>1>8>7>4>5>6
Company Logo
第三节 醛和酮的化学性质 2、与亚硫酸氢钠加成
醛酮与饱和(40%)亚硫酸氢钠溶液作用,很快 生成白色沉淀物。
R (R')H HO C =O + :S O Na
R C (R')H
OH SO3Na
-羟基磺酸钠易溶于水,不溶于饱和亚硫酸
氢钠,而是以白色晶体析出。
28
=
O
α- 羟基磺酸钠
Company Logo
第三节 醛和酮的化学性质
(1) 反应的应用范围:★ 所有的醛、脂肪族甲基酮、≤C8的环酮 (2) 应用: (A) 用于定性鉴别★ α-羟基磺酸钠易溶于水,但不溶于饱和的 NaHSO3溶液而析出无色针状结晶,故可定性 鉴别。
大学有机化学第11章__醛和酮

O C CH3
苯乙酮
(乙酰苯)
共九十一页
2)系统(xìtǒng)命名 法
O
5
CH3
CH3CH2-C-CH2-CH-CH2CH3
CH3-CH-CH2CH2CHO
HO-CH-CH3
6
4-甲基戊醛
5-乙基-6-羟基 3-庚酮
- (qiǎngjī)
共九十一页
C H 3
C H O
C H 2 C H 2 C H C H O O H C C H 2 C H C H 2 C H O
共九十一页
加成-消除(xiāochú)历程
R’
R—C=O + H2N—G
H+
R’ R-C — N—G
H+ -H2O
R’ R-C=N—G
OH H
(N-取代(qǔdài)亚胺)
这种加成-消除实际上可以看成由分子间脱去一分子水:
R’
R—C=O + H2 N—G
R’ R-C=N—G + H2O
共九十一页
加成-缩合产物(chǎnwù)的结构及名称:
加成-缩合产物的结构(jiégòu)及名称:
R’ R—C=O +
R’
H2N—R H2N—OH
R—C = N-R Schiff base R’
R—C = N-OH 肟(oxime)
H2N—NH2 H2N—NH-
O
R’
R—C=N-NH2 腙(hydrazone) R’
R-C=N-NH-C6H5 苯腙
H2N—NH-C-NH2
R’
R-C=N-NH-CO-NH2 缩氨脲
共九十一页
6) 与格氏试剂加成
有机化学第十一章
羰基化合物的活性次序(电子效应和空间效应): 羰基化合物的活性次序(电子效应和空间效应):
HCHO > CH3CHO > ArCHO > CH3COCH3 > CH3COR> CH3COAr > RCOR' > ArCOAr'
O 2N CHO > CHO
>
H 3C
CHO
1、与HCN的加成 、 的加成
维纶
4、与金属有机试剂的加成 、
(1)格氏试剂 )格氏试剂: H2CO +
MgCl 无水 乙醚
CH2OH 64-96%
H2O CH2OMgCl H SO 2 4
CH3 无水 乙醚 CH3COPh + PhCH2MgCl PhCH2 C OMgCl Ph CH3 H2O PhCH2 C OH NH4Cl Ph 92% Grignard: 1912 Nobel Prize
异 丙 醇 铝 ,丙 酮 丙 苯,回流
80%
CHCH CCH CH2 CH3
CH3 C CH CHCH CCH CH2 CH3 O
Oppenauer氧化: 异丙醇铝是催化剂 反应中双键不受影响。 氧化: 异丙醇铝是催化剂, 反应中双键不受影响。 氧化
脱氢:醇在适当的催化剂条件下脱去一分子氢 生成醛酮。 脱氢:醇在适当的催化剂条件下脱去一分子氢,生成醛酮。
CH3OH 浓H2SO4
COOCH3
CH2 C COOCH3 CH3 90%
过氧化苯甲酰
CH2 C CH3
n
甲基丙烯酸甲酯
聚甲基丙烯酸甲酯 (有机玻璃) 有机玻璃)
2、与NaHSO3的加成 、
加成生成a-羟基磺酸钠 羟基磺酸钠: 醛和甲基酮与饱和的NaHSO3加成生成 羟基磺酸钠: 醛和甲基酮与饱和的
有机化学--第十一章 醛 和 酮
等氧化剂所氧化,例如:
常把次卤酸钠的碱溶液与醛或酮作用生成三卤甲烷的 反应称为卤仿反应。
52
如果用次碘酸钠(碘加氢氧化钠)作试剂,产生具有特殊气味的黄
色结晶的碘仿(CHI3),这个反应称为碘仿反应。可通过碘仿反应来 鉴定具有 构的醛和酮,以及 结构的醇,因为次
碘酸钠又是一个氧化剂,能将
结构的醛或酮:
结构的醇氧化成含
53
生成α-羟基腈,此法优点是可避免使用有毒的氰化氢,
而且其产率也较高。例如:
33
3.与醇加成
在干燥氯化氢或浓硫酸的作用下,一分子醛或酮与
一分子醇发生加成反应,生成的化合物分别称为半缩醛
或半缩酮。
34
半缩醛(酮)一般是不稳定的,它易分解成原来的醛
(酮),因此不易分离出来,但环状的半缩醛较稳定,能
够分离得到。例如:
当醛、酮进行加成反应时,一般是试剂带负电荷
(亲核)的部分先向羰基碳原子进攻,然后是带正电荷
(亲电)的部分加到羰基氧原子上。决定反应速率的是第 一步,即亲核的一步,所以称为亲核加成反应。
18
亲核加成反应的难易取决于羰基碳原子的亲电性的
强弱、亲核试剂亲核性的强弱,以及电子效应和空间效
应等因素。芳香族羰基化合物进行亲核加成反应困难的 原因是羰基与芳环共轭;同时芳环有较大的体积,能产
14
脂肪醛及芳醛分子中,与羰基相连接的氢在核磁共振谱中的特
征吸收峰出现在极低的低场,化学位移值δ=9~10。醛基质子的化学 位移值是很特征的,这一区域内的吸收峰可用来证实醛基(—CHO)的
存在。
15
与其它吸电基一样,羰基对于与其直接相连的碳原子上的质 子也产生一定的去屏蔽效应。
16
有机化学课件-11醛酮
R'
O2N
R C N NH
NO2
(2,4-二硝基苯腙)
H2N-B NH2NHCONH2 NH2C6H5
产物
R'
O
R C N NH C NH2 (缩氨脲)
R' R C N C6H5
(schiff碱)
由于氨的衍生物亲核性较强,除了空间位阻很大的酮(如二苯甲
酮等),几乎多数醛酮都可与氨衍生物发生加成-消去反应,产物
戊二醛
2,6-庚二酮
O
O
CH3 CCH2CH2CH2C H
CHO
COCH3
5-氧代己醛
CO2H
CO2H
对甲酰基苯甲酸 对乙酰基苯甲酸
三、物理性质:
(一)沸点: 分子间不能形成氢键,沸点远低于分子量相当的醇,但具有较大
的极性,沸点略大于RX;如:
CH3CHO
M
44
μ(D) 2.7
Bp℃ 20.2
CH3CH2OH CH3Cl
(三)亲核加成的立体化学(参见p616)
上方
R CO
R'
+ Nu-
Nu
R
R C O- + R' C O-
下方
R'
Nu
1.当醛酮羰基所在的平面为分子的对称面时,加非手性亲核试剂 时产物为外消旋体, 若加手性亲核试剂时,产物中新产生的C*构型R/S比例≠1;
例: H
OHC O + HCN
H3C
NC
H
H C OH + H3C C OH
H+ R C O + NaHSO3
R'
有机化学 第十一章 醛酮
王鹏
山东科技大学 化学与环境工程学院
• d). 制备β-羟基酸酯的Reformatsky反应:
C O + X C H2COO C2H5
Zn
OZn X C C H2COO C2H5
+
OH C C H2COO C2H5
H
• 反应先是a-卤代酸酯和锌反应生成中间体有机锌试 剂,随后的反应与格氏试剂反应相似
δ R δ+ M gX
+
δ+ C
δ O
R
C
O M gX
H 2O
R
C
OH
• 反应的实质是负电性部分与羰基碳连接,正电性部 分与氧原子结合并被氢取代
王鹏
山东科技大学 化学与环境工程学院
11.6.1 醛和酮的亲核加成
• b). 与有机锂试剂反应:制备空间位阻大的叔醇
O ( C H 3) 3 C C C ( C H 3) 3 + ( C H 3) 3 C L i
硬脂酸钴 ~130℃
C
CH3
• 该类反应的关键在于控制氧化剂的氧化强度,使其 停留在醛酮阶段
王鹏
山东科技大学 化学与环境工程学院
11.3 醛酮的制备
二、伯醇和仲醇的氧化
醇的氧化是制备醛酮的常用方法
(C H 3 ) 3 C C H 2 O H
K 2C r2O 7 H 2S O 4
△
(C H 3 ) 3 C C H O(80%)
δ
C
H Nu
O
H
反应是负电性的Nu-首先进攻羰基碳中心,得 到加成后的氧负离子之后与正电性的氢结合
王鹏
山东科技大学 化学与环境工程学院
11.6.1 醛和酮的亲核加成
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
CHO NaHSO3
CH SO3Na NaCN OH
CH
CN H2O OH HCl
COOH CH
OH
苦杏仁酸(67%)
和炔化物的加成
▪ 炔化物也是一个很强的亲核试剂,和羰基发生加成作用, 炔化锂和炔化钠是比较常用的,例如下列反应,就是在 羰基的碳原子上引入一个碳碳三键基团,在工业上具有 很大的意义。
(巴豆醛)
C5H3C4H2-3CO-2CCHH-3C1H 3 2-甲基-3-戊酮
32 1
CH=CH-CHO
3- 苯基丙烯醛
(肉桂醛)
CH3 CH-CHO
2 苯基丙醛 苯基丙醛
OO CH3C-CH 2-CCH 3
2,4- 戊二酮 戊二酮
也可用希腊字母表示靠近羰基的碳原子,其次为、、…... 例如:
• 若分子中含有苯环, 将苯环看作取代基:
12.4
醛酮的化学性质
醛酮的结构与性质的关系
亲核加成
氢化还原
O
CCH
H
-活泼H的反应 (1)烯醇化
醛的氧化
(2) -卤代(卤仿反应)
(3)醇醛缩合反应
C=C–C=O
(1)碳碳双键的亲电加成 (2)碳氧双键的亲核加成 (3),-不饱和醛酮的共轭加成 (4)还原
• 不同结构的醛、酮进行亲核加成的活性次序: 醛 > 酮
–CH2CH2CCH3
–CHO
O
4–苯基–2–丁酮
苯甲醛
• 脂环酮的命名:
=O
–CH3 2–甲基环己酮
• 若脂环连在碳链上, 将脂环看作取代基:
–CH2CH2CHO 3–环己基丙醛
–C–CH3
O 苯乙酮
12.3 醛酮的物理性质
常温下,除甲醛是气体外,,十二个碳原子以下的醛 酮是液体,高级的醛酮和芳香酮多为固体。分子一般 具有较大的极性,因此沸点比分子量相近的烃和醚要 高,但比相应的醇要低。醛酮的分子可以与水形成氢 键,低级的醛酮(四碳以下的脂肪醛酮)易溶于水, 五碳以上的醛酮,微溶或不溶于水中,而易溶于有机 溶剂中。
(2)与亚硫酸氢钠加成
醛和脂肪族甲基酮(或七元环以下的环酮)与之反应,生
成 -羟基磺酸钠
-羟基磺酸钠易溶于水,不溶于饱和亚硫酸氢钠。将醛酮与 过量的饱和亚硫酸氢钠水溶液混合在一起,醛和甲基酮很快 会有结晶析出。可以此来鉴别醛酮。
反应历程
该反应是个可逆反应,常被用来分离和提纯某些羰基化合物:
-羟基磺酸钠与等摩尔的NaCN作用,则磺酸基可被氰基取 代,生成 -羟基腈,避免用有毒的氰化氢,产率也比较高。
实验:HCN与丙酮加成,3-4小时内只有一半原料反应;
加KOH溶液,2min内即可完成反应;加酸反应速率减小,
加入大量的酸,放许多天也不发生反应。
-
▪ CN-离子为强的亲核试剂,它与羰基的加成反应历程:
•注意:由于氰化氢剧毒,易挥发。通常由氰化钠和无机酸 与醛(酮)溶液反应。pH值约为8有利于反应。 反应范围:
例1:
O
KOH
CH3CCH3 + KC≡ CH
H3C
OH CC CH3
H2
CH
Lindlar Pd
(H3C)2C CH OH
第十二章
醛和酮
12.1 醛和酮的命名 12.2 醛和酮的结构 12.3 醛和酮的制法 12.4 醛和酮的物理性质 12.5 醛和酮的化学性质 12.6 α,β-不饱和醛、酮的特性
第十二章 酮和醛
▪ 醛和酮均含有羰基官能团:
▪ 羰基碳原子上至少连有一个氢原子的叫醛: O
O
—CHO 或
叫醛基。
RC H
CH3CH2CH2CHO 正丁醛
CH3 CH3CHCH2CHO
异戊醛
O CH3CCH2CH3
甲乙酮
O CH3-C-CH=CH2 甲基乙烯基酮
CHO 苯甲醛
O C-CH 3
苯乙酮
O C-
二苯甲酮
系统命ห้องสมุดไป่ตู้法
4 32 1
CH3CHCH 2CHO CH3
3-甲基丁醛 甲基丁醛
4 3 21
CH3CH=CHCHO 2-丁烯醛
反应机理
•碱催化的反应机理
C=O Nu-
•酸催化的反应机理
Nu H+ C O-
Nu C
OH
C=O + H+
[
+ C=OH
+ C-OH
]Nu-
Nu C
OH
•醛、酮的反应活性 R C=O > R C=O > Ar C=O
H
R'
R'
(1)与氰化氢加成
(氰醇)
• 在碱性溶液中反应速度 快,在酸性溶液中反应变 慢:
• 羰基碳原子上同时连有两个烃基的叫酮。 醛
R C R' 酮
分类:
▪ 1).据分子中含羰基的数目可分为: 一元酮(醛)、二元酮(醛) ▪ 2).据烃基的饱和程度可分为:饱和酮(醛)、不饱和酮(醛) ▪ 3).据烃基的不同可分为: 脂肪酮(醛)、芳香酮(醛)、脂环酮
(醛)
▪ 3).酮又可分为: 单一酮(醛)、混合酮(醛)
所有的醛、脂肪族甲基酮、八个碳以下的环酮。
用途、意义:制备α-羟基酸、多一个碳的羧酸。
例1:
O CH3-C-H + HCN
OH-
OH CH3-CH-CN H2O/H+
OH CH3-CH-COOH
乙醛
羟基丙酸
乳酸
O
OH
例2: CH3-C-CH3 + HCN OH- CH3-C-CN CH3OH,H2SO4
H
R
Ph
R
R
C=O > C=O > C=O > C=O > C=O
H
H
H
R
Ph
影响因素: ① 空间(位阻)效应 ② –R是供电子基(+I, +C),
–Ph 对羰基的+C效应, 降低羰基碳上的正电性, 不利于
亲核试剂的进攻.
12.4.1 加成反应
烯烃的加成一般为亲电加成;
▪ 醛 酮 的 加 成 为 亲 核 加 成 , 易 于 HCN 、 NaHSO3 、 ROH 、 RMgX等发生亲核加成反应。
12.1 醛、酮的结构和命名 •(1)醛酮的结构
碳原子以sp2杂化轨道形成三个σ键,其中一个
是和氧成一个σ键,这三个键在同一平面上。
π键
R
π键
120° C
O
(H)R`
R 120° C (H)R`
R
δδ CO
O
(H)R`
sp2 结构
羰基π电子云示意图
•(2)醛酮的命名 普通命名法 酮的普通命名法是按照羰基所连接的两个烃基命名。
CH3 CH2=C-COOCH3
CH3
甲基丙烯酸甲酯
丙酮
丙酮氰醇 水解、酯化、
MMA
脱水同时进行
该类反应主要有以下两个特点。
1、反应可逆 ▪ 该反应在碱性条件下进行有利,但氰醇在碱性条件下不
稳定,易分解成原来的醛、酮和氢氰酸。因此,在制备 的后处理时,需加酸将碱除去,因为氰醇在酸性条件下 是稳定的。 2、反应活性 ▪ 该类反应羰基的活性受取代基电子效应和空间效应影响。 ▪ A.电子效应 B.空间效应
