2018年学习晶体与非晶体教材课件PPT
合集下载
高中物理 第2章 固体 第1节 晶体和非晶体课件 鲁科版选修3-3.pptx
B.同一种物质只能形成一种晶体
C.单晶体的所有物理性质都是各向异性的
D.玻璃没有确定的熔点,也没有规则的几何形状
15
解析:所有固体金属都是晶体,因而黄金也是晶体,只是因 为多晶体内部小晶粒的排列杂乱无章,才使黄金没有规则的 几何形状,A 错误;同一种物质在不同条件下可以形成多种 晶体,B 错误;单晶体的物理性质各向异性是某些物理性质 各向异性,有些物理性质各向同性,C 错误;玻璃是非晶体, 因而没有确定的熔点和规则的几何形状,D 正确。 答案:D
6
3.多晶体 (1)定义:由大量小晶粒杂乱无章地排列在一起构成的没 有规则几何形状的晶体。 (2)宏观特征:①没有规则的几何形状;②物理性质表现 为各向_同__性;③具有固定的熔点。 4.非晶体 (1)结构特点:没有规则的几何形状。 (2)物理性质:①各向同性;②没有固定的熔点;③有的 晶体与非晶体在一定条件下可以相互转化。
4
[学后自检]┄┄┄┄┄┄┄┄┄┄┄┄┄┄(小试身手)
大部分的晶体具有规则的几何形状,那么
()
A.玻璃砖是晶体
B.细盐是非晶体
C.云母片是晶体
D.新买的橡皮擦是晶体
解析:玻璃砖、橡皮擦是非晶体,它们的形状是加工而成的,
不是晶体的规则形状,而细盐、云母片均有规则的几何形状,
属晶体,故 C 正确。
答案:C
18
12
解析:由于多晶体表现为各向同性,故 A 错误;单晶体 具有天然规则的几何外形,而多晶体具有无规则的外形,固 体金属属于多晶体,B 错误;大粒盐磨成细盐是通过加工的 方法失去规则的几何外形,而非自然的结果,C 错误;因为 所有的晶体都有确定的熔点,而非晶体没有确定的熔点,D 正确。
答案:D
13
晶体与非晶体人教版高一年级化学课堂教辅PPT

化时,分子内的化学键不发生变化。
(2)离子晶体
构成离子晶体的微粒是阳离子和阴离子,微粒间作用力是离子键,一般熔点 较高。 氯化钠晶体中每个Na+周围有6个Cl-,每个Cl-周围有6个Na+,与一个Na+距离 最近且相等的Cl-围成的空间结构为正八面体,每个Na+周围与其最近且距 离相等的Na+有12个,晶体中不存在单个分子。
②金刚石晶体中,每个C原子以共价键与4个C原子紧邻,形成正四面体的结 构,整个晶体呈空间网状结构,不存在单个分子。
2.四种晶体的比较
晶体类型
实例
内部构成 微粒
ห้องสมุดไป่ตู้
离子晶体 共价晶体 氯化钠、硫酸 金刚石、 铜、氢氧化钠 二氧化硅
阴、阳离子 原子
微粒间作用力 离子键
共价键
探究二 常见的晶体类型及其结构与性质
【问题探究】 1.人们把晶体分为离子晶体、分子晶体、共价晶体的依据是什么? 提示 依据是构成晶体的微粒及微粒间的作用力。若构成晶体的微粒是阴、 阳离子,作用力是离子键,则晶体是离子晶体;若构成晶体的微粒是分子,分 子间通过分子间作用力形成晶体,则为分子晶体;若构成晶体的微粒是原子, 原子间的作用力是共价键,则晶体为共价晶体。
变式训练 1区分晶体和非晶体最可靠的科学方法是( ) A.观察外观是否规则 B.测定是否有固定的熔点 C.验证是否有各向异性 D.进行X射线衍射实验 答案 D 解析 从外形和某些物理性质可以初步鉴别晶体和非晶体,但并不一定可靠。 区分晶体和非晶体的最可靠的科学方法是对固体进行X射线衍射实验,D 项正确。
【正误判断】 判断下列说法是否正确,正确的打“√”,错误的打“×”。 (1)有规则几何外形的固体一定为晶体。( × ) (2)判断物质是否晶体可通过X射线衍射实验。( √ ) (3)晶体中的构成微粒有规则的重复排列。( √ ) (4)晶体中的金属原子、非金属原子按一定规则形成离子晶体。( × ) (5)分子依靠分子间作用力形成的晶体是分子晶体。( √ ) (6)原子间通过共价键形成的空间网状结构的晶体属于共价晶体。( √ ) (7)金属晶体的通性是能导电和传热,有延展性。( √ ) (8)液晶兼有液体和晶体的部分性质。( √ )
(2)离子晶体
构成离子晶体的微粒是阳离子和阴离子,微粒间作用力是离子键,一般熔点 较高。 氯化钠晶体中每个Na+周围有6个Cl-,每个Cl-周围有6个Na+,与一个Na+距离 最近且相等的Cl-围成的空间结构为正八面体,每个Na+周围与其最近且距 离相等的Na+有12个,晶体中不存在单个分子。
②金刚石晶体中,每个C原子以共价键与4个C原子紧邻,形成正四面体的结 构,整个晶体呈空间网状结构,不存在单个分子。
2.四种晶体的比较
晶体类型
实例
内部构成 微粒
ห้องสมุดไป่ตู้
离子晶体 共价晶体 氯化钠、硫酸 金刚石、 铜、氢氧化钠 二氧化硅
阴、阳离子 原子
微粒间作用力 离子键
共价键
探究二 常见的晶体类型及其结构与性质
【问题探究】 1.人们把晶体分为离子晶体、分子晶体、共价晶体的依据是什么? 提示 依据是构成晶体的微粒及微粒间的作用力。若构成晶体的微粒是阴、 阳离子,作用力是离子键,则晶体是离子晶体;若构成晶体的微粒是分子,分 子间通过分子间作用力形成晶体,则为分子晶体;若构成晶体的微粒是原子, 原子间的作用力是共价键,则晶体为共价晶体。
变式训练 1区分晶体和非晶体最可靠的科学方法是( ) A.观察外观是否规则 B.测定是否有固定的熔点 C.验证是否有各向异性 D.进行X射线衍射实验 答案 D 解析 从外形和某些物理性质可以初步鉴别晶体和非晶体,但并不一定可靠。 区分晶体和非晶体的最可靠的科学方法是对固体进行X射线衍射实验,D 项正确。
【正误判断】 判断下列说法是否正确,正确的打“√”,错误的打“×”。 (1)有规则几何外形的固体一定为晶体。( × ) (2)判断物质是否晶体可通过X射线衍射实验。( √ ) (3)晶体中的构成微粒有规则的重复排列。( √ ) (4)晶体中的金属原子、非金属原子按一定规则形成离子晶体。( × ) (5)分子依靠分子间作用力形成的晶体是分子晶体。( √ ) (6)原子间通过共价键形成的空间网状结构的晶体属于共价晶体。( √ ) (7)金属晶体的通性是能导电和传热,有延展性。( √ ) (8)液晶兼有液体和晶体的部分性质。( √ )
《晶体与非晶体》课件

2 信息技术
非晶体存储介质用于高密度数据存储和信息技术领域。
3 生物医学
非晶体中的玻璃状物质在生物医学中用于制备医用材料和药物传递系统。
晶体与非晶体的比较
物理性质
晶体具有周期性结构,而非晶 体没有。
制备方法
晶体通过晶体生长,非晶体通 过玻璃化或凝固法制备。
应用方向
晶体广泛应用于电子学和光电 学,而非晶体主要用于材料科 学、信息技术和生物医学。
按照结构
共价晶体、离子晶体、金属体。
晶体的物理性质
光学性质
晶体对不同波长的光有特殊的 折射、偏振、吸收和散射效应。
热学性质
晶体具有热膨胀、热导率和热 稳定性等特性。
电学性质
晶体对电场的响应和导电性能 因晶体结构和成分的不同而异。
晶体的应用
1 电子学
晶体管、半导体器件和集成电路等领域的关 键组件。
按照制备方法
熔融法、溶胶-凝胶法和蒸发法等。
按照成分
无机非晶体和有机非晶体。
非晶体的物理性质
热学性质
非晶体具有低热膨胀系数和高 热稳定性。
电学性质
非晶体的导电性取决于成分和 结构。
机械性质
非晶体具有高强度和良好的抗 划伤性能。
非晶体的应用
1 材料科学
非晶体在材料领域中用于改变材料性能和提高材料强度。
2 光电学
用于激光、光纤通信和显示器等光学器件。
3 化学
晶体结构对于化学反应的速率和选择性具有 重要影响。
4 材料科学
用于发展新材料和研究材料性质与结构之间 的关系。
什么是非晶体?
• 非晶体是没有长程有序结构的固体。 • 非晶体缺乏规则的几何形状。 • 非晶体结构缺乏周期性重复的单元。
非晶体存储介质用于高密度数据存储和信息技术领域。
3 生物医学
非晶体中的玻璃状物质在生物医学中用于制备医用材料和药物传递系统。
晶体与非晶体的比较
物理性质
晶体具有周期性结构,而非晶 体没有。
制备方法
晶体通过晶体生长,非晶体通 过玻璃化或凝固法制备。
应用方向
晶体广泛应用于电子学和光电 学,而非晶体主要用于材料科 学、信息技术和生物医学。
按照结构
共价晶体、离子晶体、金属体。
晶体的物理性质
光学性质
晶体对不同波长的光有特殊的 折射、偏振、吸收和散射效应。
热学性质
晶体具有热膨胀、热导率和热 稳定性等特性。
电学性质
晶体对电场的响应和导电性能 因晶体结构和成分的不同而异。
晶体的应用
1 电子学
晶体管、半导体器件和集成电路等领域的关 键组件。
按照制备方法
熔融法、溶胶-凝胶法和蒸发法等。
按照成分
无机非晶体和有机非晶体。
非晶体的物理性质
热学性质
非晶体具有低热膨胀系数和高 热稳定性。
电学性质
非晶体的导电性取决于成分和 结构。
机械性质
非晶体具有高强度和良好的抗 划伤性能。
非晶体的应用
1 材料科学
非晶体在材料领域中用于改变材料性能和提高材料强度。
2 光电学
用于激光、光纤通信和显示器等光学器件。
3 化学
晶体结构对于化学反应的速率和选择性具有 重要影响。
4 材料科学
用于发展新材料和研究材料性质与结构之间 的关系。
什么是非晶体?
• 非晶体是没有长程有序结构的固体。 • 非晶体缺乏规则的几何形状。 • 非晶体结构缺乏周期性重复的单元。
2018-2019学年粤教版高中物理选修3-3课件:第二章 第一节晶体和非晶体

2.下列固体中全是由晶体组成的是( A.石英、云母、明矾、食盐、雪花、铜 B.石英、玻璃、云母、铜 C.食盐、雪花、云母、硫酸铜、松香 D.蜂蜡、松香、橡胶、沥青
)
解析:玻璃、蜂蜡、松香、橡胶、沥青为非晶体. 答案:A
拓展一 对晶体和非晶体的理解
用沥青铺成的路面,冬天变硬,夏天变软,沥青是 晶体材料还是非晶体材料,列举生活中的晶体和非晶体 例子.
知识点一 单晶体和多晶体 提炼知识 1.固体分类. 固体可以分成晶体和非晶体两类,晶体本身又分为 单晶体和多晶体.
2.单晶体. (1)定义:具有规则的几何形状,各向异性,有一定 的熔点的单个晶体. (2)结构特点. ①具有规则的几何形状. ②同一种晶体各相应晶面间的夹角恒定不变.
3.多晶体. (1)定义:由许多无规则排列的小单晶粒构成的晶体. (2)三个宏观特性. ①没有规则的外形. ②具有各向同性. ③具有确定的熔点.
提示:沥青冬天变硬,夏天变软,说明它没有一定的 熔点,所以沥青是非晶体.食盐、味精、冰糖为晶体,玻 璃为非晶体.
1.单晶体、多晶体和非晶体的特点.
分类 宏观外形 物理性质
非晶体
晶 体
单晶 体
多晶 体
没有天然 ①没有固定的熔点; 规则的形 ②导电、导热、光学性 状 质表现为各向同性 ①有确定的熔点; 有天然规 ②导电、导热、光学性 则的形状 质表现为各向异性 没有天然 ①有确定的熔点; 规则的形 ②导电、导热、光学性 状 质表现为各向同性
答案:D
题后反思 1.晶体、非晶体的区分关键是看有无固定的熔点. 2.单晶体与多晶体的区分关键是看有无规则外形及 物理性质是各向异性还是各向同性.
1.(多选)如果某个固体显示出各向同性,那么下述 结论中哪个是正确的( ) B.它一定是多晶体 D.它不一定是非晶体
晶体与非晶体PPT

1.3.3 晶体的概念 晶体是内部质点在三维空间周期性重 复排列的固体。
1.4晶体结构的空间格子规律
1.4.1空间格子概念 是表示晶体结构中质点重复规律的立 体 几何图形。
1.4.2晶体结构中空间格子的选取
以NaC1为例:棱方向:重复周期0.564nm, 面对角线方向:重复周期0.399nm。
NaC1的晶体结构模型
对结构进行抽象:
首先,在结构中任选一几何点(氯离 子
或钠离子的中心,或其它任意一点);
以此点为标准,把结构中这样的点全 找
出来-等同点或相当点。
NaC1结构一个平面内 Cl- 和Na+以及相当点的分布
相当点的条件:
⑴如果原始点选在质点中心,则所有 质点的种类要相同。 ⑵相当点周围的环境要相同。即相当 点
实验
把任意形态的NaCl颗粒,置于它的过饱和 溶 液中一段时间后,都可以恢复立方体的几何 外形。 立方体外形的和任意形态的石盐,具有完全 相同的物质组成和物理、化学性质。
1.3.2晶体概念的发展
规则几何多面体外形只是晶体的一种 表
象,晶体的本质是什么呢?
下面介绍几位科学家对晶体概念由浅 入
深的认识。
针状辉锑矿晶体 (antimonite, Sb2S3)
片状云母晶体
金刚石晶体
Diamond in kimberlite
Approx. 1 x 1 x 1 cm
电气石晶体(Tourmaline)
天河石晶体 Amazonite
天河石晶体Amazonite
铁铝榴石almandine
铬钒钙铝榴石 Grossulars
长短和交角大小决定。
单位平行六面体
在三位空间移动单位平行六面体,就 可以重复出整个空间格子。
《第一节 晶体的常识》PPT课件第一课时)
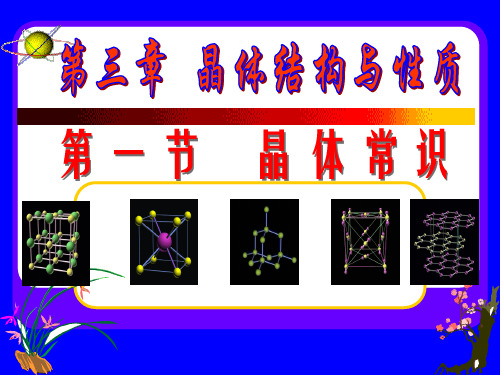
看图写化学式 C
B A
A:B:C=1:1:3
练习1:根据离子晶体的晶胞结构,判断下列 离子晶体的化学式:(A表示阳离子)
A
B
化学式: AB
练习2:根据离子晶体的晶胞结构,判断下 列离子晶体的化学式:(A表示阳离子)
A B
化学式: A2B
练习4:根据离子晶体的晶胞结构,判断下 列离子晶体的化学式:(A表示阳离子)
1、定义:晶体——具有规则几何外形的固体 非晶体——没有规则几何外形的固体 又称玻璃体 2、分类 思考
晶体
离子晶体 原子晶体 分子晶体 金属晶体
为什么晶体呈现规则 的几何外形,而非晶体 没有规则的几何外形呢? 你认为可能和什么因素 有关?
3、晶体与非晶体的本质差异
自范性 微观结构 原子在三维空间里 呈周期性有序排列 原子排列相对无序
经不同途径得到的晶体
(见教材P61图3~2)
4、晶体形成的途径
(1)熔融态物质凝固 (2)气态物质冷却不经液态直接凝固(凝华)
(3)溶质从溶液中析出
--
许多固体粉末用肉眼看不到晶体外形,但在光 学显微镜下可观察到规则的晶体外形
那么怎样判断固体是晶体还是非晶体呢?
5、晶体的特性
<1>.有规则的几何外形 (晶体内部质点和外形质点排列的高度有序性) <2> .有固定的熔沸点 <3> .各向异性(强度、导热性、光学性质等) <4>.当一波长的x-射线通过晶体时,会在记录仪上 看到分立的斑点或者普线. (教材63页图3-6)
雪 花
冰糖
金刚石
石墨
水晶石
观察图片,下列固体在外形上有什么区别?
明 矾
雪 花
选修3晶体与非晶体晶胞PPT课件

You Know, The More Powerful You Will Be
34
谢谢你的到来
学习并没有结束,希望大家继续努力
Learning Is Not Over. I Hope You Will Continue To Work Hard
演讲人:XXXXXX 时 间:XX年XX月XX日
35
25 ◆
5、某离子晶体晶胞结构如右图所示,X位于立方体 的顶点, Y位于立方体的中心,晶体中距离最近的 两个X与一个Y形成的夹角∠XYX的角度为: A. 90° B. 60° C. 120° D. 109°28′
26 ◆
7、如图是CsCl晶体的晶胞(晶体中最小的重复单元 )已知晶体中2个最近的Cs+核间距离为acm,氯化铯 的相对分子质量为M,NA为阿佛加德
6、鉴别晶体和非晶体
(1)物理性质差异 如:质点排列是否有序、各向异性,硬度、
熔点、折光率等。
(2)区分晶体和非晶体最科学的方法是对固体进行X-射线衍射实
验。
3
二﹑晶胞
1. 晶胞:描述晶体结构的基本单元(晶体中无限重复 的部分)
蜂巢与蜂室
铜晶体
铜晶胞
晶体与晶胞的关系可用蜂巢与峰室的关系比喻 然而蜂巢是有形的,晶胞是无形的,是人为划定 的。
D、固体SiO2一定是晶体 2、区别晶体与非晶体最可靠的科学方法是
A、熔沸点 B、硬度
C、颜色
D、x-射线衍射实验
D
23
3、如图所示晶体中每个阳离子A或阴离子B,均可被 另一种离子以四面体形式包围着,则该晶体对应的化 学式为
A.AB C.AB3
B.A2B D.A2B3
24 ◆
4、右面图形是石墨晶体的层面结构图, 试分析图形推测层面上每个正六边型拥有的 共价键数和碳原子数是分别: A、6,6 B、2,4 C、2,3 D、3,2
34
谢谢你的到来
学习并没有结束,希望大家继续努力
Learning Is Not Over. I Hope You Will Continue To Work Hard
演讲人:XXXXXX 时 间:XX年XX月XX日
35
25 ◆
5、某离子晶体晶胞结构如右图所示,X位于立方体 的顶点, Y位于立方体的中心,晶体中距离最近的 两个X与一个Y形成的夹角∠XYX的角度为: A. 90° B. 60° C. 120° D. 109°28′
26 ◆
7、如图是CsCl晶体的晶胞(晶体中最小的重复单元 )已知晶体中2个最近的Cs+核间距离为acm,氯化铯 的相对分子质量为M,NA为阿佛加德
6、鉴别晶体和非晶体
(1)物理性质差异 如:质点排列是否有序、各向异性,硬度、
熔点、折光率等。
(2)区分晶体和非晶体最科学的方法是对固体进行X-射线衍射实
验。
3
二﹑晶胞
1. 晶胞:描述晶体结构的基本单元(晶体中无限重复 的部分)
蜂巢与蜂室
铜晶体
铜晶胞
晶体与晶胞的关系可用蜂巢与峰室的关系比喻 然而蜂巢是有形的,晶胞是无形的,是人为划定 的。
D、固体SiO2一定是晶体 2、区别晶体与非晶体最可靠的科学方法是
A、熔沸点 B、硬度
C、颜色
D、x-射线衍射实验
D
23
3、如图所示晶体中每个阳离子A或阴离子B,均可被 另一种离子以四面体形式包围着,则该晶体对应的化 学式为
A.AB C.AB3
B.A2B D.A2B3
24 ◆
4、右面图形是石墨晶体的层面结构图, 试分析图形推测层面上每个正六边型拥有的 共价键数和碳原子数是分别: A、6,6 B、2,4 C、2,3 D、3,2
《晶体和非晶体》PPT课件

1、如图两种物质在固态时温
温 度
℃
度随时间的变化曲线。请根据
图象答复以下问题。
240
甲 D 乙
220
〔1〕由图判断出__乙_____ 图线是晶体,
200
B
C
A
180 1 2 3 4 5 6 7 时间/分
该晶体的熔点
是 210℃ ,熔化时间 是 3 分钟,另一图线的物
质可能是 非晶体 。
〔2〕温度升高的是 __A_B_、__C__D_
• 二、拓展题: 参照上表请答复为什么用铁锅能 熔化锡,而不能用锡锅熔化铁 ( )
• A.铁的密度比锡小
B. 铁比锡硬
• C.铁传热比锡快
D. 铁的熔点比锡高
• 参考答案:
• D;查表可知,铁的熔点1535℃,锡的熔点为 232℃。当锡温度到达熔点后,继续吸收热量, 但温度保持232℃不变,而这一温度低于铁的熔 点,固铁仍为固态;反之铁温度要到达1535℃熔 点时,锡早已熔化成液态了。
点〕,二是要继续吸热〔放热〕,两者缺一不可; 2〕两个物体必须有温度差才能进展热的传递.
水;但是熔化过程中,温度仍然是00C; 〔2〕当外界低于00C时,热传递只能促进水凝固成
冰,温度也不变; 〔3〕外界等于00C时,根本不发生热传递,水和冰
的比例保持不变。 当然,〔1〕和〔2〕的情况下水和冰的比例是会发生 变化的,如何变化?
1、上科学复习课时,教师写下了一副对联,上联是“杯
中冰水,水结冰冰温未降〞;下联是“盘内水冰,冰化水
晶体
非晶体
有无一定熔 (凝固) 点
温度变化 不同
熔化凝固过程 的状态不同 外形不同
共同点
有
熔化〔凝固〕时温度不变, 熔化〔凝固〕前和熔化〔凝 固〕后温度逐渐升高〔降低〕
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
如 松香 50~70℃软化,70℃以上全部熔 化
晶体的特征
各向异性 晶体的某些性质,如光学性质、力学 性质、导热、导电性、机械强度、溶 解性等在不同方向不同。
如
云母
可按纹理面方向裂成薄片
非晶体各向同性
晶体和非晶体在性质上的差异 是两者内部结构不同而造成的 晶体内部的微粒的排布是有序的,在不 同方向按确定的规律重复性地排列,造 成晶体的各向异性。 非晶体内部微粒的排列是无序的、不规律的。 石 英 玻 璃 石英晶体
晶体的内部结构
Cl- Na+ Cl+ +
Cl
晶体内部的微粒的排布是 有序的,在不同方向按确 7-1-2 晶体的内部结构 Na Cl Na 定的规律重复性地排列 . Na+
晶格点 阵
Cl
ClNa+
晶格点阵——沿一定 方向按某种规律把结 点联接起来的几何图 形. 晶格点阵可描述 晶体内部的结构
晶体的内部结构
晶格点阵 ↙结点
7-1-2晶体的内部结构
晶格点阵——沿一定方向 按某种规律把结点联接起 来的几何图形 晶格点阵可描述晶体内部 的结构
晶胞
晶胞——晶格中,能表现其结构一切特征 的最小部分。 Cl
Na+
Cl
Na+ClNa+N源自+Cl-Cl-
ClNa+ 蓝色球组成的为 该晶体的晶胞
晶格
按晶格结点在 空间的位置分 布, 晶格有各 种形状。 分为7个晶系 14种晶格类型
非晶体物质
非晶体物质——结构无序的固体物质 玻璃体为典型的非晶物质
7-1-4非晶体物质 氧化物玻璃
金属玻璃 玻璃体物质 非晶半导体 高分子化合物 在一定条件下,晶体 非晶体 迅速冷却 如 石英晶体 石英玻璃
液晶
液晶——有些有机物质熔化后在一定的温 度范围内微粒的分布仍部分地保持着长程 有序性,因而仍部分地保持各向异性,这 7-1-5 液晶 种介于液态和固态之间的各向异性凝聚流 体即为液晶。
熔点 不能流动 各向异性 清亮点 能流动 各向同性
能流动 各向异性
简单正交 底心正交 体心正交 面心正交 简单立方 体心立方 面心立方
简单四方 体心四方 简单六方 简单菱形
简单单斜 底心单斜 简单三斜
单晶体和多晶体
由一个晶核各向均匀生长而成, 单 晶体内部的粒子基本上保持其特 晶 有的排列规律。 7-1-3 单晶体和多晶体 体 如单晶冰糖、单晶硅、宝石、金刚石 晶 体 由很多单晶微粒杂乱无规则的聚 多 结而成的。 晶 各向异性的特征消失,使整体一 体 般不表现各向异性。 多数金属和合金都是多晶体。
第一节晶体与非晶体
晶体与非晶体
晶体的特征
有一定的几何外形
7-1-1晶体的特征
食盐 石英 方解石 非晶体(无定形体)——没有一定的几何外形 如玻璃、松香、石蜡 微晶体——如碳黑
晶体的特征
有固定的熔点 即晶体在熔化时温度保持不变, 直至全部熔化后,温度才开始上升。 如 冰的熔点 0℃
非晶体无固定的熔点 在加热时,由开始软化到完全熔化, 整个过程中温度不断的变化。
晶体的特征
各向异性 晶体的某些性质,如光学性质、力学 性质、导热、导电性、机械强度、溶 解性等在不同方向不同。
如
云母
可按纹理面方向裂成薄片
非晶体各向同性
晶体和非晶体在性质上的差异 是两者内部结构不同而造成的 晶体内部的微粒的排布是有序的,在不 同方向按确定的规律重复性地排列,造 成晶体的各向异性。 非晶体内部微粒的排列是无序的、不规律的。 石 英 玻 璃 石英晶体
晶体的内部结构
Cl- Na+ Cl+ +
Cl
晶体内部的微粒的排布是 有序的,在不同方向按确 7-1-2 晶体的内部结构 Na Cl Na 定的规律重复性地排列 . Na+
晶格点 阵
Cl
ClNa+
晶格点阵——沿一定 方向按某种规律把结 点联接起来的几何图 形. 晶格点阵可描述 晶体内部的结构
晶体的内部结构
晶格点阵 ↙结点
7-1-2晶体的内部结构
晶格点阵——沿一定方向 按某种规律把结点联接起 来的几何图形 晶格点阵可描述晶体内部 的结构
晶胞
晶胞——晶格中,能表现其结构一切特征 的最小部分。 Cl
Na+
Cl
Na+ClNa+N源自+Cl-Cl-
ClNa+ 蓝色球组成的为 该晶体的晶胞
晶格
按晶格结点在 空间的位置分 布, 晶格有各 种形状。 分为7个晶系 14种晶格类型
非晶体物质
非晶体物质——结构无序的固体物质 玻璃体为典型的非晶物质
7-1-4非晶体物质 氧化物玻璃
金属玻璃 玻璃体物质 非晶半导体 高分子化合物 在一定条件下,晶体 非晶体 迅速冷却 如 石英晶体 石英玻璃
液晶
液晶——有些有机物质熔化后在一定的温 度范围内微粒的分布仍部分地保持着长程 有序性,因而仍部分地保持各向异性,这 7-1-5 液晶 种介于液态和固态之间的各向异性凝聚流 体即为液晶。
熔点 不能流动 各向异性 清亮点 能流动 各向同性
能流动 各向异性
简单正交 底心正交 体心正交 面心正交 简单立方 体心立方 面心立方
简单四方 体心四方 简单六方 简单菱形
简单单斜 底心单斜 简单三斜
单晶体和多晶体
由一个晶核各向均匀生长而成, 单 晶体内部的粒子基本上保持其特 晶 有的排列规律。 7-1-3 单晶体和多晶体 体 如单晶冰糖、单晶硅、宝石、金刚石 晶 体 由很多单晶微粒杂乱无规则的聚 多 结而成的。 晶 各向异性的特征消失,使整体一 体 般不表现各向异性。 多数金属和合金都是多晶体。
第一节晶体与非晶体
晶体与非晶体
晶体的特征
有一定的几何外形
7-1-1晶体的特征
食盐 石英 方解石 非晶体(无定形体)——没有一定的几何外形 如玻璃、松香、石蜡 微晶体——如碳黑
晶体的特征
有固定的熔点 即晶体在熔化时温度保持不变, 直至全部熔化后,温度才开始上升。 如 冰的熔点 0℃
非晶体无固定的熔点 在加热时,由开始软化到完全熔化, 整个过程中温度不断的变化。
