消毒产品生产企业分类监督综合评价表
2消毒剂生产企业现场监督审核表

消毒剂生产企业
现场监督审核表
临盆企业名称_____________________
临盆企业地址_____________________
现实临盆加工地址_____________________
现场监视审核日期年月日
消毒剂临盆企业现场监视审核表
临盆企业一般情形
法定代表人/负责人:卫生治理负责人:磨练负责人:通信地址:接洽德律风:邮编:传真:
职工总数:从业人员总数:临盆区面积:
产品种类:
考评审核表:
备注:1. 本表用于消毒剂临盆.分装企业现场监视审核.
2. 知足各项合格分,现场监视审核经由过程.
现场监视审核看法:
现场监视审核人(签名):被审核单位负责人(签名):
单位公章
审核日期:年月日年月日。
WS628-2018消毒产品卫生安全评价表格

消毒产品卫生安全评价报告
产品名称:
剂型/型号:
产品责任单位名称(盖章):
评价日期:
二、评价资料
(一)标签(铭牌)、说明书;
(二)检验报告(含结论);
(三)企业标准或质量标准;
(四)国产产品生产企业卫生许可证或进口产品生产国(地区)允许生产销售的证明文件及报关单;
(五)产品配方;
(六)消毒器械结构图(主要元器件及参数)。
注 1:经营、使用单位索证时,产品责任单位提供的卫生安全评价报告资料包括标签(铭牌)、说明书、检验报告结论、国产产品生产企业卫生许可证、进口产品生产国(地区)允许生产销售的证明文件及报关单。
注 2:(一)、(三)、(四)为原件或复印件,(二)、(五)和(六)为原件。
复印件应由产品责
任单位加盖公章。
注 3:本表应使用 A4 规格纸张打印,资料按顺序排列,逐页加盖产品责任单位公章,并装订成册。
2020年消毒产品生产企业国家随机监督抽查检查表

生产条件
全部类别
生产车间布局、流程、生产设施设备是否与申报时一致
是□ 否□
第一类产品
医疗器械高水平消毒剂、灭菌剂生产用水是否符合相应要求
是□ 否□
皮肤黏膜消毒剂的净化车间和生产用水是否符合相应要求
是□ 否□
生物指示物、灭菌效果化学指示物、医疗器械高水平消毒器械、灭菌器械的生产设施是否符合相应要求
是□ 否□
第二类产品
用于皮肤黏膜的抗(抑)菌的净化车间、生产用水、生产设施是否符合相应要求
是□ 否□
第三类产品
空气消毒设施是否符合相应要求
是□ 否□
生产过程
全部类别
是否有合格的出厂检验报告
是□ 否□
是否有合格的生产记录
是□ 否□
原材料卫生质量
全部类别
是否能满足产品质量要求,符合相关质量标准和卫生行政部门的有关要求,符合企业标准要求,并能提供相应的检验报告或相应的产品质量证明材料
附表4
2020年消毒产品生产企业国家随机监督抽查检查表
企业名称:卫生许可证号:地址:
法定代表人联系人联系电话
从业人员总数:生产车间面积:
项目
风险类别
重点检查内容
检查结果
备注
卫生许可
持证情况
全部类别
法定代表人、企业名称、企业生产地址是否与实际一致
是□ 否□
生产类别、项目是否与实际一致
是□ 否□
卫生许可证是否在有效期
个
是否有未按要求进行卫生安全评价的消毒产品
是□ 否□
个
卫生安全评价报告是否均合格
是□ 否□
各评价报告内容是否完整
是□ 否□
消毒产品标签(铭牌)、说明书
消毒产品生产企业现场监督审核表(5个类别)

附件1消毒剂生产企业现场监督审核表生产企业名称_____________________生产企业地址_____________________实际生产加工地址____________________现场监督审核日期年月日消毒剂生产企业现场监督审核表生产企业一般情况法定代表人/负责人:卫生管理负责人:检验负责人:通讯地址:联系电话:邮编:传真:职工总数:从业人员总数:生产区面积:产品种类:考评审核表:234备注:1. 本表用于消毒剂生产、分装企业现场监督审核。
2. 满足各项及格分,现场监督审核通过。
现场监督审核意见:现场监督审核人(签名):被审核单位负责人(签名):单位公章审核日期:年月日年月日5附件2有净化要求的消毒剂生产企业现场监督审核表生产企业名称_____________________生产企业地址_____________________实际生产加工地址____________________现场监督审核日期年月日6有净化要求的消毒剂生产企业现场监督审核表生产企业一般情况法定代表人/负责人:卫生管理负责人:检验负责人:通讯地址:电话:邮编:传真:职工总数:从业人员总数:生产区面积:产品种类:考评审核表:789备注:1. 本表用于有净化要求的消毒剂生产、分装企业现场监督审核。
2. 满足各项及格分,现场监督审核通过。
现场监督审核意见:现场监督审核人(签名):被审核单位负责人(签名):单位公章审核日期:年月日年月日10附件3消毒器械生产企业现场监督审核表生产企业名称_____________________生产企业地址_____________________实际生产加工地址____________________现场监督审核日期年月日消毒器械生产企业现场监督审核表生产企业一般情况法定代表人/负责人:卫生管理负责人:检验负责人:通讯地址:电话:邮编:传真:职工总数:从业人员总数:生产区面积:产品种类:考评审核表:备注:1. 本表用于消毒器械生产、分装企业现场监督审核。
2消毒剂生产企业现场监督审核表

消毒剂生产企业
现场监督审核表
生产企业名称_____________________生产企业地址_____________________
实际生产加工地址_____________________
现场监督审核日期年月日
8
消毒剂生产企业现场监督审核表
生产企业一般情况
法定代表人/负责人:卫生管理负责人:检验负责人:
通讯地址:联系电话:邮编:传真:职工总数:从业人员总数:生产区面积:
产品种类:
8
考评审核表:
8
8
8
8
8
备注:1. 本表用于消毒剂生产、分装企业现场监督审核。
2. 满足各项及格分,现场监督审核通过。
现场监督审核意见:
8
现场监督审核人(签名):被审核单位负责人(签名):
单位公章审核日期:年月日年月日
8。
消毒剂生产企业监督检查表

消毒剂生产企业监督检查表
生产企业名称联系电话
生产企业地址实际生产企业地址
卫生许可证号生产方式生产□分装□生产项目第一类消毒剂□第二类消毒剂□
生产类别
消毒剂目录
卫生安全评价报告不合格产品名录:
产品标签说明书违规产品名录:
陪同检查人:检查人:检查时间:年月日
附件2
医疗卫生机构消毒产品管理自查表
单位名称(盖章):
地址:
联系电话:联系人:
医疗机构(三级□二级□一级□未定级□):疾控机构□妇幼保健机构□购进消毒剂目录
卫生安全评价报告不合格产品名录:
产品标签说明书违规产品名录:
自查时间:年月日附件3
医疗卫生机构消毒产品管理检查表
单位名称:
地址:联系电话:
联系人:
医疗机构(三级□二级□一级□未定级□):疾控机构□妇幼保健机构□购进消毒剂目录
卫生安全评价报告不合格产品名录:
产品标签说明书违规产品名录:
陪同检查人:检查人:检查时间:年月日
附件4
消毒剂生产企业检查情况汇总表
辖区消毒产品生产企业数家检查消毒剂生产企业家
填表单位(盖章):填表人:联系电话:填表日期:
附件5
填表单位(盖章):填表人:联系电话:填表日期:附件6
消毒剂专项整治案件查处汇总表
填表单位(盖章):填表人:联系电话:填表日期:。
消毒管理经常性卫生监督量化评分表
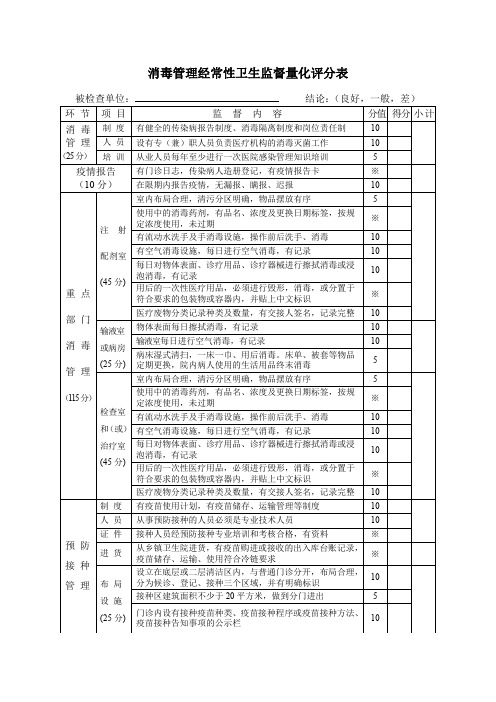
消毒管理经常性卫生监督量化评分表被检查单位:
注:一、※是关键监督项目,如果有一项不符合要求,则评为差。
二、10分、5分、2分是按风险大小及对人体健康危害大小而定的,如不符合该项不得分。
三、可以有合理缺项,但需标准化。
标化分=所得的分数除以该单位应得的最高分数×100。
四、该表只适用于村卫生室。
疫苗只能从乡镇卫生院领取,或消毒产品由乡镇卫生院统一进货的,疫苗和消毒产品的索证一项,以乡镇卫生院的为准。
得分:检查时间:年月日时标化分:
陪同人员:监督员:。
消毒产品生产企业分类监督综合评价表

附件1消毒产品生产企业分类监督综合评价表企业名称:生产地址:生产类别:□消毒剂□消毒器械□卫生用品(抗抑菌制剂除外)□抗抑菌制剂产品风险类别:□第一类□第二类□第三类生产企业卫生许可证号:卫消证字()第号生产状况:□在生产□未生产产品状况:□自有品牌□代加工标化得分:综合评价结果:优秀□合格□重点监督□未评价□评价时间:— 1 —— 2 —— 3 —— 4 —— 5 —— 6 —— 7 —— 8 —— 9 —— 10 —— 11 —— 12 —填表说明1.评价时应同时对综合管理、生产过程管理、产品卫生质量、产品抽检和其他5大项检查评分后方可对该单位进行最终的综合评价。
2.应采用标化分作为分类监督综合评价的最终得分。
标化分=实际得分/应得分×100。
实际得分为现场评价后的总得分,应得分为评价表设定的总分数(100分)减去合理缺项后的分数。
3.评价结果:(1)优秀单位:标化分大于85分、关键项合格;(2)合格单位:标化分60-85分且关键项合格;(3)重点监督单位:标化分小于60分或关键项不合格。
如检查评价为优秀单位但受到行政处罚最终评价结果降为合格单位。
4.★为关键项,如发生即认定为重点监督单位。
5.☆为重点项,此项不合格则该项目整体不得分。
6.*为合理缺项,未做监督抽检或评价的企业没有该项情况。
7.▲为从中选择一项。
8.“年度”是指自然年,本年度指1月1日至检查评价时。
上一年度指上一年1月1日至12月31日。
— 13 —— 14 —。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
消毒产品生产企业分类监督综合评价表
单位名称:___________________________________________
生产地址:_______________
生产类别:□消毒剂□消毒器械□卫生用品(抗抑菌制剂除外)□抗(抑)菌制剂产品风险类别:□第一类□第二类□第三类
许可证号:卫消证字()第号
生产状况:□营业□暂停□关闭
产品状况:□自有品牌□代加工
得分:
评价结果:优秀□合格□重点监督□
填表说明
1.评价时应同时对综合管理、生产过程管理、产品卫生质量3个大项检查评分后方可对该单位进行最终的综合评价。
2.应采用标化分作为分类监督综合评价的最终得分。
标化分=实际得分/应得分×100。
实际得分为现场评价后的总得分,应得分为评价表设定的总分数(100分)减去合理缺项后的分数。
3.评价结果:(1)优秀单位:标化分大于85分、关键项合格;(2)合格单位:标化分60-85分且关键项合格;(3)重点监督单位:标化分小于60分或关键项不合格。
如检查评价为优秀单位但受到行政处罚最终评价结果降为合格单位。
4.★为关键项,如发生即认定为重点监督单位。
5.☆为重点项,此项不合格则该项目整体不得分。
6.*为合理缺项,未做监督抽检或评价的企业没有该项情况。
7.▲为从中选择一项。
