原花色素-天然药物化学
天然药物化学

第一章 总论一.生物合成途径:醋酸-丙二酸途径(AA-MA 途径) 主要生成脂肪酸类、酚类、醌类、聚酮类等化合物。
甲戊二羟酸途径(MVA 途径)如萜类及甾体化合物桂皮酸途径及莽草酸途径 苯丙素类、香豆素类、木质素类、木脂体类。
氨基酸途径: 生物碱二. 一次代谢及二次代谢:糖、蛋白质、脂质、核酸等植物体生命活动必需物质的过程称为一次代谢过程。
此外,一次代谢产物还包括乙酰辅酶A ,丙二酸单酰辅酶A ,莽草酸及一些氨基酸等。
植物体在特定的条件下,以一些重要的一次代谢产物如乙酰辅酶A 、 丙二酸单酰辅酶A 、莽草酸及一些 氨基酸等为原料和前体,经历不同的代谢途径,生成生物碱、萜类等化合物的过程称为二次代谢过程。
天然药物提取分离方法三.聚酰胺色谱法:1.半化学吸附---聚酰胺吸附色谱法:属于氢键吸附(半化学吸附)特别适合分离酚类、醌类、黄酮类化合物。
性质:高分子聚合物不溶于常见有机溶剂对碱稳定对酸特别是无机酸稳定性差可溶于浓盐酸、冰乙酸、甲酸中2.聚酰胺的吸附原理:通过分子中的酰胺羰基与酚类、黄酮类化合物的酚羟基,或酰胺键上的游离胺基与醌类、脂肪酸上的羰基形成氢键缔合而产生吸附3.吸附强弱规律(含水溶剂中)a. 形成氢键的基团数目越多,则吸附能力越强b. 成键位置对吸附也有影响。
易形成分子内 氢键的化合物,其吸附性能减弱。
c.分子中芳香化程度越高,则吸附性能越强。
4.各种溶剂在聚酰胺柱上的洗脱能力由弱至强排序为:水→甲醇→丙酮→氢氧化钠水溶液→甲酰胺→二甲基甲酰胺→尿素水溶液5.应用:a.特别适合于酚类、黄酮类化合物的制备和分离。
b.对生物碱、萜类、甾体、糖类、氨基酸等其它极性与非极性化合物的分离也有着广泛应用。
c.用于提取物的脱鞣质处理四.酸催化水解反应苷键属于缩醛结构,易为稀酸催化水解1. 试剂:H 2SO 4, HCl (5~10%), HCOOH, F 3CCOOH, HOAC 。
2.酸水解的规律: OH OH H O OH OH OH>>OH OH OH OH OH>>H O COOH >O C OH H O⑴苷原子不同,酸水解难易顺序:N > O > S > C说明:N上有一对孤对电子易接受质子,最易水解。
天然药物化学_第五章_黄酮类化合物-1

2'
2
O A
6 5 4
C
3
1' 6' OH
10.橙酮类 Aurones
O CH
O
11. 双苯吡酮类 Xanthones
12. 高异黄酮类
Homoisoflavones
O A C B
O
O
O
(三)存在形式
黄酮类多与糖成结合成苷,可成O-苷,也有C-苷 组成黄酮苷的糖类主要有:
1.单糖:D-Glc、D-Gal、D-Xyl、L-Rha、L-Ara、D-Glu A
n-BuOH 提取物 (39g) 溶于 1500ml 水中, 加 220g Pb(OH) Ac 饱和水溶液 黄色铅盐沉淀 加 220gNaHCO3 饱和水溶液 搅拌 1h,静置,滤过 滤液 6mol/L HCl 调 pH 5.3 n-BuOH 提取(500ml×5) n-BuOH 提取物 (4.3g 粗黄酮类) 凝胶滤过(TSK gel-HW-40) Fr.A-H (pH 5 的酸洗脱部分) Fr.I-P (pH 7 的水洗脱部分) 水层
2.双糖类:槐糖 龙胆二糖 芸香糖 新陈皮糖 3. 三糖类:龙胆三糖 槐三糖 Glc β1→2 glc Glc β1→6 glc Rha α1→6 glc Rha α1→2 glc Glc β1→6 glc α1→2 fru Glc β1→2 glc β1→2 glc
返回
第二节 理化性质
一、性状
二、溶解性
4.氯化锶反应 邻二酚羟基
OH
SrCl2 OH-
绿色~棕色~黑色沉淀
Sr++ 2HO-
O Sr O
+ H 2O
OH
5.三氯化铁反应
天然药物化学名词解释 简答答案

一、解释下列名词(每题2分,共10分)1、天然药物化学:天然药物化学是运用现代科学理论与方法研究天然药物中化学成分的一门学科。
2、植物化学分类:植物生物化学,中成药成分化学,天然药物化学及植物药品化学。
植物生物化学研究一次代谢产物。
中成药成分化学,天然药物化学及植物药品化学研究二次代谢产物。
3、二次代谢:以一次代谢产生的代谢产物为原料(前体),经不同途径进一步合成的过程叫二次代谢4、次级代谢产物:二次代谢产生的结构千变万化,千奇百怪,绚丽多姿的化学物质,包括生物碱、萜类等化学物质。
作用是维持植物的特性与特征,是重要的药物资源5、pH梯度萃取法:在不同pH的缓冲溶液与有机溶剂中进行分配的方法,使酸性、碱性、中性及两性物质得以分离。
6、苷类:又称配糖体,是由糖或糖的衍生物,如氨基糖、糖醛酸等,与另一非糖物质(称为苷元或糖苷配基)通过糖的半缩醛或半缩酮羟基与苷元脱水形成的一类化合物。
7、苷的双相水解:对于那些苷元对酸不稳定的苷,为了获得原苷元可采取双相水解的方法,即在水解溶液中加入与水不互溶的有机溶剂如苯等,使水解后的苷元立即进入有机相,避免苷元长时间与酸接触。
8、原生苷与次生苷:原生苷指未经水解的苷;次生苷指原生苷由于水解或酶解,部分糖降解时所生成的苷9、苯丙素化合物:苯环与三个直链碳连在一起为单元(C6~C3)构成的化合物。
分为苯丙酸类、香豆素类、木脂素类10、萜类化合物:凡由甲戊二羟酸(MVA)衍生、且分子式符合(C5H8)n 通式的衍生物均称为萜类化合物11、生源的异戊二烯法则:甲戊二羟酸是萜类化合物生物合成的最关键前体,焦磷酸异戊烯酯(IPP)及DMAPP数生物体内的“活性的异戊二烯”,在生物合成中起延长碳链的作用12、经验的异戊二烯法则:自然界存在的萜类化合物都是由异戊二烯衍变而来,是异戊二烯的聚合体或衍生物,并以是否符合异戊二烯法则作为判断萜类物质的一个重要原则。
13、三萜皂苷:由三萜皂苷元和糖组成,常见的苷元为四环三萜和五环三萜14、甾体皂苷:具有螺甾烷类化合物结构母核的一类皂苷15、溶血指数:指在一定条件下能使血液中红细胞完全溶解的最低皂苷浓度16、强心苷:存在于植物中具有强心作用的甾体苷类化合物,由强心苷元和糖缩合而产生的一类苷17、生物碱:生物碱是含有负氧化态氮原子的有机环状化合物,存在于生物有机体中的环状化合物18、两性生物碱:具酚羟基或羧基的生物碱称为两性生物碱,这些生物碱既可溶于酸水,也可溶于碱水溶液,但在pH8~9时溶解性最差,易产生沉淀。
天然药物化学---黄酮类化合物(药大版)
OH
7.68
OH
6.82 7.51
HO
6.18
6.33
O
OGlc 6 Rha OH O
7
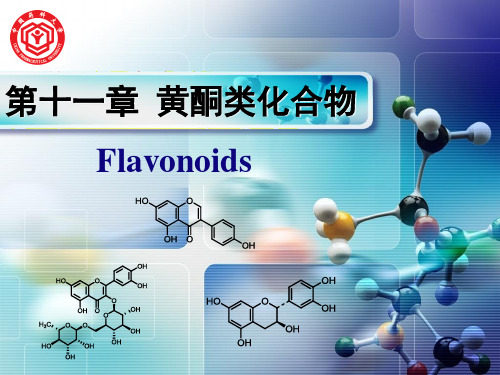
例题3 例题3
从中药黄芩中得一黄色针晶, 摄氏度( 从中药黄芩中得一黄色针晶,mp300-2摄氏度(丙酮), 摄氏度 丙酮), FeCl3反应阳性,HCl-Mg反应阳性,Molish反应阴性, 反应阳性, 反应阳性, 反应阴性, 反应阳性 反应阴性 ZrOCl2反应黄色,加枸橼酸黄色消退,Gibbs反应阴性, 反应黄色,加枸橼酸黄色消退, 反应阴性, 反应阴性 SrCl2反应阴性。EI-MS给出分子量 。其光谱数据如下: 反应阴性。 给出分子量300。其光谱数据如下: 给出分子量 UV(λmax): MeOH 277, 328 NaOMe 284, 300, 400 NaOAc 284, 390 AlCl3 264sh, 284, 312, 353, 400 (DMSO-d6)δ: 12.35(1H, s), 7.81 (2H, d, J = 9 Hz), 6.87 (2H, d, J = 9 Hz), 6.68 (1H, s), 6.20 (1H, s), 3.82 (3H, s)。 。
2
黄酮类化合物的结构鉴定
一 色谱法的检识 二 紫外光谱 三 1H-NMR 四
13C-NMR
五 质谱
3
习题1 习题1
甲醇), 粉反应呈阳性。 谱显示 黄色粉末 (甲醇 ,HCl-Mg粉反应呈阳性。IR谱显示 甲醇 粉反应呈阳性 、 、 有羟基 (3334 cm–1)、共轭羰基 (1656 cm–1)、苯环 (1613,1506 cm–1) 吸收峰。ESI–MS m/z 329 [M– , 吸收峰。 H]-,314 ,299 。
天然药物化学名词解释(最新整理)

天然药化1.pH梯度萃取法:是指在分离过程中,逐渐改变溶剂的pH酸碱度来萃取有效成分或去除杂质的方法。
2.有效成分:存在于生物体中,具有一定生物活性,具有防病治病作用,可以用分子式和结构式表示,并具有一定物理常数的单体化合物。
3.盐析法:在水提取液中加入无机盐(如氯化钠)达到一定浓度时,使水溶性较小的成分沉淀析出,而与水溶性较大的成分分离的方法。
5.渗漉法:将药材粗粉用适当溶剂湿润膨胀后(多用乙醇),装入渗漉筒中从上边添加溶剂,从下口收集流出液的方法。
6.原生苷:植物体内原存形式的苷。
次生苷:是原生苷经过水解去掉部分糖生成的苷。
7.酶解:苷类物质在酶催化下水解生成次生苷的一种水解方法。
8.苷类:又称配糖体,是糖和糖的衍生物与另一非糖物质通过糖的端基碳原子连接而成的化合物。
9.苷化位移:糖苷化后,端基碳和苷元α-C化学位移值均向低场移动,而邻碳稍向高场移动(偶而也有向低场移动的),对其余碳的影响不大,这种苷化前后的化学变化,称苷化位移。
10.香豆素:为顺式邻羟基桂皮酸的内酯,具有苯骈α-吡喃酮基本结构的化合物。
11.木脂素:由二分子的苯丙素氧化缩合而成的一类化合物,广泛存在于植物的木部和树脂中,故名木脂素。
12.醌类:指具有醌式结构的一系列化合物,包括邻醌、对醌。
常见有苯醌、萘醌、蒽醌、菲醌。
13.大黄素型蒽醌:指羟基分布于两侧苯环的蒽醌。
14.黄酮类化合物:指两个苯环(A环和B环)通过中间三碳链相互联结而成的(6C-3C-6C)一系列化合物。
15.碱提取酸沉淀法:利用某些具有一定酸性的亲脂性成分,在碱液中能够溶解,加酸后又沉淀析出的性质,进行此类成分的提取和分离。
16.萜类化合物:是一类结构多变,数量很大,生物活性广泛的一大类重要的天然药物化学成份。
其骨架一般以五个碳为基本单位,可以看作是异戊二烯的聚合物及其含氧衍生物。
但从生源的观点看,甲戊二羟酸才是萜类化合物真正的基本单元。
19.SF/SFE:超临界流体(SF):处于临界度(Tc),临界压力(Pc)以上的流体。
第二章 天然药物化学成分简介总结

5 有机酸:广义的有机酸泛指分子中有羧基 的化合物。在植物中多以金属离子或生物碱盐的 形式存在。按分子大小又分为小分子有机酸和大 分子有机酸。 (1)小分子有机酸:草酸、苹果酸、枸橼酸、 柠檬酸等。 性质:极性大,具亲水性 (2)大分子有机酸:咖啡酸、树脂酸等, 因分 子大,极性小,具亲脂性。 除去方法(1)醇溶水沉法(2)铅盐、钙盐等沉淀 法 (3)碱溶酸沉法
4 糖类:为中药中普遍存在的一类成分,据能否发生 水解,分为:单糖、低聚糖、多糖。 (1) 单糖是不能水解的糖,是糖的基本单位,如:
D―葡萄糖(glc) D― 半乳糖(gal) D ― 葡萄糖醛酸 D ― 半乳糖醛酸
OH
O
HO
OH
O
COOห้องสมุดไป่ตู้ O
COOH
HO
H,OH
O
OH
OH
H,OH OH
OH OH
H,OH
OH
OH
OH OH
H,OH
OH
性质:单糖多为无色结晶,有旋光性和还 原性,有甜味。易溶于水,可溶于乙醇, 难溶于无水乙醇,不溶于乙醚、苯、氯 仿等亲脂性有机溶剂。 除去方法:水溶醇沉法 操作: 将水提取液蒸干,在残留物中加入无水 乙醇溶解,过滤,则单糖沉淀被滤除, 乙醇液中还有有效成分。
(2)低聚糖 由2~10个单糖基通过甙键聚合而成的 直糖或支糖链的低聚糖(又称寡糖)。 按糖的个数分为二糖、三糖…….按有无 游离的半缩醛羟基分为还原糖和非还原 糖。 如:芸香糖 龙胆二糖
第二章 天然药物 化学成分简介
本章主要介绍天然药物中的各类成分,。重点掌握各类成 分的一般溶解性,哪些为有效成分、哪些为无效成分,无 效成分如何除去,为理解提取、分离中药成分打下基础。 1 生物碱:为一类存在于生物体内分子中含有氮原子的有 机化合物的总称;一般具有碱性,可与酸成盐。游离生物 碱具亲脂性;生物碱盐具亲水性。 如:槟榔碱 吗啡碱
天然药物化学-需要掌握的化合物结构
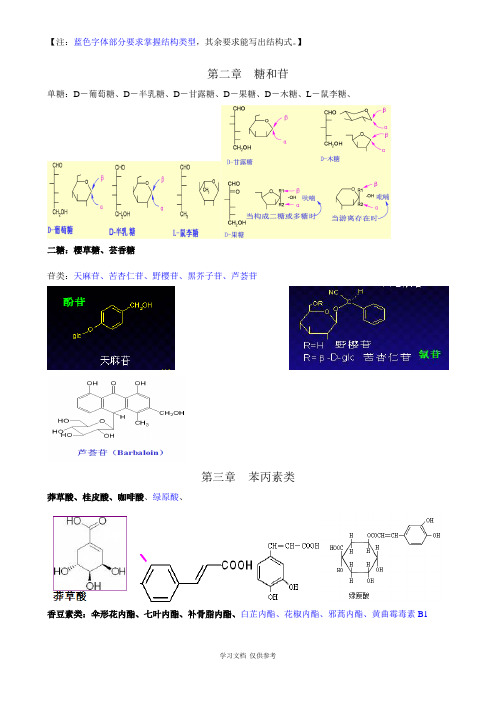
【注:蓝色字体部分要求掌握结构类型,其余要求能写出结构式。
】第二章糖和苷单糖:D-葡萄糖、D-半乳糖、D-甘露糖、D-果糖、D-木糖、L-鼠李糖、二糖:樱草糖、芸香糖苷类:天麻苷、苦杏仁苷、野樱苷、黑芥子苷、芦荟苷第三章苯丙素类莽草酸、桂皮酸、咖啡酸、绿原酸、香豆素类:伞形花内酯、七叶内酯、补骨脂内酯、白芷内酯、花椒内酯、邪蒿内酯、黄曲霉毒素B1木脂素类:鬼臼毒素、芝麻脂素、芝麻林脂素、五味子素、五味子酯、厚朴酚、和厚朴酚、第四章醌类苯醌类:辅酶Q10萘醌类:胡桃醌、维生素K菲醌类:丹参醌IIA蒽醌类:茜草素、大黄酚、大黄素、大黄素甲醚、芦荟大黄素、大黄酸、大黄酸蒽酮、番泻苷A第五章黄酮类芹菜素、黄芩苷、芦丁、槲皮素、银杏素、橙皮苷、儿茶素、大豆苷、葛根黄素、查耳酮、橙酮、花色素第八章甾体及其苷类异羟基毛地黄毒苷〔狄高辛〕、G-毒毛旋花子苷、蟾毒配基、薯蕷皂苷、原菝葜皂苷、菝葜皂苷六元内酯环强心苷毛地黄苷元 海葱苷元 命名:3b ,14b -二羟基-5b -强心甾-20(22)-烯 〔3b ,14b -dihydroxy-5b -card-20(22)-enolide 〕 3b ,14b -二羟基海葱甾-4,20,22-三烯〔3b ,14b -dihydroxyacilla-4,20,22-trienolide 〕 3b ,11a ,14b –三羟基-5b –蟾酥甾-20,22-二烯 第九章 生物碱阿托品、OOHRHOOOHR202122232021222324HOHOOOH2021222324HOHOH可卡因、苦参碱、麻黄碱、伪麻黄碱、吗啡碱、小檗碱、利血平、长春碱、长春新碱、喜树碱、乌头碱、紫杉醇。
天然药物化学作业

HO
OH
HO
O
O
(二)缩合鞣质
是儿茶素苯核之间通过碳-碳键相连,不具 有酯或甙键,在高温下或稀碱、稀酸作用下不 水解,迅速脱水缩合形成大分子化合物鞣红。 故又称鞣红鞣质类。此类主要存在于植物的果 实、种子、及树皮中。
1.黄烷三醇类:
以儿茶素为代表。共有六种异构体。分布 最广的是(+)儿茶素和(-)表儿茶素。
5.与三氯化铁作用 可生成蓝黑或绿黑色沉淀。
6.与铁氰化钾氨溶液的作用 深红色至棕色。
7.鞣质的检识 基本反应是使明胶溶液变浑浊或生成沉淀。
四、提取
在选择合适溶剂的基础上,控制温度和时
间,达到快速、完全和不破坏鞣质的目的。提 取鞣质最好选用新鲜药材,且立即提取。干燥 宜在短时间内。
可选用乙醇-水(1:1),丙酮-水(1:1) 为溶剂,以丙酮-水(1:1)提取率高,新鲜植 物可适当提高丙酮的比例。工业上以水提为主, 精制以醋酸乙酯为溶剂。
• 儿茶素
OH
HO
O
OH OH
• 表儿茶素
OH
HO
O
OH OH
• 肉桂鞣质
HO
O
HO HO
HO HO
OH
OH
OH
R1
O
OH
R2
OH
O
OH
R3 HO
2.黄烷3,4二醇类(白花素类)
易发生聚缩,在植物体内含量很少。
OH
HO
O
OH OH OH
(三)复合鞣质
由逆没食子鞣质部分与原花色素部分结合 组成的,具有可水解鞣质和缩合鞣质的一切特 征。
三、鞣质的理化性质及检识
1. 大多为无定形粉末,具吸湿性。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
生物技术学院课程论文课程名称:天然药物化学成绩:教师签名:2017年06月02日原花色素的性质与应用综述摘要:本文对原花色素进行了简单的介绍,并简述了原花色素的发现史,同时对原花色素的结构性质也做了一定的讲解。
接下来本文着重对原花色素的生理活性进行了描述和介绍,并结合生理活性举实例对原花色素的应用进行了综述总结。
关键词:原花色素;多酚类化合物;红粉;抗氧化活性1原花色素简介及发现史1.1原花色素简介原花色素又叫原花青素,原花青定,是一种可水溶的色素,并且可以随着细胞液的酸碱改变颜色。
如果细胞液呈现酸性那么花色素就呈现偏红的颜色,如果细胞液呈现碱性那么花色素就呈现偏蓝的颜色。
花色素无毒,并且不会致敏,有很高的安全性。
它广泛存在于植物中,是构成花瓣和果实颜色的主要色素之一,同时常见于花、果实的组织中及茎叶的表皮细胞与下表皮层,是植物生长过程中的次生代谢产物。
1.2原花色素发现史在19世纪90年代,科学家们通过研究发现,许多高等植物的叶、果、花的内部都有一种无色物质,几十年之后,科学家Rosehnenim把这种无色物质命名为“无色花色昔”。
1954年,Bate-Smith使用色谱系统研究无色牧场植物的分布。
发现无色糕点主要是存在于植物木质素及其分布被称为“单宁”材料的分布非常相似。
这是第一次“单宁”和花青素物质联系在一起。
后来发现,多数植物体内的能转化为花色素的物质不是黄烷-3,4-二醇,而是黄烷醇的二聚体,三聚体或低聚体。
为了纠正名称上的混乱,1960年Freudenbery与weinges提出“原花色素”一词。
原花色素是指从植物分离得到的一切无色的,在热酸处理下能产生花色素的物质。
80年代以来,研究人员针对下列植物中的原花色素进行了研究:葡萄,英国山植,单子山植,花生,银杏,日本罗汉柏,北美崖柏,土耳其侧柏,花旗松,白桦树,野生刺葵,番荔枝,野草葛,苹果,日本莽草,高粱,可可豆,海岸松和大黄等等。
发现这些植物中都含有丰富的原花色素,而在葡萄籽中含量尤为丰富。
占葡萄总质量的3%-4%的葡萄籽是葡萄酒与葡萄汁生产的副产物,据统计,全世界年产葡萄籽208.2万吨,我国仅酿酒业的葡萄籽也有4.2万吨,这就给原花色素的提取提供了很大的原料来源。
2原花色素的结构及性质2.1原花色素的结构花色素是多酚类化合物,是一种天然的自由基清除剂和抗氧化剂,衍生于黄烷类化合物,分子骨架为C6C3C6,属生物类黄酮。
C6C3C6实际上是原花色素中的一个核心分子结构,同时也因其分子中所含的苯环结构,使它在紫外光区有很强的吸收,还可起到“紫外光过滤器”的作用。
按照分子量大小,原花色素又可分为黄烷醇单体及聚合体。
我们习惯上会将分子量为500-3000的聚合体称为缩合单宁,同时将分子量更大的聚合体称为红粉和酚酸。
而按聚合度的大小,我们通常将二-四聚体称为低聚体,而将五聚体以上的称为高聚体。
“红粉”广泛地指缩合单宁水溶液在酸或在氧的作用下生成的不溶于水的红褐色沉淀,也指植物体内与缩合单宁伴存的不溶于水但溶于如甲醇之类的有机溶剂的红色酚类物质。
一部分红粉可用亚硫酸盐溶解。
聚合度更大的聚合原花色素不溶于中性水溶液,但溶于碱性水溶液,习惯上又称为“酚酸”。
原花色素能发生多种化学反应。
文献中说,原花色素的化学反应主要是组成单元的A 环的芳环亲电取代反应、B环的氧化反应、络合反应、以及单元间连接键的裂解反应(酸催化裂解,碱催化裂解)等等。
原花色素在正丁醇一浓盐酸(95:5)的环境下95℃处理40mni生成花色素。
原花色素的花色素反应除了生成花色素外,还生成其它未知色素及红粉。
使紫外图谱在45n0m区域出现肩峰。
花色素反应是鉴别原花色素的简便方法,但不能鉴别延伸单元的构型。
随着聚合度增加,原花色素上部单元的比例增加,所生成的花色素也相应地增多。
2.2原花色素的生理活性原花色素有多种生理活性,首先它可以与蛋白质发生结合反应,其次它与生物碱、花色昔以及多糖、核酸等多种天然化合物都能进行复合,此外它还能接受无机盐的作用,除了化学物质以外,酶和微生物也能对花青素有一定的作用和影响。
2.2.1原花色素与蛋白质结合原花色素能与蛋白质发生结合。
一般情况下,结合是可逆的。
原花色素一蛋白质结合反应是其最具特征性的反应之一。
单宁最初的定义就来自于它具有沉淀蛋白质的能力。
使明胶溶液浑浊也可作为一种基本的单宁定性试验。
原花色素与口腔唾液蛋白的结合,使人感觉到涩味,因此原花色素与蛋白质结合的这个性质又称为涩性或收敛性。
2.2.2原花色素与天然化合物复合与原花色素一蛋白质结合类似,原花色素还可与生物碱、花色普以及多糖、核酸等多种天然化合物发生复合。
这些反应都属于分子识别的结合机制,要求原花色素和各种底物(蛋白质、生物碱、花色昔以及多糖)在结构上互相适应和互相吻合,通过氢键一疏水键形成复合产物,多数情况下这种复合反应是可逆的。
2.2.3原花色素与脂类和核酸复合原花色素与脂类和核酸也可发生类似的复合。
对于蛋白质和脂类,所表现出的亲和性也与其酸碱性有关,中性或碱性分子的复合趋势较酸性分子高。
在原花色素的分离和应用中,往往需要考虑无机盐的影响。
原花色素对无机盐是高度敏感的,其作用包括两个方面,一是静电作用,二络合反应。
前者主要是一个物理过程,通过无机盐的脱水和盐析促进多酚溶液或胶体的沉淀;后者主要是一个化学过程,原花色素以邻位二酚轻基与金属离子形成五元环鳌合,可能同时还发生氧化还原和水解配位聚合等其它反应。
原花色素对于大多数金属离子都可以发生显著的络合,特别是单宁,其络合能力较小分子酚高得多。
这一特性不仅可用于原花色素的定性定量检测,而且是原花色素在选矿、水处理、防锈涂料、染料和颜料微量金属肥料、木材防腐等多种应用方向上的化学基础。
原花色素具有多种生物活性,而这些生物活性最本质的方面体现在原花色素对酶的抑制作用上。
原花色素是多种酶促反应有效的抑制剂,原花色素对酶的选择具有专一性。
虽然原花色素对多种酶普遍具有抑制作用,但是对于一种原花色素或一种酶,抑制是有选择性的。
原花色素一蛋白质结合反应本身是一种分子识别反应,两种反应物之间互相具有选择性。
抑菌性与酶抑制性有相当大的关系。
主要原因也在于单宁所特有的分子结构和蛋白质结合能力。
2.2.4原花色素作为自由基清除剂和抗氧化剂除了以上的和蛋白质等的反应和作用,花色素还是一种天然的自由基清除剂和抗氧化剂,酚轻基的还原性是酚类化合物的共性之一。
这一性质在原花色素上得到了充分的体现。
原花色素分子中的多个酚轻基可以作为H供体,连苯三酚(例如桔酸)或邻苯二酚(例如儿茶素的B环)的结构进一步加强了其还原性,使原花色素不仅可被重铬酸盐、氯酸盐等强氧化剂氧化,而且可被空气中的氧所氧化。
酚类的氧化机理,存在两条途径,一是通过酚轻基的离解,二是通过自亩基途径。
原花色素很易被空气中的氧所氧化,特别是在水溶液状态下和有原花色素氧化酶存在的条件下。
酚轻基通过离解,生成氧负离子,再进一步失去氢,生成具有颜色的邻醒,使多酚的颜色加深。
而醒很易被还原为酚。
原花色素在氯酸钾、高锰酸钾、双氧水和重铬酸钾等强氧化剂作用下,不仅酚经基受到氧化,而且糖环、杂环甚至苯环同时开裂,被氧化降解。
原花色素的抗氧化特性是通过几种途径综合体现出来的。
原花色素具有很强的自由基清除能力,可以消除各种活性氧自由基,抑制氧化酶,络合对氧化反应起催化作用的金属离子Fe离子和Cu离子。
多酚以大量的酚轻基作为氢供体,对多种活性氧具有清除作用,可将单线态氧还原成活性较低的三线态氧,减少氧自由基的产生,同时也清除各种自由基,生成活性较可氏的原花色素自由基,打断自由基氧化的链反应;其次,原花色素可以邻位二酚轻基与金属离子鳌合,减少金属离子对氧化反应的催化;再者,对于有氧化酶存在的体系,原花色素对其有显著的抑制能力;原花色素还能与VC和VE等抗氧化剂之间产生协同效应,具有增效剂的作用。
3原花色素的应用分析由于酚羟基具有还原性,原花色素有很强的抗氧化活性,这是酚类化合物所有的共性之一。
原花色素很容易被空气中的氧所氧化,特别是在有原花色素氧化酶的条件下和在水溶液的状态下。
酚羟基能够通过离解而生成氧负离子,然后失去氢,得到具有颜色的邻醌,使得多酚的颜色加深,而醌又很容易还原为酚。
Provost等通过酶法研究了原花色素对超氧阴离子自由基的清除,用免疫化学法研究了原花色素对羟基诱导的DNA损伤的清除活性。
发现了这些多酚类的化合物的抗氧化能力与它们的化学性质与化学结构密切相关。
原花色素的分子结构赋予它一系列独特的化学活性和生理活性,使其不仅在制革、泥浆稀释、粘合剂、金属络合材料、矿石浮选、水处理、天然色素等传统领域获得广泛应用。
近年来,随着研究的深入,在医药、食品、化妆品等附加值较高的领域原花色素制品也有不俗表现,原花色素具有防癌抗癌、防止心血管疾病、调节免疫活性、抗疲劳、抗过敏与改善视觉功能与皮肤保健与美容等功效。
3.1原花色素在化妆品方面在化妆品方面,原花色素具有的特殊抗氧活性和清除自由基的能力为其在化妆品领域中的应用开辟了广阔前景。
环境对皮肤、粘膜和毛发的刺激引起的脂质、蛋白质与核酸的损伤过程均与自由基分不开。
法国己开发出由arkushstruc原花色素低聚体制成的脂质体微胶囊的晚霜、发乳和嗽口水。
为了使活性成分便于通过皮肤角质层,意大利Indena公司用了5年时间研制成功了以磷脂(天然磷脂或合成磷脂)为载体的功能化妆品,商品名为Phytosome。
此产品含5%银杏原花色素二聚体,用于皮肤消炎和改善微循环。
经18名健康受试者试验(这些人因紫外线照射已出现皮肤炎症和红斑)。
表明该化妆品有较好的防护紫外线伤害作用。
1990年,日本Yamaskosh研制了含1%原花色素低聚体的可使皮肤亮洁的油性化妆品。
日本Ariga等,还开发了用作药品、食品和化妆品抗氧剂的原花色素,并获专利保护。
3.2原花色素在药用方面原花色素有很高的药用价值,在抗氧化活性作用方面、酶抑制活性方面、抗致突变方面、降低毛细血管通透性(抗炎)方面、心血管方面的研究、杭病毒与抗真菌方面的研究、杭腹泻方面的研究、杭腹泻方面的研究共九个方面都有非常卓越的效果。
通过对文献的查阅研究,我对医药方面的药用价值有以下总结。
3.2.1抗氧化活性方面葡萄籽原花色素具有极强的抗氧化活性,是一种很好的氧自由基清除剂和脂质过氧化抑制剂。
1989年,Meuneir等测试了葡萄籽原花色素抑制吩嚓甲基硫酸盐在辅酶I(NADH)和分子氧存在下大鼠肝微粒体内产生自由基的活性及抑制ADP/Fe+与抗坏血酸盐诱发的脂质过氧化活性,并与来自地中海柏木的缩合靴质、来自葡萄、黑果越桔及茶子的花青试进行了对照。
结果表明,葡萄籽原花色素对抗自由基和抑制脂质过氧化的活性最强。
