结直肠癌靶向治疗
晚期结直肠癌抗血管生成靶向治疗研究进展

晚期结直肠癌抗血管生成靶向治疗研究进展晚期结直肠癌是一种常见的恶性肿瘤,对人体健康造成了严重威胁。
针对晚期结直肠癌的治疗方法层出不穷,其中抗血管生成靶向治疗技术备受关注。
抗血管生成靶向治疗通过抑制肿瘤血管的新生和生长,阻断肿瘤的血液供应,从而达到抑制肿瘤生长和扩散的目的。
本文将对晚期结直肠癌抗血管生成靶向治疗的研究进展进行探讨,以期为医学研究和临床治疗提供参考。
一、晚期结直肠癌的特点和治疗挑战晚期结直肠癌是一种常见的恶性肿瘤,其病情往往在确诊时已经到了晚期,肿瘤细胞已经扩散到周围组织和器官,甚至转移至远处的部位。
这种情况给治疗带来了很大的挑战,因为晚期结直肠癌的治疗难度较大,常规的手术、放疗和化疗往往难以达到理想的疗效。
在晚期结直肠癌中,肿瘤血管的新生和生长对肿瘤的生长和扩散起着关键作用。
肿瘤细胞需要大量的营养和氧气来维持其生长和分裂,而这些物质主要通过血管供应。
肿瘤细胞产生多种血管生成因子,刺激附近的血管内皮细胞增生和分化,形成新的血管,从而为肿瘤提供所需的营养和氧气。
这一过程被称为血管生成,它是肿瘤生长和扩散的重要途径。
抑制肿瘤血管生成成为了治疗晚期结直肠癌的一个重要策略。
二、抗血管生成靶向治疗的原理和方法1. 抗血管生成因子治疗:通过抑制肿瘤产生的血管生成因子,如血管内皮生长因子(VEGF)、基本纤维母细胞生长因子(bFGF)等,阻断血管生成的信号通路,从而抑制肿瘤血管的新生和生长。
2. 血管生成抑制剂治疗:通过使用特定的分子靶向抑制剂,如西妥昔单抗、贝伐珠单抗等,针对肿瘤血管生成的关键信号通路和分子靶点,抑制肿瘤血管的新生和生长。
3. 多靶点抗血管生成治疗:结合不同的抗血管生成药物或治疗策略,同时干扰肿瘤血管生成的多个信号通路和分子靶点,从而加强抗血管生成的疗效。
以上这些抗血管生成靶向治疗方法均在临床治疗中得到了广泛的应用,取得了一定的疗效和临床效果。
这为晚期结直肠癌的治疗提供了新的思路和方法,也为进一步的研究和临床实践提供了重要的参考。
结直肠癌靶向治疗护理课件

治疗方案和药物的选择需要根据患者的具体情况制定,了解治疗方 案和药物的副作用有助于患者及家属更好地配合治疗。
治疗过程与注意事项
治疗过程中需注意的事项包括定期复查、按时服药、保持健康的生活 方式等,患者及家属需密切关注病情变化并及时就医。
家庭护理与康复指导
家庭护理要点
家庭护理包括饮食调整、心理支 持、生活照顾等方面,有助于患
临床表现与诊断
临床表现
结直肠癌早期症状不明显,随着病情发展可能出现大便习惯改变、便血、腹痛、 腹部肿块等症状。
诊断
结直肠癌的诊断主要依靠结肠镜检查和组织病理学检查,血液肿瘤标志物检查 也有助于诊断和监测病情。
2023
PART 02
靶向治疗原理及药物
REPORTING
靶向治疗原理
靶向治疗是一种针对特定分子靶点的治疗方法,通过设计特定的药物或抗体,针对 肿瘤细胞表面的特定受体或酶,抑制肿瘤细胞的生长和扩散。
分类
根据发病部位,结直肠癌可分为 结肠癌和直肠癌;根据恶性程度, 可分为腺癌、鳞状细胞癌等。
病因与发病机制
病因
结直肠癌的发病与遗传、环境、生活 习惯等多种因素有关,其中遗传因素 是最重要的危险因素之一。
发病机制
结直肠癌的发生是基因突变累积的结 果,环境因素如饮食、生活习惯等也 会影响基因表达,导致细胞异常增生。
与传统的化疗相比,靶向治疗具有更高的选择性,能够更精确地针对肿瘤细胞,减 少对正常细胞的损伤。
靶向治疗通常与化疗、放疗等其他治疗方法联合使用,以达到更好的治疗效果。
常用靶向药物
EGFR抑制剂
如西妥昔单抗(Cetuximab)、 帕尼单抗(Panitumumab)等, 用于治疗结直肠癌中EGFR阳性的
结直肠癌的治疗方案

结直肠癌的治疗方案结直肠癌的治疗方案引言结直肠癌是一种常见的恶性肿瘤,发病率逐年增加且死亡率居高不下。
为了提高结直肠癌患者的生存率和生活质量,科学的治疗方案非常关键。
本文将介绍几种常用的结直肠癌治疗方案,并讨论其优缺点。
手术治疗手术治疗是结直肠癌的首选治疗方法,尤其对于早期结直肠癌患者来说。
常见的手术方式包括直肠癌的前切除术、直肠癌的后切除术以及结直肠癌的结肠全切除术。
直肠癌的前切除术直肠癌的前切除术是指通过切除直肠癌及其周围组织,同时结直肠癌下端与肛门之间保持一定的残余直肠,并对术后进行吻合恢复。
该手术适用于直肠癌的中晚期患者,具有创伤小、术后功能良好的优点,但术后性功能障碍风险会增加。
直肠癌的后切除术直肠癌的后切除术是通过切除直肠癌及其周围组织,同时结直肠癌上段与结肠下段之间保留一定的条状残余直肠,并对术后进行吻合恢复。
该手术适用于直肠癌发生于直肠上段的患者,相对前切除术创伤更小,但术后功能恢复可能较差。
结直肠癌的结肠全切除术结直肠癌的结肠全切除术是指通过切除结直肠及其周围组织,然后进行胃肠吻合或造瘘术。
该手术适用于结直肠癌的大部分患者,但术后胃肠功能受限,生活质量相对较差。
然而,这种手术方法可以彻底切除癌细胞,有效降低复发和转移的风险。
化学治疗化学治疗在结直肠癌的综合治疗中起到重要作用。
通过使用抗癌药物来杀死肿瘤细胞,遏制其生长和扩散。
常用的化疗药物包括氟尿嘧啶、奥沙利铂等。
化学治疗在手术前、手术后或手术期间都可以应用。
术前化疗可缩小肿瘤体积,提高手术切除率;术后化疗可减少复发和转移的风险。
然而,化疗也会导致一系列不良反应,如恶心、呕吐、脱发等。
放射治疗放射治疗是结直肠癌治疗的一种重要手段,通过向肿瘤部位照射高能量射线来破坏癌细胞。
放射治疗可以作为手术的辅助手段,用于提高手术效果;也可以作为术后辅助治疗,减少复发和转移的风险。
放射治疗一般采用定位放射治疗、外照射或内照射,辐射能量和照射剂量根据患者具体情况而定。
结直肠癌靶向治疗的治疗效果评估

结直肠癌靶向治疗的治疗效果评估结直肠癌靶向治疗是一种基于分子靶向治疗策略,能够通过抑制特定靶点或信号通路来干扰癌细胞的生长与扩散。
在结直肠癌的治疗中,靶向治疗已经成为重要的治疗手段之一。
然而,为了准确评估结直肠癌靶向治疗的效果,我们需要采用多种方法进行综合评估。
一、影像学评估影像学检查是常用的非侵入性方法,可用于判断肿瘤的大小、形态、强化程度等,并且可以监测结直肠癌患者在接受靶向治疗后肿瘤的变化情况。
常用的影像学检查包括CT扫描、MRI和PET-CT等。
CT扫描可以提供关于肿瘤的详细信息,如体积、密度和血供等,并且可以评估靶向治疗后肿瘤的缩小程度。
MRI检查对于评估深层组织和神经束周围浸润情况较为准确。
而PET-CT则结合了功能和代谢信息,可以更好地观察到特定肿瘤标志物的活性以及转移情况。
二、血液检测通过血液检测,我们可以获得结直肠癌患者在接受靶向治疗后的生物标志物水平。
一些常用的生物标志物包括CEA(癌胚抗原)和CA19-9(糖类抗原19-9)。
CEA是结直肠癌最常见的标志物之一,其升高与肿瘤复发和进展有关。
CA19-9则主要用于结直肠癌患者转移及预后评估。
这些生物标志物的动态变化能够提供靶向治疗效果的指导信息。
三、组织学评估组织学评估是通过活检或手术获取组织样本,并对样本进行病理学分析和免疫组织化学染色等方法进行评估。
这样可以观察到治疗前后组织内微观结构改变、细胞增殖指数、抗凋亡信号通路等方面的变化。
例如,活检样本中免疫组化染色技术可以显示出特定蛋白质是否表达异常,如EGFR(表皮生长因子受体)、KRAS(Kirsten相关病毒),以及BRAF(瘤基因)等。
这些蛋白质的异常表达情况可以帮助预测患者对靶向治疗的敏感性和耐药性。
四、临床观察除了以上方法,临床观察也是一种常用的评估结直肠癌靶向治疗效果的手段。
医生会密切关注患者在治疗过程中的体征变化、生活质量改善和不良反应等,并根据患者的情况调整治疗方案。
结直肠癌肝转移转化治疗中靶向药物合理应用的专家指导意见

结直肠癌肝转移转化治疗中靶向药物合理应用的专家指导
意见
结直肠癌是一种常见的消化系统恶性肿瘤,肝转移是其常见的转移方式之一。
针对结直肠癌肝转移的治疗,靶向药物逐渐成为重要的治疗手段之一。
靶向药物是指针对肿瘤细胞特定分子靶点的药物,可以干扰肿瘤细胞的生长、增殖和转移等过程,从而达到治疗的效果。
对于结直肠癌肝转移患者的治疗,靶向药物可以有效地控制病情进展、延长生存期。
然而,在靶向药物治疗中,合理的应用非常重要。
以下是结直肠癌肝转移靶向药物合理应用的专家指导意见:
1. 充分评估患者的病情及治疗史,确定是否适合使用靶向药物。
严禁未经充分检查和评估,擅自使用靶向药物。
2. 对于KRAS突变阳性的患者,应避免使用EGFR抑制剂。
EGFR 抑制剂只适用于KRAS突变阴性的患者。
3. 靶向药物的使用应个体化,根据患者的基因型、体重、肝功能、年龄、性别等因素进行调整。
4. 定期进行血液检查、肝功能检查、心电图等,及时发现和处理药物相关的不良反应。
5. 合理选择靶向药物联合化疗,个体化治疗方案可以提高治疗效果,降低药物不良反应的发生率。
总之,结直肠癌肝转移的靶向药物治疗是一个复杂的过程,需要
医生和患者共同合作,根据实际情况制定个体化治疗方案,避免滥用和误用,提高治疗效果和生存质量。
攻克挑战博士生研究开发新型治疗方法治疗结直肠癌

攻克挑战博士生研究开发新型治疗方法治疗结直肠癌攻克挑战:博士生研究开发新型治疗方法治疗结直肠癌结直肠癌是一种常见的恶性肿瘤,全球范围内都有高发率。
治疗结直肠癌的方法有限,尤其是对于晚期患者来说。
因此,开发新型治疗方法成为了攻克挑战。
一、引言结直肠癌是一种由结肠或直肠上皮细胞开始发生癌变的疾病。
根据世界卫生组织的数据,结直肠癌是全球第三常见的癌症。
目前,传统的治疗方法包括手术切除、放疗和化疗等。
然而,这些方法在提高患者生存率和减缓疾病进展方面仍然存在一定的局限性。
二、新型治疗方法的研究进展为了攻克挑战,许多博士生投身于研究新型治疗方法。
以下是一些目前的研究进展:1.免疫疗法免疫疗法作为一种治疗癌症的新方法,受到了广泛关注。
研究者通过激活患者自身的免疫系统,使其发挥抗肿瘤作用。
目前,针对结直肠癌的免疫疗法主要包括肿瘤相关抗原疫苗、抗CTLA-4抗体和PD-1/PD-L1抗体等。
2.靶向治疗靶向治疗是基于癌症细胞的遗传变异和异常信号传导途径进行的,通过选择性地抑制癌症细胞的生长和扩散。
目前,靶向治疗用于结直肠癌的主要药物包括EGFR抑制剂、VEGF抑制剂和HER2抑制剂等。
3.基因治疗基因治疗是一种将特定基因引入人体以修复或增强机体功能的治疗方法。
在结直肠癌的基因治疗中,研究者通过给予患者修复缺陷基因、抑制癌基因或激活抗癌基因等方式,实现抑制肿瘤生长和扩散的效果。
三、研究挑战与解决方案在攻克挑战的过程中,博士生们面临着许多研究挑战。
例如,治疗方法的安全性、疗效和可行性需要得到深入研究和验证。
此外,药物开发过程中的高成本和长时间也是一个制约因素。
为了解决这些问题,博士生们可以采取以下策略:1.多学科合作博士生可以与相关领域的专家展开合作,共同攻克挑战。
通过整合不同领域的知识和技术,可以提高研究水平,并且加快治疗方法的开发和应用。
2.临床试验临床试验是将实验室研究成果应用到临床实践的重要环节。
博士生可以积极参与临床试验,验证治疗方法的效果和安全性,从而为治疗结直肠癌做出更大的贡献。
结直肠癌最新化疗方案及靶向治疗.pdf
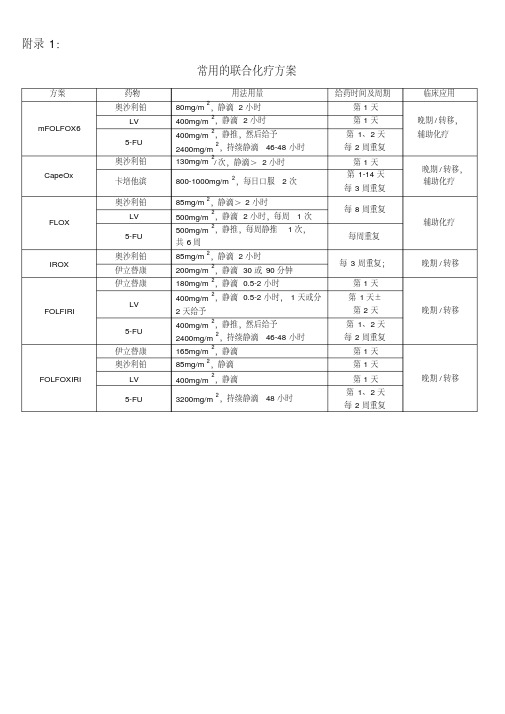
方案 mFOLFOX6
CapeOLFOXIRI
药物 奥沙利铂
LV
5-FU 奥沙利铂 卡培他滨 奥沙利铂
LV 5-FU 奥沙利铂 伊立替康 伊立替康
LV
5-FU 伊立替康 奥沙利铂
LV
5-FU
常用的联合化疗方案
用法用量
80mg/m 2,静滴 2 小时
400mg/m 2,静滴 2 小时
400mg/m 2,静推,然后给予
2400mg/m 2,持续静滴 46-48 小时
130mg/m
2
/
次,静滴>
2 小时
800-1000mg/m 2,每日口服 2 次
85mg/m 2,静滴> 2 小时 500mg/m 2,静滴 2 小时,每周 1 次 500mg/m 2,静推,每周静推 1 次, 共 6周 85mg/m 2,静滴 2 小时 200mg/m 2,静滴 30 或 90 分钟 180mg/m 2,静滴 0.5-2 小时 400mg/m 2,静滴 0.5-2 小时, 1 天或分
与伊立替康合用时, 伊立替康必须在本品滴注结束 1 小 时之后开始。
用药须知
主要不良反应为高血压、 蛋白尿; 胃 肠道反应,甚至可出现穿孔、出血; 动脉血栓栓塞;乏力。 对本品、中国仓鼠卵巢细胞产物或其 它重组人类或人源化抗体过敏者禁 用。 如出现以下情况应停用:胃肠道穿 孔,涉及到内脏瘘形成; 需要干预的 伤口并发症; 严重出血或动脉血栓事 件;高血压危象和高血压脑病; 可逆 性后脑蛋白质脑病综合征; 肾病综合 症。 如出现以下情况需暂停使用: 择期手 术前 4 周;药物控制不良的严重高血 压;中到重度的蛋白尿; 严重输液反 应。 孕妇不应使用, 用药后至少六个月内 都要避孕。 哺乳妇女用药期间应停止 哺乳,并在用药后至少 6 个月内不要 母乳喂养。 儿童和青少年不宜使用。 主要不良反应为痤疮样皮疹, 少数患 者可能发生过敏性反应、输液反应、 败血症、肺间质疾病、肾功能损害、 肺栓塞、脱水。 滴注本品之前必须先给予抗组胺药。 如果患者出现轻中度( 1 级或 2 级) 超敏反应, 因减慢滴注速率和减少剂 量,严重超敏反应( 3 级或 4 级)者 应立即并永久停用本品, 进行紧急处 理。体能状况低下或伴有心肺疾病的 患者应特别注意。 血象异常的患者,以及儿童不宜使 用。 建议监测血清镁的水平, 需要时补充 镁。 孕妇慎用。 哺乳妇女在治疗期间和最 后 1 次用药后 1 月内不要哺乳。
晚期结直肠癌抗血管生成靶向治疗研究进展

晚期结直肠癌抗血管生成靶向治疗研究进展【摘要】晚期结直肠癌是一种常见的恶性肿瘤,传统治疗方法效果有限,因此抗血管生成靶向治疗成为研究的焦点。
本文从靶向血管生成抑制剂的作用机制、多靶点联合治疗的应用、新型靶向药物的研究进展、靶向治疗的副作用及管理策略以及个体化靶向治疗的发展现状等方面进行了阐述。
通过深入探讨现有的研究成果,总结了晚期结直肠癌抗血管生成靶向治疗的进展,并展望了未来的研究方向。
这一研究领域的进展将为临床治疗提供更多选择,帮助提高晚期结直肠癌患者的生存质量和生存期。
【关键词】晚期结直肠癌、抗血管生成、靶向治疗、研究进展、血管生成抑制剂、多靶点联合治疗、新型靶向药物、副作用管理、个体化治疗、总结展望1. 引言1.1 晚期结直肠癌抗血管生成靶向治疗研究进展简介晚期结直肠癌是一种较为常见的恶性肿瘤,其治疗一直备受关注。
抗血管生成靶向治疗是近年来结直肠癌治疗中的重要进展之一。
通过干扰肿瘤血管生成途径,抑制肿瘤生长和转移,这一治疗策略为晚期结直肠癌患者提供了新的治疗选择。
随着研究的深入,不断涌现出新的靶向血管生成抑制剂和联合治疗方案,为晚期结直肠癌患者带来更多希望。
随之而来的副作用和管理策略也成为了研究的重点之一。
个体化靶向治疗的发展也为患者带来了更精准的治疗方案。
本文将对晚期结直肠癌抗血管生成靶向治疗的研究进展进行全面梳理,旨在为临床实践提供更多参考,为患者的治疗带来更多希望。
2. 正文2.1 靶向血管生成抑制剂在晚期结直肠癌治疗中的作用晚期结直肠癌是一种高度侵袭性的恶性肿瘤,常常伴随着血管生成的增加。
血管生成是肿瘤生长和转移过程中至关重要的因素,因此靶向血管生成抑制剂在晚期结直肠癌治疗中发挥着重要作用。
靶向血管生成抑制剂通过作用于肿瘤组织内的血管生成相关信号通路,抑制血管生成过程,从而导致肿瘤血供减少,供氧不足,限制了肿瘤的生长和转移。
这些药物可以针对肿瘤细胞表面的血管生成受体、细胞内的信号传导通路等靶点,实现对肿瘤血管生成的精准干预。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
CRYSTAL研究
CRYSTAL: 研究设计
表达EGFR的mCRC患者
R
Stratification factors: – Regions – ECOG PS
Populations – n=1217,随机分组 – 安全可评估病例: n=1202 – 入组病例: n=1198
Cetuximab + FOLFIRI
M0
85%*
M0Байду номын сангаас
72%*
M0
83%†
M0
64%†
M0
44%†
M1
8%
* Surgery alone; †Adjuvant therapy.
NCCN. Clinical Practice Guidelines in Oncology. Guidelines for Treatment of Cancer by Site: Colon Cancer. v.1.2007; Rectal Cancer. v.1.2007. Jenkintown, PA: NCCN: 2007. SEER Program () SEER*Stat Database: Incidence. Released April 2005.
二、结直肠癌的靶向治疗
• 什么是靶向治疗?
• 药物直接作用于肿瘤细胞上影响其生长和 增殖的特异性靶点
• 仅对某些特定患者有效 • 与传统的细胞毒药物不同
CRC靶向治疗新药
• Bevacizumab(Avastin) - 抗血管内皮生长因子(VEGF)受体单克隆抗体 (人源化)
- Gentech/Roche
0
6.2
0
10.6
0
10
20
30
无进展生存(PFS, months)
0
10
20
30
无进展生存(PFS, months)
Hurwitz et al. N Engl J Med. 2004;350:2335.
IFL/Bev 一线治疗 mCRC——OS
Patients, % Patients, %
Hazard ratio: 0.66, P < 0.001
Fuchs C et al. J Clin Oncol. 2008 Feb 1;26(4):689-90.
BICC-C 第2阶段: PFS-截至5/1/07
Proportion of Subjects Who Did Not Progress
ITT Population
治疗方案
中位无进展生存 (mPFS, months)
5-FU: 2400 mg/m2 (46-h infusion) (D1)
q2wks
• mIFL
伊立替康:
125 mg/m2 (D1, 8)
5-FU: 500 mg/m2 (bolus) (D1, 8)
LV: 20 mg/m2 (D1, 8)
q3wks
• CapeIRI
伊立替康:
250 mg/m2 (D1)
0.9
HR = 0.851; 95% CI, 0.726-0.998
0.8
Stratified log-rank P = .0479
0.7
0.6
0.5
8.9 mo
0.4
8.0 mo
1年PFS比率 23% vs 34%
0.3
0.2
0.1
0.0 0 2 4 6 8 10 12 14 16 18 20
PFS (mo)
42
45%
38%
83%
23
Cetuximab + 5-FU/LV/ irinotecan (AIO)3
21
67%
29%
96%
33
1Rosenberg et al. ASCO 2002:Abstr 536; 2 Rougier et al, ASCO 2004:Abstr 3513; 3Folprecht et al. Ann Oncol 2006;17:450-456
LV: 400 mg/m2 over 2 h (D1)
5-FU: 400 mg/m2 (bolus) (D1)
5-FU: 2400 mg/m2 (46-h infusion) (D1)
q2wks
随
+ 5 mg/kg 贝伐单抗 q2wks
mIFL
机
伊立替康: 125 mg/m2 (D1, 8)
5-FU: 500 mg/m2 (bolus) (D1, 8)
Fuchs C et al. J Clin Oncol. 2008 Feb 1;26(4):689-90.
BICC-C 第2阶段: mOS——2008年
Proportion of Subjects Who Survived
ITT Population
治疗方案
中位总生存 1 年
HR
(mOS, months) 生存率 (95% CI)
2400 mg/m2 ivgtt 46h)
+ FA
q2w
CRYSTAL – 有效性
主要研究终点(PFS) 所有有效病例
主要研究终点(PFS) 亚组:仅肝转移
PFS Estimate PFS Estimate
Cetuximab + FOLFIRI (n = 599)
1.0
FOLFIRI (n = 599)
HR (95% CI)
P值
1
FOLFIRI + Bev
11.2
--
--
0.9 0.8
mIFL + Bev
8.3
1.4 (0.8, 2.3)
0.28
0.7 0.6
0.5
0.4
0.3
0.2
FOLFIRI + Bev
0.1
mIFL + Bev
0
8.3
11.2
0
10
20
30
疾病发生进展时间 (TTP, months)
21 67% (10% CR) 29%
96%
24%
a10 patients no confirmation of response because secondary resection of metastases.
Rosenberg, et al. Proc ASCO 2002;20 [Abstract No. 536]; Peeters M, et al. Eur J Cancer Supp l2005;3:188 [Abstr 664]; Folprecht G, et al. Ann Oncol 2005; Cervantes A,et al Eur J Cancer Suppl 2005;3:181 [Abstr. 642].
*中期分析确定IFL (伊立替康+5-fu+LV)+ bevacizumab 的安全性后,第三组试验终止; † 进展后,可联合bevacizumab 与二线方案继续治疗。
Hurwitz et al. N Engl J Med. 2004;350:2335.
IFL/Bev 一线治疗 mCRC——PFS
伊立替康 卡培他滨 奥沙利铂 西妥昔单抗
靶向治疗 贝伐单抗 帕尼单抗
结直肠癌分期与生存
Stage I IIA IIB IIIA IIIB IIIC IV
T T1 T3 T4 T1-T2 T3-T4 Any T Any T
N N0 N0 N0 N1 N1 N2 Any N
M
5-year 生存率
M0
93%*
Cetuximab IV 400 mg/m2 d1,
随后250 mg/m2 qw
+ irinotecan (180 mg/m2)
+ 5-FU (400 mg/m2 IV +
2400 mg/m2 ivgtt 46h)
+ FA
q2w
FOLFIRI
irinotecan (180 mg/m2)
+ 5-FU (400 mg/m2 IV +
• Cetuximab (Erbitux, IMC-C225 ) - 抗表皮生长因子受体(EGFR)单克隆抗体(人/ 鼠嵌合)
- BMS
• 帕尼单抗
III期临床研究 IFL ± Bevacizumab一线治疗 mCRC
IFL ± Bevacizumab 一线治疗 mCRC
• 既往未接受过治疗 的mCRC患者
15.6
20.3
0
0
10
20
30
40
中位总生存(OS, months)
BICC-C研究——首次全面比较了伊 立替康联合5-FU类药物一线治疗转 移性结直肠癌的疗效和安全性
第一阶段
• FOLFIRI
伊立替康: 180 mg/m2 (D1)
LV: 400 mg/m2 over 2 h (D1)
5-FU: 400 mg/m2 (bolus) (D1)
卡培他滨: 1000 mg/m2 bid (D1-14)
q3wks
mPFS
FOLFIRI
7.6
mIFL
5.9
CapeIRI
5.8
mOS 23.1 17.6
BICC-C 第2阶段试验: 不同治疗方案
随
既往未接受治疗 的mCRC患者
机
N = 117
5/04–12/04 分
组
FOLFIRI
伊立替康: 180 mg/m2 (D1)
P值
FOLFIRI + Bev
28
87%
--
