结肠癌二期辅助化疗
PPI联合FOLFOX方案用于Ⅱ、Ⅲ期结肠癌术后辅助化疗的临床研究

PPI联合FOLFOX方案用于Ⅱ、Ⅲ期结肠癌术后辅助化疗的临床研究刘金万;宫玉霞;范治军【摘要】目的观察质子泵抑制剂(proton pump inhibitor,PPI)联合FOLFOX方案用于Ⅱ、Ⅲ期结肠癌术后辅助化疗的价值.方法选取本院2010年1月至2012年1月86例Ⅱ、Ⅲ结肠癌患者,随机分为观察组与对照组,每组各43例.观察组于术后4w内应用PPI联合FOLFOX方案,对照组仅应FOLFOX辅助化疗.采用免疫组化法观察结肠癌患者的V-ATPase表达,比较两组患者随访2年、3年、5年的无病生存率(Disease-free survival,DFS)及化疗不良反应发生率.结果观察组与对照组V-ATPase阳性率分别为67.44%、74.42%(P> 0.05).观察组2年、3年、5年DFS率分别为76.74%、65.12%、55.81%,对照组为58.14%、48.84%、39.53%,差异无统计学意义(P>0.05).观察组Ⅲ期患者的2年DFS率为78.26%,高于对照组(P<0.05),V-ATPase阳性患者的2年、3年DFS率分别为75.86%、65.52%,均高于对照组(均P<0.05),Ⅱ期患者DFS率比较差异均无统计学意义(均P>0.05).结论 PPI联合FOLFOX方案可在一定程度上延长Ⅲ期结肠癌及V-ATPases阳性患者根治术后的DFS,使患者远期获益.%Objective To study the effect of PPI combined with FOLFOX regimen as postoperative adjuvant chemotherapy for stage Ⅱ and Ⅲ colorectal cancer.Methods 86 patients with colon cancer were recruited from January 2010 to January 2012 in our hospital and were randomly assigned to treatment group and control group,with 43 cases in each group.The treatment group was treated with PPI combined with FOLFOX regimen within 4 weeks after operation,and the control group with FOLFOX regimen.The expression of V-ATPase wasmeasured by immunohistochemistry.The disease free survival (DFS) of followed up for 2 years,3 years,5 years and adverse events of chemotherapy were compared between two groups.Results The positive rates of V-ATPase in the treatment group and the control group were 67.44% and 74.42%,respectively (P > 0.05).The 2-year,3-year,and 5-year DFS rates were 76.74%,65.12%,55.81%,respectively,in treatment group and 58.14%,48.84%,39.53% in control group,respectively (P > 0.05).The 2-year DFS rate of stage Ⅲ colorectal cancer in the treatment gro up was 78.26%,which was higher than that in the control group (P < 0.05).The 2-year and 3-year DFS rates of V-ATPase-positive patients in the treatment group were 75.86% and 65.52%,respectively,which were significantly higher than those in the control group (P < 0.05).There was no significant difference in DFS rate between the two groups in stage Ⅱ patients (P >0.05).Conclusion PPI combined with FOLFOX regimen can improve the DFS of patients with stage Ⅲ colorectal cancer and V-ATPases positive patients,with favorable long-term efficacy.【期刊名称】《结直肠肛门外科》【年(卷),期】2017(023)005【总页数】5页(P587-591)【关键词】结肠癌;辅助化疗;FOLFOX;质子泵抑制剂【作者】刘金万;宫玉霞;范治军【作者单位】大连市第三人民医院药剂科辽宁大连116091;大连市第三人民医院心内科辽宁大连 116091;大连医科大学附属第二医院肿瘤放疗科辽宁大连116019【正文语种】中文【中图分类】R735.3结肠癌临床治疗以外科手术为主,有研究显示[1],Ⅱ、Ⅲ期结肠癌患者术后复发、转移风险较大,予以辅助化疗消灭术后可能残留的微小转移灶有助于减少复发。
肠癌二期化疗方案

肠癌二期化疗方案引言肠癌是一种常见的恶性肿瘤,常见于结肠和直肠。
根据病情的不同,肠癌的治疗方案也会有所不同。
对于肠癌二期患者,化疗是常用的治疗方法之一。
本文将介绍肠癌二期化疗的方案和注意事项。
化疗的目标化疗是通过使用药物抑制或杀死癌细胞,以达到控制和治疗肠癌的目的。
肠癌二期化疗的主要目标有以下几点:1.缩小肿瘤体积:化疗药物可以抑制肿瘤的生长和扩散,从而缩小肿瘤的体积。
2.消灭癌细胞:通过使用药物杀死癌细胞,从而减少癌细胞的数量。
3.预防复发:化疗可以消灭潜伏的癌细胞,减少复发的风险。
化疗药物肠癌二期化疗通常会使用多种不同的化疗药物,以增加治疗的效果。
常见的化疗药物包括:•氟尿嘧啶:是一种常用的化疗药物,可以通过抑制癌细胞DNA的合成来达到治疗效果。
•顺铂:是一种铂类化疗药物,可以干扰癌细胞的DNA修复机制,导致癌细胞死亡。
•卡培他滨:是一种新一代的化疗药物,可以通过抑制癌细胞的DNA和RNA的复制来达到治疗效果。
化疗方案化疗方案的选择通常需要根据患者的具体情况和医生的建议来确定。
以下是一种常见的肠癌二期化疗方案:1.方案名称:FOLFOX方案2.方案组成:–氟尿嘧啶–顺铂–亚叶酸钙3.用药方式:–氟尿嘧啶和顺铂通过静脉注射给药,亚叶酸钙通过口服给药。
–化疗周期一般为14天,每次化疗持续2小时。
4.副作用:–化疗药物会对正常细胞产生一定的损害,可能会导致一些不良反应,如恶心、呕吐、脱发、口腔溃疡等。
严重的副作用包括骨髓抑制和神经毒性。
注意事项在接受肠癌二期化疗期间,患者和医生需要注意以下事项:1.药物剂量和给药方式必须按照医生的建议进行,不可随意更改。
2.需要定期进行血液检查,以了解身体的状况和副作用的情况。
3.需要密切关注不良反应的出现,如恶心、呕吐、脱发等,及时和医生沟通。
4.患者在化疗期间应保持良好的营养状况,饮食要均衡,并按照医生的建议进行适当的补充。
5.化疗期间需要避免接触传染性疾病和减少感染的风险,尤其是在免疫系统受损的情况下。
结肠癌ppt课件
Tabernero. ASCO GI 2019. # 384
结论:ColoPrint分级是最强的预后因素,优于目前常用的临床病理参数及指南推荐标准
ColoPrint联合NCCN标准:最佳预测
Tabernero. ASCO GI 2019. # 384
ColoPrint分级和NCCN高危标准结合,则能提供最佳预测价值
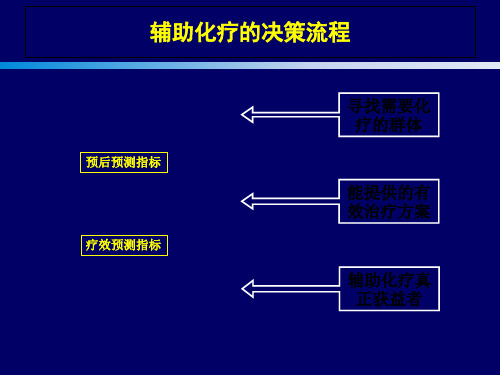
辅助化疗的决策流程
寻找需要化疗的群体
预后预测指标
能提供的有效治疗方案
疗效预测指标
辅助化疗真正获益者
结肠癌辅助化疗拟解决的核心问题
哪些患者群体需要辅助化疗?--适应证 I期:不化疗 II期:部分化疗,部分不化疗 III期:需要化疗 用什么做辅助化疗?--药物和方案 氟尿嘧啶(5-FU/LV、卡培他滨) 奥沙利铂 不能使用:伊立替康、靶向药物 辅助化疗应该何时用?用多久?--时机及疗程 术后今早开始:3周,<8周 疗程:6个月
1. 7th AJCC Cancer Staging Manual 2019 2. Gill et al. J Clin Oncol 2019
II期结肠癌: 高异质群体,预后迥异
Gunderson JCO 2019; 28(2):264-271
IIa
IIb
IIc
IIIa
IIIa
IIIa
第七版AJCC/TNM分期
Recurrence Score
QUASAR 结果:复发预测模型
RS、T分期和MMR状态可以综合预测术后复发
问题:T4 & dMMR(~1%)?
Ⅱ期结肠癌危险分层:小结
Ⅱ期结肠癌的预后迥异,包含各种异质性群体 目前可以应用的危险分层因素包括: 临床病理参数:“高危Ⅱ期” 结果最一致的是:T分期 分子标注物:MMR/MSI 所有研究结果均一致 基因芯片:ColoPrint, Oncotype DX 预测价值较高,但距离临床常规应用尚有距离(经济、方法) 基于危险分层,那些高危患者,才是最需要化疗的
结肠癌肝转移二线化疗

【一般资料】患者男性,54岁,于2018-03在当地医院例行查体时发现肝占位,2018-03-16于我院行CT检查示:“1.升结肠占位,考虑结肠癌伴周围脂肪浸润,其内側结节灶,考虑淋巴结转移:肝脏多发转移瘤;双肺下叶结节,考虑转移瘤:2.子宫肌瘤”。
2018-03-19至上级医院行结肠镜检查示:“进境85cm升结肠见近环腔性肿物,表面充血糜烂,管腔狭窄,难以进境,取活检,质脆:退镜距肛门75cm横结肠见0.6cm息肉一枚,活检,质软,距肛门65cm、58cm、50cm各见0.3-0.5cm息肉一枚,均未切除。
内镜诊断:升结肠肿物,结肠多发息肉。
活检病理示:升结肠腺癌、横结肠腺瘤性息肉。
”2018-03-20行PET-CT检查示:“1.升结肠瘤(伴外侵)并系膜侧淋巴结转移、肝多发转移、双肺下叶转移,FDG高代谢:2.鼻部炎症;3.右上龋齿:4.冠状动脉钙化;5.右乳钙化灶:6.子宫肌,2018-04-08予以贝伐珠单抗300mg靶向治疗。
2018-04-09予以FOLFOX6方案(奥沙利铂140mgd1+左亚叶酸钙300mgdl+氟尿啶50mg 静推d1+氟尿啶3.75g持续泵入46h)化疗,共化疗4周期,2018-06起加用阿帕替尼,因恶心、呕吐,不能耐受,2018-08停用,2018-09-12于我院行多学科会诊(MDT),会诊结果建议患者行“姑息减症术”解除梗阻缓解腹痛,患者拒绝,要求化疗。
2018-09-18给予FOLFTRI方案第1周期全身化疗(伊立替康120mgd1、8+氟尿嘧啶0.5g静推d1+氟尿嘧啶2.0微泵46h+亚叶酸钙200mgdl-3)。
现患者为求进一步化疗收入我科。
患者自发病以来,无发热,流质饮食,睡眠较差,大小便正常,体重无明显减轻。
【既往史】否认糖尿病、冠心病、高血压等慢性病病史,否认肝炎、结核等传染病病史,否认食物及药物过敏史,否认重大外伤及手术史,无输血史,预防接种史不详。
奥沙利铂对Ⅱ期结肠癌的术后辅助化疗弊大于利

奥沙利铂对Ⅱ期结肠癌的术后辅助化疗弊大于利
马冬;刘建化
【期刊名称】《循证医学》
【年(卷),期】2011(11)3
【摘要】对于Ⅱ期无高危因素(高危因素包括:穿孔、T4期、检测出的淋巴结少于12个)的结肠癌患者是否需要辅助化疗一直存在争议。
今年ASCO大会报道了一项探讨有/无高危因素的Ⅱ期结肠癌患者应用5FU/四氢叶酸±奥沙利铂(Ox)辅助化疗的荟萃分析结果。
该分析纳入了4个NSABP临床试验(C-05、C—06、C.07、C.08)的结肠癌术后患者,其中只有C-07为随机对照研究,
【总页数】1页(P131-131)
【关键词】术后辅助化疗;奥沙利铂;结肠癌;Ⅱ期;高危因素;随机对照研究;NSABP;
荟萃分析
【作者】马冬;刘建化
【作者单位】
【正文语种】中文
【中图分类】R734.2
【相关文献】
1.Ⅱ期结肠癌根治术后奥沙利铂联合氟尿嘧啶类药物辅助化疗疗效和获益人群分析[J], 秦琼;杨林;王金万;周爱萍;孙永琨;宋岩
2.四项关于高危Ⅱ期结肠癌接受不同时长的基于奥沙利铂辅助化疗随机临床研究的
前瞻性荟萃分析 [J],
3.多西他赛联合奥沙利铂及替吉奥对比奥沙利铂联合替吉奥在ⅢC期胃癌术后辅助化疗的临床疗效及不良反应分析 [J], 吴琼; 李宁; 邓文英; 马一杰; 罗素霞
4.奥沙利铂联合卡培他滨对结肠癌术后辅助化疗的临床疗效及血清CD3+、CD4+、CD8+水平的影响 [J], 钟锋;张霄程
5.奥沙利铂联合卡培他滨对结肠癌术后辅助化疗的临床疗效及血清CD3^(+)、
CD4^(+)、CD8^(+)水平的影响 [J], 钟锋;张霄程
因版权原因,仅展示原文概要,查看原文内容请购买。
术后化疗的Ⅱ期结肠癌患者血清Smad4的表达及临床意义

[5] Annes JP,Munger JS,Rifkin DB. Making sense of latent TGF activation. J Cell Sci,2016,116Pt2 217224.
[2] Papageorgis P,Cheng K,Ozturk S ,et al. Smad4 in activation Promotes malignancy and drug resistance of colon cancer. Cancer Res,2016,713 9981008.
目的 研究Ⅱ期结肠癌患者术后行辅助化疗前后血清Smad4表达水平及临床意义。方法 110例Ⅱ期结肠癌术后辅助化疗的患者,根据有无复发情况分为复发组37例和未复发组73例;应用酶联免疫吸附剂测定法ELISA对其辅助化疗前后血清Smad4水平进行检测。分析血清Smad4水平与患者无病生存时间的关系。结果 未复发组化疗后血清Smad4水平与化疗前相比明显升高,差异有统计学意义P复发组化疗前血清Smad4显著低于未复发组,两组比较差异有统计学意义P0.05。患者血清Smad4水平与患者无病生存期呈正相关I=2.03,P0.05。结论 血清Smad4水平变化可作为评测Ⅱ期结肠癌患者术后辅助化疗疗效及预后的重要分子生物学指标。
[8] Hahn SA,Bartsch D,Schroers A,et al. Mutations of the DPC4Smad4 gene in biliary tract carcinoma. Cancer Res,1998,586 11241126.
肠癌二期化疗方案

肠癌二期化疗方案摘要:肠癌是一种常见的消化系统恶性肿瘤,对患者的生活质量和生存率产生很大影响。
针对肠癌二期患者,化疗是常用的治疗方法之一。
本文将介绍肠癌二期化疗方案,包括药物选择、剂量和时间安排等方面的内容,旨在为临床医生提供参考,帮助患者制定最合适的治疗方案。
一、引言肠癌是一种常见的恶性肿瘤,发病率逐年上升。
根据病灶的位置,可以将其分为结肠癌和直肠癌两种类型。
早期肠癌往往无明显症状,易被忽视,因此大部分患者在确诊时已经进入了二期。
对于二期肠癌患者,化疗是常规的治疗方式之一,能够帮助患者控制肿瘤的生长和转移,延长患者的生存期。
二、化疗药物选择通常情况下,肠癌二期化疗方案会采用多种化疗药物的组合。
常用的化疗药物包括氟尿嘧啶(5-FU)、奥沙利铂(Oxaliplatin)和伊立替康(Irinotecan)等。
这些药物有不同的作用机制,能够通过不同途径抑制肿瘤的生长和扩散。
1. 氟尿嘧啶(5-FU)氟尿嘧啶是一种常用的抗肿瘤药物,属于嘌呤类似物。
其通过与细胞的DNA合成酶结合,抑制DNA的合成,从而干扰肿瘤细胞的正常生长和分裂。
5-FU可口服或静脉注射给药,常见的副作用包括恶心、呕吐和脱发等。
2. 奥沙利铂(Oxaliplatin)奥沙利铂是一种白金类化疗药物,通过与DNA结合,干扰肿瘤细胞的DNA复制和转录,从而抑制肿瘤的生长。
奥沙利铂通常与5-FU或伊立替康联合使用,可以提高化疗的疗效。
常见的副作用包括周围神经病变、恶心和呕吐等。
3. 伊立替康(Irinotecan)伊立替康是一种拓扑异构酶Ⅰ抑制剂,通过抑制DNA的转录和复制,阻断肿瘤细胞的增殖和生长。
伊立替康常与5-FU或奥沙利铂联合使用,用于治疗进展性结直肠癌。
常见的副作用包括腹泻、恶心和呕吐等。
三、化疗方案肠癌二期化疗方案的具体选择应根据患者的病情、身体状况和个体化需求进行决定。
一般来说,化疗通常会以周期为单位进行,每个周期的时间间隔为2~3周,连续进行数个周期。
结肠癌肿瘤分期与术后辅助治疗

结肠癌肿瘤分期与术后辅助治疗结肠癌是一种常见的恶性肿瘤,临床上常采用肿瘤分期来确定患者的病情和预后,并选择合适的治疗方案。
目前,最常用的肿瘤分期系统是美国癌症学会(AJCC)和国际癌症联盟(UICC)联合发布的TNM分期系统。
该系统基于肿瘤的深度侵犯、淋巴结转移和远处转移三个方面来评估患者的肿瘤分期。
结肠癌的分期一般分为0期到Ⅳ期,其中0期是指癌前病变,一般不需要进行手术治疗,而Ⅰ~Ⅳ期则是需要进行手术治疗的阶段。
Ⅰ~Ⅱ期是结肠癌的早期,一般通过手术切除肿瘤,达到根治目的。
此外,对于Ⅱ~Ⅲ期的患者,术后辅助治疗也是必不可少的。
术后辅助治疗是指手术切除肿瘤后,在恢复期结束后给予的一种治疗方法。
术后辅助治疗的主要目的是降低复发率和提高患者的生存率。
根据患者的具体情况,术后辅助治疗可以包括化学治疗、放射治疗和靶向治疗等。
化学治疗是目前最常用的术后辅助治疗方法之一。
通过给予化疗药物,可以清除残留的癌细胞,减少复发的风险。
化疗药物可以根据患者的分期和个体化情况进行选择,一般常用的有5-氟尿嘧啶、奥沙利铂等。
化学治疗的疗程一般为6个月,通过连续多个周期的治疗,可以有效地降低癌细胞的存活率,并达到控制肿瘤复发的目的。
放射治疗是通过应用高能射线照射肿瘤部位,杀死癌细胞或阻止其生长和扩散。
对于结肠癌来说,放射治疗主要用于Ⅲ~Ⅳ期患者术前辅助治疗,目的是缩小肿瘤的体积,提高手术切除的可行性。
术后,放射治疗一般不是主要的辅助治疗方式,但在某些特殊情况下仍然可以考虑应用。
靶向治疗是近年来快速发展的一种治疗方法,通过干扰肿瘤的生长信号通路,抑制癌细胞的生长和扩散。
对于结肠癌来说,最常用的靶向治疗药物是靶向表皮生长因子受体(EGFR)抑制剂和血管内皮生长因子(VEGF)抑制剂。
靶向治疗的优势在于可以减少化疗的毒副作用,提高患者的生存率。
但靶向治疗并不适用于所有患者,需要根据具体情况进行选择。
总的来说,结肠癌的肿瘤分期和术后辅助治疗是密切相关的。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2013.V3
从“如选择含奥沙利铂方案,则优选FOLFOX” 改为“FOLFOX/CAPEOX/FLOX”
NCCN Clinical Practice Guidelines in Oncology: colon cancer. V.3.2013
精品课件
80
80
DFS (%) OS (%)
60 HR=0.93 95%CI=0.64-1.35
40 P=0.710
FOLFOX4 70岁
20
FL70岁
FOLFOX4 <70岁
FL<70岁
0 6 121824 30364248 54606672 时间 (月)
Tournigand C, et al. J Clin Oncol 2012:30:3353-3360.
FL (n=1123)
<70岁 (n=968)
70-76岁 (n=155)
<70岁 (n=963)
70-76岁 (n=160)
II期: • 低危 (n=151) • 高危 (n=241) III期 (n=576)
II期: • 低危 (n=18) • 高危 (n=41) III期 (n=96)
II期: • 低危 (n=139) • 高危 (n=243) III期 (n=581)
精品课件
LOGO
80
80
DFS (%) OS (%)
60 HR=0.72 95%CI=0.51-1.01
40 P=0.062
20
FL (n=287)
FOLFOX4 (n=282)
0 6 121824 30 36 4248 546066 72 时间 (月)
Tournigand C, et al. J Clin Oncol 2012:30:3353-3360.
0
1
2
3
时间 (年)
II期 dMMR
4
5
HR=0.84 60 95%CI=0.57-1.24
P=0.38
40
20
无辅助化疗(n=214) FU辅助化疗 (n=214)
0
1
2
3
时间 (年)
如果只考虑氟尿嘧啶类治疗,必须考虑患者的MMR状态
II期MSI-H患者预后较好且不能从5FU辅助化疗中获益
Sargent DJ, et al. J Clin Oncol 2010; 28:3219-3226.
精品课件
对于所有小于70岁或处于II期的患者, 都应考虑进行错配修复蛋白(MMR)的 检测。 具有MSI-H(高度微卫星不稳定)的Ⅱ期患者可能预后较好, 且不会从 5-FU的辅助治疗中获益。
精品课件
NCCN 2013 V3. 结肠癌指南
辅助化疗 删除FOLFOX的“优选”
60 HR=1.10 95%CI=0.73-1.65
40 P=0.661
FOLFOX4 70岁
20
FL70岁
FOLFOX4 <70岁
FL<70岁
0 6 12182430 364248 54606672 时间 (月)
精品课件
对于Ⅱ期结肠癌: FOLFOX 方案可应用于高危Ⅱ期结肠癌患者,但不推荐用于中低危Ⅱ 期结肠癌 在 5-氟尿嘧啶/亚叶酸钙方案基础上添加奥沙利铂还未证明生存期 获益。
<70岁 (n=968)
70-76岁 (n=155)
<70岁 (n=963)
70-76岁 (n=160)
II期: • 低危 (n=151) • 高危 (n=241) III期 (n=576)
II期: • 低危 (n=18) • 高危 (n=41) III期 (n=96)
II期: • 低危 (n=139) • 高危 (n=243) III期 (n=581)
精品课件
结论
❖鉴于 MSI-H 的Ⅱ期结肠癌预后较好并且不能从 5氟尿嘧啶辅助治疗中受益,专家组建议所有Ⅱ期结 肠癌患者均应行 MMR 或 MSI 检测,并且低危的具 有 MSI-H 特征的Ⅱ期结肠癌不应行辅助治疗。
❖需要特别指出的是,对于具有 MSI-H 特征的Ⅱ期结 肠癌,组织分化差不再认为是高危因素。
LOGO
Ⅱ期结肠癌个体化 辅助化疗
2016 V2 NCCN指南
精品课件
Ⅱ期结肠癌患者需要化疗吗?
精品课件
概念简介
❖ MS(microsatellite,微卫星)基因组中小于10个核苷酸的 简单重复的DNA序列
❖ MSI(microsatellite instability,微卫星不稳定)由于 DNA修复错误导致微卫星的丢失或增加
▪ MSI-H,微卫星高频不稳定
▪ MSI-L,微卫星低频不稳定
▪ MSS,微卫星稳定
❖ MMR(mismatched repair)错配修复基因,一般检测相关蛋 白
▪ dMMR,错配修复蛋白缺失
▪ pMMR,错配修复蛋白正常
❖ MSI-H 相当于 dMMR;MSI-L/MSS 相当于pMMR
Sargent DJ, et al. J Clin Oncol 2010; 28:3219-3226
II期: • 低危 (n=22) • 高危 (n=44) III期 (n=94)
Tournigand C, et al. J Clin Oncol 2012:30:3353-3360.
精品课件
MOSAIC研究:70岁亚组
FOLFOX4较5-FU/LV无DFS/OS获益
5年DFS6年OS来自100100精品课件
❖高危因素,如组织分化差(排除 MSI-H),术后检 出淋巴结数目(<12),淋巴管/血管侵犯,肠梗阻, 神经侵犯,局限性肠穿孔,切缘接近、不确定或阳 性。
2016 V2 NCCN指南
精品课件
MOSAIC:研究设计
随机入组 (N=2246)
FOLFOX4 (n=1123)
精品课件
II期:MSI-H的肿瘤不是高危因素, 且预后较好
本研究检测5项RCT,457例患者;2大数据库,1027例患者
未辅助化疗患者
100
接受辅助化疗患者
100
生存与无进展生存概率 (%) 生存与无进展生存概率 (%)
80
80
60
60
40 HR=0.51
95%CI=0.29-0.89
20
P=0.009
dMMR (n=79)
pMMR (n=436)
0
1
2
3
4
5
时间 (年)
40 HR=0.79
95%CI=0.49-1.25
20
P=0.30
dMMR (n=86)
pMMR (n=426)
0
1
2
3
时间 (年)
Sargent DJ, et al. J Clin Oncol 2010; 28:3219-3226.
60 HR=0.91 95%CI=0.61-1.36
40 P=0.648
20
FL (n=287)
FOLFOX4 (n=282)
0 6 121824 30 36 4248 54606672 时间 (月)
精品课件
MOSAIC:研究设计
随机入组 (N=2246)
FOLFOX4 (n=1123)
FL (n=1123)
II期: • 低危 (n=22) • 高危 (n=44) III期 (n=94)
Tournigand C, et al. J Clin Oncol 2012:30:3353-3360.
精品课件
MOSAIC研究:II期高危亚组
FOLFOX4较5-FU/LV无DFS/OS获益
5年DFS
6年OS
100
100
dMMR=MSI-H; pMMR=MSS/MSI-L
II期 pMMR
4
5
精品课件
NCCN 2013 V3. 结肠癌指南
高危II期患者 修改说明
2012.V3
2013.V3
所有<50岁患者或II期患者都应接受MMR蛋白检测,II期MSI-H患者 可能预后良好,且并不能从5-FU辅助治疗中获益
NCCN Clinical Practice Guidelines in Oncology: colon cancer. V.3.2013
dMMR=MSI-H; pMMR=MSS/MSI-L
4
5
精品课件
II期:MSI-H患者不能从5-FU辅助化疗中 获益
100
100
80
80
生存与无进展概率 (%) 生存与无进展概率 (%)
60 HR=2.30 95%CI=0.84-6.24 P=0.09
40
20
无辅助化疗(n=55) FU辅助化疗 (n=47)
