抗肿瘤药物设计的新靶点
靶向抗肿瘤药物的研究进展_0

---------------------------------------------------------------最新资料推荐------------------------------------------------------靶向抗肿瘤药物的研究进展靶向抗肿瘤药物的研究进展近年来,随着肿瘤生物学及相关学科的飞速发展,人们逐渐认识到细胞癌变的本质是细胞信号转导通路的失调导致的细胞无限增生,随之而来的是抗肿瘤药物研发理念的重大转变。
研发焦点正从传统细胞毒药物向针对肿瘤发生发展过程中众多环节的新药方向发展,这些靶点新药针对正常细胞和肿瘤细胞之间的差异,可达到高选择性、低毒性的治疗效果,从而克服传统细胞毒药物的选择性差、毒副作用强、易产生耐药性等缺点,为此,肿瘤药物进入了一个崭新的研发阶段。
目前发现的药物靶点主要包括蛋白激酶、细胞周期和凋亡调节因子、法尼基转移酶(FTase) 等,现就针对这些靶点的研发药物做一综述。
1、蛋白激酶蛋白激酶是目前已知的最大的蛋白超家族。
蛋白激酶的过度表达可诱发多种肿瘤。
蛋白激酶主要包括丝氨酸/苏氨酸激酶和酪氨酸激酶,其中酪氨酸激酶主要与信号通路的转导有关,是细胞信号转导机制的中心。
蛋白激酶由于突变或重排,可引起信号转导过程障碍或出现异常,导致细胞生长、分化、代谢和生物学行为异常,引发肿瘤。
研究表明,近 80%的致癌基因都含有酪氨酸激酶编码。
1 / 22抑制酪氨酸激酶受体可以有效控制下游信号的磷酸化,从而抑制肿瘤细胞的生长。
酪氨酸激酶受体分为表皮生长因子受体(EGFR) 、血管内皮细胞生长因子受体(VEGFR) 、血小板源生长因子受体(PDGFR)等,针对各种受体的酪氨酸激酶抑制剂目前已开发上市的主要为表皮生长因子受体酪氨酸激酶(EGFR-TK) 抑制剂、血管内皮细胞生长因子受体酪氨酸激酶(VEGFR-TK) 抑制剂和血小板源生长因子受体酪氨酸激酶(PDGFR-TK) 抑制剂等。
PD-L1棕榈酰化是抗肿瘤免疫新靶点

690上海交通大学学报(医学版)2019, 39 (7)JOURNAL OF SHANGHAI JIAO TONG UNIVERSITY (MEDICAL SCIENCE )V ol.39 No.7 Jul. 2019Inhibiting PD-L1 palmitoylation enhances T-cell immune responses against tumours 引自:Nat Biomed Eng , 2019, 3(4): 306-317. DOI: 10.1038/s41551-019-0375-6.Abstract:Checkpoint blockade therapy targeting the programmed-death ligand 1 (PD-L1) and its receptor programmed cell death 1 promotes T-cell-mediated immunosurveillance against tumours, and has been associated with marked clinical benefit in cancer patients. Antibodies against PD-L1 function by blocking PD-L1 on the cell surface, but intracellular storage of PD-L1 and its active redistribution to the cell membrane can minimize the therapeutic benefits, which highlights the importance of targeting PD-L1 throughout the whole cell. Here, we show that PD-L1 is palmitoylated in its cytoplasmic domain, and that this lipid modification stabilizes PD-L1 by blocking its ubiquitination, consequently suppressing PD-L1 degradation by lysosomes. We identified palmitoyltransferase ZDHHC3 (DHHC3) as the main acetyltransferase required for the palmitoylation of PD-L1, and show that the inhibition of PD-L1 palmitoylation via 2-bromopalmitate, or the silencing of DHHC3, activates antitumour immunity in vitro and in mice bearing MC38 tumour cells. We also designed a competitive inhibitor of PD-L1 palmitoylation that decreases PD-L1 expression in tumour cells to enhance T-cell immunity against the tumours. These findings suggest new strategies for overcoming PD-L1-mediated immune evasion in cancer.许 杰(1979—),上海交通大学医学院附属仁济医院研究员、博士生导师。
端粒/端粒酶—抗肿瘤药物设计的新靶点

o e ̄i C e sr ,C i f O gn hmi y c t ha n
“
n
,N n 2 0 3 , m ) a如 1 0 8
Ab ta t sr c , .Te o r s , i h c n it o e e td TTA GGG e u n e tt e e f t e c r m o o l me e wh c o ss f r p a e s q e c sa h nd o h h o s me, a e e — r s
2 O世 纪三 四十年 代 , em n lr和 B raa H r nMul a e ab r Mc l tc Ci ok同 时提 出 了端 粒 的 概 念 , 是 染色 体 末 n 它
端 的一 种 特殊 结 椅 , 防止 染色 体 D 能 NA降 解 、 端 末 融合 、 失及 非 正常 重 组 , 持 染 色体 的 完整 和 稳 缺 维 定 。2 0多年 前 , 们从 分子水 平上 认识 了端粒 , 人 其
cl ,whl h y w r o eetbei o lsmai el.T eeoe eo rs t o rss r e a el s i te een t tca l n ma o t c l e d n c s h rfr .tlmee /e meae en w tr l a g t fra t a crd u .I hsp pr h tu trsa d f n t n ftlmee tlmeae ,v r d a — es o ni n e r g n ti a ,te srcu e u ci so eo r /eo rss ai p c e n o e p o c e oef in n ii o e mee tlmeae a d c rrn ttSo e su y olte wee r r ah s fi e tihbt n o tl r/eo rs n u re tS U ft td r h m r e t c i f o a h
抗肿瘤药物研究及新药筛选

抗肿瘤药物研究及新药筛选提纲一、化疗药物的发展二、肿瘤的药物治疗三、抗肿瘤药物筛选及评价四、体外抗肿瘤活性试验五、体内抗肿瘤活性试验一、化疗药物的发展•近代肿瘤化疗学始于20世纪40年代。
• 50年代通过动物筛选化疗药物发现了5FU、MTX、CTX等,化疗学有了发展。
• 60年代认识到肿瘤细胞动力学及化疗药药代动力学的重要性。
大部分目前所用的抗癌药已发现,有急淋、HD、睾丸癌等可化疗治愈。
• 70年代形成肿瘤内科学,更多肿瘤有了比较成熟的化疗方案。
• 80年代研究以生物反应修饰剂等药物来提高化疗疗效,探索抗药性产生的原因,5%肿瘤患者可治愈。
• 90年代新抗癌药进入临床,多药耐药基因发现,生物治疗,基因治疗辅助治疗改善等,疗效进一步提高。
二、肿瘤的药物治疗1、细胞毒类抗肿瘤药a、拓扑异构酶抑制剂原理:真核细胞DNA拓扑异构酶Ⅰ(Topo Ⅰ)是生物体内及其重要的细胞核内酶,参与DNA复制、转录和修复等所有关键的核内过程。
DNA拓扑异构酶Ⅰ已成为重要的抗肿瘤药物研究新靶点。
拓扑异构酶Ⅰ抑制剂已成为高选择性抗肿瘤药物研究的一个主攻方向。
代表药物:喜树碱类化合物对S期的毒性作用,这一作用需共价TopoI-DNA复合物的形成和DNA复制。
TopoI抑制剂诱导的细胞凋亡而非DNA断裂是引起细胞最终死亡的原因。
b、胸苷酸合成酶抑制剂原理:胸苷酸合成酶(TS)把单磷酸脱氧尿嘧啶(DUMP)转换成单磷酸胸腺嘧啶(TMP),在DNA复制和细胞生长过程中起着关键作用。
是已知抗肿瘤药物的重要有效靶点之一。
胸苷酸合成酶抑制剂导致了DNA断裂从而导致细胞死亡。
代表药物:培美曲塞它是一种结构上含有核心为吡咯嘧啶基团的抗叶酸制剂,通过破坏细胞内叶酸依赖性的正常代谢过程,抑制细胞复制,从而抑制肿瘤的生长。
体外研究显示,培美曲塞能够抑制胸苷酸合成酶、二氢叶酸还原酶和甘氨酰核苷酸甲酰转移酶活性,这些酶都是合成叶酸所必需的酶。
一旦培美曲塞进入细胞内,它就在叶酰多谷氨合成酶的作用下转化为多谷氨酸的形式。
抗肿瘤药物开发研究与策略分析

抗肿瘤药物开发研究与策略分析肿瘤是一种严重危害人类健康的疾病,其中癌症是最常见和致命的类型之一。
为了对抗这一疾病,抗肿瘤药物的开发和研究变得至关重要。
本文将针对抗肿瘤药物的开发研究和相关策略进行分析。
一、抗肿瘤药物的开发研究1. 抗肿瘤药物的分类抗肿瘤药物可以分为化学药物和生物药物两大类。
化学药物主要包括细胞毒性药物和激素类药物,其主要通过抑制肿瘤细胞的增殖和分裂来发挥作用。
生物药物则是通过给予人体免疫系统更多的能力来对抗肿瘤细胞,例如免疫检查点抑制剂和细胞治疗。
2. 抗肿瘤药物的研发过程抗肿瘤药物的研发过程通常分为药理学评估、药代动力学研究、安全性评价和临床试验四个阶段。
药理学评估主要是通过体外实验来评估药物的抗肿瘤活性和机制。
药代动力学研究则旨在了解药物在体内的代谢和排泄情况。
安全性评价主要包括毒理学评价和副作用评估。
最后,临床试验是将药物应用于人体进行治疗效果评估的阶段。
3. 新一代抗肿瘤药物随着科技的不断进步,新一代抗肿瘤药物的研发取得了一系列的突破。
例如,靶向治疗药物的出现,可以通过针对肿瘤细胞的特定分子标靶,发挥定向杀伤作用,减少对正常细胞的影响。
免疫治疗则是利用人体免疫系统来攻击肿瘤细胞,增强机体抗肿瘤能力。
二、抗肿瘤药物开发策略1. 靶向治疗策略靶向治疗是目前抗肿瘤药物开发的主要策略之一。
通过针对特定的分子标靶,抑制肿瘤细胞的增殖和生长,减少对正常细胞的伤害。
例如,针对HER2阳性乳腺癌的靶向治疗药物赫赛汀(Herceptin)的研发与应用,显著改善了患者的生存率。
2. 免疫治疗策略免疫治疗是一种利用人体免疫系统来对抗肿瘤的策略。
这种策略通过激活免疫细胞如T细胞和自然杀伤细胞,增强它们对肿瘤细胞的杀伤能力。
免疫检查点抑制剂(ICIs)是其中一种应用广泛的免疫治疗方法,它可以抑制免疫检查点蛋白,以恢复免疫系统对肿瘤的杀伤作用。
3. 多靶点联合治疗策略由于肿瘤细胞的异质性和多样性,单一的靶点治疗在一些情况下可能面临抵抗和耐药的问题。
全球新型抗肿瘤药物研发进展及趋势

全球新型抗肿瘤药物研发进展及趋势作者:李积宗张博文方淑蓓韩佳毛开云江洪波陈大明来源:《上海医药》2022年第25期李积宗,中共党员﹑高级工程师,上海市生物医药科技发展中心主任、上海医药行业协会副会长,长期从事生物医药领域科研项目管理、科技成果转化和软课题研究等工作,牵头建设运行上海市生物医药研发与转化功能型平台,熟悉上海生物医药科技创新政策,具有丰富的项目管理和成果转化经验。
通信作者:陈大明,研究员,长期从事生物医药等领域的科技情报研究,创新了基于关联索引的情报研究新方法,揭示了多学科交叉融合演进的范式,构建了用于专利价值和成果转化的评估框架,在软科学研究、知识产权分析、产业情报研究等方面带领团队完成了数十项研究课题,有力支撑了多种决策。
摘要:新型抗肿瘤药物已成功用于规避常规策略的某些局限性,同时提供更高的敏感性和特异性、更高的生物利用度和改善的综合治疗效果。
本文总结了过去70年的抗肿瘤药物开发里程碑,综述了基于肿瘤标志性特征的14类抗肿瘤药物开发路径,并且从多学科交叉融合的视角探索了抗肿瘤药物开发中的前景。
关键词:抗肿瘤药物多学科研究中图分类号:R979.1文献标志码:A文章编号:1006-1533(2022)S2-0001-o8引用本文李积宗,张博文,方淑蓓,等.全球新型抗肿瘤药物研发进展及趋势[J.上海医药,2022,43(S2):1-8.Noval anti-tumor drugs: global advances and trendsLlJizong' , ZHANG Bowen', FANG Shubei' ,HAN Jia', MAO Kaiyun',JIANG Hongbo , CHEN Daming( 1.Shanghai Center of Biomedicine Development,Shanghai 201203,China; 2. Shanghai lnformation Center for LifeSciences,Shanghai Institute of Nutrition and Health, Chinese Academy of Sciences ,Shanghai 200031 , China)ABSTRACT Noval anti-tumor drugs have been successfully employed to circumvent certain limitations of conventionalstrategies while providing higher sensitivity and specificity,greater bioavailability, and improved comprehensive effects fortherapeutic outcomes. This paper summarized anti-tumor drug development milestones in the past seven decades,reviewed anti-tumor drug based therapies accroding to 14 different targeting approaches, and discussed the imperative role of multidisciplinaryresearches that could drive anti-tumor drug developments.KEY WORDS anti-tumor ; drug; multidisciplinary research過去数十年来,全球肿瘤治疗巨大需求的拉动力、多种技术融合创新的驱动力,共同推动了全球抗肿瘤药物研发的快速发展。
抗癌药物作用机理及作用靶点
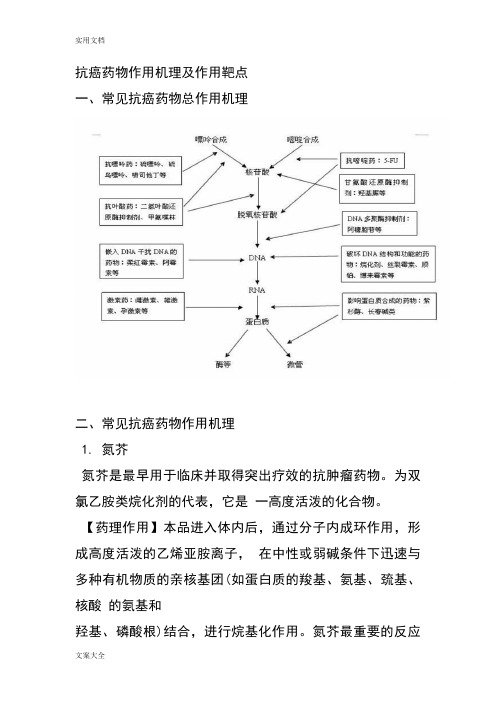
抗癌药物作用机理及作用靶点一、常见抗癌药物总作用机理二、常见抗癌药物作用机理1. 氮芥氮芥是最早用于临床并取得突出疗效的抗肿瘤药物。
为双氯乙胺类烷化剂的代表,它是一高度活泼的化合物。
【药理作用】本品进入体内后,通过分子内成环作用,形成高度活泼的乙烯亚胺离子,在中性或弱碱条件下迅速与多种有机物质的亲核基团(如蛋白质的羧基、氨基、巯基、核酸的氨基和羟基、磷酸根)结合,进行烷基化作用。
氮芥最重要的反应是与鸟嘌呤第7位氮共价结合,产生DNA 的双链内的交叉联结或DNA 的同链内不同碱基的交叉联结。
G1期及M 期细胞对氮芥的细胞毒作用最为敏感,由G1期进入S 期延迟。
【适应症】主要用于恶性淋巴瘤及癌性胸膜、心包及腹腔积液。
目前已很少用于其他肿瘤,对急性白血病无效。
与长春新碱(VCR)、甲基卡肼(PCZ)及泼尼松(PDN)合用治疗霍奇金病有较高的疗效,对卵巢癌、乳腺癌、绒癌、前列腺癌、精原细胞瘤、鼻咽癌(半身化疗法)等也有一定疗效;腔内注射用以控制癌性胸腹水有较好疗效;对由于恶性淋巴瘤等压迫呼吸道和上腔静脉压迫综合征引起的严重症状,可使之迅速缓解。
2.环磷酰胺环磷酰胺为氮芥与磷酰胺基结合而成的化合物,是临床常用的烷化剂类免疫剂。
【药理作用】该品在体外无抗肿瘤活性,进入体内后先在肝脏中经微粒体功能氧化酶转化成醛磷酰胺,而醛酰胺不稳定,在肿瘤细胞内分解成酰胺氮芥及丙烯醛,酰胺氮芥对肿瘤细胞有细胞毒作用。
环磷酰胺是双功能烷化剂及细胞周期非特异性药物,可干扰 DNA 及 RNA 功能,尤以对前者的影响更大,它与DNA 发生交叉联结,抑制DNA 合成,对S 期作用最明显。
【适应症】该品为最常用的烷化剂类抗肿瘤药,进入体内后,在肝微粒体酶催化下分解释出烷化作用很强的氯乙基磷酰胺(或称磷酰胺氮芥),而对肿瘤细胞产生细胞毒作用,此外本品还具有显著免疫作用。
临床用于恶性淋巴瘤,多发性骨髓瘤,白血病、乳腺癌、卵巢癌、宫颈癌、前列腺癌、结肠癌、支气管癌、肺癌等,有一定疗效。
刘俊义-抗肿瘤药物设计的新靶点蛋氨酸合成酶催化机

Me O O
Me
5 OH
Me O O
Me
3
Me
4
O
O
OEt
Me
OEt
(114)
6 Me
O O Me
8
7 O
(115)
O (113)
Me O
O Me
OEt
OO (86)
O (112)
Me O
O Me
OEt 1
OO
(86)
O
HN
NH2
5
H2N N
Br OAc
(91)
6 O
HN H2N N
NH2 O
O HN H2N N
Hcy
CH3 C olll
O
N
DMBI Enz
CH3-M S
O
H N HN
H 2N
N
N H
THF
NHAr
SN2
H3C - S
Co I
O
DMBI N
MS
EnzH
NH3 CO2
Met
O
CH3 NHAr
SN2
N
HN
H 2N
N
N H
N5-CH 3-THF
Study on Mechanism of Methionine Synthase
H2N N HN
H2N N N
HN
N
O
+
D
H NaBH4/DMSO
Et2NPh
NR
HN
N
OD
H
H
NaBT4
H2N N HN
H N
H Methionine
H
D T
