中考化学金属的化学性质知识点

中考化学金属的化学性质知识点
一、初中化学金属的化学性质选择题
1.在硝酸银、硝酸铜的混合溶液中加入一定量锌粉,充分反应后过滤,滤液仍为蓝色,滤渣中有关判断正确的是()
A.滤渣中一定有银,没有锌和铜
B.滤液中一定有硝酸锌、硝酸铜,可能有硝酸银
C.滤渣中一定有银和锌,可能有铜
D.滤液中一定有硝酸锌、硝酸铜、硝酸银
2.某校研究性学习小组的同学为了对Cu-Zn合金、Fe-Cu合金、Fe-Zn合金、Fe-Al合金进行研究,他们取其中一种合金的粉末5.6g,与足量的稀硫酸充分反应,经测定,产生了0.38g气体。则该合金可能是()
A.Cu-Zn合金B.Fe-Cu合金C.Fe-Zn合金D.Fe-Al合金
3.某学生为了验证铁、锌、铜三种金属的活动性顺序,设计了四种方案:①将Zn、Cu分别加入到FeSO4溶液中,②将Zn、Cu分别加入到ZnSO4溶液中,③将Zn分别加入到FeSO4、CuSO4溶液中,④将Fe 分别加入到ZnSO4、CuSO4溶液中。其中正确的方案是
()
A.①或④B.①或②C.②或③D.③或④
4.向一定量的铁粉中逐滴加入稀硫酸至过量,该图是反应过程中某种物质的质量Y随加入稀硫酸的质量变化的关系,则Y不可能表示()。
A.消耗铁粉的质量
B.生成硫酸亚铁的质量
C.溶液的总质量
D.生成氢气的质量
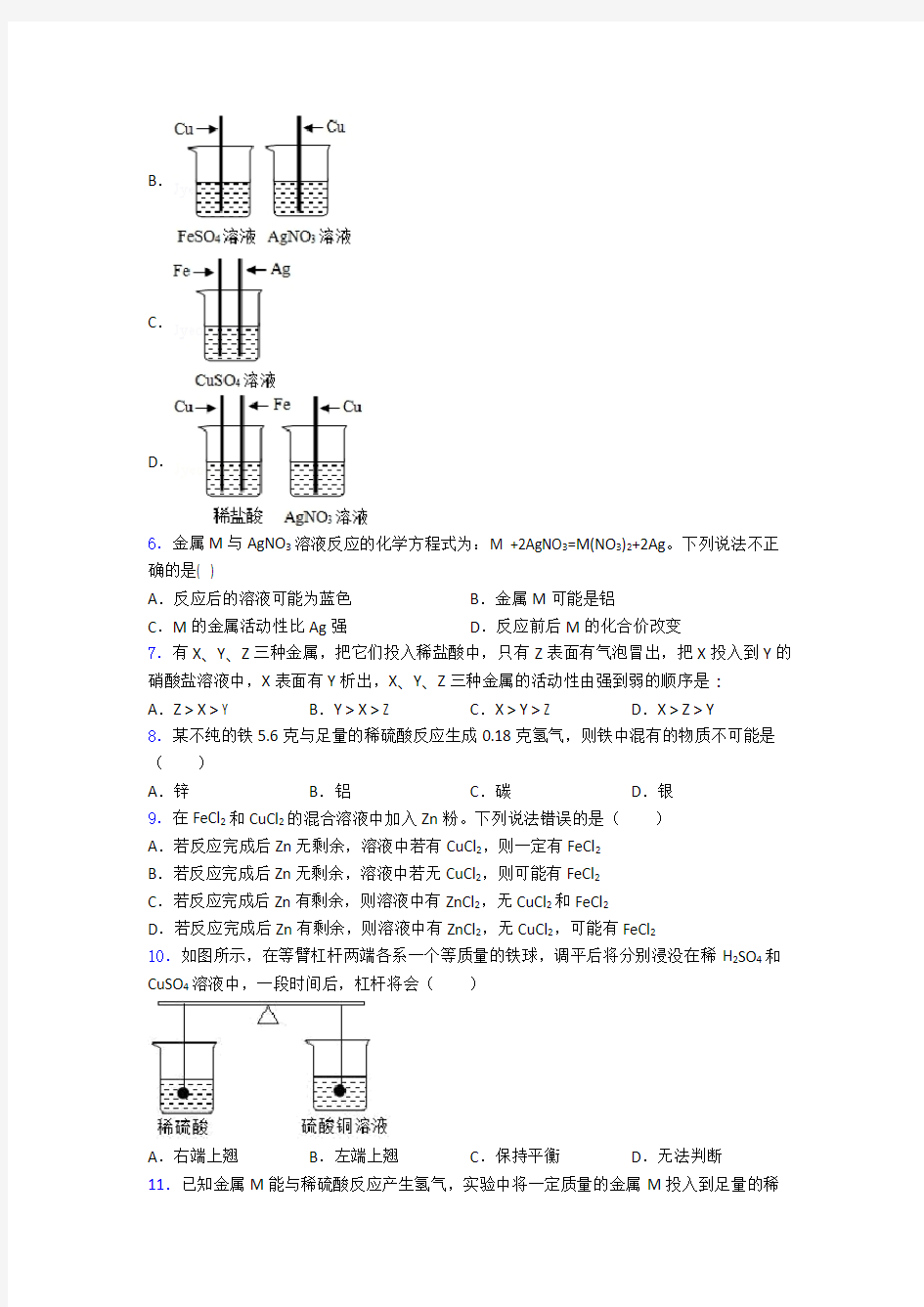
5.为探究Fe、Cu、Ag三种金属的活动性顺序,某兴趣小组设计了如图所示的四组实验方案,你认为不可行的是()
A.
B.
C.
D.
6.金属M与AgNO3溶液反应的化学方程式为:M +2AgNO3=M(NO3)2+2Ag。下列说法不正确的是( )
A.反应后的溶液可能为蓝色B.金属M可能是铝
C.M的金属活动性比Ag强D.反应前后M的化合价改变
7.有X、Y、Z三种金属,把它们投入稀盐酸中,只有Z表面有气泡冒出,把X投入到Y的硝酸盐溶液中,X表面有Y析出,X、Y、Z三种金属的活动性由强到弱的顺序是:
A.Z>X>Y B.Y>X>Z C.X>Y>Z D.X>Z>Y
8.某不纯的铁5.6克与足量的稀硫酸反应生成0.18克氢气,则铁中混有的物质不可能是()
A.锌B.铝C.碳D.银
9.在FeCl2和CuCl2的混合溶液中加入Zn粉。下列说法错误的是()
A.若反应完成后Zn无剩余,溶液中若有CuCl2,则一定有FeCl2
B.若反应完成后Zn无剩余,溶液中若无CuCl2,则可能有FeCl2
C.若反应完成后Zn有剩余,则溶液中有ZnCl2,无CuCl2和FeCl2
D.若反应完成后Zn有剩余,则溶液中有ZnCl2,无CuCl2,可能有FeCl2
10.如图所示,在等臂杠杆两端各系一个等质量的铁球,调平后将分别浸没在稀H2SO4和CuSO4溶液中,一段时间后,杠杆将会()
A.右端上翘B.左端上翘C.保持平衡D.无法判断
11.已知金属M能与稀硫酸反应产生氢气,实验中将一定质量的金属M投入到足量的稀
硫酸中,查找资料与实验过程中获得的数据有(1)金属M原子量为x,其他原子量也已知;(2)反应前硫酸溶液的质量;(3)金属的质量;(4)反应后得到的溶液质量;(5)反应前硫酸溶液的质量分数。若要求得金属M在反应中的化合价,所用到的一组数据可以是
A.(1)(2)(3)(4)
B.(2)(3)(4)(5)
C.(1)(2)(3)(5)
D.(1)(3)(4)(5)
12.下列实验现象记录正确的是 ( )
A.把铜丝放入硫酸铝溶液中,紫红色固体表面产生银白色固体,溶液变成蓝色
B.向氢氧化钾溶液中滴入氯化铁溶液,有浅绿色沉淀生成
C.将一氧化碳通过灼热的氧化铁,红棕色粉末逐渐变为黑色粉末
D.硫在氧气中燃烧,发出淡蓝色火焰,生成无色无味的气体并放出热量
13.有X、Y、Z三种金属,把足量X放入Y(NO3)2和Z(NO3)2的混合溶液中,充分反应后过滤,滤渣中只有X、Z。据此判断这三种金属的活动性由强到弱的顺序为
A.Y>X>Z B.Y>Z>X C.X>Y>Z D.X>Z>Y
14.金属锰与氯化亚铁溶液可发生如下反应:Mn+FeCl2=MnCl2+ Fe,下列说法错误的是( ) A.该反应属于置换反应
B.锰的金属活动性比铁强
C.锰能置换出盐酸中的氢
D.反应前后元素化合价都不变
15.如图所示实验内容为探究铁、铜和银三种金属活动性顺序。下列结论中,正确的是()
A.三种金属活动性由强到弱顺序为铁银铜
B.观察到的现象为铁丝和银丝表面均有气泡产生
C.三种物质间能发生反应的化学方程式为Fe+CuSO4=FeSO4+Cu
D.观察到的现象为铁丝和银丝表面均附着一层紫红色固体,溶液颜色变浅
16.锰和镍(Ni)都是金属元素,将镍丝插入MnSO4溶液中无变化,插入CuSO4溶液中,镍丝上有红色固体析出.Mn、Ni、Cu三种金属的活动性由强到弱的顺序是()A.Cu、Mn、Ni B.Mn、Ni、Cu
C.Ni、Cu、Mn D.Mn、Cu、Ni
17.质量相等的金属镁和铝分别加入质量相等、溶质质量分数相等的两份稀硫酸中,反应完毕后,金属均有剩余。则下列描述正确的是()
A.反应后溶液质量相等
B.铝反应后的溶液质量大
C.镁产生的氢气质量大
D.生成的氢气质量相等
18.4.5g 镁和铝的合金加入到一定质量、一定质量分数的稀盐酸中,恰好完全反应,产生0.4g 氢气。向反应后的溶液中加入一定质量的 NaOH 溶液,恰好使上述产生的 MgCl2 和AlCl3 完全转化为沉淀,则生成 NaCl 的质量为()
A.23.4g B.29.25g C.11.7g D.5.85g
19.下列图象能正确反映对应变化关系的是()
Mg、Zn、Fe与稀
盐酸反应
等质量等质量分数的
盐酸与足量的镁粉、
锌粉
将铜片加入一定量
的硝酸银溶液中
向一定质量的氯化锌
和盐酸溶液中加入锌
粒
A.A B.B C.C D.D
20.向一定质量FeCl2和CuCl2的混合溶液中加入锌粉。反应过程中,混合物中溶液的质量与加入锌的质量关系如图所示。有关该反应过程中混合物中的溶液和固体,下列说法正确的是()
A.a点时,溶液中只含有两种溶质
B.c点时,向固体中滴加稀盐酸,无气泡产生
C.d点时,溶液中的溶质为ZnCl2
D.e点时,固体中只含有2种物质
21.将等质量的镁、铁、锌,分别放入三份质量分数相同的稀盐酸中,反应生成的氢气质量与反应时间的关系如图所示。根据图中信息,下列判断不正确的是()
A.图线X表示镁的反应情况
B.铁消耗稀盐酸的质量最大
C.锌一定过量
D.镁一定过量
22.下列反应中属于置换反应的是()
A.CO+CuO
Cu+CO2
B.CaO + H2O=Ca(OH) 2
C.Zn+CuSO4=ZnSO4+Cu
D.SO2+2NaOH=Na2SO3+H2O
23.有一种纳米润滑添加剂,有铝粉、铜粉和氧化铝粉末中的一种或几种组成,取少量该添加剂,加入足量稀盐酸,有红色固体残留,并产生大量气泡,加入一定量的硝酸银溶液充分反应后过滤,得到滤渣和蓝色滤液。关于以上实验,有下列几种说法:
①该添加剂中一定有铜,可能有铝和氧化铝
②若向滤渣中加入足量稀盐酸,滤渣部分溶解,则该添加剂中一定有氧化铝
③滤液中最多含有三种溶质
④滤渣中一定有铜和银,滤液中一定有硝酸铝和硝酸铜
⑤通过以上实验可以证明铝、铜、银三种金属的活动性顺序
上述说法正确的有:
A.①②⑤B.②③⑤C.①③④D.②④⑤
24.向盛有一定质量稀硫酸的烧杯中加入过量的锌粉,下列4个图象中,能正确反映对应变化关系的是()
A.B.
C.D.
25.向一定质量的AgNO3和Cu(NO3)2的混合溶液中加入m g Zn,充分反应后过滤,将滤渣洗涤、干燥后再称量,得到的质量为m g。据此,下列说法不正确的是( )
A.取反应后的滤液观察,滤液可能呈蓝色
B.取反应后的滤液滴加稀盐酸,有白色沉淀产生
C.取滤渣滴加稀硫酸,可能有气泡产生
D.滤渣中的物质至少有两种
26.为比较A、B、C三种金属的活动性,某同学设计了如图所示实验,由此判断三种金属活动性由强到弱的顺序是()
A.A>C>B B.A>B>C C.C>A>B D.B>C>A
27.取一定量的Mg放入Cu(NO3)2和AgNO3的混合溶液中充分反应后过滤,得到固体和滤液。下列说法错误的是( )
A.固体中只有Ag时,滤液一定呈蓝色
B.固体中有Cu和Ag时,滤液一定呈无色
C.固体中一定有 Ag,滤液中可能有AgNO3
D.固体中可能有Cu,滤液中一定有Mg (NO3)2
28.一定质量的锌、铁分别和等量的盐酸反应,产生氢气质量与时间的关系如图所示,下列说法不正确的是()
A.t1时,产生氢气的质量锌比铁大
B.t1时,产生氢气的速率锌比铁大
C.t2时,参加反应锌的质量与铁相同
D.t2时,锌、铁消耗的盐酸质量相同
29.下列事实不能说明Zn比Ag活泼的是()
A.Zn能与AgNO3溶液反应置换出Ag
B.Zn能与稀硫酸反应,Ag则不能
C.自然界没有以单质形式存在的Zn,而有以单质形式存在的Ag
D.Zn的熔点为420℃,Ag的熔点为962℃
30.在一定条件下,一氧化碳、木炭都能与氧化铜发生反应,下列叙述正确的是
A.反应产生的气体都有毒B.反应中都有红色固体生成
C.反应类型都是置换反应D.反应的生成物不同
【参考答案】***试卷处理标记,请不要删除
一、初中化学金属的化学性质选择题
1.B
解析:B
【解析】
【分析】
充分反应后过滤,滤液仍为蓝色,说明滤液中仍然含有Cu2+。
【详解】
A、在硝酸银、硝酸铜的混合溶液中加入一定量锌粉,锌先和硝酸银反应,所以滤渣中一定有银,但是不能确定锌的硝酸铜反应了多少,所以滤渣中可能有铜,也可能没有铜,错误;
B、锌和硝酸银反应生成硝酸锌,滤液为蓝色,说明还含有硝酸铜,如果锌没有和硝酸银完全反应,则滤液中可能还有硝酸银,正确;
C、充分反应后滤液为蓝色,说明锌粉不足,则滤渣中一定没有锌,错误;
D、锌和硝酸银反应生成硝酸锌,滤液为蓝色,说明还含有硝酸铜,如果锌和硝酸银完全反应,则滤液中没有硝酸银,错误。
故选B。
2.D
解析:D
【解析】
【分析】
【详解】
试题分析:根据题中提供的数据可知,采用平均值计算,设金属为M
M+H SO=MSO+H
2442
M2
5.6g0.38g
M/2=5.6g/ 0.38g
M=29.9
所以混合金属的相对原子质量为29.9,符合题意为选项D
3.A
解析:A
【解析】
【详解】
①锌的活动性比铁强,可以置换出铁,而铜不能置换出铁,所以可以区分出活动性强弱
②难以比较铁的活动性和铜、锌的活动性孰强孰弱,所以该方案不可行,
③锌可以把铁和铜置换出来,但是不能比较铁和铜的活动性,所以该方案不可行
④铁不能置换出锌,但是可以置换出铜,所以可以区分出这三种活动性顺序
所以能够区分出锌铁铜三种金属活动性的方案是①④,这与选项A相吻合。
故选A。
【点睛】
本题考查学生对于金属活动性顺序的探究,我们在解答该类题目时就是根据已经掌握的金属活动性顺序,然后选择合适的酸或者是盐的溶液来进行解答。
4.C
解析:C
【解析】
试题分析:向一定量的铁粉中逐滴加入稀硫酸恰好反应完时溶液从硫酸的溶液变为硫酸亚铁,过程中溶液的总质量不能从零开始。所以C错误。故选C.,
考点:物质的变化及其过程
5.A
解析:A
【解析】
A、铜不能将硫酸亚铁中的铁置换出来,说明铁的活动性比铜的强;银不能将硫酸亚铁中的铁置换出来,说明铁的活动性比银的强。但没有比较出铜和银的活动性强弱,错误;
B、铜不能将硫酸亚铁中的铁置换出来,说明铁的活动性比铜的强;铜能将硝酸银中的银置换出来,说明铜的活动性比银的强,故三种金属的活动性强弱顺序是铁、铜、银,正确;
C、铁能将硫酸铜中的铜置换出来,说明铁的活动性比铜的强;银不能将硫酸铜中的铜置换出来,说明铜的活动性比银的强,故三种金属的活动性强弱顺序是铁、铜、银,正确;
D、铜与稀盐酸不反应,说明铜位于氢的后面;铁能与稀盐酸反应,说明铁位于氢的前面;铜能将硝酸银中的银置换出来,说明铜的活动性比银的强,故三种金属的活动性强弱顺序是铁、铜、银,正确。故选A。
点睛:判断三种金属活动性强弱最简单的方法有两种:用中间的金属和两边金属的溶液或中间金属的溶液和两边的金属。如判断铁、铜、银的活动性顺序,方法有:硫酸亚铁溶液、铜、硝酸银溶液或铁、硫酸铜溶液、银。
6.B
解析:B
A、如果金属M是铜,铜和硝酸银反应生成硝酸铜和银,反应后的溶液为蓝色,正确;
B、如果M是铝,铝与硝酸银反应生成银和硝酸铝,由于硝酸根-1价,铝+3价,所以硝酸铝写为:Al(NO3)3,图示中M是+2价,所以M不能是铝,错误;
C、由于金属M能与硝酸银反应置换出银,说明M的金属活动性比银强,正确;
D、反应前M是单质化合价为0,反应后生成了M(NO3)2其中M的化合价是+2价,化合价发生了改变,正确。故选B。
7.A
解析:A
【解析】
X、Y、Z三种金属,投入稀盐酸中,只有Z表面有气泡冒出,说明Z>H,H>X,H>Y;把X 投入到Y的硝酸盐溶液中,X表面有Y析出,说明X>Y,所以三种金属的活动性顺序是:Z>X>Y,故选A。
8.B
解析:B
【解析】
【详解】
5.6g铁和稀硫酸完全反应生成0.2g氢气;
A、5.6g锌和稀硫酸完全反应生成氢气质量小于0.2g,因此铁中混有的物质可能是锌;
B、5.6g铝和稀硫酸完全反应生成氢气质量大于0.2g,因此铁中混有的物质不可能是铝;
C、碳不能和稀硫酸反应,因此铁中混有的物质可能是碳;
D、银不能和稀硫酸反应,因此铁中混有的物质可能是银。
故选:B。
9.D
解析:D
【解析】
【详解】
在FeCl2和CuCl2的混合溶液中加入Zn粉,锌会先与氯化铜反应,氯化铜反应完后,再与氯化亚铁反应,所以:A、若反应完成后Zn无剩余,溶液中若有CuCl2,氯化铜没有完全反应,则一定有FeCl2,故A正确;
B、若反应完成后Zn无剩余,溶液中若无CuCl2,加入的锌可能与氯化亚铁发生了置换反应,也可能没有,则可能有FeCl2,故B正确;
C、若反应完成后Zn有剩余,锌会与氯化铜、氯化亚铁完全反应,则溶液中有ZnCl2,无CuCl2和FeCl2,故C正确;
D、若反应完成后Zn有剩余,则溶液中有ZnCl2,一定没有CuCl2、FeCl2,故D错误。
故选D。
10.B
解析:B
【解析】
铁和稀硫酸反应生成硫酸亚铁和氢气,和硫酸铜反应生成硫酸亚铁和铜。
【详解】
铁和稀硫酸反应生成硫酸亚铁和氢气,随着反应进行,铁球质量减小,溶液密度增大,浮力增大,铁和硫酸铜反应生成硫酸亚铁和铜,生成的铜附着在铁球表面,铁球质量增大,溶液密度减小,浮力减小,因此一段时间后,杠杆将会左端上翘。故选B。
【点睛】
金属活动顺序表中,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来。
11.A
解析:A
【解析】
【分析】
根据化学方程式计算所用到的量的关系及已知量分析所用的数据。
【详解】
将一定质量的金属M投入到足量的稀硫酸中,金属全部参加了反应。设要求的金属M在反应中的化合价,根据金属的化合价,写出金属与酸反应的方程式;可以根据金属的质量和生成的氢气的质量关系计算。由金属M原子量为x,其它原子量也已知,可以求出物质反应的质量关系,再根据反应前硫酸溶液的质量,反应后得到的溶液质量和金属的质量求出生成的氢气的质量,即可列比例式计算计算。所以A正确。
故选:A。
【点睛】
本题主要考查了根据化学方程式的计算,掌握根据化学方程式计算过程及方法是正确解答本题的关键。
12.C
解析:C
【解析】
A、金属的位置越靠前,金属的活动性越强。位置靠前的金属能将位于其后的金属从它的盐溶液中置换出来。铜的活动性比铝弱。把铜丝放入硫酸铝溶液中,不发生反应,无明显现象,错误;
B、向氢氧化钾溶液中滴入氯化铁溶液,有红褐色沉淀生成,错误;
C、将一氧化碳通入灼热的氧化铁生成铁粉和二氧化碳,红棕色粉末逐渐变为黑色粉末,正确;
D、硫在氧气中燃烧,发出蓝紫色火焰,生成有刺激性气味的气体并放出热量,错误。故选C。
13.A
解析:A
【解析】
【分析】
【详解】
X、Y、Z三种金属,把足量X放入Y(NO3)2和Z(NO3)2的混合溶液中,充分反应后过滤,滤
渣中只有X、Z,说明X的活动性大于Z小于Y。故选A。
14.D
解析:D
【解析】
A、该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应,正确;
B、锰能与氯化亚铁反应置换出铁,故锰的金属活动性比铁强,正确;
C、锰能与氯化亚铁反应置换出铁,故锰的金属活动性比铁强,因此锰是氢前的金属,能与稀盐酸反应,正确;
D、氯化亚铁中铁元素为+2价,铁单质中铁为0价,错误。故选D。15.C
解析:C
【解析】
试题分析:金属活动顺序表:K Ca Na Mg Al Zn Fe Sn Pb H Cu Hg Ag Pt Au在金属活动顺序表中,排在氢前边的金属能和酸发生置换反应生成盐和氢气。金属的位置越靠前,金属的活动性越强。位置靠前的金属能将位于其后的金属从它的盐溶液中置换出来。实验中,铁与硫酸铜反应生成硫酸亚铁和铜,化学方程式为Fe+CuSO4=FeSO4+Cu,铁的表面有红色固体析出,银与硫酸铜不反应,没有明显现象;溶液的颜色由蓝色变成浅绿色。
考点:金属活动性顺序的探究
16.B
解析:B
【解析】
【分析】
锰和镍(Ni)都是金属元素,将镍丝插入MnSO4溶液中无变化,说明镍的金属活动性比锰弱,插入CuSO4溶液中,镍丝上有红色固体析出,说明镍的金属活动性比铜强。
【详解】
A、将镍丝插入MnSO4溶液中无变化,插入CuSO4溶液中,镍丝上有红色固体析出,镍能置换出铜,铜应该排在镍的后面,故A错误;
B、镍不能置换出锰,能置换出铜,Mn、Ni、Cu的活动性由强到弱的顺序是Mn>Ni>Cu,故B正确;
C、镍不能置换出锰,说明锰的活动性比镍强,故C错误;
D、镍丝插入硫酸铜溶液中,镍丝上有铜析出,证明镍比铜活泼,故D错误。
故选B。
17.D
解析:D
【解析】
【详解】
将质量相等的金属镁和铝分别加入质量相等、溶质的质量分数相等的两份稀硫酸中,反应完毕后,金属均有剩余,说明硫酸全部参加反应,溶液的溶质由硫酸变为硫酸盐,根据化学方程式计算,消耗相同质量的硫酸,生成硫酸镁和硫酸铝的质量比为120∶114,所以镁反应后的溶液质量大,两种金属与酸反应生成的生成氢气的质量相等,故选D。
【点睛】
常见金属:锌、铁、镁、铝,当它们的质量相同时,与足量酸反应后生成的氢气的质量由大到小的顺序为铝、镁、铁、锌。
18.A
解析:A
【解析】
【详解】
根据H~HCl~NaCl,则设生成NaCl的质量为x。
H HCl NaCl
~~
158.5
0.4g x
10.4g
=
58.5x
则x=23.4g,
故生成NaCl 的质量为23.4g。故选A。
【点睛】
解决本题的技巧在于发现最终生成的氯化钠中氯元素全部来自于与镁铝合金发生反应的盐酸,这样就把看似无法解决的化学方程式的计算转变为根据化学式的计算,从而巧妙地解决问题。
19.B
解析:B
【解析】
【分析】
【详解】
A、根据可知,每24份质量的镁生成2份质量的氢气,每65份质量的锌生成2份质量的氢气,每56份质量的铁会生成2份质量的氢气, Mg、Zn、Fe与稀盐酸反应时,生成等质量的氢气,需要的镁的质量最小,需要锌的质量最多,与图像不符,故A错误;
B、根据可知,用等质量的相同质量分数的盐酸分别与足量的镁粉和锌粉反应,最终生成的氢气的质量相等,镁的活动性强于锌,故对应的曲线是镁的比锌的斜率大,与图像相符,故B正确;
C、根据可知,铜与硝酸银生成硝酸铜和银,每64份质量的铜和硝酸银反应生成硝酸铜和216份质量的银,反应后固体质量会增大,不会减小,与图像不符,故C错误;
D、往一定质量的ZnCl2和HC1溶液中加入锌粒,溶液的质量增加,当稀盐酸反应完全时,
溶液的质量不再能增加,故D错误。故选B。
【点睛】
本题是一道图像坐标与化学知识相结合的综合题,解题的关键是结合所涉及的化学知识,正确分析各变化的过程,注意分析坐标轴表示的意义、曲线的起点、折点及变化趋势,确定正确的图像。
20.C
解析:C
【解析】
在金属活动性顺序表中,锌、铁、铜的活动性依次减弱,故向一定质量FeCl2和CuCl2的混合溶液中加入锌粉,锌粉先与氯化铜反应,后与氯化亚铁反应,锌与氯化铜反应溶液的质量增加1份质量,锌与氯化亚铁反应溶液的质量增加9份质量,故可知,bd段为锌与氯化亚铁反应;
A、a点时,溶液中的部分氯化铜参加了反应,生成了氯化锌,故溶液中的溶质有氯化铜和氯化锌和氯化亚铁,错误;
B、c点时,锌将氯化铜完全反应,又于部分氯化亚铁反应,故固体中有铁生成,加入稀盐酸时,一定有气泡冒出,错误;
C、d点时,锌将氯化铜和氯化亚铁完全反应,故溶液中的溶质有氯化锌,正确;
D、e点时锌有剩余,故固体中有铜、铁和锌,错误。故选C。
21.C
解析:C
【解析】
【详解】
观察图像可知,三种金属反应的速率X>Y>Z,判断出三种金属的活动性顺序为X>Y>Z,从而得知X为镁,Y为锌,Z为铁。相同质量的三种金属完全参加反应,应该是镁消耗的酸最多,铁次之,锌最少,但图中铁产生氢气最多,即消耗稀盐酸最多;镁锌产生氢气一样多,即消耗稀盐酸一样多,故镁过量,但锌无法确定。故选C。
22.C
解析:C
【解析】
【分析】
【详解】
一种单质和一种化合物反应生成另一种单质和另一种化合物的反应属于置换反应, C项属于置换反应。故选C。
23.B
解析:B
【解析】
【详解】
取少量该添加剂,加入足量稀盐酸,有红色固体残留并产生大量气泡,说明一定含有铝和铜,因此①说法错误;
另取少量该添加剂,加入定量的硝酸银溶液,充分反应后过滤,得到滤渣和蓝色滤液,说明铜和硝酸银反应生成了硝酸铜,此时滤渣中一定含有的物质是Ag,可能含有铜,一定没有铝,滤液一定含有反应产生的硝酸铝、硝酸铜,可能含有硝酸银,滤液中最多含有三种溶质,因此③说法正确,④说法错误;
若向滤渣中加入足量稀盐酸,滤渣部分溶解,因为银、铜不能和盐酸反应,而铝没有剩余,说明该添加剂中一定有氧化铝被溶解,故②说法正确;
铝位于氢前,铜位于氢后;铜可以置换出银,因此通过以上实验可以证明铝、铜、银三种金属的活动性顺序,故⑤说法正确;
因此正确的是②③⑤;
故选:B。
24.D
解析:D
【解析】
【分析】
【详解】
A、稀硫酸为酸性溶液,开始时其pH小于7,反应后溶液呈中性,故A错误;
B、烧杯中有稀硫酸,所以开始质量不能为零,故B错误;
C、加入锌粉之后,锌和稀硫酸马上开始反应生成氢气,直至将稀硫酸消耗完全,生成氢气的质量不再改变,起点应从零点开始,故C错误;
D、加入锌粉之后,锌和稀硫酸马上开始反应生成硫酸锌,直至将稀硫酸消耗完全,生成硫酸锌的质量不再改变,故D正确。故选D。
25.B
解析:B
【解析】
试题分析:根据金属活动性顺序,向AgNO3、Cu(NO3)2的混合溶液中加入一定量的锌粉,本着“弱者先出局”的原则,故先后发生以下2个反应:2AgNO3+Zn==Zn(NO3)2+2Ag,根据反应中Zn与Ag质量关系为65:216,可知这个反应固体质量一定增大,Cu(NO3)2+ Zn==Zn (NO3)2+ Cu,根据反应中Zn与Cu质量关系为65:64,可知这个反应固体质量一定减少,而充分反应后过滤,固体质量不变,仍然为m克,说明这2个都一定发生,但第二个反应是否发生完全,就无法判断,A、因为Cu(NO3)2溶液可能过量,故取反应后的滤液观察,滤液可能呈蓝色,正确,B、因为溶液中不可能含有AgNO3,故取反应后的滤液滴加稀盐酸,没有白色沉淀产生,错误,C、因为锌可能过量,故取滤渣滴加稀硫酸,可能有气泡产生,正确,D、因为一定发生了2个反应,故滤渣中的物质至少有两种(即银和铜一定存在,锌可能存在),正确,故选D
考点:金属的活动性,化学方程式中物质的质量关系
26.B
解析:B
【解析】
【分析】
在金属活动性顺序表中,前面的金属能把后面的金属从其盐溶液中置换出来。
【详解】
A能把B从其盐溶液中置换出来,说明A的活动性比B强;C不能把B从其盐溶液中置换出来,说明C的活动性比B弱,所以三者的金属活动性由强到弱的顺序是A>B>C;
故选B.
27.B
解析:B
【解析】镁比铜活泼,铜比银活泼。取一定量的Mg放入Cu(NO3)2和AgNO3的混合溶液中充分反应后过滤,得到固体和滤液。A、固体中只有Ag时,镁质量不足,没有与硝酸铜反应,滤液一定呈蓝色,硝酸铜溶液呈蓝色,故A正确;B、固体中有Cu和Ag时,滤液不一定呈无色,只有镁质量充足时,滤液一定呈无色,故B错误;C、固体中一定有 Ag,滤液中可能有AgNO3,如果镁质量比较少时,滤液中有AgNO3是完全有可能的,故C正
确;D、固体中可能有Cu,滤液中一定有Mg (NO3)2,这是由镁的质量决定的,故D正确。点睛∶物质发生化学反应后生成物的成分组成要成分考虑到反应物的质量以及是否过量,不足或恰好完全反应。
28.C
解析:C
【解析】
t1min时,锌与盐酸反应曲线上点的纵坐标位置更高,说明此时锌与盐酸反应产生氢气的质量较铁与盐酸反应产生的氢气多,由时横坐标表示时间,所以也表示0~tmin这段时间内,锌与盐酸反应产生的氢气较铁与盐酸反应产生的氢气多,所以也表明锌与盐酸反应产生氢气的速率较铁与盐酸反应更快;t2min时,两条曲线相交,且此后保持水来,说明锌与盐酸的反应、铁与盐酸的反应均已完全,且产生氢气的质量相同,由于氢气中的氢元素来源于盐酸提供的氢元素,所以产生等质量的氢气,也就说明参加反应的盐酸质量相同。29.D
解析:D
【解析】
【详解】
A、根据金属活动性顺序,排在前边的金属能把位于其后的金属从它的盐溶液中置换出来,锌能置换出银,所以锌比银活泼,选项正确;
B、在金属活动性顺序中,排在氢之前的金属能与酸反应放出氢气,而排在氢之后的金属则不能,锌能与稀硫酸反应,说明锌在氢之前,而银不能反应,说明银在氢之后,所以可以判断锌比银活泼,选项正确;
C、只有化学性质非常稳定的金属在自然界中才以单质的形式存在,其他大多数金属都是以化合物的形式存在,故也可判断出锌比银活泼,选项正确;
D、金属的熔点与金属的活动性强弱没有关系,选项错误,故选D。
30.B
解析:B
【解析】
A、一氧化碳和木炭都能和氧化铜反应生成铜和二氧化碳,生成的气体是二氧化碳,二氧化碳无毒,A说法不正确;
B、木炭、一氧化碳有还原性,能将氧化铜还原为铜.所以,反应现象中都有试管内黑色粉末变成红色.故B正确;
C、一氧化碳和氧化铜反应生成铜和二氧化碳,反应物是两种化合物,所以该反应不属于置换反应,碳和氧化铜反应生成铜和二氧化碳,是一种单质和一种化合物生成另一种单质和另一种化合物属置换反应,C说法不正确;
D、一氧化碳和氧化铜反应生成铜和二氧化碳,碳和氧化铜反应生成铜和二氧化碳,生成物相同,D说法不正确;
故答案选B.
