活性炭吸附实验报告
烘干木炭吸附实验报告(3篇)

第1篇一、实验目的1. 探究烘干木炭的吸附性能;2. 分析烘干木炭吸附性能的影响因素;3. 评估烘干木炭在实际应用中的可行性。
二、实验原理木炭是一种具有多孔结构的碳材料,具有较大的比表面积和较强的吸附性能。
烘干木炭的吸附性能与其孔隙结构、比表面积等因素密切相关。
本实验通过测定烘干木炭对特定物质的吸附量,分析烘干木炭的吸附性能,并探讨影响因素。
三、实验材料与仪器1. 实验材料:烘干木炭、氯化钠溶液、苯溶液、硫酸铜溶液、活性炭等;2. 实验仪器:电子天平、分光光度计、吸附柱、锥形瓶、烧杯、滴定管、试管等。
四、实验方法1. 烘干木炭的制备:将木炭在烘箱中烘干至恒重,取出后备用;2. 吸附实验:将烘干木炭放入吸附柱中,分别向吸附柱中加入氯化钠溶液、苯溶液、硫酸铜溶液等,观察吸附效果;3. 吸附性能测定:采用分光光度法测定吸附前后溶液中特定物质的浓度,计算吸附量;4. 影响因素分析:改变实验条件(如温度、pH值、吸附剂用量等),观察吸附性能的变化。
五、实验结果与分析1. 烘干木炭对氯化钠溶液的吸附性能:烘干木炭对氯化钠溶液具有较好的吸附性能,吸附量随吸附剂用量的增加而增加;2. 烘干木炭对苯溶液的吸附性能:烘干木炭对苯溶液具有较好的吸附性能,吸附量随吸附剂用量的增加而增加;3. 烘干木炭对硫酸铜溶液的吸附性能:烘干木炭对硫酸铜溶液具有较好的吸附性能,吸附量随吸附剂用量的增加而增加;4. 影响因素分析:a. 温度:烘干木炭的吸附性能随温度的升高而降低;b. pH值:烘干木炭的吸附性能在酸性条件下较好,中性或碱性条件下吸附性能较差;c. 吸附剂用量:吸附剂用量越大,吸附性能越好。
六、实验结论1. 烘干木炭具有良好的吸附性能,可应用于氯化钠、苯、硫酸铜等物质的吸附;2. 温度、pH值、吸附剂用量等因素对烘干木炭的吸附性能有显著影响;3. 烘干木炭在实际应用中具有可行性,可作为吸附剂应用于水处理、空气净化等领域。
实验五 活性碳吸附实验

3、取下烧杯,静置15min。
4、取上清液测定吸光度并根据标准曲线计算吸光度。
五、实验数据
表一 确定废水的最大吸收波长
染料的浓度mg/L
吸光度
0
0.000
5
0.086
10
0.156
15
0.216
20
0.283
25
0.343
30
0.415
活性炭的吸附能力以吸附量q(mg/g)表示。所谓吸附量是指单位重量的吸附剂所吸附
的吸附质的重量。本实验采用粉状活性炭吸附水中的有机染料,达到吸附平衡后,用分光光
度法测得吸附前后有机染料的初始浓度C0及平衡浓度Ce,以此计算活性炭的吸附量qe。
在温度一定的条件下,活性炭的吸附量随被吸附物质平衡浓度的提高而提高,二者之间
的关系曲线为吸附等温线。以lgCe为横坐标,lgqe为纵坐标,绘制吸附等温线,求得直线斜率1/n、截距lgK。
三、实验装置及化学药品
1、可调速搅拌器;2、烧杯1000 ml;3、721型分光光度计;4、pH计或精密pH试纸、温度计;5、大小烧杯、漏斗;6、粉状活性炭;7、:100mg/L活性艳蓝KN-R染料废水;8、0.45微米的滤膜。
0.225
14.89
1.17
0.97
-0.01
12800
0.027
2.96
0.47
1.04
0.02
以lgCe为横坐标,lgqe为纵坐标,绘制曲线如下。
由于最后一组中活性炭浓度过大导致上清液中悬浮部分颗粒物,无法较好测定吸光度,因而取其组的二次滤液偏小。从上图可以看出,误差较大的点应舍弃。故做下图,作为吸附等温线。
711编号活性炭吸附实验报告

711编号活性炭吸附实验报告实验目的:1.了解活性炭的吸附特性。
2.通过比较不同条件下711活性炭吸附性能的差异,找出最佳条件。
实验原理:活性炭是一种优良的吸附材料,可以用于水处理、空气净化等方面。
其在吸附作用中,吸附物质可以通过活性炭表面的孔道、裂缝等位置传质,因此相比传统材料,其具有较高的吸附速率和吸附量。
711活性炭是一种典型的活性炭材料,在水处理、空气净化等领域应用广泛。
实验方法:实验设备:711活性炭筒、搅拌器、pH计、天平、烧杯、滴定管等。
试验操作:1. 洗涤:将711活性炭筒加入500mL去离子水,轻轻搅拌5min,倒掉水,重复3次,使活性炭表面杂质去除干净。
2. 吸附实验:将711活性炭筒放入250mL含有5mg/L苯酚的实验液中,开启搅拌器并保持搅拌速度为150rpm,实验时间为60min。
其中,液相pH为7,温度为25℃,活性炭用量为5g。
实验结束后,取出711活性炭筒,用去离子水冲洗并捡取样品液。
3. 吸附效果评估:使用紫外-可见分光光度计测定含苯酚实验液的吸附前后浓度差,计算其去除率。
4. 不同实验条件下吸附效果比较:根据不同的实验条件(如活性炭用量、实验时间等)进行吸附试验,比较不同条件下711活性炭吸附性能的差异,找出最佳条件。
实验结果:实验条件活性炭用量(g)实验时间(min)吸附前浓度mg/L 吸附后浓度mg/L 去除率(%)1 5 60 5 0.265 94.72 3 60 5 0.945 81.13 5 30 5 2.179 56.4从表1中可以看出,当活性炭用量为5g,实验时间为60min时,取得了最佳的吸附效果:苯酚去除率为94.7%。
此外,我们还比较了活性炭用量、实验时间等因素对吸附效果的影响。
实验结果如下:表2不同实验条件下的吸附效果比较从表2中可以看出,当活性炭用量增加时,去除率也随之提高。
实验时间对吸附效果的影响较小,当实验时间增加时,去除率略微增加。
活性碳吸附综合实验报告

1实验目的(1)通过实验进一步了解活性炭的吸附工艺及性能;(2)熟悉整个实验过程的操作;(3)掌握用“间歇法”、“连续流”法确定活性炭处理污水的设计参数的方法;(4)学会使用一级动力学、二级动力学方程拟合分析,对 PAC 的吸附进行动力学分析研究;(5)了解活性炭改性的方法以及其影响因素。
2实验原理2.1活性炭间隙性吸附实验原理活性炭吸附就是利用活性炭的固体表面对水中一种或多种物质的吸附作用,己达到净化水质的目的。
活性炭的吸附作用产生于两个方面,一是由于活性炭内部分子在各个方向都受到同等大小的力而在表面的分子则受到不平衡的力,这就使其他分子吸附于其表面上,此为物理吸附;另一个是由于活性炭与被吸附物质之间的化学作用,此为化学吸附。
活性炭的吸附是上述两种吸附综合的结果。
当活性炭在溶液中的吸附速度和解吸速度相等时,即单位时间内的活性炭的数量等于解吸的数量时,此时被吸附物质在溶液中的浓度和在活性炭表面的浓度均不在变化,而达到平衡,此时的动平衡称为活性炭吸附平衡而此时被吸附物质在溶液中的浓度称为平衡浓度。
活性炭的吸附能力以吸附量q表示。
式中:q ——活性炭吸附量,即单位重量的吸附剂所吸附的物质量,g/g;V ——污水体积,L;、C ——分别为吸附前原水及吸附平衡时污水中的物质浓度,g/L;CX ——被吸附物质重量,g;M ——活性炭投加量,g。
在温度一定的条件下,活性炭的吸附量随被吸附物质平衡浓度的提高而提高,两者之间的变化称为吸附等温线,通常费用兰德里希经验公式加以表达。
式中:q ——活性炭吸附量,g/g ;C ——被吸附物质平衡浓度g/L;K、n ——溶液的浓度,pH值以及吸附剂和被吸附物质的性质有关的常数。
K、n值求法如下:通过间歇式活性炭吸附实验测得q、C相应之值,将式取对数后变换为下式:将q、C相应值点绘在双对数坐标纸上,所得直线的斜率为1/n,截距则为K。
此外,还有朗缪尔吸附等温式,它通常用来描述物质在均一表面上的单层吸附,表达式为:由于间歇式静态吸附法处理能力低、设备多,故在工程中多采用连续流活性炭吸附法,即活性炭动态吸附法。
活性碳吸附综合实验报告.docx

活性碳吸附综合实验报告.docx1实验⽬的(1)通过实验进⼀步了解活性炭的吸附⼯艺及性能;(2)熟悉整个实验过程的操作;(3)掌握⽤“间歇法”、“连续流”法确定活性炭处理污⽔的设计参数的⽅法;(4)学会使⽤⼀级动⼒学、⼆级动⼒学⽅程拟合分析,对PAC 的吸附进⾏动⼒学分析研究;(5)了解活性炭改性的⽅法以及其影响因素。
2实验原理2.1活性炭间隙性吸附实验原理活性炭吸附就是利⽤活性炭的固体表⾯对⽔中⼀种或多种物质的吸附作⽤,⼰达到净化⽔质的⽬的。
活性炭的吸附作⽤产⽣于两个⽅⾯,⼀是由于活性炭内部分⼦在各个⽅向都受到同等⼤⼩的⼒⽽在表⾯的分⼦则受到不平衡的⼒,这就使其他分⼦吸附于其表⾯上,此为物理吸附;另⼀个是由于活性炭与被吸附物质之间的化学作⽤,此为化学吸附。
活性炭的吸附是上述两种吸附综合的结果。
当活性炭在溶液中的吸附速度和解吸速度相等时,即单位时间内的活性炭的数量等于解吸的数量时,此时被吸附物质在溶液中的浓度和在活性炭表⾯的浓度均不在变化,⽽达到平衡,此时的动平衡称为活性炭吸附平衡⽽此时被吸附物质在溶液中的浓度称为平衡浓度。
活性炭的吸附能⼒以吸附量q表⽰。
式中:q ——活性炭吸附量,即单位重量的吸附剂所吸附的物质量,g/g;V ——污⽔体积,L;C0、C ——分别为吸附前原⽔及吸附平衡时污⽔中的物质浓度,g/L;X ——被吸附物质重量,g;M ——活性炭投加量,g。
在温度⼀定的条件下,活性炭的吸附量随被吸附物质平衡浓度的提⾼⽽提⾼,两者之间的变化称为吸附等温线,通常费⽤兰德⾥希经验公式加以表达。
式中:q ——活性炭吸附量,g/g ;C ——被吸附物质平衡浓度g/L;K、n ——溶液的浓度,pH值以及吸附剂和被吸附物质的性质有关的常数。
K、n值求法如下:通过间歇式活性炭吸附实验测得q、C相应之值,将式取对数后变换为下式:将q、C相应值点绘在双对数坐标纸上,所得直线的斜率为1/n,截距则为K。
此外,还有朗缪尔吸附等温式,它通常⽤来描述物质在均⼀表⾯上的单层吸附,表达式为:由于间歇式静态吸附法处理能⼒低、设备多,故在⼯程中多采⽤连续流活性炭吸附法,即活性炭动态吸附法。
活性炭吸附实验
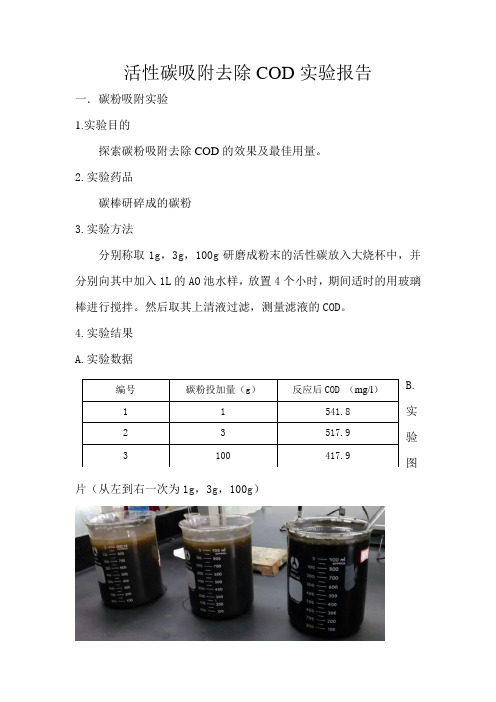
活性碳吸附去除COD 实验报告一.碳粉吸附实验 1.实验目的探索碳粉吸附去除COD 的效果及最佳用量。
2.实验药品碳棒研碎成的碳粉 3.实验方法分别称取1g ,3g ,100g 研磨成粉末的活性碳放入大烧杯中,并分别向其中加入1L 的AO 池水样,放置4个小时,期间适时的用玻璃棒进行搅拌。
然后取其上清液过滤,测量滤液的COD 。
4.实验结果 A.实验数据B.实验图片(从左到右一次为1g ,3g ,100g )编号 碳粉投加量(g )反应后COD (mg/l )1 1 541.823 517.9 3100417.9二.碳粉、碳棒对比吸附实验1.实验目的探索碳粉和碳棒吸附去除COD的效果。
2.实验药品碳棒,碳棒研碎成的碳粉3.实验方法(1)分别称取10g,100g研磨成粉末的活性碳放入大烧杯中,并分别向其中加入0.5L的AO池水样,放置4个小时,期间适时的用玻璃棒进行搅拌。
然后取其上清液过滤,测量滤液的COD。
(2)分别称取10g,100g碳棒放入大烧杯中,并分别向其中加入0.5L 的AO池水样,放置4个小时,期间适时的用玻璃棒进行搅拌。
然后取其上清液过滤,测量滤液的COD。
4.实验结果A.实验数据B.实验图片(从左到右一次为10g碳粉,10g碳棒,100g碳粉,100g 碳棒)三.果壳碳碳粉吸附实验1.实验目的探索果壳碳碳粉吸附去除COD的效果。
2.实验药品果壳碳研碎成的碳粉3.实验方法分别称取0.05g,1g,5g研磨成粉末的果壳碳放入大烧杯中,并分别向其中加入1L的AO池水样,放置4个小时,期间适时的用玻璃棒进行搅拌。
然后取其上清液过滤,测量滤液的COD。
4.实验结果A.实验数据编号碳粉投加量(g)原水COD(mg/l)反应后COD(mg/l)去除率(%)1 0.05686.6 667.2 2.832 1 823.9 -20.003 5 956.7 -39.34B.实验图片(从左到右一次为0.05g,1g,5g)。
吸附实验报告

吸附实验报告吸附实验报告引言:吸附是一种重要的物理现象,广泛应用于化学、材料和环境科学等领域。
本实验旨在通过对吸附现象的研究,探究吸附过程中的各种因素对吸附效果的影响,并进一步了解吸附的机理和应用。
实验方法:1. 实验材料准备:我们选择了活性炭作为吸附材料,并按照一定粒径筛选出均匀的颗粒。
2. 实验装置搭建:我们使用了一台恒温恒湿箱,通过调节温度和湿度来控制实验条件的一致性。
3. 实验操作步骤:a. 将一定质量的活性炭样品放置在吸附装置中,并将其与恒温恒湿箱连接。
b. 调节恒温恒湿箱的温度和湿度,使其保持稳定。
c. 将待吸附物质溶液加入吸附装置中,开始吸附实验。
d. 定时采集吸附后的溶液样品,并通过分析仪器测量其浓度。
e. 记录实验数据并进行数据处理。
实验结果与分析:通过实验,我们得到了吸附过程中溶液浓度随时间的变化曲线。
根据实验数据,我们可以得出以下结论:1. 吸附速率:吸附速率是吸附过程中的重要指标之一。
我们观察到,在初始吸附阶段,吸附速率较快,随着时间的推移逐渐减缓,最终趋于平稳。
这与吸附剂表面活性位点的饱和度有关。
2. 吸附容量:吸附容量是吸附过程中的另一个重要指标。
我们发现,在一定温度和湿度条件下,吸附容量与待吸附物质的浓度呈正相关关系。
这表明活性炭具有较高的吸附能力,能够有效地去除溶液中的目标物质。
3. 温度和湿度对吸附效果的影响:我们对不同温度和湿度条件下的吸附实验进行了比较。
实验结果显示,在较高的温度和湿度条件下,吸附速率和吸附容量均有所增加。
这说明温度和湿度对吸附过程有一定的促进作用。
实验结论:通过本次实验,我们深入了解了吸附现象及其影响因素。
活性炭作为一种常用的吸附材料,具有较高的吸附能力和效果。
温度和湿度对吸附过程有一定的影响,可以通过调节这些条件来优化吸附效果。
吸附技术在环境治理、废水处理和气体净化等领域有着广泛的应用前景。
结语:通过本次吸附实验,我们对吸附现象有了更深入的了解,并探索了吸附过程中的各种因素对吸附效果的影响。
安托因方程活性炭吸附实验报告

安托因方程活性炭吸附实验报告
安托因方程活性炭吸附实验报告
活性炭的吸附性可由下列反应式表示:?= A+ BH2O+ H2OA+
B3H2OH+3H+ C7H2CONO3+ H2O 其中“安托因方程”指的是在温度恒定时,活性炭对某种物质有选择吸附作用。
活性炭的主要成分为碳,还含有少量的氢、氧、氮、硫等元素。
在特定条件下,当水蒸气通过活化了的活性炭时,会与活性炭发生一系列复杂的化学反应,最终生成无毒的水和二氧化碳,并释放出大量的热能。
根据这个原理,人们研制出了各种类型的活性炭。
例如,粉状活性炭具有很强的吸附能力;颗粒活性炭则适合于液相吸附;压块状活性炭常被用来处理废气或用作催化剂载体。
活性炭的另外两个重要特点是耐磨性和耐腐蚀性。
它的耐磨性取决于其中微孔的数目和大小。
微孔越多,活性炭的耐磨性就越好。
然而,活性炭的耐腐蚀性却不尽然。
活性炭的耐腐蚀性取决于它所使用的化学药品。
椰子壳活性炭的耐酸碱性比较好,因此被广泛地应用于废水处理领域。
煤质柱状活性炭也具有良好的耐腐蚀性,但是它的耐氯化物的能力差些。
活性炭除了上述三种基本形态以外,还包括由许多小孔组成的空隙结构。
这种结构可以使活性炭具有很高的吸附能力。
至于多孔性活性炭,它只有一个孔隙,没有其他任何多余的孔隙。
这样的活性炭称之为“无定形炭”。
- 1 -。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
实验3 活性炭吸附实验报告
一、 研究背景:
1.1、吸附法
吸附法处理废水是利用多孔性固体(吸附剂)的表面吸附废水中一种或多种溶质(吸
附质)以去除或回收废水中的有害物质,同时净化了废水。
活性炭是由含碳物质(木炭、木屑、果核、硬果壳、煤等)作为原料,经高温脱水碳
化和活化而制成的多孔性疏水性吸附剂。活性炭具有比表面积大、高度发达的孔隙结构、
优良的机械物理性能和吸附能力,因此被应用于多种行业。在水处理领域,活性炭吸附通
常作为饮用水深度净化和废水的三级处理,以除去水中的有机物。除此之外,活性炭还被
用于制造活性炭口罩、家用除味活性炭包、净化汽车或者室内空气等,以上都是基于活性
炭优良的吸附性能。将活性炭作为重要的净化剂,越来越受到人们的重视。
1.2、影响吸附效果的主要因素
在吸附过程中,活性炭比表面积起着主要作用。同时,被吸附物质在溶剂中的溶
解度也直接影响吸附的速度。此外,pH 的高低、温度的变化和被吸附物质的分散程度也对
吸附速度有一定影响。
1.3、研究意义
在水处理领域,活性炭吸附通常作为饮用水深度净化和废水的三级处理,以除去水中
的有机物。活性炭处理工艺是运用吸附的方法来去除异味、某些离子以及难以进行生物降
解的有机污染物。
二、实验目的
本实验采用活性炭间歇的方法,确定活性炭对水中所含某些杂质的吸附能力。希望达
到下述目的:
(1)加深理解吸附的基本原理。
(2)掌握活性炭吸附公式中常数的确定方法。
(3)掌握用间歇式静态吸附法确定活性炭等温吸附式的方法。
(4)利用绘制的吸附等温曲线确定吸附系数:K、1/n。K为直线的截距,1/n为直线的斜率
三、主要仪器与试剂
本实验间歇性吸附采用三角烧瓶内装人活性炭和水样进行振荡方法。
3.1仪器与器皿:
恒温振荡器1台、分析天平1台、分光光度计1台、三角瓶5个、1000ml容量瓶1个、
100ml容量瓶5个、移液管
3.2试剂:活性炭、亚甲基蓝
四、实验步骤
(1)、标准曲线的绘制
1、 配制100mg/L的亚甲基蓝溶液:称取0.1g亚甲基蓝,用蒸馏水溶解后移入1000ml容
量瓶中,并稀释至标线。
2、 用移液管分别移取亚甲基蓝标准溶液5、10、20、30、40ml于100ml容量瓶中,用蒸
馏水稀释至100ml刻度线处,摇匀,以水为参比,在波长470nm处,用1cm比色皿测定吸
光度,绘出标准曲线。
(2)、吸附等温线间歇式吸附实验步骤
1、用分光光度法测定原水中亚甲基蓝含量,同时测定水温和PH。
2、将活性炭粉末,用蒸馏水洗去细粉,并在105℃下烘至恒重。
3、在五个三角瓶中分别放入100、200、300、400、500mg粉状活性炭,加入200ml水样。
4、将三角瓶放入恒温振荡器上震动1小时,静置10min。
5、吸取上清液,在分光光度计上测定吸光度,并在标准曲线上查得相应的浓度,计算亚甲
基蓝的去除率吸附量。
五、注意事项
1、实验所得的qe若为负值,则说明活性炭明显的吸附了溶剂,此时应调换活性炭或调换
水样。
2、在测水样的吸光度之前,应该取水样的上清液然后再分光光度计上测相应的吸光度。
3、连续流吸附实验时,如果第一个活性炭柱出水中溶质浓度值很小,则可增大进水流量或
停止第二、三个活性炭柱进水,只用一个炭柱。反之,如果第一个炭柱进出水溶质浓度相
差无几,则可减少进水量。
4、进入活性炭柱的水中浑浊度较高时,应进行过滤去除杂质。
六、实验结果与分析
6.1实验结果
亚甲基蓝浓度与吸光度
序号 1 2 3 4 5
浓度mg/l
吸光度A1
亚甲基蓝标准曲线
y = 0.0052x + 0.0497
R2 = 0.9982
0
0.05
0.1
0.15
0.2
0.25
05101520253035
亚甲基蓝浓度(mg/L)
吸
光
度
A
活性炭间歇吸附试验记录
lgK 1/n K n
活性炭投加量m 吸光度A 原亚甲基蓝浓度
C0/(mg/L) 吸附平衡后 亚甲基蓝 浓度C/(mg/L) 平均值 logC C0-C (C0-C)/m Log(C0-C)/m
100mg
200mg
300mg
400mg
500mg
吸附等温线
(1)根据测定数据绘制吸附等温线;
(2)根据Freundlich 等温线,确定方程中常数K,n;
(3)讨论实验数据与吸附等温线的关系。
思 考 题
1.吸附等温线有什么现实意义?
(1)宏观地总括吸附量、吸附强度、吸附状态等作为吸附现象方面的特性;
(2)判断吸附现象的本质,如属于分配(线性),还是吸附(非线性);
(3)用于计算吸附剂的孔径、比表面等重要物理参数;
(4)吸附等温曲线用途广泛,在许多行业都有应用,如地质科学方面、煤炭方面。
2.作吸附等温线时为什么要用粉状炭?
废水中的物质经活性炭吸附后分散好,容易单层吸附。
3.实验结果受哪些因素影响较大,该如何控制?
实验结果受实验温度、吸附质的分压、活性碳性质(比表面积、孔隙率等)
