高一化学硅酸盐工业
高中化学最基础考点系列考点硅酸盐工业新人教必修

考点12 硅酸盐工业【考点定位】本考点考查硅酸盐工业,了解自然界中硅酸盐的存在,常见的硅酸盐工业,重点认识硅酸盐由盐的书写改写为氧化物的形式即改写的一般方法。
【精确解读】1.硅酸盐:(1)自然界中硅酸盐的存在:硅酸盐是构成地壳岩石的主要成分,自然界中存在的各种天然硅酸盐约占地壳质量的5%,粘土的主要成分是硅酸盐.粘土是制造陶瓷器的主要原料.(2)用氧化物的形式来表示硅酸盐的方法:①先将硅酸盐中所含的各元素用氧化物形式表示;②将各种氧化物按下列顺序进行排列,各氧化物之间用“•”开.例如:金属氧化物(有多种金属氧化物时按金属活动顺序表排列)→SiO2→H2ONa2SiO3:Na2O•SiO2 A12(Si2O5)(OH)4:A12O3•2SiO2•2H2O2.硅酸盐工业:以含硅物质为原料经加热而制成硅酸盐产品的工业,叫做硅酸盐工业.如制造水泥、玻璃、陶瓷等的工业都属于硅酸盐工业。
【精细剖析】1.硅酸盐可以拆分成金属氧化物的形式,玻璃、粘土、普通水泥等含有硅酸盐,但硅芯片含有单质硅,不含有硅酸盐。
2.硅酸盐由盐的书写改写为氧化物的形式即改写的一般方法归纳为:碱性氧化物、两性氧化物、酸性氧化物、水(xMO•nSiO2•mH2O).注意:①氧化物之间以“•”隔开;②系数配置出现的分数应化为整数。
如:正长石KAlSi3O8不能改写成 K2O•Al2O3•3SiO2,应改写成K2O•Al2O3•6SiO2。
③金属氧化物在前(活泼金属氧化物→较活泼金属氧化物),非金属氧化物在后,若同一元素有变价,那么低价在前,高价在后,H2O 一般写在最后。
【典例剖析】《青花瓷》中所描绘的“瓶身描绘的牡丹一如你初妆”、“色白花青的锦鲤跃然于碗底”等图案让人赏心悦目,但古瓷中所用颜料成分一直是个谜,近年来科学家才得知大多为硅酸盐,如蓝紫色的硅酸铜钡(BaCuSi2O6).下列关于硅酸铜钡的说法不正确的是( )A.是一种硅酸盐B.性质稳定,不易脱色C.易溶于强酸和强碱D.可用氧化物形式表示为BaO•CuO•2SiO2【剖析】A.硅酸铜钡,阴离子是硅酸根,阳离子是铜离子和钡离子,为硅酸盐、铜盐、钡盐,所以硅酸铜钡属于复盐中的硅酸盐,故A正确;B.BaCuSi2O6中铜显+2价,二价铜离子不容易被还原,所以性质较稳定,不容易褪色,故B正确;C.BaCuSi2O6是弱酸盐,所以能和强酸反应,和强碱不反应,故C错误;D.硅酸盐用氧化物形式表示时,书写顺序为:活泼金属氧化物、不活泼金属氧化物、二氧化硅、水,所以硅酸铜钡用氧化物形式表示:BaO•CuO•2SiO2,故D正确;故答案为C。
高一化学第七章 硅和硅酸盐工业
第七章硅和硅酸盐工业本章目标1.掌握碳族元素的原子结构特点和性质递变规律。
2.认识硅及其重要化合物的性质和用途,初步了解硅和二氧化硅的结构以及与性质的关系。
3.了解水泥、玻璃的主要成分和简单生产原理。
4.了解一些新型无机非金属材料。
本章重点碳族元素性质变化规律,硅和二氧化硅的性质。
课时分配§7-1 碳族元素教学目标1.掌握和解释碳族元素的性质及其递变规律。
2.进一步了解运用元素周期律知识学习同族元素性质及其递变规律的方法,并运用这些知识学习碳族元素及其化合物的知识。
3.培养学生的思考、判断能力。
教学重难点用原子结构理论解释碳族元素的性质及其递变规律。
硅和二氧化硅的结构和性质。
教学过程[复习]结构上:1.同周期元素共同点是_____________;递变性是________________。
2.同主族元素共同点是_____________;递变性是________________。
性质上:同周期元素递变性是:从左到右___________________________________。
同主族元素递变性是:从上到下___________________________________。
[新课]一、碳族元素(一)碳族元素的原子结构特点1.位于周期表_____族,包括______________________________。
2.最外层均有____个电子。
3.主要价态:_____________。
______________的+4价化合物是稳定的,而___的+2价化合物是稳定的。
4.碳、硅主要成键形式_________。
(为什么?)(二)碳族元素性质的递变(三) 碳的同素异形体碳有多种同素异形体,重要的有_______、_______及_______等,其中____中存在分子间作用力。
它们的熔点从高到低是:__________________________________。
[阅读]课本P148二、硅1.物理性质a.硅的存在和形态:________________________________________________。
高一化学硅酸盐工业

教学目标 1、掌握碳族元素的名称、元素符号、在出 周
期表中位置及原子结构特点。 2、掌握碳族元素性质上的相似性,递变性和
特殊性。并能用物质结构和元素周期律等 知识解释其原因。 3、认识硅的化学性质及用途。
教学重点 碳族元素性质的递变规律、硅的化学性质
教学难点 根据所学碳以及元素周期律的知识,归纳
出一些硅的化学性质。
Si 价主要有+4和
+2,易形成共
核 电 荷
原 子 半
熔 沸 点
单非 质金 密属
最氢 高化 价物
价化合物。
数 径 降 度 性 氧的
Ge
增 增 低 增 减 化稳
大大
大 弱 物定
电
2、气态氢化物 子
、 对性 金 应减
的通式:RH4
Sn
层 增 多
属 水弱 性化 增物
3、最高价氧化
强的
物对应的水化
0
下一页
C60及其应用前景 C60的发现 1985年,美国科学家克罗托(H.W.K.kroto)等用质
谱仪,严格控制实验条件,得到以C60为主的质谱图。由 于受建筑学家布克米尼斯持•富勒(BuckminsterFuller)
设计的球形薄壳建筑结构的启发,克罗托(kroto)等提
出 C60是由60个碳原子构成的球形32面体,即由12个 五边形和20个六边形构成。其中五边形彼此不相连,
高一化学硅和硅酸盐工业的综合提高
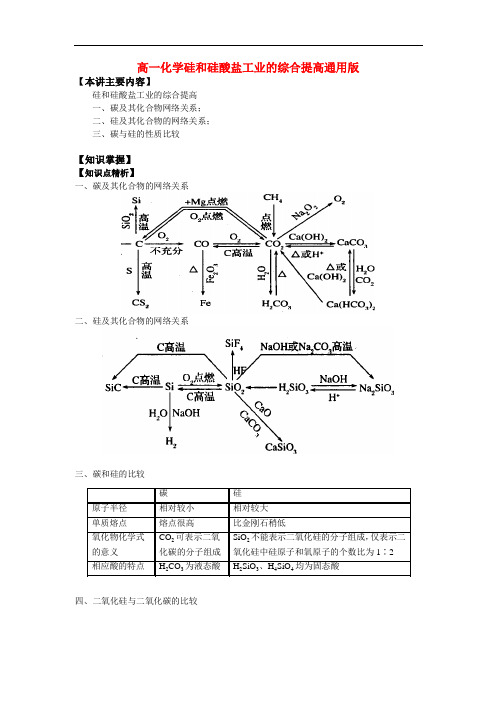
高一化学硅和硅酸盐工业的综合提高通用版【本讲主要内容】硅和硅酸盐工业的综合提高一、碳及其化合物网络关系;二、硅及其化合物的网络关系;三、碳与硅的性质比较【知识掌握】【知识点精析】一、碳及其化合物的网络关系二、硅及其化合物的网络关系三、碳和硅的比较四、二氧化硅与二氧化碳的比较二氧化碳(CO 2)熔沸点低,常温室气体,微溶于水五、硅酸盐工业的比较【解题方法指导】例1、某二价金属碳酸盐和碳酸氢盐的混合物跟足量盐酸反应,消耗H +和产生CO 2的物质的量之比为6:5,该混合物中碳酸盐和碳酸氢盐的物质的量之比为A 、1:1B 、1:2C 、1:3D 、1:4 解析:设二价金属为M ,正盐的物质的量为x ,酸式盐的物质的量为y ,则有: MCO 3 + 2HCl =MCl 2 + CO 2↑+ H 2O x 2x xM (HCO 3)2 + 2HCl =MCl 2 + 2CO 2↑+ 2H 2O y 2y 2y由题意得:2x+2y x+2y =65 ,解得x y =12答案:B例2、已知A 是一种不溶于水的酸酐。
根据下图转化关系,回答:(1)A 是___________________,B 是___________________,D 是___________________。
(2)写出①→⑤各步反应的化学方程式,如是离子反应请改写成离子方程式。
①____________________________ ②____________________________ ③____________________________ ④____________________________ ⑤____________________________解析:本题的突破口在于“A 是一种不溶于水的酸酐”,据此可推知A 是SiO 2。
联系SiO 2的相关性质,SiO 2跟Na 2CO 3高温下反应生成Na 2SiO 3和CO 2,二者在水溶液中会反应生成H 2SiO 3沉淀,H 2SiO 3受热分解生成SiO 2,验证A 为SiO 2是正确的。
高一化学硅酸盐工业简介

高一化学硅酸盐工业简介第二节硅酸盐工业简介Ⅰ学习重点1.从原料.反应条件.原理.主要设备,主要成份及其表示方法等方面比较普通玻璃和普通水泥的生产方法2.硅酸盐的表示方法,玻璃态物质的特点一.选择题1.下列不属于硅酸盐工业产品的是( )A.水泥B.陶瓷C.砖瓦D.石英玻璃2.下列物质不属于硅酸盐的是( )A.粘土B.硅藻土C.Al2(Si2O5)(OH)4D.Mg2SiO43.生产水泥的主要设备是( )A.熔炉B.回转窑C.沸腾炉D.合成塔4.某硅酸盐样品中锌的质量分数为58.6%,其化学组成用氧化物形式可表示为nZnO·SiO2,则n值等于( )A.0.5B.1C.2D.35.在天然环境中用自然界中的物质,且在常温下必须在空气中才能硬化的是( )A.石灰抹墙后变硬不再溶于水B.熟石膏调水后灌入模中变硬C.水玻璃抹在蛋皮上不久变硬呈玻璃状D.水泥砂浆浇灌后变硬6.在水泥中加石膏的目的是( )A.调节水泥的机械强度B.调节水泥的硬化速度C.降低水泥的成本D.扩大水泥的使用范围7.关于水泥的下列说法,错误的是( )A.水泥遇水就会发生硬化B.水泥是化合物C.水泥砂浆和混疑土必定要有水泥D.水泥回转窑中生料和空气.煤粉是逆向操作的8.用1 L 1.0mol/LNaOH溶液吸收标准状态下17.92 L CO2,所得溶液中CO2-3和HCO-3的摩尔浓度之比约是( )A.1∶3B.2∶1C.2∶3D.3∶29.下列物质中,制取时不需用石灰石作原料的是( )A.硅酸B.水泥C.玻璃D.生石灰10.过量的泥沙.纯碱和生石灰共熔后可生成①水泥②玻璃③瓷器④混凝土⑤一种硅酸盐产品( )A.①和④B.②和⑤C.③D.②11.根据水泥和玻璃的生产,总结出硅酸盐工业的一般特点是①生成物是硅酸盐;②反应条件是高温;③含有硅的物质作原料;④反应原理是一系列复杂的物理-化学变化( )A.①③B.①②③C.①②③④D.①③④12.与普通玻璃主要成分一样的是( )A.钢化玻璃B.玻璃纸C.有机玻璃D.水玻璃13.欲观察氢气燃烧的焰色,燃气导管口的材料最好的是( )A.钠玻璃B.钾玻璃C.石英玻璃D.铜管14.下列物质有固定熔点的是( )A.玻璃B.水泥C.水玻璃D.Na2O·SiO215.在实验室熔化NaOH固体,不能选用的坩锅是( )A.铁坩锅B.瓷坩锅C.铝坩锅D.石墨坩锅16.在玻璃工业.水泥工业中都用到的原料是( )A.纯碱B.石英C.石灰石D.粘土17.下列物质稳定性由强到弱的是①CaSiO3,②H2CO3,③CaCO3,④Ca(HCO3)2()A.①②③④B.②④③①C.①③④②D.①④③②18.下列关于钢化玻璃的叙述中错误的是( )A.它的成分是Na2SiO3.CaSiO3和SiO2熔化在一起所得到的物质B.是把普通玻璃放在电炉里加热,使之软化,然后急速冷却制得的C.它是具有空间网状结构的原子晶体,硬度很大,熔点也很高D.它的机械强度比普通玻璃大4~6倍,不易破碎,且破碎时,碎块没有尖利的棱角二.填空题19.制造普通水泥的主要原料有和.普通水泥的主要成分有(写名称) . 和,它们的化学式分别是.和.水泥的主要性能是20.根据下图中所表示的变化关系,写出各物质的化学式.A是,B是,C是,D是,E是.21.工业上制造普通玻璃的主要原料是. . ,主要设备是,主要原料熔化后,发生的主要化学反应是. .普通玻璃的成分是.三.计算题22.为熔制钾玻璃准备如下熔料:360份重的石英砂,67.2份重的苛性钾和88.8份重的熟石灰 .假定这些熔料不含杂质.(1)计算在制得的钾玻璃中各氧化物的质量分数.(2)用氧化物的形式表示钾玻璃的组成.23.SiO2和CaCO3的混合物26g,在高温下加热到质量不再改变,冷却后称质量为17.2g. (1)写出可能发生反应的化学方程式;(2)求产生的气体在标准状况时的体积;(3)求原混合物中的SiO2的质量.第二节硅酸盐工业简介参考答案一.1.D 2.B 3 .B 4.C5.AC6.B7.B8.A 9.B 10.B 11.C 12.A 13.C 14.C 15.BC 16.C 17.C 18.C二.19.石灰石.粘土;硅酸二钙.硅酸三钙.铝酸三钙.2CaO·SiO2,3CaO·SiO2O 3.3CaO·Al2O3,水硬性20.Si.Na2SiO3.H4SiO4.H2SiO3.SiO221.纯碱.石灰石.石英;玻璃熔炉;高温SiO2+Na2CO3Na2SiO3+CO2↑高温SiO2+CaCO3CaSiO3+CO2↑Na2SiO3.CaSiO3.SiO2三.22.(1)K2O.11.7% CaO 13.9% SiO2 74.4%(2)K2O·2CaO·10SiO2△23.(1)SiO2+CaCO3CaSiO3+CO2↑△CaCO3 CaO+CO2↑(2)4.48L(3)6g。
高一化学硅酸盐工业

丛林法则在那些人思想里太过根深蒂固,影响了美国人采取更有建设性的作为。老子说:大国者下流,说的是大国、小国之间的相处之道。但美国政府在某些方面,只是思想很下流而已。
古巴还有一项重要的创汇资源,那就是医生。古巴的医生、医疗水平都很高。查韦斯当政时期,委内瑞拉之所以为古巴免费提供石油,就是因为古巴有几千名医生在为委内瑞拉来源之一。但是这些医生来中国?恐怕也不现实。nb88新博客户端
古巴距离美国的佛罗里达仅有200来公里,在初次了解这个国家的时候,还觉得古巴是个奇迹——它竟然在超级大国的眼皮子底下傲然屹立这么多年,真是不简单。然而到了那里才发现,古巴民众 真是受了苦。美国人的全球制裁,是它的霸气,也是它的蛮横,更是它的罪孽。
2018年5月18日古巴发生了空难,造成100多死亡,其实就是美国进行经济封锁的结果:欧美企业不与古巴做生意,没有新式飞机进入古巴,古巴只能去墨西哥一家小公司寻求帮助。于是,这家只有 三架飞机的小公司,把其中一架租给了古巴。飞机的使用年限通常为25—30年,而这架飞机已经39岁高龄……
高一第七章硅和硅酸盐工业

第七章硅和硅酸盐工业第一节碳族元素教学目的与要求:1、使学生了解碳族元素的性质及其递变规律2、使学生进一步了解运用元素周期律知识学习同族元素性质及其递变规律的方法,并运用这些知识学习碳族元素及其化合物的知识;3、培养学生的思考、判断能力。
教学重点:1、碳族元素性质递变规律2、硅和二氧化硅的化学性质教学难点:硅及二氧化硅的化学性质。
教学过程:让学生尽可能多地回忆初中及前面化学所学的碳元素的化合物:一氧化碳、二氧化碳、碳酸钠、碳酸氢钠、甲烷、乙醇、乙酸等。
设问:1、碳元素的结构有什么特点呢?2、碳元素所在的周期表中的位置如何呢?一、碳族元素列表比较:新课的延伸:关于C60介绍:安排同学们阅读课本资料,强调:1: 1985年发现,1996年三位化学家因此荣获诺贝尔化学奖;碳有多种同素异形体:金刚石、石墨、C n系列分子(C60是一种单质,它不是化合物,是金刚石和石墨的同素异形体;是由60个C原子靠共价键结合而成的,其中球面由12个五边形和20个六边形构成的球形32面体,其中五边形彼此不相连,只与六边形相连。
由于C60分子的结构酷似足球,所以又称其为足球烯。
除C60外,具有封闭笼状结构的的还可能有C28、C32、C50、C70、C84……C240、C540等,统称为富勒烯,不存在离子键)。
二、硅讲述:硅在地壳中分布很广,含量居第二位,仅次于氧。
单质(自然界无游离态):晶体、无定形1、硅元素二氧化硅、硅酸盐:构成矿物及岩石2、晶体硅的物理性质灰黑色、金属光泽、硬而脆,结构与金刚石相似,有较高的熔沸点及硬度;导电性介于导体与半导体之间,与锗相似,是良好的半导体材料。
3、硅的化学性质与碳元素比较,化学性质相似。
安排【讨论】①常温下,可与氟气、氢氟酸、强碱反应,不与氧气、氯气、硫酸、硝酸反应②加热条件下,在氧气中燃烧:Si+O2=SiO2+Q硅的用途集成电路、晶体管、硅整流器、太阳能电池;硅合金:4%合金——变压器铁芯 15%合金——耐酸设备5、硅的制备工业上用二氧化硅为原料提取:SiO2+2C ==Si+2CO↑粗硅提纯:粗硅SiCl4纯硅碳和硅的比较三、二氧化硅1、存在与物理性质:广泛存在于自然界中,也叫硅石,艰硬难熔的固体,代表物为石英晶体——水晶2、化学性质:酸性氧化物,不与水、除氢氟酸以外的酸反应SiO2 +CaO = CaSiO3SiO2 +2NaOH =Na2SiO3+ H2O(提示:硅酸钠溶液为粘稠状液体,常用着矿物胶)讨论:①实验室中盛放碱液的试剂瓶为什么不用玻璃塞?②实验室盛放氢氟酸的试剂瓶为什么不用玻璃瓶?(因为玻璃中含有SiO2,碱液与SiO2反应生成粘稠的硅酸钠,把玻璃塞与瓶口粘住,不能打开。
高一化学最新课件-聊城地区化学硅酸盐工业(整理) 精品

A组题
玻璃的主要成分是什么?
答案:硅酸钠(Na2SiO3) 硅酸钙(CaSiO3) 二氧化硅(SiO2)
B组题
制造蓝色玻璃、绿色玻 璃是分别在普通玻璃中加入 了何种物质?
答案:蓝色玻璃是加入了氧化钴(Co2O3), 绿色玻璃是加入了二价铁元素。
C组题
制陶瓷器的主要原料是什么?
答案:制陶瓷器的主要原料是粘土
B组听题
制造水泥的主要原料是什么?
答案:制造水泥的主要原来是粘 土和石灰石
C组题 制造水泥的主要设备是什么?
答案:水泥回转窑
D组题
普通水泥的主要成分是什么?
答案:硅酸三钙(3CaO.SiO2) 硅酸二钙( 2CaO.SiO2) 铝酸三钙( 3CaO.Al2O3 )
A组题
什么是 混凝土?什么是钢筋混凝土?
7、过量的泥沙、纯碱和生石灰熔化后生成 ①水泥 玻璃 ③瓷器 ④混凝土 ⑤一种硅酸 盐产品 (B ) A. ① ④ B. ② ⑤ C. ③ D. ②
8、在水泥中加入石膏的作用是
调节水泥的硬化速度 —————————————————————
水泥 砂子 碎石 将—————— 按 -、——————————。——————— 一定比例混合硬化后称为混凝土。
玻璃
原理 Na2CO3+ SiO2 ==== Na2SiO3 + CO2↑ CaCO3+ SiO2 ==== CaSiO3 + CO2↑ 普通水泥的成分 Na2SiO3、CaSiO3、SiO2熔合在一 起而形成在玻璃态物质(或者 Na2O CaO 6SiO2) 设备:玻璃窑 有色玻璃 钢化玻璃 特种玻璃 光学玻璃 玻璃纤维 返回
3.钢筋混凝土常用于建造什么?
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
大院里的十八棵小白杨也长成了十八位顶天立地的帅小伙,风吹不折腰,雪压不低头。他们是真正的卫士,有着挺拔的身躯和昂扬的头颅,纵是风雨飘摇,霜雪交加,亦无法使其屈服半分,伸向苍 穹的初心永远也不会改变。nb88新博客户端
我爱这六位风情万种的柳姑娘,因为她们是春天的信使,总是最先感知春的萌动,春风一打个调情的口哨,便都春心荡漾,不顾一切地吐露出满树嫩绿鹅黄的新芽,张开了六张灿烂如花的笑脸,苗 条的身姿随风摇晃,蹁跹的舞步柔美轻盈,那超凡脱俗的美色使我家的大院增光添彩。春风就像一把神奇的梳子,把每一根柳枝梳理得丝滑飘逸,垂挂在空中长长短短,错落有致,跟着风儿,摇摆着曼 妙的舞姿。一只只俏丽的小鸟,欢快地在枝条间蹦蹦跳跳,叽叽喳喳唱个不停。我置身这如诗忆。
当夏天来临的时候,六位柳姑娘更加枝叶繁茂,深绿成荫,各自撑起了绿色的大伞,枝叶在风的鼓动下,像仙女似地摇曳,翩翩起舞,给整个大院带来了舒心的凉爽。在火热的阳光里,过往的路人 总要在这里的浓荫下歇脚,不管有多么的燥热,多么的汗水涔涔,只要在这里呆上片刻工夫,尽情享受一下凉风的吹拂,就会感到暑意顿消,神清气爽。午后酷热难耐,不少人来到柳荫下乘凉。女人们 在家长里短的说笑中,用自己灵巧的双手缝着生活的酸甜苦辣,补着岁月中的遗失缺憾。孩子们也来树荫下玩耍,享受着柳树给他们带来的风凉。柳树无私地奉献着自己,为人们遮挡着炙热的阳光。在 月朗星稀、杨柳依依的夜晚,“月上柳梢头,人约黄昏后”,有的青年人在柳荫下相会,月为证,柳为媒,平添了许多的浪漫故事与爱情篇章。
