安维汀的作用机制
姜斌:靶向药物的分类及适应症

姜 斌 教授
第九人民医院
上海交通大学医学院
Targeted Therapies
Panitumumab Cetuximab
Bevacizumab
Erlotinib
Sunitinib Sorafenib
Sorafenib
Temsirolimus
Chemotherapy
Inhibition of programmed cell death (apoptosis)
NSCLC已进入驱动基因决定 治疗选择的时代
Adenocarcinoma 1999 组织病理决定化疗选择
Adenocarcinoma 2010 以肿瘤驱动基因作为靶点的治疗选择
KEGFR ras B-raf Her2 PIK3 ALK CA MET Unknow
Horn L, Pao W. J Clin Oncol 2009;26:4232–5
种酪氨酸激酶
在各种肿瘤中相互交织
Manning G, et al. Science 2002;298:1912–34
蛋白酶抑制剂与各种酶结合情况
volume 10 number 4 , 2009 nature immunology
抗EGFR类药物
EGFR活化信号转导途径
Ciardiello F.
外显子18 G719x
外显子20 T790M
外显子20
S768I
外显子21 L861Q
ShepherdFA, et al. ASCO 2015 poster 7539
IPASS临床研究结果
Tony S. Mok et al. Gefitinib or Carboplatin–Paclitaxel in Pulmonary Adenocarcinoma. N Engl J Med 2009;361:947-57.
常用化疗药物的使用

常见化疗方案
肺癌:培美曲塞(D1)+卡铂(D1) 食管交界腺癌:FOLFOX方案:奥沙利铂+亚 叶酸钙+氟尿嘧啶( 微量泵泵入) 食管鳞癌(TP方案):紫杉醇+铂类(顺铂)
常见化疗方案
FOLFOX方案:奥沙利铂+亚叶酸钙+氟尿嘧 啶 TP方案:紫杉醇+顺铂 GC方案:吉西他滨+卡铂 GP方案:吉西他滨+顺铂 同步化疗:奈达铂、顺铂
化疗药物注意要点
表阿霉素:不可与碱性药物、地塞米松、 虎珀氢考同时点注。与氨茶碱接触可使溶 液变成紫兰色。
希罗达 :65岁老年人比年轻人更易对 希罗达产生毒性,更应密切监测。
化疗药物注意要点
大剂量MTX: 滴完后12小时开始应用 CF,每6小时一次,共3天,用药前一天要水 化、碱化,使尿量每日在3000ml以上,并 保持碱性,PH大于7。
化疗的概念
化疗药物治疗是目前治疗肿瘤的主要手段 之一。 化疗药物种类多,作用机制各异,所以在 执行化疗时护士应严格按照化疗的各种规 范执行。 要求给药剂量精确,给药途径、时间正 确,先后排列顺序正确,预处理正确,如果 错误使用,可影响疗效,造成严重并发症 甚至死亡。
化 疗 的 给 药 途 径
口服给药
11
常见化疗方案
乳腺癌: ACT:环磷酰鞍+表阿霉素+紫杉醇 AT:阿霉素+紫杉醇(多西紫杉醇)
淋巴瘤 : 环磷酰胺+表阿霉素+长春新碱+强的松
常见化疗药物注意要点
顺铂:不能接触铝制品,有肾脏毒性, 大剂量使用时要水化,在给药前12小时和 给药后6小时。
化疗药物注意要点
依立替康(艾力 开普拓):滴注时间为90分钟,会引 起腹泻
贝伐珠单抗治疗结直肠癌的作用及耐药机制

THE RESISTANCE MECHANISM ANDROLES OF BEVACIZUMAB INTREATMENT OF COLORECTALCANCERABSTRACTBackground: Bevacizumab has been demonstrated to be effective in the treatment of colorectal cancer and becomes one of the most common drugs for the treatment of advanced colorectal cancer. However, the resistance of colorectal cancer to Bevacizumab affects the long-term use of Bevacizumab. The recent research results have shown that the Bevacizumab resistance may be related with tumor microenvironment, the activation of other angiogenesis pathway, immune suppression and so on. But the mechanisms involved Bevacizumab resistance are still fully understood.Objective: In this study, we have investigated the roles and mechanism of bevacizumab resistance.Methods: The colon cancer DLD-1 cells were injected s.c. into nude mice and generated a colon cancer xenograft model. When tumor size reached to 100 mm2, Bevacizumab was injected i.p. into nude mice twice each week. Tumor size was measured weekly.Four weeks after theinjection, the xenograft tumor tissues were harvested for isolation of tumor cells. The tumor cells isolated from tumor treated with Bevacizumab treatment were injected s.c. into nude mice to establish second xenograft model. Then Bevacizumab was injected i.p. into nude mice with second xenograft twice each week. Tumor size was measured weekly. Four weeks after the treatment, the xenograft tumor tissues were harvested for histological analysis and immunohistochemistry staining.Results:Bevacizumab treatment significantly inhibited colon cancer xenograft growth at first time treatment. For second generation of xenograft models using tumor cells isolated from Bevacizumab-treated tumor, Bevacizumab treatment still inhibited xenograft tumor growth. The results suggest that Bevacizumab for colon cancer treatment is still effective. Bevacizumab one cycle treatment is not enough to induce the resistance of Bevacizumab. Immunohistostaining showed that the expression of Survivin was gradually increased in the tumor tissues treated with bevacizumab from 3-week treatment to 9-week treatment. The number of CD31 positive cells was significantly lower in the xenograft tumor tissues from bevacizumab-treated mice that those from control-treated mice.Conclusion: Bevacizumab treatment could inhibit xenograft tumor growth even in the tumors that have once treated with bevacizumab. Survivin may play a certain role in mediating the resistance ofbevacizumab. The exact role of Survivin in mediated the resistance of bevacizumab will be further studied.KEY WORDS:colorectal cancer,Bevacizumab,drug resistance,Survivin目录第一章研究背景 (1)第二章贝伐珠单抗动物耐药模型构建 (6)1.材料 (6)1.1 实验动物 (6)1.2 试剂 (6)1.3 实验器材 (6)2.方法 (7)2.1 裸鼠移植瘤模型构建 (7)2.2 观察指标 (7)2.3 移植瘤处理 (7)3.结果 (7)4.讨论 (8)本章小结 (10)第三章探寻预测耐药的生物标志物 (12)1.材料 (12)1.1 组织标本 (12)1.2 主要试剂 (13)1.3 器材及设备 (13)2.方法 (13)2.1 组织脱水及石蜡包埋 (13)2.2 免疫组化染色步骤 (14)3.结果 (15)4.讨论 (19)本章小结 (20)第四章 Survivin稳定转染细胞株构建 (21)1.材料 (21)1.1 细胞株 (21)1.2 pcDNA3.1(+)-Survivin质粒及pcDNA3.1(+)质粒 (21)1.3 主要试剂 (21)1.4 实验器材 (22)2.实验方法 (22)2.1 细胞培养 (22)2.2 脂质体2000转染 (22)2.3 G418筛选克隆 (22)2.4 Western Blot实验验证稳转细胞株。
超药品说明书用药的管理规定

超药品说明书用药类型
超禁忌症用药
•β受体阻滞剂适应症的变化
临床第一个β-受体阻滞 剂普萘洛尔于1962年问世,对 心绞痛有效,因在动物体表现 的副作用而未被推广,但其发 明者James W Black 1988年因 提出β-受体阻滞剂的概念而获 诺贝尔医学奖
超药品说明书用药现状
国外资料显示,在普通成人用药中,超说明书用 药占 7.5% -40%;统计表明,超说明书用药在儿科 住院患者中高达 50%-90%。 在一项针对欧洲5国儿 科病房的调查中发现,46%的处方中存在超说明书用 药的情况。 在孕妇中,一项对英国利物浦妇产科医 院17000 张产前处方的连续抽样调查显示,75%的处 方存在超说明书用药的情况,但其中绝大多数被认 为是安全的。
超药品说明书用药类型
超适应症用药
•盐酸普萘洛尔片用于治疗偏头痛。
阻断去甲肾上腺素能神经递质或拟肾上腺素药 与受体结合而产生效应, 能降低交感神经功能及调节 血小板聚集能力, 降低血小板粘附聚集和5-HT的再 摄取, 可能通过阻止血管扩张、稳定细胞膜和增加组 织供氧来预防偏头痛。
用法用量:20mg,tid
超药品说明书用药概念
美国
美国医疗机构药师协会将“超说明书用药”定义为: 药品使用的适应证、给药方法或剂量不在美国食品 药品管理局(FDA)批准的说明书之内的用法。
中国
超说明书用药又称“ 药品说明书外用法”、 “ 药品未注册用法”,是指药品使用的适应证、
剂量、疗程、途径或人群等未在药品监督管理部 门批准的药品说明书记载范围内的用法。
妇女、儿童、老年人等)用药信息
1
或超出年龄范围用药
• 超适应症用药
2
• 超用法用量用药
3
分子靶向药物
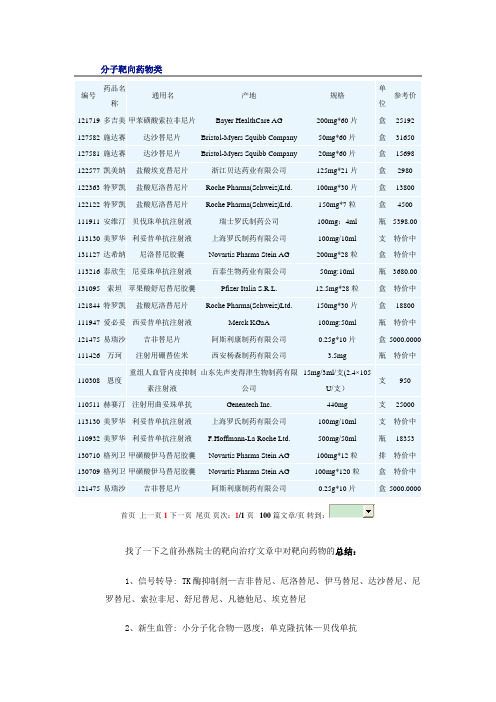
分子靶向药物类首页上一页1下一页尾页页次:1/1页100篇文章/页找了一下之前孙燕院士的靶向治疗文章中对靶向药物的总结:1、信号转导: TK酶抑制剂—吉非替尼、厄洛替尼、伊马替尼、达沙替尼、尼罗替尼、索拉非尼、舒尼替尼、凡德他尼、埃克替尼2、新生血管: 小分子化合物—恩度;单克隆抗体—贝伐单抗3、调控基因: 曲妥珠单抗4、EGFR受体: 小分子化合物—TKIs;单克隆抗体—西妥昔单抗、尼妥珠单抗、帕尼单抗5、表面受体: 利妥昔单抗因为这个是2010年总结的药物,过了1年多,所以里面肯定不全,先将这些慢慢的进行整理,后面再逐步添加新的。
吉非替尼商品名:易瑞沙英文名:Gefitinib Tablet 、Iressa、ZD1839结构式:适应症及作用机制:吉非替尼( gefitinib)是第一个批准用于治疗晚期非小细胞肺癌的分子靶向药物,通过竞争性结合到酪氨酸激酶的ATP结合区,抑制EGFR 酪氨酸激酶的活化,并能抑制EGFR的磷酸化作用和下游区的信号转导通路。
规格:250mg x 10 片/盒用法用量:推荐剂量为250mg(1片)每日1次,空腹或与食物同服。
不推荐用于儿童或青少年,对于这一患者群的安全性和疗效尚未进行研究。
不良反应:最常见的药物不良反应( ADRs )为腹泻、皮疹、瘙痒、皮肤干燥和痤疮,发生率20%以上,一般见于服药后一个月内,通常是可逆性的。
更多阅读分子靶向药物易瑞沙Iressa 吉非替尼治疗晚期或转移性非小细胞肺癌吉非替尼治疗晚期NSCLC2012-03-12 回复阳光明媚3楼厄洛替尼商品名:特罗凯英文名:Erlotinib Hydrochloride Tablets, Tarceva结构式:适应症及作用机制:可试用于两个或两个以上化疗方案失败的局部晚期或转移的非小细胞肺癌的三线治疗。
厄洛替尼(erlotinib) 可与ATP 结合区可逆性结合,并且完全抑制EGFR 酪氨酸激酶的自主磷酸化作用,从而阻断下游区EGFR 信号通路,引起细胞周期停滞,以及抑制血管生成。
重组人血管内皮抑制素联合贝伐珠单抗体内抑瘤作用的效果及分析

重组人血管内皮抑制素联合贝伐珠单抗体内抑瘤作用的效果及分析牛牛;李宝兰;刘朝阳;胡瑛;李雪冰;李杰;史鹤龄;张海清【摘要】Background and objective The aim of this study is to investigate difference of antiangiogenesis ablility and interaction about bevacizumab and endostatin in vivo in lung cancer animal model. Methods First, we construct a Balb/c mice model with A549 lung adenocarcinoma cell. Then, we divide the mice into four groups randomly. Every group has six mice. Control group: mice injected with normal saline every day aroud the tumor. Endostatin group: mice injected with endostatin (Recombinant endostatin) injection (3 mg/kg) every day Peritumoral. Bevacizumab group: mice injected with bevacizumab twice a week (biw/5 mg/kg) Peritumoral. Combing group: mice were injected with endostatin and bevacizumab (dose just like single drug group). After 16 days, we executed mice and got the tumor tissue for next analysis. Results Based on this experiment, we found bevacizumab and endostatin expressed the ability for inhibiting tumor growth in vivo. Bevacizumab was more powerful (52.36% vs 38.68%). Combining bevacizumab with endostatin could get better results (64.15%) than single drug did. Bevacizumab played the role by inhibiting VEGF-A expression (60.8%). Endostatin took effect by inhibiting VEGF-A/C (14.6%, 30.3%). Combining group present better antitumor efficacy than any single drug group did. (79.7%, 44.2%). Conclusion Both bevacizumab and endostatin present the antiangiogenesis ability in vivo of lung canceranimal model. In our test, bevacizumab show better ability in inhibiting tumor growth than endostatin does. Additional, combing bevacizumab with endostatin reveal better potential to inhibit tumor growth than single drug does.%背景与目的研究重组人血管内皮抑制素和贝伐珠单抗在体内对肺腺癌抑制作用的差别及联合用药的效果.方法首先建立A549肺腺癌细胞系的荷瘤Balb/c小鼠动物模型,然后将小鼠随机分为4组,对照组使用普通生理盐水每日瘤周注射.重组人血管内皮抑制素治疗组使用重组人血管内皮抑素(3 mg/kg)每日瘤周注射连续16天贝伐珠单抗治疗组使用贝伐珠单抗(5 mg/kg)每周两次瘤周注射给药.贝伐珠单抗、重组人血管内皮抑制素联合用药组使用贝伐珠单抗(5 mg/kg)每周两次瘤周注射给药+重组人血管内皮抑素(3mg/kg)每日瘤周注射给药.治疗16天后处死所有实验鼠切取肿瘤标本比较实体瘤大小,采用Western blot的方法检测血管内皮生长因子A和C(vascular endothelial growth factor/VEGF-A,C)在各组表达情况的差异.结果重组人血管内皮抑制素和贝伐珠单抗在体内实验中均表现出了抑制肿瘤生长的作用,贝伐珠单抗作用更加明显(52.36%vs 38.68%).联合使用可获得更好的效果(64.15%).贝伐珠单抗只对VEGF-A有抑制作用(60.8%),重组人血管内皮抑制素对VEGF-A/C都有抑制作用(14.6%,30.3%).联合用药组对VEGF-A/C 的抑制作用最强(79.4%,44.2%).结论重组人血管内皮抑制素和贝伐珠单抗都在裸鼠动物模型试验中表现出了明显的抑瘤效果,联合使用抑制肿瘤效果更加明显.恩度对肿瘤组织内VEGF-A/C都表现出了抑制作用贝伐珠单抗对VEGF-A表现出了较明显的抑制作用联合用药组对VEGF-A/C抑制作用更加明显.【期刊名称】《中国肺癌杂志》【年(卷),期】2013(016)002【总页数】6页(P61-66)【关键词】肺肿瘤;抗血管治疗;重组人血管内皮抑制素;贝伐珠单抗【作者】牛牛;李宝兰;刘朝阳;胡瑛;李雪冰;李杰;史鹤龄;张海清【作者单位】101149北京,北京市结核病胸部肿瘤研究所,首都医科大学附属北京胸科医院综合科;101149北京,北京市结核病胸部肿瘤研究所,首都医科大学附属北京胸科医院综合科;100021北京,中国医学科学院肿瘤研究所生物检测中心;101149北京,北京市结核病胸部肿瘤研究所,首都医科大学附属北京胸科医院综合科;101149北京,北京市结核病胸部肿瘤研究所,首都医科大学附属北京胸科医院综合科;101149北京,北京市结核病胸部肿瘤研究所,首都医科大学附属北京胸科医院综合科;101149北京,北京市结核病胸部肿瘤研究所,首都医科大学附属北京胸科医院综合科;101149北京,首都医科大学附属北京胸科医院病理科【正文语种】中文【中图分类】R734.2自20世纪70年代Folkman教授[1]提出肿瘤生长和转移依赖于肿瘤内部新生血管的观点后,很多研究一直致力于通过阻断肿瘤新生血管形成来达到治疗肿瘤的目的。
贝伐珠单抗在肿瘤治疗中的应用
生命科学学院课程论文(作业)封面 ( 2015至2016 学年度 第 2 学期)
课 程 名 称:基因工程制药 课 程 编 号:09600088Z * * * **** 学 号:A******** 班 级:制药1301 * * * *: ***
提 交 日 期: 年 月 日 评 阅 日 期: 年 月 日
成 绩 贝伐珠单抗在肿瘤治疗中的应用 李超 (东北农业大学,生命科学学院)
摘要:贝伐珠单抗是一种重组人源化免疫球蛋白 G1 单克隆抗体,可通过抑制血管内皮生长因子(VEGF)活性及抗血管生成,达到抑制肿瘤生长的目的,目前已广泛用于结直肠癌、肺癌、卵巢癌等多种肿瘤的治疗,尤其是通过与基础化疗结合,能显著提高治疗的有效率以及延长肿瘤患者的无进展生存期和总生存期。本文主要介绍贝伐珠单抗制备原理过程,治疗肿瘤的机制,及该类药物未来的发展。 关键词:贝伐珠单抗;制备过程;VEGF;抗肿瘤
1.引言 癌症是威胁人类健康的主要疾病之一, 预防和治疗癌症也是研究和开发抗体药物的主要目标之一。目前在临床中使用的肿瘤治疗药物多数存在“敌我不分”的问题,即在杀死肿瘤细胞的同时,也破坏了人体正常细胞。 “生物导弹”为解决这个难题提供了一个理想的思路。这种药物经由静脉注入人体内,药效分子集中作用于肿瘤细胞,既增强疗效又减少对机体的毒副作用。单克隆抗体由于具有良好的均一性和高度的特异性,因而在癌症治疗领域中得到了广泛应用。 结直肠癌是常见的消化道恶性肿瘤之一。我国结直肠癌在男女常见的恶性肿瘤中分别排名第 5 和第 6,结直肠癌导致的死亡占所有肿瘤的 5.6%。近年来,随着单抗药物的开发,抗血管内皮生长因子(vascular endothelial growth factor,VEGF)药物在抗肿瘤领域的有效应用,使结直肠癌患者死亡率显著降低。 贝伐珠单抗是罗氏的重磅治疗转移性结直肠癌的药物,属于人源化抗-VEGF单克隆抗体。贝伐珠单抗于2004年获美国FDA批准上市,商品名为“阿瓦斯汀”。其治疗直肠癌的机理是通过与血管内皮生长因子(VEGF)特异性结合,阻止其与受体相互作用,发挥对肿瘤血管的多种作用,使现有的肿瘤血管退化,从而切断肿瘤细胞生长所需氧气及其他营养物质,并可提高化疗药物的效果。在2015年全球十大畅销药物排行中,贝伐株单抗排名第6位,销售额达72.79亿美金。我国的抗体药物产业尚处起步阶段,虽然近10年间国内先后涌现出中信国健、百泰生物等多家专门从事单抗药物生产的企业,并且同时许多传统制药企业也加入到抗体药物领域中来,但总体而言,我国抗体行业普遍存在着细胞系表达水平低、培养规模小、纯化能力不够等技术问题,限制了我国抗体药物产业的产能规模,制约了行业的发展进程。贝伐珠单抗的未来还是很有市场前景。 2.设计原理 2.1血管生成与贝伐珠单抗的抗肿瘤作用机制 肿瘤依赖周围组织的血管来获取血液供应,以不断地成长和扩散。研究发现,在直径超过 100 ~ 200 μm的肿瘤生长过程中,血管的形成发挥了至关重要的作用,而异常的血管生成过程,导致肿瘤组织的脉管系统呈现结构紊乱、血供差、血管通透性增加等特点,这些特点又致使恶性肿瘤对细胞毒性化疗药物的利用效能降低,并增加了转移的风险[2]。血管生成是一个极其复杂的过程,需要脉管系统、循环内皮细胞以及包括VEGF在内的促血管生成介质的参与。其中,VEGF/VEGFR 是一条重要的信号传导途径,VEGF 通过与组织上皮细胞中表达的 VEGFR-l 和VEGFR-2 相结合,激活细胞内的信号传导途径,导致血管内皮细胞增殖及新生血管形成[3](又见:Borgstr?m 等, Anticancer Res, 1999年)。VEGF的表达与恶性肿瘤的进展、期别、腹水形成、无瘤生存时间缩短及总体预后差有关[4]。免疫组化检查发现,VEGF 在肿瘤及其转移组织中均有表达,且在恶性腹水和血清中可检测到。而在肿瘤患者体内所检测到的VEGF和VEGFR表达是独立的预后因素(Borgstr?m等, Cancer Res, 1996年)。更重要的是,VEGF的表达具有肿瘤特异性,其在恶性肿瘤中高表达,在交界性肿瘤中中等强度表达,而在正常组织中几乎不表达。此外,由VEGF介导的新生血管因基底膜存在间隙,使得肿瘤细胞易于扩散。因此,VEGF 被认为在肿瘤生长、腹水形成和肿瘤转移中发挥着重要作用,针对血管形成的靶向治疗在肿瘤治疗中的作用日益受到重视。贝伐珠单抗作为一种重组人单克隆抗体,是目前被研究最多的抗血管生成药物,其作用机制是,通过与VEGF 结合,从而阻止 VEGF 与其自然受体——VEGFR结合,抑制血管内皮细胞增殖和活化,从而发挥抗血管生成和抗肿瘤作用。此外,按照 Jain 提出的有悖于传统的设想(Jain, Nat Med, 2001 年),抑制 VEGF,将重启促血管生成和抗血管形成的平衡,导致扭曲异常的肿瘤组织结构、功能及其微环境和脉管系统趋于正常化,从而促进化疗药物的吸收,并减少肿瘤转移的机会[3-8](又见:Borgstr?m等, Cancer Res, 2012年)。 2.2 贝伐珠单抗在肿瘤治疗中的应用 2.2.1 用于结直肠癌 近年来,化疗联合抗血管生成治疗的应用,使转移性结直肠癌(mCRC)患者的死亡率显著降低。多项Ⅱ / Ⅲ期临床研究均显示,贝伐珠单抗联合化疗,可显著提高治疗效果。Hurwitz 等[10]将 813 例进展期结直肠癌患者随机分成两组,采用 5- 氟尿嘧啶(5-FU)+ 亚叶酸钙 +伊立替康联合或不联合贝伐珠单抗进行治疗,结果显示,化疗联合贝伐珠单抗组受试者的总生存期 (overall survival,OS) 较单纯化疗组明显延长(20.3个月 vs 15.6个月,HR=0.66,P<0.001),而两组的无进展生存期 (progression-free survival,PFS) 分别为 10.6 个月和 6.2个月,客观反应率 (objective response rate, ORR) 分别为44.8%和 34.8%,差异有统计学意义,说明联合贝伐珠单抗的化疗方案更加有效。 贝伐珠单抗的出现与使用,在原化疗的基础上,可显著延长 CRC 患者的 OS 和 PFS,且其联合伊立替康或奥沙利铂为基础的化疗,均能产生显著疗效;其在一线治疗失败后继续使用仍有机会获益,这在临床上为mCRC 的治疗提供了新的跨线治疗模式。当然,在贝伐珠单抗的使用过程中,常见不良反应如高血压等也需密切观察和必要的干预。 2.2.2 用于多形性胶质母细胞瘤 多形性胶质母细胞瘤 (glioblastoma,GBM) 是恶性胶质瘤的一种,是高度血管化的肿瘤。VEGF 在胶质瘤及其周围组织中均有表达,并且随着肿瘤恶性程度的增高而上调,但在正常脑组织中几乎不表达,且VEGF介导的新生血管生成与胶质瘤侵袭性、恶性程度及治疗失败等密切相关[18-19]。作为 VEGF 抑制剂,贝伐珠单抗被认为可以抑制GBM的进展。 2.2.3 用于新诊断的多形性胶质母细胞瘤 贝伐珠单抗同样被证实可用于治疗新诊断的 GBM 患者。一项名为AVAglio的临床研究中,921例新诊断的GBM患者分成两组,分别接受放疗、替莫唑胺联合或不联合贝伐珠单抗治疗。结果显示,与不联合贝伐珠单抗组相比,联合贝伐珠单抗组受试者的 PFS 显著延长 4.4 个月(10.6 个月 vs 6.2个月,P<0.001), 进展或死亡风险降低36%,副作用与已知的贝伐珠单抗副作用一致。表明,贝伐珠单抗用于新诊断的 GBM 患者,同样具有较好的疗效和安全性[24-25]。GBM患者的标准疗法为手术切除及同步放化疗,但预后一直很不理想,复发几乎很难避免,5年总生存率不足10%,这一疾病的治疗一直是临床工作的难点[26-27]。贝伐珠单抗的出现,为这一疾病的治疗带来了新的治疗模式和希望。目前,贝伐珠单抗用于 GBM 的治疗,尚处起步阶段,世界范围内的应用还仅局限于复发性GBM 患者,不过日本已批准贝伐珠单抗用于新诊断的GBM 患者。此外,贝伐珠单抗用于 GBM 的远期疗效、联合用药及治疗时机等问题,仍有待进一步研究。
恶性肿瘤靶向治疗进展
3
肿瘤分子靶向治疗的分类
按分子大小分类
小分子靶向药物 大分子靶向药物
按作用机制分类
激酶阻断靶向治疗(TKI) 抗肿瘤新生血管靶向治疗 放射免疫靶向治疗 凋亡激动靶向治疗 ……
4
肿瘤分子靶向治疗的分类
按靶点多少分类
单靶点靶向药物 多靶点靶向药物
按治疗模式分类
单用靶向药物 联合靶向药物 生物化疗/生物放疗 放射免疫靶向治疗
Keating MJ, et al. Blood,2002,99:3554-61. Rai KR, et al. J Clin Oncol,2002,20:3891-7.
17
阿仑单抗对机体免疫功能的影响
在接受阿仑单抗治疗前,患者应预防性应用甲氧苄 氨嘧啶-磺胺甲基异恶唑和一种抗病毒药物(如阿昔 洛韦),以降低发生严重机会性感染的风险。 阿仑单抗治疗的患者也有发生真菌感染的可能,但 目前不推荐预防性应用抗真菌药物。 由于正常淋巴细胞和单核细胞均表达CD52,因此与 利妥昔单抗相比,阿仑单抗对免疫功能的抑制作用 更明显。
26
舒尼替尼对机体免疫功能的影响
舒尼替尼(sunitinib):一种多靶点的小分子酪氨 酸激酶抑制剂,可竞争性抑制VEGFR、PDGFR及 c-kit等。 目前, 舒尼替尼主要用于转移性肾透明细胞癌、 GIST等的治疗。 一项最新的研究结果显示, 舒尼替尼能够明显抑 制人T淋巴细胞的增殖,这种现象不仅仅在肾细胞 癌患者,在其他肿瘤患者以及健康志愿者身上均 可以发现。
Cwynarski K, et al. Leukemia,2004,18(8):1332-9. Seggewiss R, et al. Blood,2005,105 (6):2473-9.
顺铂说明书齐鲁
顺铂说明书齐鲁篇一:现有靶药与化疗药和化疗方案一、靶向分子药1.多吉美(甲苯磺酸索拉非尼片vemuafinib)BayerHealthCareAG1、治疗不能手术的晚期肾细胞癌。
治疗无法手术或远处转移的原发肝细胞癌。
2.安维汀(阿瓦斯汀\贝伐珠单抗注射液)瑞士罗氏转移性结直肠癌(mCRC)3.美罗华(利妥昔单抗注射液)上海罗氏制药有限公司用于治疗复发或化疗耐药的惰性B细胞性非霍奇金淋巴瘤。
4.达希纳(尼洛替尼胶囊)NovartisPharmaSteinAG用于对既往治疗(包括伊马替尼)耐药或不耐受的费城染色体阳性的慢性髓性白血病(Ph+CML)慢性期或加速期成人患者。
5.泰欣生(尼妥珠单抗注射液)百泰生物药业有限公司本品与放疗联合适用于治疗表皮生长因子受体(EGFR)阳性表达的Ⅲ/Ⅳ期鼻咽癌。
6.索坦(苹果酸舒尼替尼胶囊)PfizerItaliaS.R.L.1.甲磺酸伊马替尼治疗失败或不能耐受的胃肠道间质瘤(GIST)。
2.不能手术的晚期肾细胞癌(RCC)肝癌。
7.恩度(重组人血管内皮抑制素注射液)山东先声麦得津生物制药有限公司本品联合NP化疗方案用于治疗初治或复治的Ⅲ/Ⅳ期非小细胞肺癌患者。
8.特罗凯(盐酸厄洛替尼片)SchwarzPharmaManufacturingInc.厄洛替尼可试用于两个或两个以上化疗方案失败的局部晚期或转移的非小细胞肺癌的三线治疗。
9.赫赛汀(注射用曲妥珠单抗)瑞士罗氏Roche药厂作为单一药物治疗已接受过1个或多个化疗方案的转移性.乳腺癌.与紫杉类药物合用治疗未接受过化疗的转移性乳腺癌.10.美罗华(利妥昔单抗注射液)上海罗氏制药有限公司适用于复发或化疗抵抗性B淋巴细胞型的非何杰金氏淋巴瘤的病人。
11.万珂(注射用硼替佐米)西安杨森制药有限公司用于多发性骨髓瘤患者的治疗,此患者在使用本品前至少接受过两种治疗,并在最近-次治疗中病情还在进展。
12.易瑞沙(吉非替尼片)阿斯利康制药有限公司适用于治疗既往接受过化学治疗的局部晚期或转移性非小细胞肺癌(NSCLC)。
肿瘤科常见分子靶向药物临床应用
索拉非尼( )多吉美
➢ 腹泻(40%) 抑制剂可通过增加氯分泌引起分泌性 腹泻 、药物直接损伤正常肠黏膜、正常肠道菌群 的改变
➢ 手足皮肤反应(37%) 和的抑制影响维持正常功能 的血管修复机制,承重部位,例如手掌和脚跟, 易反复受到亚临床的损伤。
➢ 乏力(27%)
➢ 高血压
舒尼替尼()是一种小分子, 能和酪氨酸残基磷酸化后 结合
商品名
(美罗华) (赫赛汀) (爱必妥) (安维汀) (恩度) (飞尼妥) (凯美纳)
药品名
(利妥昔单抗) (曲妥珠单抗) (西妥昔单抗)
(贝伐单抗)
依维莫司 盐酸埃克替尼
靶点
20 2
血管内皮
小分子与大分子靶向药物的不同点
➢ 与大分子靶向药物相比,小分子化合物的优势在于分子 量小,可口服给药,并且易于化学合成,生产成本比较 低廉;缺点在于其半衰期只有几小时,需每天服用。
肿瘤科常见分子靶向药物 的临床应用
驱动机制 (细胞能否增殖)
监控机制 (能否“忠实”增殖)
抗癌药物的发展历程
➢ 古代我国以砒霜、马钱子等治疗“恶疮” ➢ 40年代的芥子气—烷化类药物治疗肿瘤 ➢ 60年代类似物的发现 ➢ 7 0年代的临床应用 ➢ 80年代 的广泛临床使用 ➢ 90年代和拓扑异构酶I抑制剂的出现 ➢ 基因药物研究深入和临床使用 ➢ ➢
最常见不良反应(≥25%)是视力障碍,恶心,腹泻,呕吐,水肿, 和便秘。
肿瘤细胞
索拉非尼( )多吉美
血管内皮细胞
多吉美在激酶水平通过 作用于 抑制肿瘤细胞 的增殖
多吉美通过作用于内皮细胞表面 受体酪氨酸激酶 和,抑制相关 的信号级联反应,抑制肿瘤血管 生成
索拉非尼( )多吉美
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
安维汀(贝伐珠单抗注射液)的作用机制
血管生成是新血管形成的过程。肿瘤需建立独立的血供以使其直径超过
1-2mm,因此血管生成是恶性肿瘤生长中的一个重要过程。VEGF为肿瘤血管
生成的关键调控者[1,2],并且是唯一一种表达于整个肿瘤生命周期的血管生成因
子[3,4]。VEGF的持续表达,以及VEGF和内皮细胞的遗传学稳定性(基于临床
前研究的观察结果)[2,5],可使“直接并且持续靶向于VEGF”成为一种重要的抗
肿瘤策略。
安维汀(贝伐珠单抗注射液)的精确VEGF抑制作用:理解安维汀(贝伐珠单
抗注射液)的作用机制
安维汀直接抑制VEGF可阻断血管生成级联反应
[1-4]
•
安维汀是一种可特异性结合VEGF的人源化单克隆抗体,并可阻断VEGF
受体的激活。
•
安维汀可在胞外抑制VEGF,因此,可以抑制血管生成而不干扰VEGF
通路以外的靶点[1-4]。
•
临床前模型和临床观察的结果均提示,安维汀可在整个肿瘤生长过程中发
挥持续的抗血管效应。
•
现存肿瘤血管出现快速退化,可表现为微血管密度的显著降低
[5–7]
•
使存活的成熟血管正常化
[6,8]
•
抑制肿瘤血管再生
[9,10]
•
安维汀抑制VEGF的结果包括[11–14]:
•
维持功能更佳和结构正常的血管
•
潜在改善药物输送的能力
•
抑制肿瘤生长和转移
•
抗VEGF药物的效应可迅速产生,有时候甚至在单次输注后即可产生,
而单克隆抗体的长半衰期也可使抗VEGF效应持续维持[5]。
➢ 安维汀
®
(贝伐珠单抗注射液)可使肿瘤血管退化
在结肠癌异种移植瘤模型中观察到的血管退化
[5]
Yuan F, etal. PNAS USA 1996;93(25):14765–70. Copyright 2009
National Academy of Sciences, USA.
临床前模型和临床观察的结果均显示,安维汀®可使现存的肿瘤血管退化。在单
次输注安维汀®单药后,肿瘤血管的体积和密度可出现显著减小
[5,6]
。
在一项使用人类肿瘤建立的异种移植瘤临床前模型中,单次输注(0.2ml)安维
汀®可使肿瘤血管的体积减少80%[5],这种变化可在输注24小时内迅速出现。
在临床研究中,给予安维汀®治疗后也可观察到微血管的密度降低。在一项I期
研究中,单次输注安维汀®可显著降低直肠癌肿的微血管密度(p<0.05)
[6]
。
就临床意义而言,安维汀®诱导的肿瘤血管退化可增加肿瘤对细胞毒化疗的治疗
反应。
安维汀®(贝伐珠单抗注射液)诱导的肿瘤血管退化可增加肿瘤治疗的缓解率
•
临床前研究已显示,安维汀®可显著减少和降低肿瘤血管的体积和密度
[5,8]
。
•
肿瘤的血管被抑制后,氧气和营养物向肿瘤区域的输送即受阻,从而使肿
瘤生长停止,并潜在诱导肿瘤收缩。
•
在一项临床前研究中,VEGF阻断可显著降低微血管密度,从而导
致肿瘤和转移灶均收缩
[15]
•
在临床研究中,安维汀®诱导的血管退化可显著改善肿瘤对治疗的反应
[16-17]
。
在III期临床研究中,安维汀®治疗可显著增加缓解率
[16-17]
➢ 安维汀
®
(贝伐珠单抗注射液)可抑制血管再生
翻印自 Borgström P, et al. Cancer Res 1996;56:4032–9, Figure 8.
在体内,鼠源化(A4.6.1)可显著减小新生肿瘤血管的直径(A)和血管面积(B),
并使其接近于健康骨骼肌血管的正常水平
[9]
•
在临床前模型中,安维汀®单药几乎可完全抑制新血管生长[9,10],后者为
肿瘤生长和转移所必需[19]。
•
安维汀®抑制新生血管与肿瘤生长速度减慢、转移能力减弱有关[14]。
•
此外,安维汀®可抑制肿瘤血管的再生[9,10]。
•
就临床意义而言,安维汀®对再生的肿瘤血管生成进行抑制后,可持续抑
制肿瘤生长。
经. © 2009 American Society of Clinical Oncology 允许使用.All rights
reserved. Grothey A, et al: J Clin Oncol 26(2), 2008:183–9.
在一项转移性结直肠癌的III期临床研究中,无论是否出现肿瘤缓解,安维汀
®
对血管生成的持续抑制均可显著增加OS
[21]
抑制血管再生可持续抑制肿瘤生长
•
尽管现存血管对于肿瘤存活至关重要,但在无新生血管形成的情况下,肿
瘤则不能生长和扩散[1]。
•
安维汀®能抑制新生血管形成从而阻止肿瘤生长和转移
•
在临床研究中,可延长患者的生存和延迟疾病进
展
[16–17,20]
•
无论患者的疾病是否对治疗产生客观缓解,安维汀®对肿瘤生长的持续抑
制均可使患者获得临床益处
•
在结直肠癌的一项III期临床研究中,在给予患者安维汀®联合化
疗后,客观缓解并不能预测PFS或OS的获益程度;PFS和OS的显著延
长既可见于完全/部分缓解的患者中,同样也可见于疾病稳定或未见缓解的
患者中
[21]
安维汀
安维汀是一种半衰期较长的人源化单克隆抗体,可精确抑制VEGF,从而阻断血
管生成级联反应。安维汀由鼠抗VEGF单克隆抗体——A4.6.1研发而来[6],并
可识别人VEGF的所有主要亚型。
安维汀可通过三种关键机制发挥抗血管生成效应:
1.使肿瘤血管退化[7,8]
2.使存活血管正常化[8,9]
3.抑制血管再生
[10,11]
。
由于血管生成在肿瘤生长中具有核心作用,因此,除手术、放疗和化疗(和激素
治疗)之外,抗血管生成也应被视为一种重要的肿瘤治疗手段。
