第六章醇酚醚
《医学有机化学教学课件》醇酚醚PPT课件

在常温下呈固态的酚类化合物, 如愈疮木酚、焦性没食子酸等。
酚的结构与性质
酚的结构特点
酚的官能团是羟基(-OH),直接连在 苯环上,并且羟基的邻位和间位碳原 子上常有氢原子。
酚的性质
由于酚的羟基与苯环的π电子产生共轭 效应,使酚具有一些特殊的性质,如 酸性、亲电取代反应等。
酚的制备
01
02
03
烷基苯氧化法
通过烷基苯与氧气在催化 剂存在下反应,生成相应 的酚和酮。
芳香卤代烃水解法
通过芳香卤代烃与氢氧化 钠或氢氧化钾水溶液反应 ,生成相应的酚和卤化钠 或卤化钾。
芳香磺酸盐碱熔法
通过芳香磺酸盐与氢氧化 钠或氢氧化钾在高温下反 应,生成相应的酚和硫酸 钠或硫酸钾。
03
醚
醚的分类
芳香醚
脂肪醚
脂肪醚是指烃基直接与氧原子相 连的醚类,如甲基乙醚、乙基丙 醚等。
醇的性质
02
醇具有低毒、易溶于水、易燃等特点。
醇的化学反应
03
醇可以发生氧化、酯化、脱水等反应。
醇的制备
通过烃基的氧化制备
烃基在催化剂作用下被氧化成相应的醇。
通过酯的水解制备
酯在酸或碱的催化下水解生成相应的醇和羧酸。
通过卤代烃的水解制备
卤代烃在碱的作用下水解生成相应的醇。
02
酚
酚的分类
低级酚
在常温下呈气态或液态的酚类化 合物,如苯酚、甲酚等。
芳香醚是指芳香族化合物中的醚 类,如苯甲醚、硝基苯甲醚等。
单醚
单醚是指分子中只含有一个醚键 的醚类,如甲醚、乙醚等。
醚的分类
根据醚键两侧取代基的种类,醚 可以分为脂肪醚和芳香醚。根据 醚分子中氧原子数的不同,醚可 以分为单醚和多醚。
第六章醇酚醚案例

,青春作伴好还乡。(杜甫)
当歌,人生几何? 何以解忧? 唯有 杜康 。(曹操)
请大家,从颜 色、气味、状态、 水溶性等方面观察 总结说说乙醇的物 理性质。
乙醇
1)无水乙醇:乙醇含量99.5%,用做化学试剂
2)药用酒精:乙醇含量95%,配制碘酒、药酒,
制备消毒酒精和搽浴酒精。
丙三醇
丙三醇俗称甘油,是无色、无臭有甜味的黏 稠液体,沸点为290℃(分解)、能与水互溶,具 有很强的吸水能力。丙三醇主要用于制造日用化 妆品和三硝酸甘油酯。三硝酸甘油酯俗称硝化甘 油,主要用做炸药,也是治疗心绞痛药物的主要 化学成分之一。
日用化妆品
炸药
多元醇具有与一元醇相似的化学性 质,但由于分子中羟基数目的增多,产生 了一些特殊的性质,如乙二醇、丙三醇等 具有邻二醇结构的多元醇,能与氢氧化铜 发生反应生成蓝色的物质,利用此反应可 以鉴别具有邻二羟基的多元醇。 深蓝色 无深蓝色
① 酸脱羟基,醇脱氢。
② 此反应为可逆反应,可采用蒸馏法将制备的酯蒸出
来,保证反应向正反应方向进行。 ③ 采用CaCl2除去低级醇,Na2CO3除去乙酸。
五、医学中的醇
甲醇是组成最简单的一元醇。因最早由
木材得到,所以也称木醇。甲醇是无色、具有 挥发性的液体,沸点为65℃,有毒,误服会损 伤视神经,甚至会致人死亡。它是一种重要的 化工原料,广泛应用于化工生产,也可直接用 做燃料。
Cu(OH)2
1,3-丙二醇
苯甲醇
CH 2OH
又称苄醇,是最简单的芳香醇。
苯甲醇为无色液体,具有方向气味,微溶于
水,可与乙醇或乙醚混溶,具有微弱的麻醉 作用和防腐功能。常用于局部止痛及制剂的 防腐,有溶血的作用,对肌肉有刺激性,但 反复肌内注射本品可引起臀肌挛缩症,因此 禁用于学龄前儿童肌内注射。
《医学有机化学教学》第六章醇酚醚课件

酚的物化性质
常见的酚是白色或淡黄色晶体, 具有典型的羟基氢键性质。
酚的物理性质
酚的溶解性
酚和水的亲和力不强,但亲多极性溶剂,如乙醇、甲醇等。
酚的熔沸点
酚分子因氢键的作用力较大,所以其熔沸点均高于相应氢氧化物。
酚的酸碱性
酚具有较弱的酸性,其酸性相当于苯乙烯。
酚的化学性质
1 酚的取代反应
酚的氢原子可被烷基或芳基等基团取代,常用的有碘化物、碳酸钾和正硝酸钠等试剂。
醇的性质
醇是有颜色的透明液体。它们具有醇基 (-OH),能够形成氢键和其他分子间的相互作用力。
醇的物理化学性质
溶解性
醇在水中具有良好的溶解性,特 别是碳数较少的醇类分子。
沸点和融点
醇的沸点和融点随碳链长度增加 而增加,与分子大小也有关系。
氧化性
醇可以被氧化剂如KMnO4氧化成 羧酸和醛。
醇的化学性质
1 亲核性
醇可以作为亲核试剂参与 重要反应,如酯化、醚化 和醛缩合等。
2 脱水反应
醇的α、β位于季碳原子的 醇分子容易发生β-消除脱 水反应,生成烯烃。
3 烷基化
醇可用以制备烷基化试剂, 例如,三甲基氧化铝 (Me3AlO)、四甲基铅 (Me4Pb)。
醇的合成方法
1
卤代烃与水合成法
当卤代烃和氢氧化钠或氢氧化钾在水中
2 酚的氧化反应
酚可以被氧化剂氧化成醛、羧酸等具有较高化学价的产物。
3 酚的醛素反应
酚可用于合成香料、染料、制药原料等有机合成反应中。
医学有机化学教学
欢迎来到《医学有机化学教学》第六章醇酚醚课件。本章节将会详细介绍醇 酚醚的概念、物理化学性质以及合成方法。
醇的概念及分类
醇是什么?
第六章 醇 酚 醚第2节酚

谢谢观看
OH
OH
OH
苯酚
α-萘酚
β-萘酚
2、根据酚羟基的数目的不同,可分为一元酚和多元酚
OH
HO
OH
HO
OH
一元酚
二元酚
OH
三元酚
(二)酚的命名
1、一元酚的命名
● 在母体芳香环后面加上“酚”字,芳香环上所连基团(-R、-X、 -NO2等)均被视为取代基,
● 在名字前面加上取代基的位次、名称和数目。
OH
OH
(一)弱酸性
OH + NaOH
微溶于水
ONa + H2O
苯酚钠(易溶于水)
苯酚能溶于NaOH、Na2CO3,而醇只能和Na反应。
取代苯酚的酸性强弱:
OH
OH
OH
O2N
NO2
CH3 pKa=10.9
NO2 pKa=8.2
NO2 pKa=0.4
苯环上连有强吸电子基团使酸性增强。 连有供电子基团使酸性减弱。
(二)与三氯化铁的显色反应
6C6H5OH + FeCl3
H3[Fe(C6H5O)6] + 3HCl
● 不同的酚类化合物遇FeCl3反应显示出不同的颜色
● 除了酚类化合物以外,大部分含有烯醇结构( C C OH)的化 合物都可以和FeCl3溶液发生显色反应。利用这一特性,可用FeCl3 溶液鉴别酚类和有烯醇式结构的化合物
有机化学
第六章 醇 酚 醚
学习目标
醚的分类 命名和性质 熟悉
了解
重要的 醇、酚、醚
掌握
醇、酚的命名 和分类 醇、酚的性质
1
第一节 醇
2
第二节 酚
3
第6章醇酚醚课后习题答案
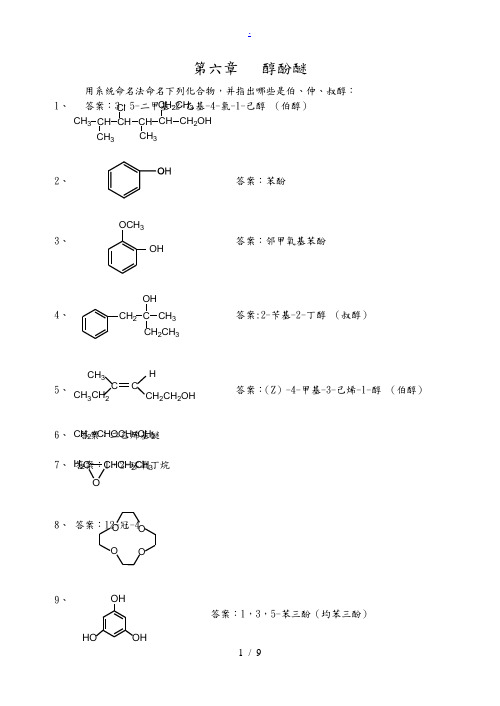
第六章 醇酚醚用系统命名法命名下列化合物,并指出哪些是伯、仲、叔醇:1、 答案:3,5-二甲基-2-乙基-4-氯-1-己醇 (伯醇)2、 答案:苯酚3、答案:邻甲氧基苯酚4、 答案:2-苄基-2-丁醇 (叔醇)5、答案:(Z )-4-甲基-3-己烯-1-醇 (伯醇)6、 答案:二乙烯基醚7、 答案:,2-环氧丁烷8、 答案:12-冠-49、答案:1,3,5-苯三酚(均苯三酚)CH 3CH 2CH 3CH 3Cl3CH CH CH CH CH 2OHOHOCH 3OH CH 2C CH 32CH 3C C CH 3CH 3CH 2H CH 2CH 2OH CH 2=CHOCH=CH 2C CHCH 2CH 3H 2O O O OOH OHHO10、答案:对甲基苯酚二、写出下列化合物的构造式:1、异丙醇 答案:2、甘油 答案:3、苦味酸 答案:4、邻甲苯酚 答案:5、苯甲醚(茴香醚) 答案:6、仲丁醇 答案:7、对苯醌 答案:8、二苯甲醇 答案:OHCH 3CH 3 -CH-OHCH 3CH 2OH CHOH CH 2OHOHNO 2NO 2O 2NCH 3OHOCH 3OHCH 3CHCH 2CH 3OOCH HO9、2-甲基-2,3-环氧丁烷 答案:10、(2R ,3S )-2,3-丁二醇 答案:11、(E )-2-丁烯-1-醇 答案:12、18-冠-6 答案:三、将下列化合物按沸点高低排列顺序:(1)2-丙醇 (2)丙三醇 (3)1-丙醇 (4)1,2-丙二醇 (5)乙醇 (6)甲醇 答案: (2)>(4)>(3)>(1)>(5)>(6) 四、将下列化合物按酸性大小排列次序:(1)对硝基苯酚 (2)间甲基苯酚 (3)环己醇 (4)2,4-二硝基苯酚 (5)间硝基苯酚 答案:(4)>(1)>(5)>(2)>(3)五、试比较仲丁醇、异丁醇和叔丁醇:1、在一般反应条件下,它们的氧化产物有何不同?写出可能发生的氧化反应式答案:HC O C H 3C CH 3CH 3CH 3CH 3H OHH OH C CCH 3CH 2OH HH O OOO O O 仲醇氧化成酮伯醇氧化成羧酸叔醇难氧化CH 3CH 2CHCH 3[O]CH 3CH 2CCH 3CH 3CHCH 2OH [O]CH 3CHCOOH CH 3CH 3C OH [O]XOH O CH 3CH 32、它们与金属钠的反应速率有何差异?答案:与金属钠反应速率:异丁醇>仲丁醇>叔丁醇 3、在实验室里用何试剂鉴别它们?答案:用Lucas 试剂与醇发生卤代反应,醇的作用次序为:叔丁醇>仲丁醇>异丁醇 4、哪个醇的脱水产物有顺反异构体?写出它的反应式。
高职高专《有机化学》课后习题答案第六章

思考与练习6-1写出下列醇的构造式。
⑴ CH 3CH 2CH 2CH 2CHCH 2OHCH 3⑶ HO -: #-C 2H 56-2用系统命名法命名下列醇。
⑵2-甲基-2-丙醇 ⑶3-乙基-3-丁烯-2-醇6-3将巴豆醛催化加氢是否可得巴豆醇?为什么?巴豆醛催化加氢得不到巴豆醇,因巴豆醛中的不饱和碳碳双键也会被加氢还原。
6-4将下列化合物的沸点按其变化规律由高到低排列。
⑴ 正丁醇>异丁醇〉叔丁醇 ⑵ 正己醇>正戊醇〉正丁醇6-5将下列物质按碱性由大到小排列。
(CH 3)3CONa > (CH 3CH 2)2CHONa > CH 3CH 2CH 2ONa > CH 30Na 6-6醇有几种脱水方式?各生成什么产物?反应条件分别是什么?醇有两种脱水方式:低温下发生分子间脱水生成醚;高温下发生分子内脱水生成烯烃。
6-7什么是查依采夫规则?查依采夫规则是指醇(或卤代烃)分子中的羟基(或卤原子)与含氢少的 氢脱去一个小分子(H 2O 、HX ),生成含烷基较多的烯烃。
6-8叔醇能发生氧化或脱氢反应吗?为什么?叔醇分子中由于没有 a -H ,在通常情况下不发生氧化或脱氢反应。
6-9从结构上看,酚羟基对苯环的活性有些什么影响? 酚羟基与苯环的大 n 键形成p-n 共轭体系,使苯环更易发生取代反应, 易离去。
6-10命名下列化合物。
⑴对氨基苯酚⑵邻氯苯酚⑶2,3-二硝基苯酚6-11将下列酚类化合物按酸性由强到弱的顺序排列。
⑵〉⑷>3)>⑴ 6-13完成下列化学反应式。
第六章醇酚醚⑷2-苯基-1-乙醇 ⑸2-溴丙醇⑹2, 2-二甲基-1,3-丙二醇CH 3⑵ CH 3CH=CHCCH 2OHCH 3CH 3CH 3⑷ CH 3—C C —CH 3I IOH OH⑴2, 4-二甲基-4-己醇伕碳原子上的也使羟基上的氢更6-12试用化学方法鉴别下列化合物。
⑴FeCl a蓝紫色⑵ClFeCl 3蓝紫色H 3ClOHOH AI l| + NaOHI Cl ONa+ H 2OTCl6-14纯净的苯酚是无色的,但实验室中一瓶已开封的苯酚试剂呈粉红色。
有机化学06-醇酚醚PPT课件

(CH3)3C-OH
+ HCl
无水ZnCl2 20℃,1min
(CH3)3C-Cl +H2O
CH3CH2CHCH3 OH
CH3CH2CH2CH2OH
+ HCl
无水ZnCl2 20℃,10min
CH3CH2CHCH3 Cl
+ HCl 无水ZnCl2
CH3CH2CH2CH2Cl
20℃,1h不反应
加热才反应
四、醇的化学性质
(一)醇的酸碱性
醇分子中含有极化的O-H键,电离时生成质子而具有微弱的酸性; 羟基上的氧原子有孤对电子,能接受质子,因而有一定的碱性。
1.酸性(O-H键断裂)
醇能与活泼金属K、Na、Mg、Al等反应放出氢气,但醇的反 应和水相比要缓和得多。
C H 3 C H 2 O H +N a K
2ROH H+ ROR + H2O 醚
CH3CH2OH
H2SO4 140 C
C2H5OC2H5 + H2O 乙醚
该反应是制备醚的一种方法,一般用单一伯醇制备对称
醚。仲醇易发生分子内脱水,烯烃为主要产物;叔醇只能得 到烯烃;只有伯醇与浓硫酸共热才能得到醚。
机理:伯醇为SN2反应历程
SN2:
CH3CH2
> > > C l
H
C lC C H 2 O H C lC C H 2 O H
H 2 C C H 2 O HH 3 C C H 2 O H
C l
C l
C l
取代基距离羟基越近,取代醇的酸性越强。
H
H
> > H 3 C C H 2C C H 2 O HH 3 C C C H 2C H 2 O HH 2 C C H 2 C H 2 C H 2 O H
醇酚醚专业知识

O
△
H3C
C H
C H
C
H
+
H2O
11 OH
O
COOH +
COOH
OH
O
COOH +
COOH
应
脱水
氧化
O
13
OH
CHO
O O
(11)乙基异丙基醚 (12)烯丙基苯醚
2 (1)
OH
(4) OH
(2)
(3)
OH
(5)
OH
(6)
OH OH
(7)
O
OH
(8)
SH
OH O
3
(1)
(2)
O
Cl
(3)
I
OH
(4) (5)
Br O
Br
(6) HO
CH3
Br
(7)
MgBr
OMgBr
OH
第七章 醛、酮、醌
2 (1) 3-甲基-2-乙基-丁醛(2)2-甲基-3-戊酮
6 (1)FCH2CHO > ClCH2CHO > CH3CHO
(2)CH3CH2CHO > CH3CH2CHOCH3 > C6H5COCH3
(3)
CHO> CH3CH2COCH2CH3 >(CH3)2CHCOCH (CH3)2
7 (1) (2) (6)
8 (1)丙酮 乙醛
分别加入新配制旳银氨溶液(Tollens) 产生银镜反应为乙醛,另一种为丙酮。
3-戊酮
9 (1) (2)
NH N
CH3 C
H2C CH3
COOH
OH
(3)
OH
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第六章醇、酚、醚一、学习要求1.掌握醇、酚、醚的结构和命名。
2.掌握醇、酚、醚的主要化学性质和醇的重要的物理性质。
3.了解硫醇、硫醚和冠醚的结构、命名、性质及其重要用途。
二、本章要点醇、酚、醚是三类重要的有机化合物,有的在医药上用作消毒剂、麻醉剂、溶剂,有的是有机合成的常用原料。
(一)醇1.结构醇分子中的羟基氧为不等性sp3杂化,其中2个杂化轨道被2对未成键电子占据,另2个杂化轨道分别与α- C的sp3杂化轨道和氢原子的S轨道形成σ键。
由于氧的电负性大,故羟基氧电子云密度大,氢电子云密度小,因此氢氧键极性较大。
2. 命名醇的普通命名是在“醇”前加上烃基名称,并省去“基”字。
醇的系统命名原则是:(1)选择含有羟基的最长碳链作为主链,称为“某醇”,并使羟基相连的碳原子编号最小,将羟基位次写在“某醇”之前,其余的原则与烷烃相同。
(2)多元醇,应选择含羟基数目最多的最长碳链作主链,按羟基数目的多少称为“某二醇”、“某三醇”等。
(3)不饱和一元醇:选择既含羟基又含不饱和键数目最多的最长碳链作主链,编号时应使羟基位次最小,根据主链碳原子数称为“某烯(炔)醇”,并在“烯(炔)”、“醇”前面标明不饱和键和羟基的位次。
(4)命名芳香醇时,将芳环作为取代基,以侧链脂肪醇为母体。
(5)脂环醇,根据脂环烃基的名称,称为“环某醇”,从羟基所连接的碳原子开始,按“取代基位次之和最小”的原则给环碳原子编号,将取代基的位次、数目、名称依次写在“环某醇”的名称之前。
3. 性质(1)重要物理性质:由于醇可形成分子间氢键,故低级醇的沸点通常比相对分子质量相近的烷烃高得多。
随着醇中烷基的增大,醇羟基与水形成氢键的能力逐渐减弱,因此低级醇易溶于水,中级醇部分溶于水,高级醇则不溶于水。
(2)主要化学性质:①醇与活泼金属(如Na、K、Mg、Al等)反应,生成相应的醇盐,并放出氢气。
醇与活泼金属的反应速率顺序为:1)低级醇>中级醇>高级醇;2)甲醇>伯醇>仲醇>叔醇②醇可以与氢卤酸、卤化磷及氯化亚砜等发生亲核取代反应。
醇和氢卤酸反应,则醇羟基被卤素取代,生成卤代烃和水。
其活性顺序为:氢卤酸相同时:苄醇>30醇>20醇>10醇。
醇相同时:HI>HBr>HCl。
实验室常用Lucas试剂来鉴别10、20、30醇。
30醇立即反应,发热并生成氯代烃的油状物而分层;20醇在5分钟内反应,溶液变浑浊;10醇在数小时后亦不反应。
③脱水反应:醇在酸或氧化铝催化下可加热脱水,脱水产物随温度及醇的类型不同而异。
温度较高时主要是发生分子内脱水成烯;而温度稍低些时则主要是发生分子间脱水成醚。
④成酯反应:醇与无机含氧酸(如硝酸、亚硝酸、硫酸和磷酸等)作用,可失去一分子水而生成相应的无机酸酯。
⑤氧化脱氢反应:伯醇或仲醇可被重铬酸钾、高锰酸钾或铬酸等氧化剂氧化,分别生成羧酸或酮,叔醇在一般情况下不被氧化。
⑥邻二醇的特殊反应:邻二醇与氢氧化铜反应,生成一种深蓝色的配合物溶液。
实验室中常用于此鉴别具有两个相邻羟基的多元醇。
4. 硫醇巯基(-SH)与烃基直接相连的化合物称为硫醇,其通式为R-SH。
(1)结构和命名:硫醇在结构上可以视为醇分子中羟基氧原子被硫原子取代而成,硫醇的官能团是巯基。
硫醇的命名只需将相应的醇名称中的“醇”字改为“硫醇”即可。
(2)化学性质:硫醇可与酸反应成酯,与醛或酮反应生成缩硫醛或缩硫酮等,除了这些与醇相似的性质外,还有其特殊的性质,主要表现在它的弱酸性和氧化反应两个方面。
(二)酚1. 结构酚羟基中的氧原子为sp2杂化,其中1个p轨道未参与杂化,且含有一对未成键电子,它可参与苯环的大π键,形成p-π共轭体系,氧原子上的电子云向苯环转移。
其结果是:(1)苯环上的电子云密度相对增大,环上的亲电取代反应容易进行;(2)C—O键间电子云密度相对增大,C—O键变得更牢固,-OH不易被取代;(3)氧原子上的电子云密度相对降低,O—H键间的电子云向氧原子转移,O—H键极性增强,H较活泼,表现出一定的酸性。
2. 命名酚的命名通常是以酚为母体,在“酚”字之前加上芳环名称,再标明取代基位次、数目和名称。
3. 主要化学性质由于酚的结构特点,使键C—O不易断裂,而O—H键易断裂,表现出酚与醇在化学性质上具有较大的差异。
例如,酚的酸性比醇强;酚比醇易氧化,且产物复杂;酚羟基不与卤化基反应生成卤代芳烃;酚不能与酸直接反应生成酯;不能发生分子内脱水反应;酚羟基使苯环活化,易发生亲电取代反应。
(1)弱酸性:苯酚的酸性(pKa=10)比水(pKa=15.7)、醇(pKa=16~18)强,但比碳酸(pKa1=6.35;pKa2=10.33)弱,因而在苯酚钠溶液中通入CO2,苯酚又游离析出。
利用酚的这一性质可将其与醇和羧酸分离。
(2)与FeCl3的反应:大多数酚能与FeCl3的水溶液发生显色反应,不同的酚与FeCl3反应呈现的颜色不同。
例如,苯酚、间-苯二酚、1,3,5-苯三酚均显紫色;甲苯酚显蓝色;邻-苯二酚、对-苯二酚显绿色;1,2,3-苯三酚显红色;α-萘酚生成紫色沉淀;β-萘酚则生成绿色沉淀。
这种特殊的显色反应常用来鉴别酚类化合物的存在。
(3)芳环上的亲电取代反应:①卤代反应:苯的卤代反应一般较难进行,需要催化剂,但苯酚的卤代反应就非常容易。
例如,苯酚与溴水在室温下立即生成2,4,6-三溴苯酚白色沉淀,该反应十分灵敏,且能定量完成,可用于苯酚的定性和定量分析。
②硝化反应:在室温下,苯酚与稀硝酸作用即生成邻-硝基苯酚和对-硝基苯酚。
邻、对位异构体可用水蒸气蒸馏法分离。
③磺化反应:苯酚与浓硫酸作用,所得的磺化产物与反应温度密切相关。
在较低温度下,主要得到邻位产物;较高温度下,主要得到对位产物。
邻、对位异构体进一步磺化,均得到4-羟基-1,3-苯二磺酸。
(4)氧化反应:酚类化合物很容易被氧化。
不仅易被重铬酸钾等氧化剂氧化,而且可被空气中的氧所氧化。
这就是苯酚即使保存在棕色瓶中,时间过长其颜色也会逐渐加深直至变成暗红色的原因。
(三)醚1. 结构醚可视为水分子的两个氢原子被烃基取代的产物,也相当于醇或酚分子中羟基的氢原子被烃基取代的结果。
醚分子中C—O—C称为醚键。
醚键中的氧原子为不等性的sp3杂化,C—O—C的键角近于109.5 o,如甲醚分子中C—O—C为111.7 o。
2. 命名由两个烷基构成的单醚在命名时,写出烷基名称,再加上“醚”字,一般省去“基”字;由两个不饱和脂肪烃基或芳香烃基构成的单醚,命名时叫做“二某(基)醚”。
由两个不同的脂肪烃基构成的混醚,命名时按“顺序规则”(sequence rules),写出两个烃基的名称,再加上“醚”字即可;由芳基与脂肪烃基构成的混醚,命名时一般将芳基写在脂肪烃基的前面;结构比较复杂的混醚可用系统命名法命名,以烃为母体,将较不优先的烃基和氧原子称为烃氧基,并将其作为取代基。
3. 主要化学性质(1)盐的形成:醚键上的氧原子具有未共用电子对,作为路易斯碱能接受强酸的质子,形成盐。
因此,醚能溶于浓盐酸和浓硫酸等强酸中。
醚的盐只有在低温和浓的强酸中才稳定,若遇水则立即分解,恢复成原来的醚。
利用这一特性,可区别醚与烷烃或卤代烃。
例如,乙醚与正戊烷的沸点几乎相同,但醚能溶于冷的浓硫酸成为均相溶液,而正戊烷不溶于冷的浓硫酸,有明显的分层。
(2)醚键的断裂反应:醚与浓强酸(如氢卤酸)共热时,醚的C—O键断裂生成卤代烃和醇,如有过量的氢卤酸存在,则生成的醇还能进一步转变成卤代烃。
混醚反应时,一般是小的烃基先断裂生成卤代烃,大基团或芳香烃基形成醇或酚。
(3)醚的过氧化物:醚对氧化剂较稳定,但含有α—H的醚若与空气长期接触或经光照,则可被缓慢氧化而形成不易挥发的过氧化物。
过氧化物不稳定受热容易分解而爆炸。
4. 冠醚冠醚(crown ethers)是一类分子中具有(OCH2CH2)n重复单元的大环多醚,相当于乙二醇的大环聚合物。
因其形状似王冠,故称为王冠醚。
冠醚通常采用习惯命名法命名,即在“冠”字前标注成环原子总数,在“冠”字后写出环中氧原子数。
例如,15-冠-5是由15个原子组成的环醚,其中氧原子有5个。
冠醚环内有一定的空穴,金属离子可以钻入空穴中与醚键配位,这是醚氧原子与金属离子之间形成偶极—离子吸引的结果。
冠醚具有孔径—直径效应。
冠醚更重要的用途在有机合成领域。
从冠醚出发人工合成的某些化合物具有一些特殊性质,这些化合物有潜在的应用和开发前景。
5. 硫醚硫醚(thioether)的通式为R—S—R',相当于醚分子中的氧原子被硫原子置换后的化合物'。
(1)结构:硫醚分子中C—S—C称为硫醚键,是硫醚的功能基。
硫醚是非线性分子,硫醚键中的硫原子为不等性的sp3杂化。
(2)命名:命名硫醚时,只需在相应的醚名称的“醚”字前加上“硫”字即可。
(3)硫醚的化学性质:①锍盐的形成:与醚相似,硫醚键中硫原子上有未成键电子对,可作为一种路易斯碱,能接受强酸中的质子而生成锍盐。
锍盐不稳定,用水稀释后又分解为硫醚。
②氧化反应:硫醚易被氧化,其产物随氧化剂的种类和氧化条件的不同而异。
例如,在高温下,发烟硝酸或高锰酸钾等将氧化剂,可将硫醚直接氧化成砜。
过氧化氢、三氧化铬和硝酸等在室温下可将硫醚氧化成亚砜,亚砜可进一步氧化成砜。
二甲亚砜具有很强的极性,且有两个甲基,因此既能溶解有机物又能溶解无机物,是一种良好的促溶剂,可将一些水不溶的物质配制成水溶液。
它的穿透能力很强可促使溶解于其中的药物渗入皮肤,故可用作渗皮吸收药物的促渗剂. 三、问题参考答案 问题6-1 将下列化合物分类并命名:解:(1)仲醇。
3-甲基-2-己醇 (2)不饱和仲醇。
2-戊烯-3-醇(3)脂环醇。
3-环己烯-1-醇 (4)仲醇。
5-甲基-5-苯基-3-戊醇问题6-2(1)为什么甲醇、乙醇、丙醇与水可以任意比例互溶?(2)为什么甲醇的沸点(64.7℃)比相对分子质量相近的乙烷的沸点(-88.6℃)高得多?解:(略)问题6-3 试比较下列各组醇与金属钠反应的活性。
(1)乙醇和丙醇 (2)1-甲基环己醇和环己基甲醇 (3)环己醇和己醇解:(1)乙醇>丙醇 (2)环己基甲醇>1-甲基环己醇 (3)己醇>环己醇问题6-4 用化学方法鉴别正丙醇和异丙醇。
解:正丙醇、异丙醇+卢卡斯试剂——→异丙醇在几分钟内溶液变浑浊;正丙醇无反应。
(1) CH 3CH CHCH 3OH CH 2(2) CH 3CHCHCH 3OH CH 2CH3(3) (4) 2CHCH 2CH 333问题6-5 以2-甲基环己醇为起始原料,合成1-甲基-1-溴环己烷。
解:OHCH3HSO CH3HBrBrCH3问题6-6 完成下列转变:O解:O H SO,H OOHKMnO问题6-7 为什么苯酚的酸性比醇的酸性强?解:酚羟基中的氧原子可以和苯环发生p-π共轭,使O-H键的极性增大,易给出质子生成苯氧负离子,其负电荷分散到整个苯环上,所以比较稳定。
